Advances in Analytical Chemistry
Vol.3 No.3(2013), Article ID:12440,6 pages DOI:10.12677/AAC.2013.33004
Electrochemical Sensor for Acetaminophen Based on Gold Nanoparticles*
1College of Chemistry and Chemical Engineering, Liaoning Normal University, Dalian
2College of Material Science and Engineering, Guilin University of Electronic Technology, Guilin
Email: #xufen@guet.edu.cn
Received: Sep. 4th, 2013; revised: Sep. 10th, 2013; accepted: Sep. 17th, 2013
Copyright © 2013 Ying Pang et al. This is an open access article distributed under the Creative Commons Attribution License, which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
ABSTRACT:
A kind of GNPs/GC modified electrode was prepared by electrodeposited gold nanoparticles on the surface of glassy carbon electrode based on the cyclic voltammetry. Electrochemical properties and surface morphology of the modified electrode were characterized. The electrochemical behaviors of acetaminophen (ACOP) at GNPs/GC electrode were investigated by cyclic voltammetry and electrochemical impedance spectrum (EIS). The influences of different experimental conditions on the electrode performance were discussed. Under optimal conditions, a linear relationship of ACOP concentration with peak current was obtained over the concentration range of 2.0 × 10−7 - 2.0 × 10−5 mol∙L−1 and 1.4 × 10−4 - 3.78 × 10−3 mol∙L−1, respectively. The detection limit was 3.6 × 10−8 mol∙L−1 (S/N = 3:1) and the recovery was 97.7% - 101.0%.
Keywords: Acetaminophen; Au Nanoparticles; Modified Electrode; Cyclic Voltammetry
基于金纳米粒子的对乙酰氨基酚传感器的研究*
庞 莹1,徐 芬1,2#,孙立贤2
1辽宁师范大学化学化工学院,大连
2桂林电子科技大学材料科学与工程学院,桂林
Email: #xufen@guet.edu.cn
摘 要:
本文采用循环伏安法将金纳米粒子修饰在玻碳电极表面,制备了GNPs/GC修饰电极。对修饰电极进行电化学及表面形貌的表征,并通过循环伏安法和交流阻抗法研究了ACOP在GNPs/GC电极上的电化学行为。本文探讨了不同实验条件对电极性能的影响,在最优条件下,ACOP线性浓度范围分别为2.0 × 10−7~2.0 × 10−5 mol∙L−1和1.4 × 10−4~3.78 × 10−3 mol∙L−1,其检出限为3.6 × 10−8 mol∙L−1(S/N = 3:1),回收率为97.7%~101.0%。
收稿日期:2013年9月4日;修回日期:2013年9月10日;录用日期:2013年9月17日
关键词:对乙酰氨基酚;金纳米粒子;修饰电极;循环伏安法
1. 引言
对乙酰氨基酚(ACOP或Paracetamol)是世界上广泛采用的药物之一,作为人们长期使用的乙酰苯胺类药物,具有解热镇痛作用;可用于抵抗轻度至中度疼痛。但过量的摄入对乙酰氨基酚会影响人体的消化系统、泌尿系统、血液系统、呼吸系统,严重会抑制呼吸中枢,并导致肝损伤[1]。因此,其质量检测十分重要。电化学法操作简便,检测速度快,具有较高灵敏度[2]。
近年来,采用电化学方法测定ACOP的研究取得了很大进展。Mingqi Li[3]等制备了PANI-MWCNTs复合材料修饰电极灵敏测定ACOP的含量。Fen Xu[4]等研制了一种新型的DA电聚合膜用来测定ACOP,大大提高了灵敏度。王正国[5]等将ACOP在纳米金/十二烷基苯磺酸钠修饰电极上的电化学行为进行了研究。段连生[6]等制备了碳纳米管粉末微电极(CNTPME),研究了ACOP在CNTPME上的电化学行为。Gareth P. Keeley[7]等制备了热解碳薄膜,采用电化学法同时测定了对乙酰氨基酚和多巴胺。Chun-Xuan Xu[8]等人采用TiO2-GR/PMR修饰玻碳电极测定ACOP,灵敏度较高。
金纳米粒子(GNPs)具有很好的电催化行为和加速电子传输的能力,利用这些特性制备的金纳米粒子修饰电极已应用于电化学分析[9,10]。由于金纳米粒子有上述特点,本文将氯金酸溶液作为修饰电极的材料,采用循环伏安法(CV)制备了GNPs/GC修饰电极,并通过扫描电镜和电化学法对电极形貌和化学特性进行了表征。同时,研究了ACOP在该电极上的电化学行为。
2. 实验部分
2.1. 试剂与仪器
HAuCl4∙4H2O购自天津光复精细化工研究所;对乙酰氨基酚(ACOP)为分析纯,购自Aladdin Chemistry Co. Ltd.,并用无水乙醇配制成1.0 × 10−2 mol∙L−1 ACOP储备液,使用时用磷酸盐缓冲溶液稀释至所需浓度;铁氰化钾,氯化钾等其它试剂均为分析纯。用Na2HPO4和NaH2PO4配制成0.1 mol∙L−1磷酸盐缓冲溶液(pH = 6.2)。实验中所用水均为二次蒸馏水,所有实验均在室温下进行。
电化学实验是在IM6e电化学工作站(ZahnerElektrik, Kronach, German)上进行的;所有电化学实验均采用三电极系统,修饰的玻碳电极(直径3 mm,购于武汉高仕睿联科有限公司)为工作电极,Ag/AgCl (饱和KCl)电极为参比电极,Pt电极为对电极。SK3310 LHC超声波清洗器(购于上海科导超声仪器有限公司)。交流阻抗在5.0 × 10−3 mol∙L−1 K3[Fe(CN)6]/K4[Fe(CN)6] + 0.1 mol∙L−1 KCl溶液中进行,交流电压的振幅为5 mV,频率变化范围为0.1~100 kHz。扫描电镜分析(SEM)在JSM-5610LV SEM (JEOL, Japan)仪器上进行。
2.2. 实验方法
在修饰前将玻碳电极分别在1500目和2000目的金相砂纸上打磨后,依次在1.0、0.3 μm的氧化铝粉上打磨抛光至镜面,然后在1:1 HNO3 (V/V)、无水乙醇、二次蒸馏水中各超声洗涤15 min,室温下晾干备用。采用循环伏安法将玻碳电极置于含0.5 mg∙L−1的HAuCl4混合溶液中进行循环伏安扫描60圈,其扫描速度为100 mV∙s−1,扫描电位范围为−1.5~2.5 V,即得到GNPs/GC电极。将所制备的修饰电极在室温下,保存于pH 6.2 PBS缓冲溶液中备用。
将浓度为1.0 × 10−2 mol∙L−1的ACOP储备液用pH 6.2的磷酸盐缓冲溶液稀释至2.0 × 10−4 mol∙L−1,移取15 ml至电解池中,以GNPs/GC电极作为工作电极,采用循环伏安法进行扫描,电位范围−0.2~0.8 V,扫描速度为50 mV∙s−1,得到ACOP再修饰电极上的循环伏安曲线;并对所得到的曲线进行分析。
3. 结果与讨论
3.1. 修饰电极的扫描电镜分析
用扫描电子显微镜(SEM)对裸玻碳电极和GNPs/GC电极的表面形貌进行表征,如图1。图1(a)为裸玻碳电极的SEM图,其表面是光滑的,没有物质;而在GNPs/GC电极表面(见图1(b))可看到有一层分布均匀的颗粒,这说明金纳米粒子被成功修饰在电极表面上。由于金纳米粒子均匀地分布在电极表面,因此,它增大了电极的比表面积,促进了电极表面的电子转移,起到了电催化的作用。
3.2. 修饰电极的电化学性质
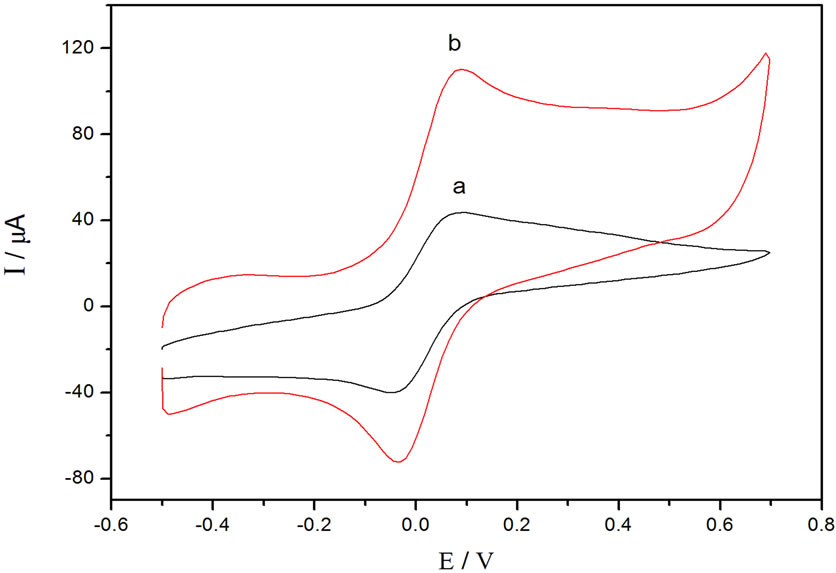
将裸玻碳电极、GNPs/GC电极分别在5.0 × 10−3 mol∙L−1 K3[Fe(CN)6]/K4[Fe(CN)6] + 0.1 mol∙L−1 KCl溶液中进行循环伏安扫描,扫描速度为100 mV∙s−1,结果见图2。比较两支电极的CV曲线,可观察到修饰了GNPs后的玻碳电极的CV曲线的氧化峰和还原峰电流均较裸玻碳电极的峰电流有所增大,且峰电位差变小,这说明金纳米粒子使电极的比表面积增大,促进了[Fe(CN)6]3−/[Fe(CN)6]4−电子对在电极上的电子转移,具有很好的导电性能。

(a) GC electrode; (b) GNPs/GC electrode.
Figure 1. SEM images of the modified electrodes
图1. 不同电极的扫描电镜图
(a) GC electrode; (b) GNPs/GC electrode.
Figure 2. Cyclic voltammograms of different electrodes in 5.0 × 10−3 mol∙L−1 K3[Fe(CN)6]/K4[Fe(CN)6] + 0.1 mol∙L−1 KCl solutions
图2. 不同电极在5.0 × 10−3 mol∙L−1 K3[Fe(CN)6]/K4[Fe(CN)6] + 0.1 mol∙L−1 KCl中的CV曲线
图3为裸玻碳电极和GNPs/GC电极在5.0 × 10−3 mol∙L−1 K3[Fe(CN)6]/K4[Fe(CN)6] + 0.1 mol∙L−1 KCl中的交流阻抗图谱。对交流阻抗图谱进行电路模拟(等效电路图见图3),其中裸玻碳电极(见图3中a曲线)的阻抗(Ret)约为300 Ω。而修饰上GNPs后,电极表面发生电化学反应的阻抗大大降低(见图3中b曲线),经拟合约为30 Ω。这进一步说明GNPs起到了增强电子传输的作用,促进了[Fe(CN)6]3−/4−电子对与电极间的电子转移。
3.3. ACOP在修饰电极上的电化学行为
图4为裸玻碳电极和GNPs/GC电极在2.0 × 10−4 mol∙L−1 ACOP溶液中的CV曲线,其扫描速率为50 mV∙s−1。从图中可看出,ACOP在裸玻碳电极上只有一个氧化峰,是典型的不可逆电极过程;而在GNPs/GC电极上其CV曲线上出现了一对氧化还原峰,且氧化峰电流明显提高,约为裸玻碳电极的10
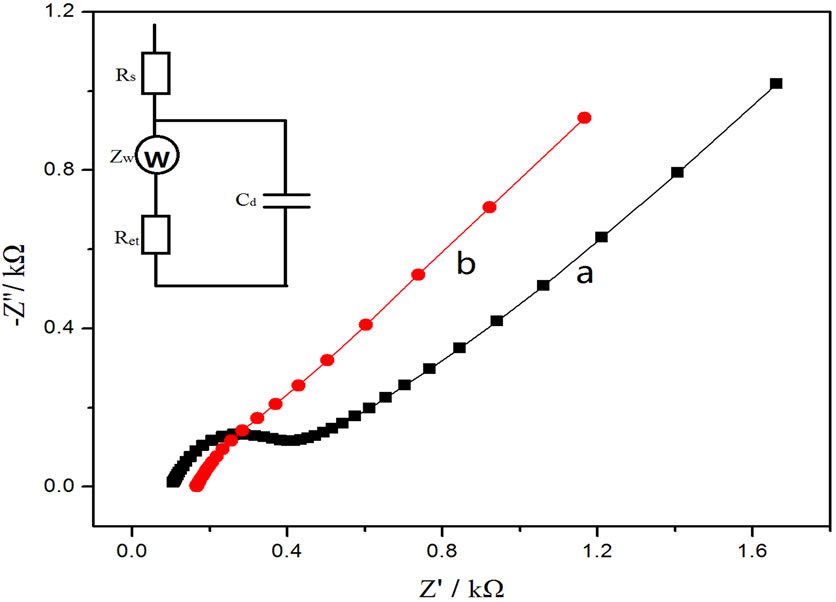
(a) GC electrode; (b) GNPs/GC electrode.
Figure 3. Curves of EIS of different electrodes in the 5.0 × 10−3 mol∙L−1 K3[Fe(CN)6]/K4[Fe(CN)6] + 0.1 mol∙L−1 KCl solution
图3. 不同电极在5.0 × 10−3 mol∙L−1 K3[Fe(CN)6]/K4[Fe(CN)6] + 0.1 mol∙L−1 KCl溶液中的交流阻抗

(a) GC electrode; (b) GNPs/GC electrode.
Figure 4. Cyclic voltammograms of different electrodes in PBS (pH 6.2) with 2.0 × 10−4 mol∙L−1 ACOP
图4. 不同电极在2.0 × 10−4 mol∙L−1ACOP的PBS (pH 6.2)的CV曲线
倍以上。这表明金纳米粒子使ACOP电极反应变为准可逆过程,并且对电子传递起到了良好的促进的作用。
如图4中b曲线,ACOP的氧化峰的峰电位为0.235 V,与裸玻碳电极相比负移了0.085 V,表明ACOP的氧化过电位明显降低;其还原峰电位在0.205 V处,氧化峰与还原峰的电位差ΔEp为30 mV。由文献[11]可知,根据能斯特体系可逆性的判断依据[ΔEp = 2.303RT/(nF)],即ΔEp = 59.16/n (测试温度为25℃),可得ΔEp理论 = 29.58 mV。可见ΔEp实验值与理论值非常接近,这表明在玻碳电极上修饰了GNPs后,ACOP在此电极上的电化学可逆性得到明显改善。
3.4. 缓冲溶液pH值的影响
由于ACOP的分子结构中既有羧基、又有羟基,所以选择具有适当pH值的缓冲溶液对ACOP的氧化峰峰电流响应有很大影响,本文考察了底液pH值(5.8~7.0)对ACOP氧化峰电流和峰电位的影响(见图5)。由图5(a)可知,随pH值的增加,ACOP在修饰电极上的峰电流先增大后减小,pH值在6.2时峰电流达到最大。因此本实验选择pH为6.2的磷酸盐缓冲溶液。
由图5(b)可看出,ACOP在修饰电极上的氧化峰电位随pH的增加而负移,氧化峰电位随pH的增加呈线性变化,即Epa(V) = −0.09643 pH + 0.86071 (r= −0.9966),这说明ACOP的反应过程有质子参与[12]。
3.5. 修饰圈数的影响
金纳米粒子的修饰量对ACOP的峰电流有影响,可通过控制修饰圈数来控制修饰量。分别制备修饰圈数为10圈、20圈、40圈、60圈、80圈、100圈的GNPs/GC电极,通过循环伏安法检测不同修饰量的GNPs/GC电极对ACOP的响应(见图6)。实验结果表明:当扫描圈数从10圈增加至60圈,ACOP的氧化峰电流随着圈数的增加而增大;当扫描圈数继续增大到100圈后,氧化峰电流随着圈数的增加有所降低。
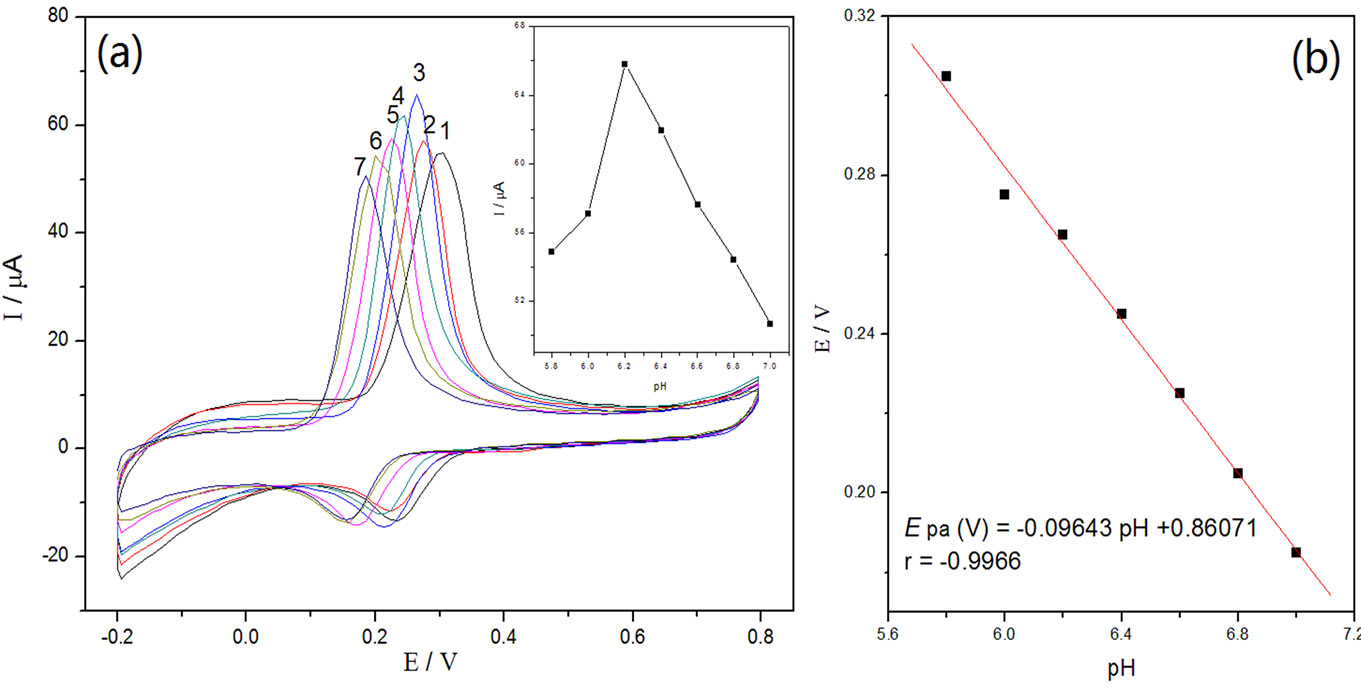
1-7: pH 5.8, 6.0, 6.2, 6.4, 6.6, 6.8, 7.0.
Figure 5. Effects of solution pH on the oxidation peak current and the oxidation peak potential of ACOP
图5. 缓冲溶液pH对ACOP氧化峰电流和峰电位的影响
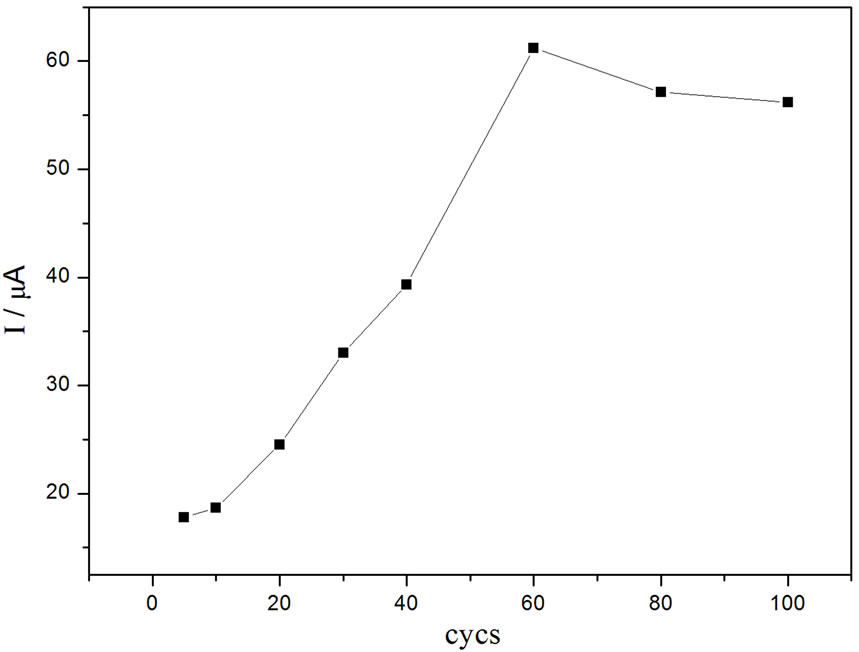
Figure 6. Effect of scan cycles on the oxidation peak current of ACOP
图6. 不同修饰圈数对ACOP峰电流的影响
这由于当修饰的GNPs超过一定量后可能发生了团聚,因而增大了电极表面的电阻,导致ACOP与电极之间的电子交换受阻所致。由实验结果可知,当修饰量为60圈时电流响应最佳,故本文选用的GNPs/GC电极修饰圈数为60圈。
3.6. 扫描速率的影响
扫描速率会影响ACOP的电化学行为。将修饰电极置于含2.0 × 10−4 mol∙L−1 ACOP的溶液(PBS, pH 6.2)中,测定CV曲线,改变扫描速度观察实验现象(见图7(A))。结果表明,扫描速率在20~250 mV/s范围内,随着扫速的增加,氧化峰的峰电流逐渐增大,氧化峰电位逐渐正移。ACOP的峰电流与扫描速率的平方根(v1/2)呈线性关系(见图7(B)),其氧化峰电流线性回归方程为Ipa(μA) = −13.27951 + 10.87205v1/2 (r = 0.99763),还原峰电流线性回归方程为Ipc(μA) = 8.32017 − 3.27488v1/2 (r = 0.9997)。说明ACOP在GNPs/GC修饰电极上的电化学反应是扩散控制过程[13]。当扫描速率较小时,氧化峰电流较小,灵敏度较低;同时随扫描速率的增大,还原峰电位发生负移,氧化峰电位发生正移。这表明随扫描速率增大,氧化峰电流增大、灵敏度增大;但峰电位差也增大,ACOP在该电极上的可逆性变差。因此,电化学实验选择扫描速率为50 mV/s。
3.7. 氧化峰电流与药物浓度的线性关系及电极的重复性、重现性
在最佳条件下,ACOP在2 × 10−7~2.0 × 10−5 mol∙L−1和1.4 × 10−4~3.78 × 10−3 mol∙L−1范围内,ACOP的浓度与氧化峰电流呈良好线性关系(见图8),其回归方程分别为Ipa(μA) = 1.13782c (μmol∙L−1) + 1.45035 (r = 0.99965)和Ipa(μA) = 0.0263c (μmol∙L−1) + 57.1029 (r = 0.99952),ACOP的检出限为3.6 × 10−8 mol∙L−1(S/N = 3:1)。实验考察了所制备的GNPs/GC电极的重复性和重现性。用同一支GNPs/GC修饰电极在2.0 × 10−4 mol∙L−1的ACOP中连续测试10次,得到的标准偏差为1.5%。另外,在相同条件下制备5支不同的GNPs/GC修饰电极,分别在2.0 × 10−4 mol∙L−1的ACOP中进行测量,得到的标准偏差为2.0%,这表明该药物传感器具有良好的重复性和重现性。
3.8. 干扰试验
参考文献[14]以常见的无机离子和常用药物等共存物质对修饰电极进行了干扰测试。实验表明:对于2 × 10−4 mol/L的ACOP及测量误差在±5%以内,500倍的K+、Na+、Mg2+、甘露醇、蔗糖、β-环糊精,200倍的维生素B2、葡萄糖,100倍的L-谷氨酸、L-赖氨酸及50倍的维生素B12对ACOP测定均不产生干扰。表明该电极具有一定的抗干扰能力。
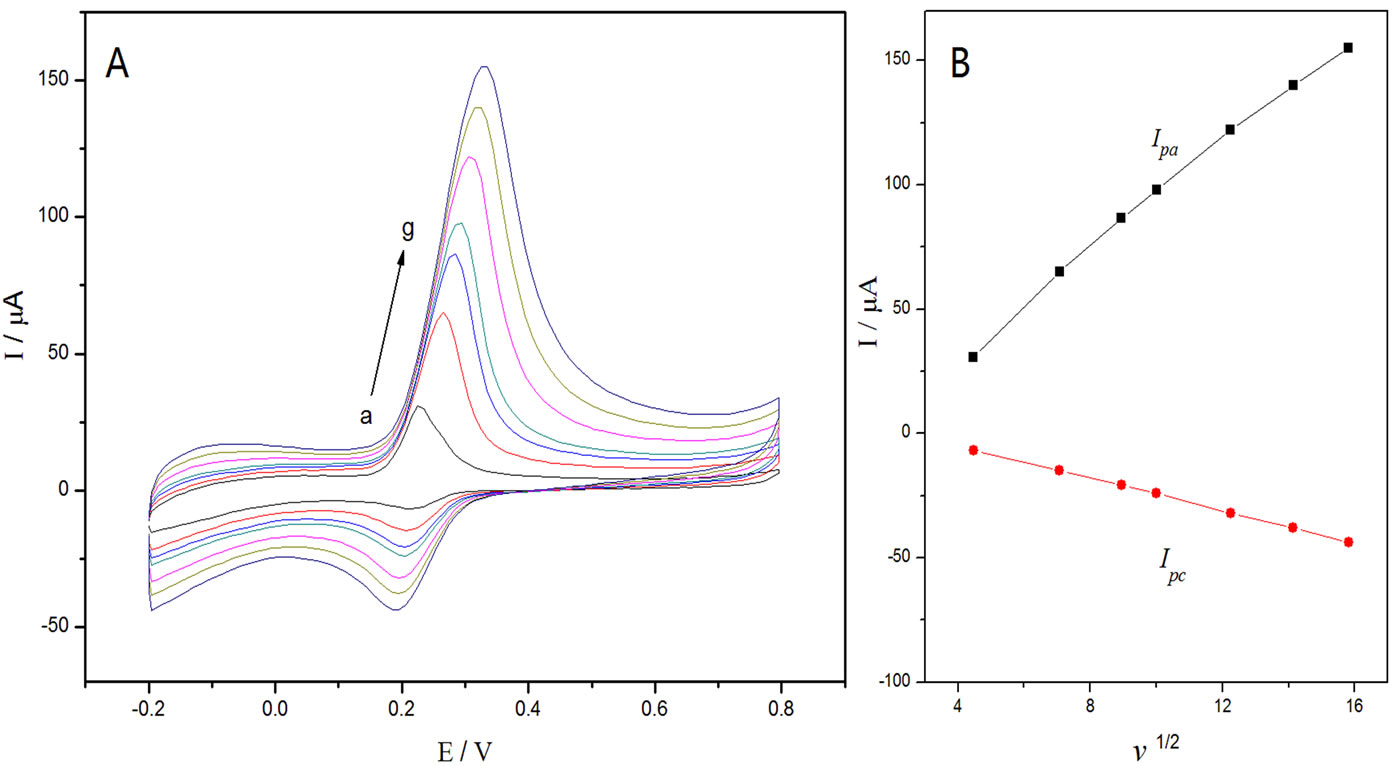
Figure 7. (A) Cyclic voltammograms of GNPs /GC electrode in 2.0 × 10−4 mol∙L−1 ACOP solution at various scan rates (from a to g): 20, 50, 80, 100, 150, 200, 250 mV∙s−1, respectively; (B) The relationship between the peak currents and v1/2
图7. (A) 不同扫速下GNPs/GC电极在2.0 × 10-4 mol∙L−1 ACOP溶液中的CV曲线;(B) 氧化峰电流和还原峰电流与v1/2的关系
3.9. 回收率实验及修饰电极的寿命
用已知浓度的ACOP原料配置三种不同浓度的样品,按照本实验方法进行操作。利用加标回收法测定ACOP的含量,结果见表1。由表1可知,其回收率为97.7%~101.0%。
本文还考察了所制备的GNPS/GC电极的储存稳定性。GNPS/GC电极不用时,储存在室温下pH 6.2的磷酸盐缓冲液中,每隔一段时间测试其在2.0 × 10−4 mol∙L−1 ACOP溶液中的氧化峰电流值。结果表明:该电极连续测量20天后,其峰电流仅降低了原来的5.5%。说明该电极具有较好的储存稳定性。
4. 结论
本文采用循环伏安法将金纳米粒子修饰在玻碳电极表面,制备了GNPS/GC电极,并对其实验条件进行了优化。结果表明:当修饰圈数是60圈,扫描速率是50 mV/s,磷酸盐缓冲溶液pH = 6.2时,修饰
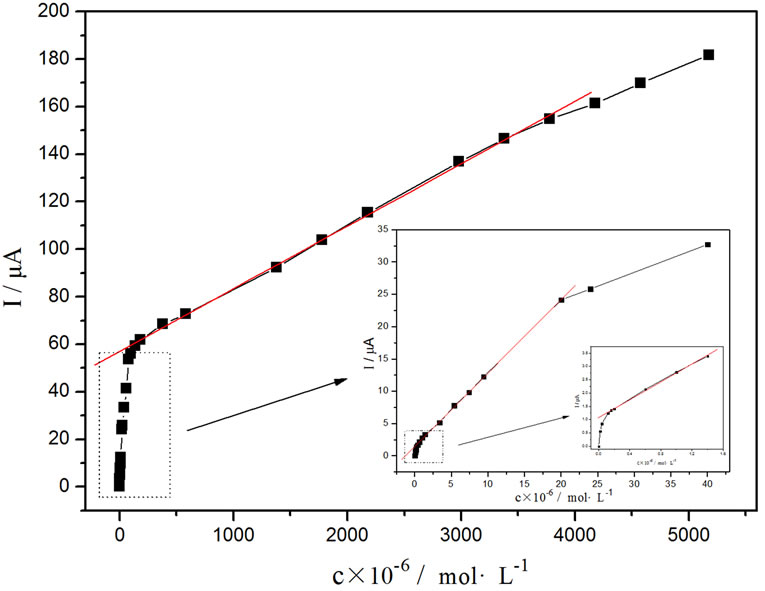
Figure 8. Calibration curves of the modified electrode for detecting ACOP
图8. ACOP浓度与氧化电流的关系
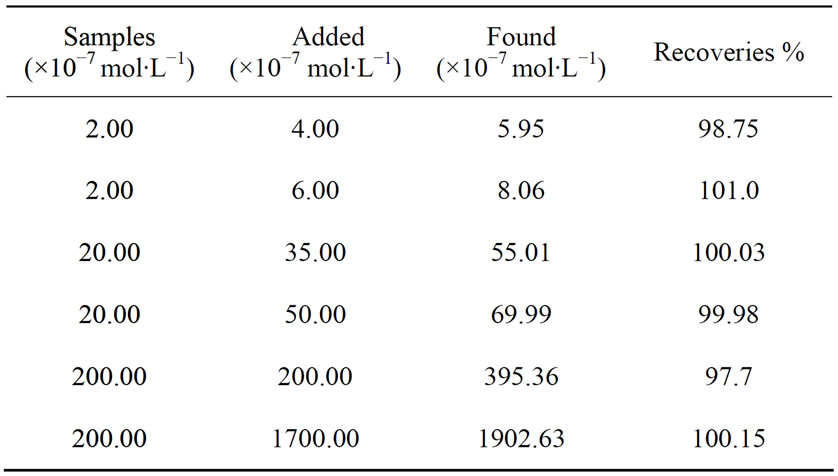
Table 1. Recovery test of ACOP (n* = 5)
表1. ACOP的回收率(n* = 5)
电极对ACOP的催化效果最好。氧化峰峰电流随ACOP浓度在2.0 × 10−7~2.0 × 10−5 mol∙L−1和1.4 × 10−4~3.78 × 10−3 mol∙L−1范围内呈线性关系,相关系数分别为0.99965和0.99952。检出限是3.6 × 10−8 mol∙L−1 (S/N = 3:1)。该电极用于测定ACOP具有灵敏度高、重复性和重现性好,稳定性好的特点。样品回收率在97.7%~101.0%。
5. 致谢
感谢国家自然科学基金项目(21173111、51071081、51071146、50671098、51071146、21075011),广西信息材料重点实验室重点基金(桂科能1210908-217-Z)对本文的资金资助。
参考文献 (References)
[1] B. D. Clayton, Y. N. Stock. Basic pharmacology for nurses. Mosby Inc., Harcourt Health Sciences Company, St. Louis, 2001.
[2] J. C. Song, J. Yang, J. F. Zeng, J. Tan and L. Zhang. Graphite oxide film-modified electrode as an electrochemical sensor for acetaminophen. Sensors and Actuators B: Chemical, 2011, 155 (1): 220-225.
[3] M. Q. Li, L. H. Jing. Electrochemical behavior of acetaminophen and its detection on the PANI-MWCNTs composite modified electrode. Electrochimica Acta, 2007, 52(9): 3250-3257.
[4] F. Xu, H. Y. Ru, L. X. Sun, Y. J. Zou, C. L. Jiao, T. Y. Wang, J. M. Zhang, Q. Zheng and H. Y. Zhou. A novel sensor based on electrochemical polymerization of diglycolic acid for determination of acetaminophen. Biosensors and Bioelectronics, 2012, 38 (1): 27-30.
[5] 王正国, 邓勤, 郑韵英, 石海信. 对乙酰氨基酚在纳米金/十二烷基苯磺酸钠修饰电极上的电学行为研究[J]. 化学研究与应用, 2012, 24(2): 175-180.
[6] 段连生, 曾国平. 对乙酰氨基酚在碳纳米管粉末微电极上的电化学行为[J]. 应用化学, 2008, 25(12): 1464-1467.
[7] G. P. Keeley, N. McEvoy, H. Nolan, S. Kumar, E. Rezvani, M. Holzinger, S. Cosnier and G. S. Duesberg. Simultaneous electrochemical determination of dopamine and paracetamol based on thin pyrolytic carbon films. Analytical Methods, 2012, 4(7): 2048-2053.
[8] C. X. Xu, K. J. Huang, Y. Fan, Z. W. Wu and J. Li. Electrochemical determination of acetaminophen based on TiO2-graphene/ poly (methyl red) composite film modified electrode. Journal of Molecular Liquids, 2012, 165(1): 32-37.
[9] G. M. Zeng, Z. Li, L. Tang, M. S. Wu, X. X. Lei, Y. Y. Liu, C. Liu, Y. Pang and Y. Zhang. Gold nanoparticles/water-soluble carbon nanotubes/aromatic diamine polymer composite films for highly sensitive detection of cellobiose dehydrogenase gene. Electrochimica Acta, 2011, 56(13): 4775-4782.
[10] N. F. Atta, R. A. Ahmed, H. M. A. Amin and A. Galal. Monodispersed gold nanoparticles decorated carbon nanotubes as an enhanced sensing platform for nanomolar detection of tramadol. Electroanalysis, 2012, 24(11): 2135-2146.
[11] 郑艳洁, 陈敬华, 张亚锋, 万红艳, 游勇基, 林新华. 对乙酰氨基酚在多壁碳纳米管修饰电极上的电化学行为及其测定[J]. 药物分析杂志, 2007, 27(02): 204-207.
[12] 茹慧瑛, 徐芬, 孙立贤, 刘青山, 刘娜. 基于层层自组装技术的对乙酰氨基酚药物电化学传感器研究[J]. 药学学报, 2011, 46(10): 1225-1230.
[13] D. X. Ye, Y. H. Xu, L. Q. Luo, Y. P. Ding, Y. L. Wang and X. J. Liu. LaNi0.5Ti0.5O3/CoFe2O4-based sensor for sensitive determination of paracetamol. Journal of Solid State Electrochemistry, 2012, 16(4): 1635-1642.
[14] 马心英, 吴义芳, 李霞. 石墨烯修饰电极的制备及其对对乙酰氨基酚的伏安测定[J]. 应用化学, 2012, 29(7): 824-829.
NOTES
*本文得到国家自然科学基金项目(21173111, 51071081, 51071146, 50671098, 51071146, 21075011);广西信息材料重点实验室重点基金(桂科能1210908-217-Z)的资金资助,特此感谢。
#通讯作者。