Material Sciences
Vol.2 No.2(2012), Article ID:602,4 pages DOI:10.4236/ms.2012.22011
Ti-DBS-LDHs as a Photocatalyst under Simulated Solar Radiation for Removal of Malachite Green
1College of Science, Northeast Forestry University, Harbin
2Post-Doctoral Mobile Research Station of Forestry Engineering, Northeast Forestry University, Harbin
Email: *ccx1759@163.com
Received: Dec. 28th, 2011; revised: Jan. 14th, 2012; accepted: Jan. 27th, 2012
ABSTRACT:
Ti-DBS-LDHs were fleetly prepared by the technology of the microwave-crystallization and low saturated state of coprecipitation. The purposed samples were characterized by XRD and SEM. The results show that the synthesized Ti-DBS-LDHs with the slice layer have the structure of LDHs, indicating their preparations are successful under microwave irradiation. Ti-DBS-LDHs was then applied to the decolorization of malachite green (MG). The effects of Ti/Mg molar ratio, MG concentration, catalyst dosage, dye type and circle life on the decolorization were investigated. It is shown the percentage of decolorization can reach 100% under the optimum conditions. In addition, Ti-DBS-LDHs was reusable, the average decolorization percentage of 89.37% could be obtained, the decolorization performance was stable after 3 times usage without significant loss of its decolorization activity. Therefore, TiDBS-LDHs is a novel and efficient photocatalyst for the decolorization of MG.
Keywords: Layered Double Hydroxides (LDHs); Dodecyl Benzene Sulfonate (DBS); Malachite Green (MG); Microwave Irradiation; Photocatalyst
Ti-DBS-LDHs光催化除去印染污水中的孔雀石绿
陈春霞1,2*,乔 淇1,郭 涛1,吕占傲1,李 斌1
1东北林业大学理学院,哈尔滨
2东北林业大学林业工程博士后流动站,哈尔滨
Email: *ccx1759@163.com
摘 要:
本文采用低饱和态共沉淀法,辅助微波手段,快速制备了具有膜片结构的十二烷基苯磺酸钠(DBS)改性的含钛层状双氢氧化物(Ti-DBS-LDHs),并将其用于孔雀石绿(MG)的废水处理中,光催化条件下,考察了MG的初始浓度、Ti-DBS-LDHs催化剂投加量、催化剂重复利用等一系列影响因素,探索了最佳工艺。在MG的浓度50 mg·L–1、催化剂的用量是200 mg·L–1、150 W的灯照射1个小时的条件下,MG可达到完全脱色。并且Ti-DBS-LDHs可重复利用,重复使用3次,其平均脱色率为89.37%。
收稿日期:2011年12月28日;修回日期:2012年1月14日;录用日期:2012年1月27日
关键词:LDHs;微波晶化;DBS;孔雀石绿;光催化
1. 引言
孔雀石绿、亚甲基蓝和甲基紫是常见的染色剂,广泛用于羊毛、麻织品、真丝、造纸、食品、皮革等领域,对人体之危害如呕吐、心脏、皮肤等,直接排放会造成环境污染。其中,孔雀石绿(Malachite green,简称为MG)是一种带有金属光泽的绿色结晶体,属三苯甲烷类染料[1]。由于“孔雀石绿”中的化学功能团三苯甲烷具有高毒、高残留及“三致”(致畸、致癌、致突变)作用,MG进入人体后,可引起肝、肾、心脏、脾、皮肤、眼睛、肺等多器官质变,是难降解的有机物,残留在水体中会产生较大的污染,已被许多国家列为不得检出的禁用物质[2,3],因此MG的废水处理是特别值得关注的课题。吸附是常用的处理废水的方法之一,常用的吸附剂有活性炭[4,5]、泥炭块[6,7]、甲壳素[8]、硅土[9]等,它们对不同染料废水的脱色都能取得一定的效果。但是吸附仅仅是把有害物质从一个物体转移到另一个物体,并没有从根本上除去污染物。光催化方法以其无二次污染,相对于常用的物理方法和生物方法,光催化降解技术以其广谱适用性和对有毒有机物的敏感性,为有机染料废水处理提供了一条新的、有工业化实际应用价值的途径[10-17]。近几年利用光催化降解有机污染物引起了广泛关注,光催化能有效地降解烃类、卤化物、染料、农药、酚类等有机物,最终矿化为CO2、H2O和有机物中所带的无机离子[18]。采用无机纳米材料处理染料废水的研究受到了极大的关注。
层状双氢氧化物(LDHs)由于这类化合物具有层状微孔结构,其层板上的Mg2+、Al3+离子可被光催化活性体阳离子同晶(如钛、钯、锌等)取代,其层间距可通过插入不同尺寸大小的阴离子基团来加以调控,从而可以制备出具有特殊光催化性能的材料[19-21]。目前,一些开拓性的文献[22-27]以层状双氢氧化物(LDHs)或其氧化物(LDO)作为光催化剂降解废水中的污染物,得到一些令人鼓舞的结果,然而这些LDHs的制备过程复杂,光催化活性有待进一步提高。LDHs是一种具有层状结构的无机材料,而处理的染料剂是有机化合物,无机有机很难相容,为了增加催化剂与处理对象的相容性,采用表面活性剂改性LDHs,即可增加LDHs的层间距,增加催化剂的吸附容量,也可以增加与印染剂的接触面积,从而提高催化剂对有机物的处理效果。又因钛是很好的光催化剂活性体,为了提高LDHs的疏水性能增加LDHs对印染剂的光催化性能,在活性中心钛的光催化作用下,其染料分子上发色官能团被破坏,从而达到快速脱色。因此本文采用低饱和态共沉淀法,辅助微波手段快速制备了表面活性剂十二烷基苯磺酸钠(DBS)修饰的LDHs,并根据LDHs的可设计性,部分同晶取代了镁离子添加了钛,制备DBS修饰的含钛LDHs即Ti-DBS-LDHs,并将其对MG进行光催化降解,通过MG初始浓度、Ti/Mg摩尔比、催化剂投加量以及Ti-DBS-LDHs循环寿命等系列影响因素,探索最佳工艺,以利于实际工业应用。
2. 实验部分
2.1. Ti-DBS-LDHs的制备
按一定比例量取1 mol·L–1的Mg(NO3)2、Ti(SO4)2、Al(NO3)3溶液组成混盐溶液(其中Ti/Mg的摩尔比从1/7~1/1;(Ti + Mg)/Al摩尔比为4),另取1.0 mol·L–1 NaOH和饱和十二烷基苯磺酸钠(DBS)的混合碱溶液。以80℃的温度,剧烈搅拌下两种溶液按一定的流速同时慢慢滴入恒温水浴的圆底三口烧瓶中,控制反应溶液的pH为8,1 h滴加完成,继续反应1 h,在70℃下微波晶化10 min,然后离心洗涤至中性,烘箱中干燥,制得不同Ti/Mg摩尔比的Ti-DBS-LDHs。样品的晶体结构采用日本理学生产的D/MAX 2200VPC型X射线衍射仪测试;样品的形貌用FEI-sirion型扫描电子显微镜进行测试。
2.2. MG光催化处理
分别称取一定质量(10~50 mg)的Ti-DBS-LDHs于100 mL烧杯中,再加入一定浓度(10~72 mg·L–1)的MG溶液,于多头磁力搅拌仪上,70℃的温度,一定的搅拌速度下,光源是中国生产的LZG型(220~240 V)舞台灯,采用CASON佳信仪器LX-1010B的数字式照度计测量光强,光照1 h后,离心分离,然后取其上清液在紫外–可见分光光度计中测定吸光度,根据Lambert-Beer定律可知,在一定范围内,染料的浓度与其在最大吸收波长的吸光度值呈正比的关系,即可得到标准曲线,然后计算得相应条件下MG溶液浓度,从而可得MG的脱色率。孔雀石绿脱色率(Decoloration rate/%)的计算公式如下式,其中C0为MG的初始浓度,C为MG光照后的浓度,MG的最大吸收波长为617 nm。
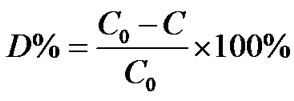
3. 结果与讨论
3.1. Ti-DBS-LDHs的表征
图1是Ti-DBS-LDHs(Ti/Mg摩尔比为1/5)的XRD图谱,从XRD图中可以看出,在2θ = 11.4˚、22.9˚、34.8˚、60.8˚附近处出现LDHs的(003)、(006)、(009)、(110)面的特征峰,位置与标准LDHs基本一致,XRD图都没有表现出Mg(OH)2和Al(OH)3等的衍射杂质峰,这说明通过低饱和态共沉淀方法能够成功制备出晶形好,结构较规整的Ti-DBS-LDHs。
从图2Ti-DBS-LDHs的SEM照片可以看出,有膜片的出现,这可能是因为DBS插层反应时其离子较大导致LDHs发生膨胀,层间距随着DBS离子逐渐进入逐渐增大,当层间距增大到层间的相互作用力完全消失,LDHs就以单片层的形式呈现出来,然后以单片层为构筑单元在存在氢氧根的DBS饱和溶液中自组装成薄膜Ti-DBS-LDHs。
3.2. Ti-DBS-LDHs对不同印染剂脱色性能的考察
在相同的水处理条件下:催化剂的用量是200 mg·L–1,用150 W的LZG型(220 V)舞台灯光照一个小时,考察了Ti-DBS-LDHs(Ti/Mg摩尔比为1/5)对染料的初始浓度为50 mg·L–1的孔雀石绿、亚甲基蓝和甲基紫的脱色性能的影响,其结果见表1。从表中可以看出Ti-DBS-LDHs对孔雀石绿的脱色效果最好,几乎完全脱色,甲基紫的脱色效果最差,达到71.00%,因此在下面的实验中以孔雀石绿探讨其它的实验参数。
3.3. Ti含量对MG的光催化性能的影响
在其它条件相同的条件下,即MG的浓度50 mg·L–1、催化剂的用量是200 mg·L–1、150 W的灯照射1个小时后测量脱色率,考察了Ti含量对MG的光催化性能的影响。从表2可知,当Ti/Mg摩尔比为0,即纯LDHs时,光照1小时对MG的降解率只有80.73%。当Ti/Mg摩尔比为1/7时,脱色率达到96.88%,随着钛含量的增加,MG的脱色率先增加后减小。当Ti/Mg摩尔比增加为1/5时,催化剂的活性最佳,脱色率为99.42%。这可能是因为随着Ti含量的增加,Ti具有很强的接受电子能力,降低了空穴–电子对的复合,提高光催化效率。但Ti的固载量过大的话,这时活性成分过多,出现活性成分的部分重叠,降低了有效的活性点,因此造成了光催化性能的相应减弱。因此,以下的光催化反应所用的Ti-DBS-LDHs催化剂均用4号样品。
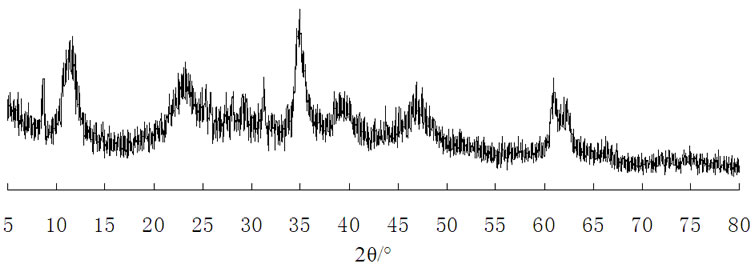
Figure 1. XRD patterns of Ti-DBS-LDHs
图1. Ti-DBS-LDHs的XRD图谱

Figure 2. SEM images of Ti-DBS-LDHs
图2. Ti-DBS-LDHs的SEM照片

Table 1. Comparison of catalytic properties of Ti-DBS-LDHs for three dyes
表1. Ti-DBS-LDHs 对不同印染剂脱色性能的考察
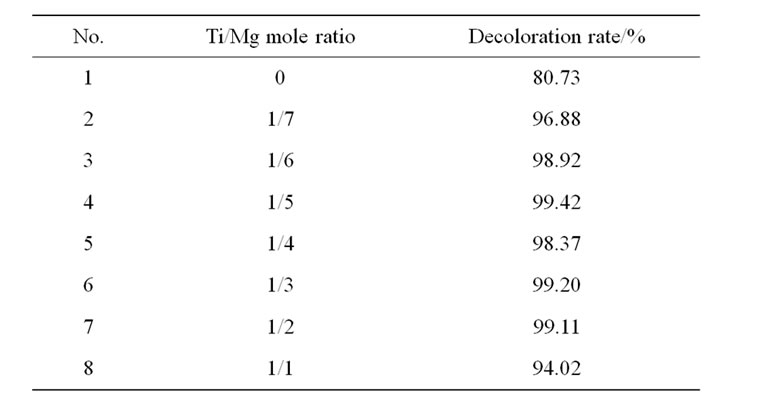
Table 2. Influence of Ti/Mg mole ratio on Ti-DBS-LDHs photocatalytic performance for MG
表2. Ti/Mg摩尔比对MG的光催化性能的影响
3.4. 催化剂用量对MG脱色率的影响
在反应器中分别加入100、200、300、400和500 mg·L–1的催化剂,研究催化剂用量对MG脱色率的影响,其结果如图3所示。由图3可知,催化剂浓度
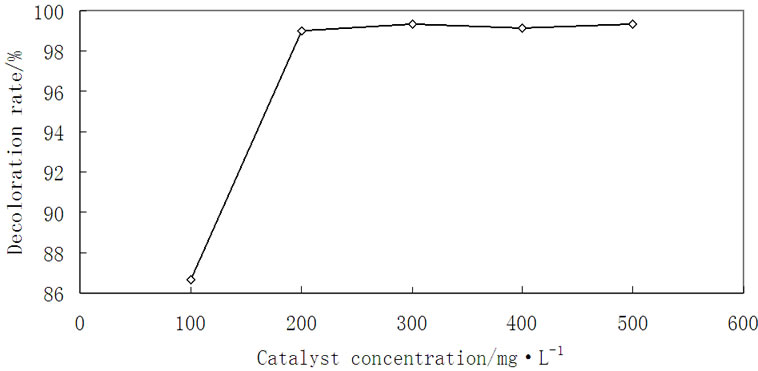
Figure 3. Effect of catalyst loading on the MG photodecolorization
图3. 催化剂的用量对MG脱色的影响
较低时,随着催化剂量的增加,D值增大的较快,催化剂的投加量为200 mg·L–1时,此时的D值为98.98%。随着催化剂投加量的增加对MG的降解率也增加,这是因为催化剂量越多,其捕捉到的光子越多,就能形成更多的光致空穴–电子对,加快反应速率;但是当催化剂用量增加到一定程度时,降解率趋于平缓,当催化剂的投加量为300 mg·L–1,此时的D值达到最大99.33%,虽比200 mg·L–1时有所增加,但增加比较缓慢,D值仅增加了0.45%,故从性能比上说,催化剂的最佳投放量为200 mg·L–1。
3.5. MG的初始浓度的影响
目标污染物MG的初始浓度对光催化降解率来说是一个重要的影响因素,考察了相同浓度的Ti-DBS-LDHs对10~72 mg·L–1不同浓度的MG溶液的脱色性能,其结果如图4所示。由图可见,随着初始浓度的增加,MG的脱色率先增加,当MG的浓度为50 mg·L–1时,脱色率达到最大,而后下降缓慢。这可能是因为吸附容量和吸附速率是吸附性能的两个表现,在其它条件相同,脱色剂质量保持不变,初始浓度增加,吸附速率可能增加了,在相同的时间内吸附的物质增多,使得催化剂表面参与染料平衡的活性

Figure 4. Effect of initial concentration of MG on decolorization
图4. MG浓度对脱色率的影响
基点增加,在MG的浓度10~50 mg·L–1的浓度下,Ti-DBS-LDHs的吸附容量增加,故此时吸附率增大,而MG的浓度从50~72 mg·L–1时,吸附剂Ti-DBSLDHs和吸附质MG的比率达到临界值,使得TiDBS-LDHs的脱色率减少。而且染料浓度过大引起色度增大,导致光源产生的紫外光的穿透溶液的能力减弱,减少了对紫外光的有效利用,因此,可导致光催化降解率降低。
3.6. Ti-DBS-LDHs的使用寿命
催化剂的循环使用寿命是催化剂的重要性质之一。在相同的条件下,即MG的浓度50 mg·L–1、催化剂的用量是200 mg·L–1、150 W的灯照射1个小时后测量脱色率,考察了Ti-DBS-LDHs对MG的使用寿命,在每次脱色结束后,将反应液离心分离,回收使用过的脱色剂,充分干燥后,再重复使用。由于每次回收的脱色剂都会有损失,故每次重复使用前,都要对脱色剂进行准确称量,以确保每次测定反应液中固液质量浓度比均为一样的,以排除回收损失对活性测定的影响。在同样条件下如此反复实验,考察TiDBS-LDHs使用寿命,其结果见表3。可以看出重复使用3次,第一次使用时,MG几乎完全脱色,第二次使用92.22%,第三次75.89%,其平均脱色率为89.37%,表现出Ti-DBS-LDHs优异的脱色稳定性。
影响LDHs稳定性的因素很多,而本文中最主要的原因是LDHs具有结构记忆效应,即LDHs受热分解,但在一定的环境下发生可使之恢复到层状结构的状态,也就是可以经一定物理化学变化逆向恢复原有结构的能力,但须注意的是,记忆效应与热分解的温度有关,当温度过高时,一般超过500℃,分解产物无法恢复至LDHs的层状结构。同时,此种恢复不是百分之百的恢复,且在恢复过程中,可能改变其层间的阴离子种类,这与所处的环境有关。本文中的反应温度较温和(70℃),即使LDHs在反应的过程发生变形,但经过染料剂的水溶液,也会进行结构的重建,使得保持原有的特殊层状结构,结构决定性质,因此,

Table 3. Cycle lifetime of Ti-DBS-LDHs in decolorization of MG
表3. Ti-DBS-LDHs的使用寿命
催化剂能够循环使用且保持较高的脱色率。
4. 结论
采用低饱和态共沉淀方法,辅助微波手段,在反应溶液pH = 8,反应温度80℃,微波晶化时间为10 min的条件下,以剥离再组装技术快速制备了具有层状结构的膜材料Ti-DBS-LDHs。考察了Ti-DBS-LDHs对孔雀石绿、亚甲基蓝和甲基紫的脱色性能,其结果表明在相同条件下,Ti-DBS-LDHs对MG的光催化性能最好。并考察了MG初始浓度、Ti/Mg摩尔比、催化剂投加量等条件下的Ti-DBS-LDHs光催化性能,且探讨了Ti-DBS-LDHs循环寿命,优化了Ti-DBS-LDHs对MG的光催化性能。以![]() ,在150 W的光照强度下,光照1个小时,催化剂的用量是200 mg·L–1,对MG的浓度50 mg·L–1溶液几乎完全脱色,并具有良好的循环寿命。因此对于污水中的MG染料,Ti-DBS-LDHs是一种环境友好型的高效光催化剂,具有很大的潜在研究价值。
,在150 W的光照强度下,光照1个小时,催化剂的用量是200 mg·L–1,对MG的浓度50 mg·L–1溶液几乎完全脱色,并具有良好的循环寿命。因此对于污水中的MG染料,Ti-DBS-LDHs是一种环境友好型的高效光催化剂,具有很大的潜在研究价值。
5. 致谢
感谢中国博士后科学基金(20100480955),中央高校基本科研业务费专项资金项目(DL11CB06)以及黑龙江省自然科学基金项目(B201014)对本文的资助。
参考文献 (References)
[1] Y. G. Liu, Y. Ohko, R. Q. Zhang, et al. Degradation of malachite green on Pd/WO3 photocatalysts under simulated solar light. Journal of Hazardous Materials, 2010, 184(103): 386-391.
[2] S. Srivastava, R. Sinha and D. Roy. Toxicological effects of malachite green. Aquatic Toxicology, 2004, 66(3): 319-329.
[3] B. H. Hameed, T. W. Lee. Degradation of malachite green in aqueous solution by Fenton process. Journal of Hazardous Materials, 2009, 164(2-3): 468-472.
[4] K. V. K. Rao. Inhibition of DNA synthesis in primary rat hepatocyte cultures by malachite green: A new liver tumors promoter. Toxicology Letters, 1995, 81(2-3): 107-113.
[5] L.G. Rushing, E. B. Hansen. Confirmation of malachite green, crystal violet and their leuco analogs in catfish and trout tissue by high-performance liquid chromatography utilizing electrochemistry with ultraviolet-visible diode array detection and fluorescence detection. Journal of Chromatography, 1997, 700: 223-231.
[6] Y. S. Ho, G. McKay. Sorption of dye from aqueous solution by peat. Chemical Engineering Journal, 1998, 70(2): 115-124.
[7] K. R. Ramakrishna, T. Viraraghavan. Dye removal using low cost adsorbents. Water Science Technology, 1997, 36(2): 189- 196.
[8] G. McKay, H. S. Blair and J. R. Gardner. Rate studies for the adsorption of dyestuffs on chitin. Journal of Colloid and Interface Science, 1983, 95(1): 108-119.
[9] G. McKay. Analytical solution using a pore diffusion model for a pseudo irreversible isotherm for the adsorption of basic dye on silica. AIChE Journal, 1984, 30: 692-697.
[10] M. Farooq, I. A. Raja and A. Pervez. Photocatalytic degradation of TCE in water using TiO2 catalyst. Solar Energy, 2009, 83(9): 1527-1533.
[11] A. A. Ismail. Single-step synthesis of a highly active photocatalyst for oxidation of trichloroethylene. Applied Catalysis B: Environmental, 2008, 85(1): 33-39.
[12] M. M. Joshi, N. K. Labhsetwar, P. A. Mangrulkar, et al. Visible light induced photoreduction of methyl orange by N-doped mesoporous titania. Applied Catalysis A: General, 2009, 357(1): 26-33.
[13] Y. M. Ju, S. G. Yang, Y. C. Ding, et al. Visible light induced photoreduction of methyl orange by N-doped mesoporous titania. The Journal of Physical Chemistry A, 2008, 112(37): 11172- 11177.
[14] S. K. Mohapatra, N. Kondamudi, S. Banerjee, et al. Functionalization of self-organized TiO2 nanotubes with Pd nanoparticles for photocatalytic decomposition of dyes under solar light illumination. Langmuir, 2008, 24(19): 11276-11281.
[15] S. K. Pardeshi, A. B. Patil. A simple route for photocatalytic degradation of phenol in aqueous zinc oxide suspension using solar energy. Solar Energy, 2008, 82(8): 700-705.
[16] H. Tian, J. F. Ma, K. Li, et al. Photocatalytic degradation of methyl orange with W-doped TiO2 synthesized by a hydrothermal method. Materials Chemistry and Physics, 2008, 112(1): 47-51.
[17] A. Watcharenwong, W. Chanmanee, N. R. de Tacconi, et al. Anodic growth of nanoporous WO3 films: Morphology, photoelectrochemical response and photocatalytic activity for methylene blue and hexavalent chrome conversion. Journal of Electroanalytical Chemistry, 2008, 612(1): 112-120.
[18] M. R. Hoffmann, S. T. Martin, W. Y. Choi, et al. Environmental applications of semiconductor photocatalysis. Chemical Reviews, 1995, 95(1): 69-96.
[19] F. Cavani, F. Trifiro and A. Vaccari. Hydrotalcite-type anionic clays: Preparation, properties and app1ications. Catalysis Today, 1991, 11(2): 173-301.
[20] C. X. Chen, C. H. Xu, L. R. Feng, et al. Effect of rare earth doping on the catalytic activity of copper-containing hydrotalcites in phenol hydroxylation. Advanced Synthesis & Catalysis, 2005, 347(14): 1848-1854.
[21] A. Vaccari. Preparation and catalytic properties of cationic and anionic clays. Catalysis Today, 1998, 41(1-3): 53-71.
[22] Y. F. Zhao, M. Wei, J. Lu, et al. Biotemplated hierarchical nanostructure of layered double hydroxides with improved photocatalysis performance. ACS Nano, 2009, 3(12): 4009-4016.
[23] Y. Zhi, Y. Li, Q. Zhang, et al. ZnO nanoparticles immobilized on flaky layered double hydroxides as photocatalysts with enhanced adsorptivity for removal of acid red G. Langmuir, 2010, 26(19): 15546-15553.
[24] S. Huang, H. Peng, W. W. Tjiu, et al. Assembling exfoliated layered double hydroxide (LDH) nanosheet/carbon nanotube (CNT) hybrids via electrostatic force and fabricating nylon nanocomposites. Journal of Physical Chemistry B, 2010, 114 (50): 16766-16772.
[25] J. S. Valente, F. Tzompantzi and J. Prince. Highly efficient photocatalytic elimination of phenol and chlorinated phenols by CeO2/MgAl layered double hydroxides. Applied Catalysis B, 2011, 102(1-2): 276-285.
[26] S. C. Gomes, Y. Bouizi, V. Fornés, et al. Layered double hydroxides as highly efficient photocatalysts for visible light oxygen generation from water. Journal of American Chemical Society, 2009, 131(38): 13833-13839.
[27] Y. F. Zhao, S. He, M. Wei, et al. Hierarchical films of layered double hydroxides by using a sol-gel process and their high adaptability in water treatment. Chemical Community, 2010, 46: 3031-3033.
NOTES
*通讯作者。