Hans Journal of Nanotechnology
Vol.05 No.04(2015), Article ID:16288,8 pages
10.12677/NAT.2015.54009
Preliminary Study on the Purification and Surface Modification Procedures of Graphite Encapsulated Iron Nanoparticles
Shang-Shih Li*, Mao-Hua Teng
Department of Geosciences, National Taiwan University, Taipei Taiwan
*通讯作者。
Received: Oct. 13th, 2015; accepted: Oct. 31st, 2015; published: Nov. 3rd, 2015
Copyright © 2015 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
The novel ultrafine material of graphite encapsulated metal (GEM) nanaoparticles was first discovered in 1993. The outer shells of GEM material are composed of graphitic layers with superior adsorbing property and the inner core is composed of nanocrystalline metal. Due to the excellent catalytic ability of ferromagnetic metal to transform carbon to graphite, the researches about synthesizing graphite encapsulated ferromagnetic metal nanoparticles are most common. In this study, we focused on the purification and surface modification procedures of FeGEM. It is found that the purification steps with hydrochloric acid can reduce the impurities of oxides and preserve high percentage of well-encapsulated nanoparticles. We also found that after the purification, the following refluxing procedure with nitric acid under 80˚C can modify the surface of FeGEM nanoparticles from hydrophobicity to hydrophilicity and maintain the suspension of FeGEM in water or ethanol for more than 24 h. The modification processes not only overcome the agglomeration problem of FeGEM nanoparticles but also enhance the potential applications of the material.
Keywords:Ferromagnetic, Refluxing, Modification, Hydrophobicity, Hydrophilicity

石墨包裹纳米铁晶粒的纯化及表面改质程序之初步研究
李尚实*,邓茂华
国立台湾大学地质科学系,台湾 台北

收稿日期:2015年10月13日;录用日期:2015年10月31日;发布日期:2015年11月3日

摘 要
石墨包裹纳米金属晶粒(Graphite Encapsulated Metal nanoparticles, GEM)是一种在1993年偶然间发现的新超威复合材料,外层由吸附效果佳的多片石墨层所组成,内核则包裹有纳米金属晶粒,而由于铁、钴和镍等铁磁性金属具有催化碳变为石墨的能力,故以合成石墨包裹纳米铁磁性金属晶粒的研究最为普遍。本研究系以石墨包裹纳米铁晶粒(FeGEM)做为主要研究材料,针对该材料的合成纯化步骤及表面改质程序,进行操作条件的分析改良,成功发现使用盐酸进行FeGEM颗粒的酸溶纯化步骤可降低产物中氧化物杂质的产生,并可保留最佳包裹良率;而利用硝酸进行升温回流程序,则可以在较低的升温条件(80℃)下达到改质FeGEM表面特性的目的,使颗粒表面由亲油性转变为亲水性,且可稳定悬浮于去离子水或乙醇等极性溶剂中24小时以上,有效解决颗粒容易团聚的缺点,大幅提升FeGEM的应用潜力。
关键词 :铁磁性,回流,改质,亲油性,亲水性

1. 前言
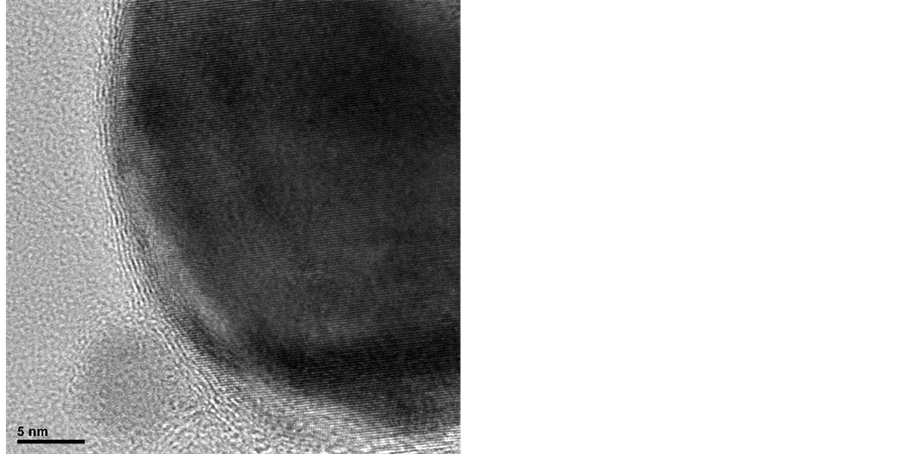
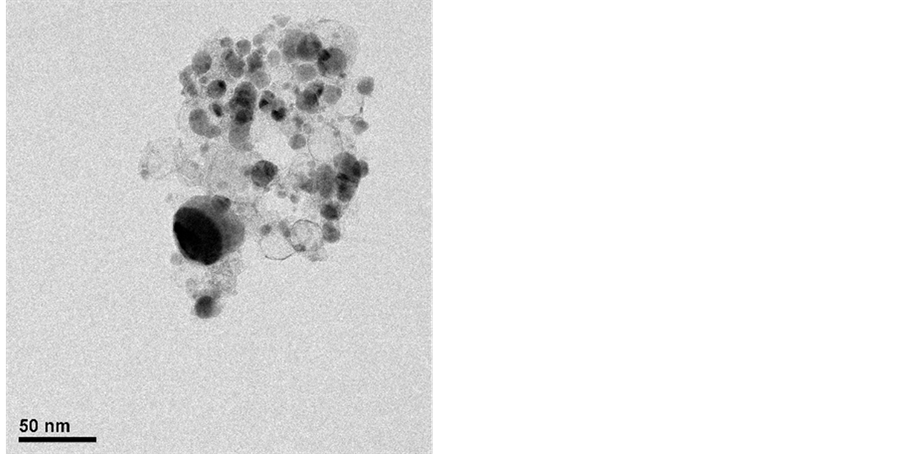
石墨包裹纳米铁磁性金属晶粒(FeGEM),为一种纳米碳复合材料,由图1(a)和图1(b)显示其颗粒大小为5~100纳米[1] -[5] ,系利用石墨层作为外壳来包覆内部核心的铁磁性金属晶粒,使该金属晶粒于纳米尺度下不易受到外在环境影响而氧化、酸蚀,保有其金属特性,因此藉由该材料具有纳米尺度、磁性质以及外层包覆与生物兼容性高的碳质壳层等优势,预期FeGEM纳米颗粒应可适用于例如药物载体 [6] 、磁流体 [7] 、吸附剂 [8] 以及示踪剂等领域。本研究团队近十几年一直致力于增进石墨包裹纳米磁性金属晶粒之产量和良率 [9] ,藉由改善电弧放电系统之构件、调整纯化处理方式和步骤以及选用甲烷或钻石粉等不同碳源进行GEM颗粒合成,其中又以铁原料含量及其特性潜能最具有开发应用之潜力,然在合成石墨包裹纳米铁晶粒的改良上,却受限于铁溶碳率大于钴和镍金属而导致包裹不完全的现象,于收集初产物的过程中便会因接触到空气而产生自燃形成大量氧化铁,致使FeGEM产率大幅下降。直到2012年,本研究团队尝试以液态醇类作为合成GEM颗粒之碳源 [10] ,由真空舱外部直接注入,发现不仅石墨包裹纳米镍或钴晶粒之良率有显着提升,更重要的是藉由所使用的液态碳源,可稳定合成出大量的石墨包裹铁晶粒,不会产生剧烈的自燃现象,对于以往因FeGEM之制程产量过低,导致无法合成足够材料来进行分析和研究之难题得以解决,故本研究便是利用液态碳源的添加来稳定合成FeGEM之初产物,藉此进行后续纯化和表面改质的研究。
 (a)(b)
(a)(b)
Figure 1. (a) and (b) are the HRTEM images of FeGEM nanoparticles
图1. (a)和(b)为FeGEM纳米颗粒的HRTEM照片
然而虽然FeGEM具有众多材料特性上的优势,却因为颗粒之间存在凡得瓦力和磁力的吸引,导致颗粒严重团聚,降低纳米尺度下材料具有高比表面积的应用优势,相较于纳米碳管和石墨烯的分散研究,FeGEM材料则鲜少有相关文献探讨,本研究团队于2011尝试使用接口活性剂来增加颗粒之间的空间屏障效应,配合流变仪的使用建立一套胶体悬浮系统的检测程序 [11] ,但仍无法使FeGEM颗粒稳定悬浮于极性溶液中。
为了改善之前分散研究的缺点以及对FeGEM颗粒的了解,本研究目的系建立标准之FeGEM材料纯化步骤,并透过材料表面改质程序来调整颗粒表面的亲水特性,使FeGEM颗粒可稳定悬浮于极性溶剂中,增加其应用潜能。
2. 实验
本研究材料的制备过程,系使用1995年Dravid等人所建立的改良式钨电弧放电系统来进行 [12] ,阳极选用内部可放置金属原料的石墨坩埚;阴极则采用钨棒,配合2012年Chiu等人设计液态碳源注入装置 [10] ,于电弧放电过程中注入液态醇类,藉以提供FeGEM材料所需之碳源,其中合成步骤及条件,可参考2012年Chiu等人之文献 [10] 。
合成所得之初产物会由装置的舱体内壁收集获得,其中包含有1) 未包裹完全或是无包裹之金属铁颗粒、2) 碳杂质以及3) 包裹良好之FeGEM颗粒等,前两者属于本研究所谓之杂质,针对不同金属包裹之复合材料,本研究进行不同酸液之溶蚀分析,目的系为了得到最佳的纯化条件,不会过度破坏包裹良好的FeGEM颗粒,并达到移除杂质的效果。
根据图2之实验步骤,先于室温下选用一般常见之硫酸(97%)、硝酸(60%)和盐酸(37%)等强酸来进行FeGEM初产物的浸泡处理,用以移除初产物中的金属杂质,于酸液中可明显观察到溶液颜色呈现黄色,此为铁金属杂质被酸溶后形成铁离子的结果,之后利用去离子水洗涤残留的酸液,接着利用强磁铁的磁性,收集带有磁性质的FeGEM颗粒,藉以将不具有磁性的碳杂质分离移除,最后将纯化出来的FeGEM颗粒置于抽风柜中风干后进行称重收集。

Figure 2. The purification procedure of FeGEM nanoparticles
图2. 纯化FeGEM纳米颗粒之程序
除了前述以不同酸液进行产物纯化程序之分析,本研究另外针对纯化后的FeGEM颗粒进行表面改质步骤,其目的系为了增加FeGEM颗粒表面的亲水特性,因此需要于FeGEM壳层表面接上含氧官能基如-COOH或-OH,本研究选用硝酸、硫酸和盐酸等强酸作为强氧化剂,于80℃加热条件下进行FeGEM颗粒表面改质步骤,先选取一定量之纯化FeGEM纳米颗粒以及20 ml之三种强酸,使用传统回流程序 [13] 进行升温氧化处理2小时,再经由去离子水重复洗涤去除颗粒表面残留的酸液,最后进行材料的干燥、秤重回收及特性分析。
3. 结果与讨论
针对FeGEM的纯化处理,其目的系为保留最大量包裹完整的FeGEM产量,以及降低内部杂质的含量,经由室温条件下单纯比较硝酸、硫酸和盐酸等强酸对FeGEM纳米颗粒的纯化影响,利用SEM和EDS的分析,由图3(a)~(c)可明显观察到硝酸此种含氧强酸会于产物中形成非铁磁性三氧化二铁之杂质;而图4(a),图4(b)显示硫酸亦会于产物中形成高的氧含量,呈现最低氧含量的为图5(a),图5(b)以盐酸进行纯化处理之样品,且对于盐酸纯化处理之SEM分析结果,可直接观察到产物呈现均匀的球状颗粒样貌,相较硝酸和硫酸纯化处理之产物中存在多种不同晶形之组成成分,可清楚说明于室温条件下利用硝酸或硫酸作为FeGEM纳米颗粒纯化处理之酸蚀溶液,会造成产物纯化过程中杂质含量的提升,亦会降低材料单位重量所具有的磁性质。
进一步将不同强酸溶液纯化后之产物进行Raman测试,观察使用不同强酸对于FeGEM颗粒表面石墨外壳的影响,根据图6分析结果无论使用何种酸液进行纯化,FeGEM颗粒均显示位于1585 cm−1附近,存在碳原子以sp2键结进行E2g声子对称震动之G峰讯号,同时位于1335 cm−1附近则可观察到碳原子以A1g振动模式显示出的D峰讯号,该D峰讯号主要来自平面原子晶格上的缺陷或杂质,可视为石墨二维晶格中sp3键结造成之结果,而一般常用D峰和G峰的强度比值(ID/IG)来定义待测物表面石墨晶格的缺陷程度,当比值越高表示石墨晶格的缺陷或非晶质碳的比例越高,反之则表示较佳石墨化晶格结构 [14] - [16] 。
因此根据Raman检测结果,其中选用硝酸进行纯化之FeGEM颗粒呈现较小的ID/IG比值,结合之前使用EDS分析已证实硝酸的氧化能力可形成完全氧化态之铁锈成分(Fe2O3),故推论在纯化过程中,硝酸的氧化能力不仅可使铁杂质形成氧化铁,同时会氧化移除部分FeGEM颗粒外壳中的非晶质碳,因此呈现较佳的石墨晶格壳层,然对于纯化目的而言,保留大量包裹好的FeGEM颗粒并降低产物中的杂质含量,才有利于之后材料的应用及特性分析,故纯化步骤使用盐酸进行酸处理可根据式(1)有效移除铁杂质而不会形成氧化铁成分,且其ID/IG比值最大,即表示纯化后产物中会保留部份为非晶质碳组成之包裹完全的FeGEM纳米颗粒,因此对于FeGEM材料的纯化程序选用盐酸较硝酸和硫酸适合。
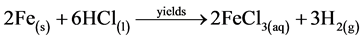 (1)
(1)
经过前述纯化步骤的分析探讨,使用盐酸可以避免过多氧化物杂质的存在,得到较佳的纯化产物,故本研究选用盐酸纯化处理之FeGEM颗粒进行其表面改质程序,藉由在颗粒表面接上如-COOH或-OH等含氧官能基来将原本为亲油性之FeGEM颗粒改质为亲水性,如此可增加FeGEM颗粒于水性溶剂中的分散度,降低团聚所造成的沉淀现象。
 (a)
(a)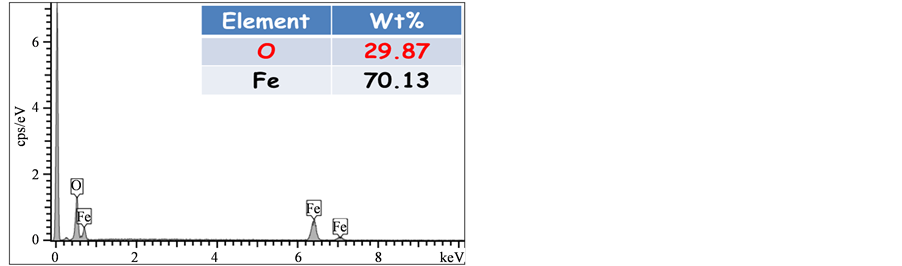
 (b) (c)
(b) (c)
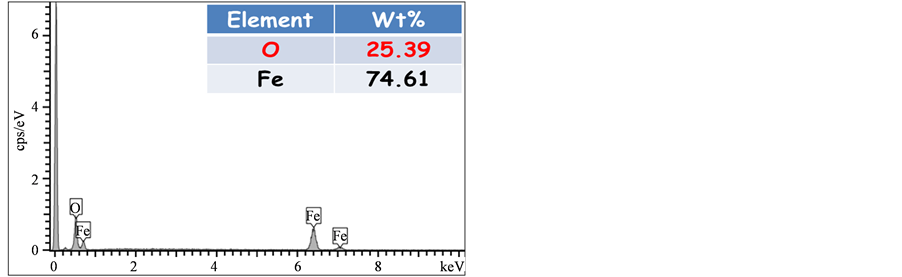
Figure 3. (a) SEM image of FeGEM nanoparticles which were purified by HNO3; (b) and (c) The EDS results of rectangle area in SEM image show the impurities of iron oxide
图3. (a)经过硝酸纯化处理之FeGEM颗粒SEM照片;(b)和(c)分别为SEM照片中两个方型区块的EDS元素分析,呈现氧化铁杂质的组成成分

 (a) (b)
(a) (b)
Figure 4. (a) SEM image of FeGEM nanoparticles which were purified by H2SO4; (b) The EDS result of rectangle area in SEM image
图4. (a)经过硫酸纯化处理之FeGEM颗粒SEM照片;(b)为SEM照片中方型区块的EDS元素分析结果

 (a) (b)
(a) (b)
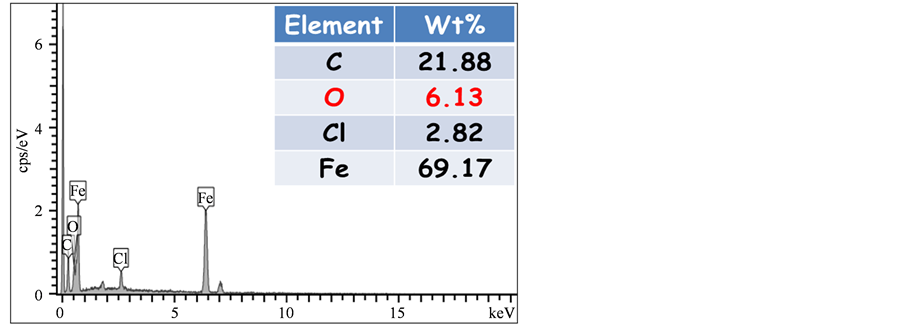
Figure 5. (a) SEM image of FeGEM nanoparticles which were purified by HCl; (b) The EDS result of rectangle area in SEM image
图5. (a)经过盐酸纯化处理之FeGEM颗粒SEM照片;(b)为SEM照片中方型区块的EDS元素分析结果
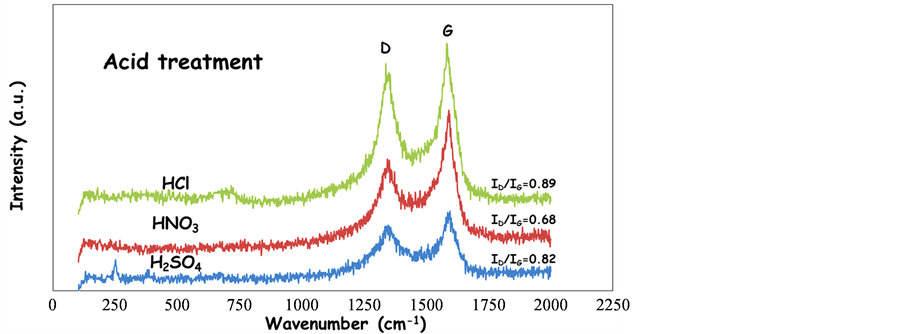
Figure 6. Raman results of FeGEM nanoparticles purified by different acid
图6. 使用不同强酸进行纯化处理之FeGEM纳米颗粒的Raman分析结果
实验过程同样选用三种酸作为颗粒表面之改质剂,以回流程序将选用之强酸升温至约80℃,根据硝酸、硫酸及盐酸三种强酸之基本特性,硝酸的沸点最低为83℃,由于本研究希望可降低产物于改质过程中被破坏之比例,因此选用接近硝酸沸点的温度作为回流实验之固定变因,而使用不含氧盐酸作为改质剂系做为与纯化步骤之比较。
经由图7的Raman分析可观察到升温酸处理对于FeGEM颗粒外壳的影响,当分别使用盐酸和硫酸进行升温回流步骤,FeGEM颗粒之ID/IG比值均显着下降,反之使用硝酸回流则会造成ID/IG比值上升,根据分析结果可解释对于盐酸和硫酸,升温所造成之效果,主要反应在对FeGEM壳层中非晶质碳的蚀刻破坏和移除,因此降低具有缺陷之石墨结构的比例;硝酸对FeGEM颗粒之影响则不仅在非晶质碳的破坏,更因升温条件而强化其对石墨壳层的氧化能力,使其表面改质接上亲水性的含氧官能基-COOH和-OH,也因此增加石墨壳层中的不规则结构比例,致使ID/IG的比值上升,此部份可由图8(a)~(c)沉降实验的观察直接证实经由硝酸回流之FeGEM颗粒,具有良好的亲水特性,可稳定悬浮于极性溶剂如去离子水或乙醇中达24小时以上。
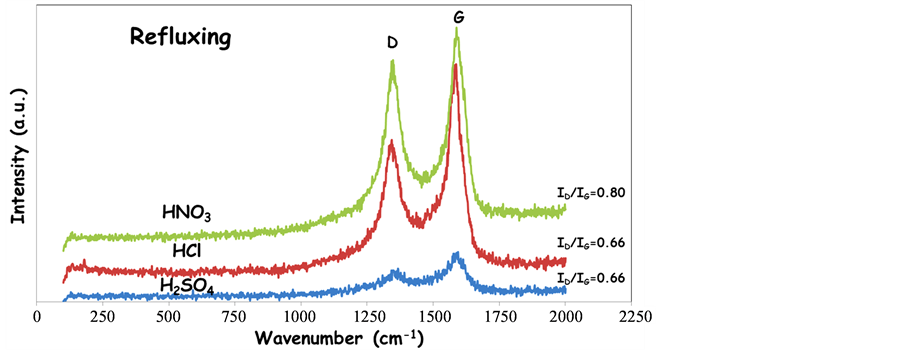
Figure 7. Raman results of FeGEM nanoparticles refluxing with different acid
图7. 使用不同强酸进行回流处理之FeGEM纳米颗粒的Raman分析结果
 (a)
(a)
 (b)
(b) (c)
(c)
Figure 8. The observation results of FeGEM particles. From left to right the FeGEM nanoparticles are treated by HCl acid treatment only (in deionized water), H2SO4- refluxing (in deionized water), H2SO4-refluxing (in alcohol), HNO3-refluxing (in alcohol) and HNO3-refluxing (in deionized water). The pictures show the appearance after (a) 30 min, (b) 60 min, and (c) 24 h
图8. FeGEM颗粒之沉降观察实验,由左而右之样品分别为盐酸纯化处理(去离子水)、硫酸回流(去离子水)、硫酸回流(乙醇)、硝酸回流(乙醇)以及硝酸回流(去离子水),分别静置(a) 30分钟、(b) 60分钟以及(c) 24小时
4. 结论
本研究对于FeGEM纳米颗粒的合成纯化步骤及表面改质程序进行了系统性的探讨与分析,并针对每一步骤之目的建立较佳的反应条件,其中使用盐酸进行FeGEM纳米颗粒的纯化可避免过多氧化物杂质,并得到最大量包裹完整的FeGEM产物,有效维持材料的磁性质。对于具有表面亲油特性之FeGEM纳米颗粒,利用硝酸进行升温回流步骤,可成功将其表面由亲油性改质为亲水性,使其能稳定悬浮于如去离子水或乙醇等极性溶剂中,并可维持24小时以上,有效提升FeGEM纳米颗粒的应用潜能,并降低颗粒因团聚而产生沉淀以及低比表面积之缺点。针对本研究室自行合成之FeGEM纳米复合颗粒,经由初步实验之分析结果,已成功建立使用盐酸进行FeGEM纯化以及利用硝酸进行FeGEM改质之程序,可有效增加FeGEM纳米复合颗粒之应用潜能。
文章引用
李尚实,邓茂华. 石墨包裹纳米铁晶粒的纯化及表面改质程序之初步研究
Preliminary Study on the Purification and Surface Modification Procedures of Graphite
Encapsulated Iron Nanoparticles[J]. 纳米技术, 2015, 05(04): 63-70. http://dx.doi.org/10.12677/NAT.2015.54009
参考文献 (References)
- 1. Tomita, M., Saito, Y. and Hayashi, T. (1993) LaC2 Encapsulated in Graphite Nano-Particle. Japanese Journal of Applied Physics, 32, L280. http://dx.doi.org/10.1143/JJAP.32.L280
- 2. Ruoff, R.S., Lorents, D.C., Chan, B., Malhotra, R. and Subramoney, S. (1993) Single Crystal Metals Encapsulated in Carbon Nanoparticles. Science, 259, 346-348. http://dx.doi.org/10.1126/science.259.5093.346
- 3. Taylor, A., Krupskaya, Y., Costa, S., Oswald, S., Krämer, K., Füssel, S., Klingeler, R., Büchner, B., Borowiak-Palen, E. and Wirth, M.P. (2010) Functionalization of Carbon Encapsulated Iron Nanoparticles. Journal of Nanoparticle Research, 12, 513-519. http://dx.doi.org/10.1007/s11051-009-9773-0
- 4. Host, J.J., Dravid, V.P. and Teng, M.H. (1998) Systematic Study of Graphite Encapsulated Nickel Nanocrystal Synthesis with Formation Mechanism Implications. Journal of Materials Research, 13, 2547-2555. http://dx.doi.org/10.1557/JMR.1998.0355
- 5. Teng, M.H., Hsiao, C.I. and Hsiao, Y.L. (2009) Formation Me-chanism of Microcrystalline Spherical Graphite Particles in Solidified Nickel. Diamond and Related Materials, 18, 396-398. http://dx.doi.org/10.1016/j.diamond.2008.08.006
- 6. Shubayev, V.I., Pisanic, T.R. and Jin, S. (2009) Magnetic Nanoparticles for Theragnostics. Advanced Drug Delivery Reviews, 61, 467-477. http://dx.doi.org/10.1016/j.addr.2009.03.007
- 7. Jeong, U., Tneg, X., Wang, Y., Yang, H. and Xia, Y. (2007) Superparamagnetic Colloids: Controlled Synthesis and Niche Applications. Advanced Materials, 19, 33-60. http://dx.doi.org/10.1002/adma.200600674
- 8. Bystrzejewski, M., Pyrzyńska, K., Huczko, A. and Lange, H. (2009) Biodistribution and Accumulation of Intravenously Administered Carbon Nanotubes in Mice Probed by Raman Spectroscopy and Fluorescent Labeling. Carbon, 47, 1189-1192. http://dx.doi.org/10.1016/j.carbon.2008.12.031
- 9. Teng, M.H., Tsai, S.W., Hsiao, C.I. and Chen, Y.D. (2007) Using Diamond as a Metastable Phase Carbon Source to Facilitate the Synthesis of Graphite Encapsulated Metal (GEM) Nanoparticles by an Arc-Discharge Method. Journal of Alloys and Compounds, 434-435, 678-681. http://dx.doi.org/10.1016/j.jallcom.2006.08.275
- 10. Chiu, C.C., Lo, J.C. and Teng, M.H. (2012) A Novel High Efficiency Method for the Synthesis of Graphite Encapsulated Metal (GEM) Nanoparticles. Diamond and Related Ma-terials, 24, 179-183. http://dx.doi.org/10.1016/j.diamond.2012.01.015
- 11. Lee, S.S. and Teng, M.H. (2011) Dispersion of Graphite Encapsulated Nickel Nanoparticles in a NP-9 Colloidal System. Diamond and Related Materials, 20, 183-186. http://dx.doi.org/10.1016/j.diamond.2010.11.028
- 12. Dravid, V.P., Host, J.J., Teng, M.H., Elliott, B., Hwang, J.H., Johnson, D.L., Mason, T.O. and Weertman, J.R. (1995) Controlled-Size Nanocapsules. Nature, 374, 602. http://dx.doi.org/10.1038/374602a0
- 13. Chen, C.C., Chen, C.F., Chen, C.M. and Chuang, F.T. (2007) Modifica-tion of Multi-Walled Carbon Nanotubes by Microwave Digestion Method as Electrocatalyst Supports for Direct Me-thanol Fuel Cell Applications. Electrochemistry Communications, 9, 159-163. http://dx.doi.org/10.1016/j.elecom.2006.06.031
- 14. Ferrari, A.C. (2007) Raman Spectroscopy of Graphene and Graphite: Disorder, Electron-Phonon Coupling, Doping and Nonadiabatic Effects. Solid State Communications, 143, 47-57. http://dx.doi.org/10.1016/j.ssc.2007.03.052
- 15. Ferrari, A.C. and Robertson, J. (2001) Resonant Raman Spectroscopy of Disordered, Amorphous, and Diamondlike Carbon. Physical Review B, 64, Article ID: 075414. http://dx.doi.org/10.1103/PhysRevB.64.075414
- 16. Lespade, P., Marchard, A., Couzi, M. and Cruege, F. (1984) Caracterisation de Materiaux Carbones par Microspec- trometrie Raman. Carbon, 22, 375-385. http://dx.doi.org/10.1016/0008-6223(84)90009-5