Journal of Advances in Physical Chemistry
Vol.1 No.2(2012), Article ID:915,3 pages DOI:10.4236/JAPC.2012.12002
Synthesis of Brönsted Acid Ionic Liquid and Application in Catalytic Synthesis of Ethyl Acetate
Yantai Darbond Technology Co. Ltd., Yantai
Email: lwx0015@gmail.com
Received: Jul. 16th, 2012; revised: Jul. 21st, 2012; accepted: Aug. 13th, 2012
ABSTRACT:
A novel Brönsted acid ionic liquid was synthesized using benzyl chloride, N-diethyl imidazole and sulfuric acid as materials. Its structure was confirmed through IR and 1H NMR. The catalytic activity of the acidic ionic liquids for the esterification of acetic acid with ethanol was measured. Ethyl acetate with a yield of 72.35% was obtained under the following conditions: molar percentage of catalyst relative to the reactants 5%, reaction temperature 80˚C and reaction time 90 min. The ionic liquid can be reused for more than four times without remarkable loss of catalytic activity.
Keywords: Acidic Ionic Liquids; Synthesis; Ethyl Acetate; Catalysis
Brönsted酸性离子液体的合成及催化酯化反应的应用
骆万兴,赵晓艳,骆明月
烟台德邦科技有限公司,烟台
Email: lwx0015@gmail.com
摘 要:
以苄基氯、N-乙基咪唑、浓硫酸为原料,合成了一种含有磺酸基的新型Brönsted酸性离子液体,通过IR、1H NMR对其结构进行了表征。将其应用于催化乙酸和乙醇的酯化反应,考察了其反应条件和循环使用性能。结果表明最佳反应条件为:反应时间90 min,催化剂用量5%,反应温度80℃。此条件下产率为72.35%。离子液体循环使用4次,其催化效率基本不变。
收稿日期:2012年7月16日;修回日期:2012年7月21日;录用日期:2012年8月13日
关键词:酸性离子液体;合成;乙酸乙酯;催化
1. 引言
离子液体又称室温液体盐,是由有机阳离子和无机阴离子构成的、在室温或近室温下呈液态的有机盐类。离子液体的种类比较多,经历了对水敏感的氨盐/三氯化铝体系阶段,对空气、水稳定的六氟磷酸、四氟硼酸咪唑、吡啶鎓盐体系阶段,目前朝向功能化方向发展,成为可以设计的绿色溶剂/催化剂功能体系[1]。
乙酸乙酯是有机合成的重要原料,是应用最广的酯类之一。工业生产中通常使用浓硫酸作催化剂。由于浓硫酸存在一定的环境污染,并且对设备有腐蚀,近年来,为了解决此类问题,出现了固体超强酸、杂多酸、强酸性阳离子交换树脂等多种酯化催化剂[2-4]。但是这些催化剂的制备过程比较复杂,也有一定的局限性。因此,开发具有功能化的酯化催化剂就显得尤其重要。2002年Cole[5]等首次报道了Brönsted酸性离子液体的合成,并成功地用于酯化、成醚等需要酸催化的合成反应,自此,Brönsted酸性离子液体得到了广泛研究和发展。酸性离子液体既具有酸高密度反应活性的优点[6],又具有不挥发、酸强度分布均匀以及易循环使用等优点,具有替代浓硫酸作为酯化催化剂的潜力[7]。
本文设计合成了一种新型的Brönsted酸性离子液体,其分子中阳离子部分含有磺酸基,阴离子为[HSO4]–,因此具有很强的酸性。酯化催化实验结果表明该离子液体对乙酸乙酯的合成反应具有良好的催化性能。反应结束后,通过简单的相分离就可以实现产物与离子液体的分离,分离后的离子液体经过真空脱水处理后可以重复使用。
2. 实验部分
2.1. 主要仪器与试剂
Magana550型傅立叶红外光谱仪(美国);Bruker Avance-400型核磁共振仪(瑞士);DF-101s集热式恒温加热磁力搅拌器;DZF-6021型真空干燥箱(上海)。
N-乙基咪唑(工业级,使用前干燥纯化,收集104℃/15 mmHg馏分),苄基氯,浓硫酸,冰醋酸,无水乙醇,乙酸乙酯,乙醚,碳酸钠,氯化钠,氯化钙,无水硫酸镁等均为市售分析纯试剂。
2.2. 酸性离子液体的合成
2.2.1. 离子液体合成路线
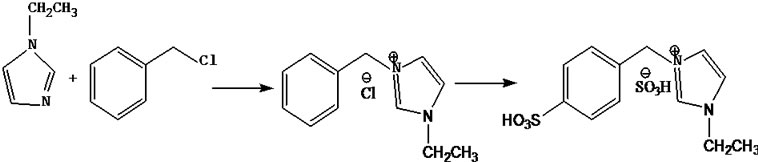
2.2.2 合成方法
100 mL三口烧瓶中加入15 mL甲苯、7.7 mL(0.08 mol)N-乙基咪唑、9.0 mL(0.08 mol)苄基氯,搅拌,80℃搅拌反应24 h,反应结束后,倾倒出上层甲苯,用乙酸乙酯洗涤3次,80℃减压蒸馏得到白色粘稠状液体Ⅰ,产率为89.3%。
100 mL三口烧瓶置于冰水浴中,加入7 mL 98%的浓硫酸,搅拌,将液体Ⅰ缓慢滴入三口瓶中,保持反应温度为0℃,24 h反应结束,用乙醚洗涤除去多余的硫酸,减压蒸馏得到淡红色粘稠状液体Ⅱ,产率为87.2%。IR(KBr),ν(cm–1):3132(磺酸基中的-OH),3074(芳环C-H);1557,1499,1447(苯环骨架);1260,1023(SO2);852(苯环C-H变形振动);657(S-O)。1H NMR(D2O),δ:1.37(m,3H,CH3);3.91~4.29(m, N-CH2);5.25(s,2H,Ph-CH2);7.33~7.43(m,6H,Ar-H);8.76(s,1H,咪唑环上的氢)。
2.3 离子液体溶解性的测定
分别取一定量的离子液体,加入5 mL不同的溶剂,进行溶解性能测试[8]。
2.4 离子液体催化酯化反应[9-11]
150 mL三口烧瓶中加入适当比例的冰醋酸、无水乙醇及离子液体,混合摇匀,在一定温度下搅拌反应1~4 h,反应结束后,在沸水浴中进行减压蒸馏,直至不再有馏出物为止,得到粗乙酸乙酯。在摇动状态下向馏出液中慢慢加入饱和碳酸钠水溶液,直至不再有气泡冒出,有机相对pH试纸呈中性为止。将液体转入分液漏斗中,分去水相,有机相依次用饱和氯化钠溶液、饱和氯化钙溶液洗涤两次,弃去下层液,酯转入干燥的锥形瓶用无水硫酸镁干燥,将干燥后的乙酸乙酯滤入蒸馏瓶中,在沸水浴上进行蒸馏,收集73℃~ 78℃馏分。最后称重计算产率。每次反应完毕后催化剂经过适当的洗涤和真空脱水后可重复使用。
3. 结果与讨论
3.1. 离子液体谱图分析
通过红外谱图可以观察到化合物Ⅱ中有苯环骨架振动吸收:1557 cm–1,1499 cm–1,1447 cm–1;2984(芳环C-H伸缩振动);同时也观察到了磺酸基团的振动吸收:1260 cm–1,1023 cm–1(SO2),657 cm–1(S-O)。由于化合物Ⅰ中的乙基咪唑环已经带有正电荷,电子密度小,所以在磺化时磺酸基引入到苯环上,而谱图中852 cm–1处出现的吸收峰为苯环上对位取代后两个邻位氢的振动吸收,也说明磺化时磺酸基引入到苯环上。再结合核磁氢谱的结果,重水交换后,氢的数目与对位取代后芳环及N-乙基上的氢的数目完全相符,因此可以确认得到了目标化合物。
3.2. 离子液体溶解性的测定
溶解性测定结果表明该离子液体溶于水、乙酸,常温下微溶于乙醇,不溶于乙酸乙酯和乙醚,其在极性较大并具有氢键的溶剂中具有较好的溶解性(见表1)。溶解性实验结果表明该离子液体应用于乙酸乙酯
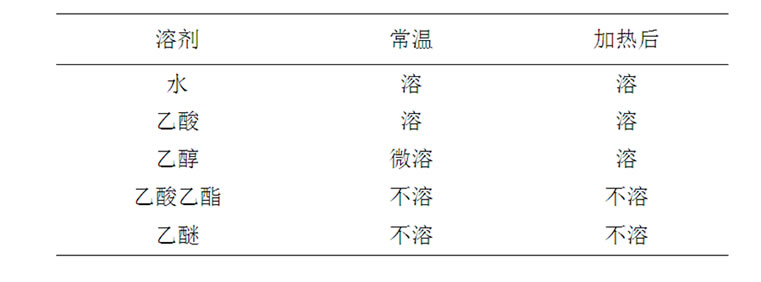
Table 1. Solubility of ionic liquid in different solvents
表1. 离子液体在不同溶剂中的溶解性
的合成反应时,反应为均相催化。反应过程中生成的产物和离子液体自动分层,有利于正反应的进行。反应结束后,离子液体只需经过简单的相分离和减压蒸馏就可以回收利用。
3.3. 离子液体催化乙酸乙酯合成
3.3.1. 催化剂用量对乙酸乙酯产率的影响
首先考察了离子液体用量对酯化反应的影响,并与浓硫酸作催化剂进行了比较。在固定乙酸与无水乙醇的物质的量比为1:1.5,回流时间为90 min,反应温度为80℃的条件下,离子液体的用量对乙酸乙酯的产率影响见表2,催化剂用量按总投料的摩尔百分比计算。单独使用浓硫酸作催化剂时乙酸乙酯的产率为44.59%。
由表2可以看出,离子液体对乙酸乙酯的合成有明显的催化作用,且随着催化剂用量的增多,乙酸乙酯的产率有增加的趋势,当催化剂用量超过5%时,再增加催化剂用量,产率提高不明显。因此,本实验选择催化剂最佳用量为5%,此时乙酸乙酯的产率为72.35%,与单独使用浓硫酸作催化剂相比产率提高27.76%。
3.3.2. 反应温度对乙酸乙酯产率的影响
不同反应温度对酯化反应的实验结果见表3。
从表3可以看出,升高反应温度可以提高乙酸乙酯的产率,但当反应温度由60℃上升到80℃时,产率提高并不明显,说明在接近回流温度时反应逐渐趋于平衡,因此,本实验选择最佳反应温度为回流温度80℃。
3.3.3. 反应时间对乙酸乙酯产率的影响
从表4可以看出,随着反应时间的增加,酯化产率逐渐升高,但当反应超过90 min时,延长反应时间,产率变化不大,说明此时酯化反应趋于平衡。从能耗

Table 2. Esterification yields under different amount of ionic liquid
表2. 催化剂用量对酯化产率的影响

Table 3. Esterification yields under different reaction temperatures
表3. 反应温度对酯化产率的影响
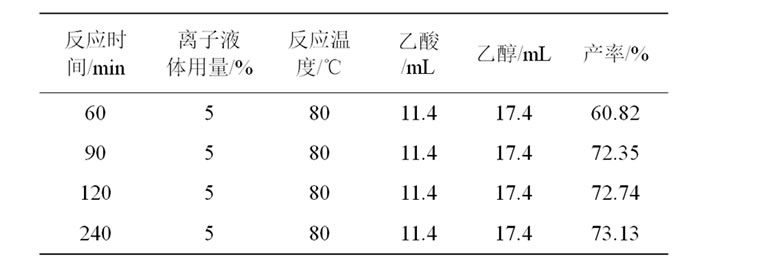
Table 4. Esterification yields under different reaction times
表4. 反应时间对酯化产率的影响
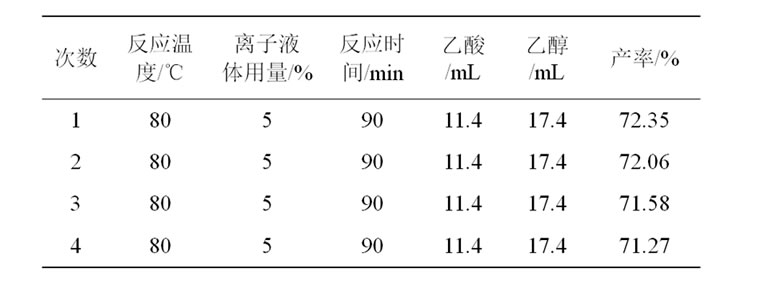
Table 5. Esterification yields under reuse of ionic liquid
表5. 离子液体的循环使用结果
角度考虑,本实验选择反应时间90分钟为最佳反应时间。
3.3.4. 离子液体循环使用性能
循环使用性能是离子液体的一个重要特点,因此本实验也考察了离子液体循环使用的催化情况,结果见表5。从表中可以看出,离子液体重复使用4次,酯化反应产率变化不大,说明该离子液体具有良好的循环使用性能。乙酸乙酯的产率略有下降可能是由于在循环使用中的少量损失或脱水不完全所致。
4. 结论
通过两步反应合成了一种新型含磺酸基的酸性离子液体,IR和1H NMR分析确认了其结构。对乙酸乙酯的催化合成研究表明,该离子液体具有明显的酯催化作用,在离子液体用量为5%,反应时间90 min,温度80℃,n(乙酸):n(乙醇)=1:1.5摩尔比的条件下,酯化产率可达72.35%。与传统的浓硫酸作催化剂相比,酯化产率提高27.76%,且催化剂用量少,反应后的离子液体易于分离。分离后的离子液体重复使用4次,催化活性基本保持不变。
参考文献 (References)
[1] 顾彦龙, 石峰, 邓友全. 室温离子液体: 一类新型的软介质和功能材料[J]. 科学通报, 2004, 49(6): 515-521.
[2] 张小曼. 稀土固体超强酸对合成乙酸乙酯的催化性能研究[J]. 化学试剂, 2002, 24(4): 233-234.
[3] 王新平, 叶兴凯, 吴越等. 用杂多酸固载化催化剂催化酯化反应[J]. 精细石油化工, 1994, 2: 15-20.
[4] 杨亚婷, 赵维, 刘静等. Lewis 固体酸催化合成乙酸乙酯的研究[J]. 应用化工, 2003, 32(6): 23-24.
[5] A. C. Cole, J. L. Jensen, I. Ntai, et al. Novel Brönsted acidic ionic liquids and their use as dual solvent-catalysts. Journal of the American Chemical Society, 2002, 124: 5962-5963.
[6] 吴芹, 董斌琦, 韩明汉等. 新型Brönsted酸性离子液体的合成与表征[J]. 光谱学与光谱分, 2007, 20(10): 2027-2031.
[7] 黄宝华, 汪艳飞, 杜志云等. 酸性离子液体的合成和光谱表征[J]. 分析测试学, 2007, 26(4): 478-483.
[8] 叶天旭, 张予辉, 刘金河等. 烷基咪唑类室温离子液体的合成及其溶解性能研究[J]. 现代化工, 2003, 1: 15-18.
[9] 王清廉, 沈凤嘉. 有机化学实验[M]. 北京: 高等教育出版社, 2003: 160-162.
[10] 唐晓丽, 王少君, 魏莉等. 咪唑类离子液体催化合成乙酸乙酯的研究[J]. 大连轻工业学院学报, 2007, 26(2): 140-142.
[11] 郝巍, 李存雄. 离子液体在酯化反应中的应用[J]. 贵州师范大学学报, 2006, 24(4): 117-120.