Journal of Advances in Physical Chemistry
Vol.05 No.03(2016), Article ID:18262,8
pages
10.12677/JAPC.2016.53008
Measurement of Fluorescence Spectra and Quantum Yield of Carbon Nanoparticles Made from Monosodium Glutamate
Nannan Zheng1, Xianfeng Chu2, Lizhi Pan2, Senlin Bi1, Sha Ding1, Xingping Zhou1
1College of Chemistry, Chemical Engineering and Biotechnology, Donghua University, Shanghai
2Blasting and Coating Department, Shanghai Waigaoqiao Shipbuilding Co., Ltd., Shanghai

Received: Jul. 24th, 2016; accepted: Aug. 12th, 2016; published: Aug. 16th, 2016
Copyright © 2016 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
In this article, fluorescent carbon nanoparticles (Glu-FCN), made by monosodium glutamate pyrolysis, have been researched, mainly including measurements of Glu-FCN fluorescent spectra and quantum yields. On one hand, pH dependence has been shown to be present in Glu-FCN according to our works. The fluorescence intensity is pretty low when surrounding pH is less than 3.0 or over 12.0. In contrast, it will become quite high when the pH is between 3.0 and 9.0. On the other hand, luminous position of Glu-FCN is very fixed. Optimal excitation and emission wavelengths are respectively located at 338 nm and 391 nm in a stable state. Importantly, good linear relationship exists between fluorescence intensity and concentration of Glu-FCN neutral aqueous solutions. The linear range is 0.20 - 50.0 μg/mL, with 0.20 μg/mL limitation. Eventually, quantum yields of Glu-FCN have been determined using quinine sulfate as a reference under different excitations. And Glu-FCN quantum yield is concluded to be as high as 51.5% under the optimal excitation (338 nm), implying its feasibility for being a fluorescent marker.
Keywords:Monosodium Glutamate, FCN, pH Property, Fluorescent Marker

谷氨酸钠碳纳米颗粒的荧光光谱 及量子产率测定
郑楠楠1,楚险峰2,潘立志2,毕森林1,丁莎1,周兴平1
1东华大学化学化工与生物工程学院,上海
2上海外高桥造船有限公司涂装部,上海

收稿日期:2016年7月24日;录用日期:2016年8月12日;发布日期:2016年8月16日

摘 要
本论文主要以高温热解谷氨酸钠得到的荧光碳纳米颗粒(Glu-FCN)为研究对象,对其荧光光谱及其量子产率进行研究。结果显示:一方面,Glu-FCN存在pH依赖性,当pH在3.0到9.0之间时它的荧光强度最强,而其他范围荧光较弱;另一方面,此荧光碳纳米颗粒水溶液发光位置稳定,最佳激发波长为338 nm和发射波长为391 nm,荧光稳定性极佳。在中性环境下,Glu-FCN水溶液的荧光强度和浓度之间存在很好的线性关系,线性范围在0.2~50 μg/mL,检出下限为0.2 μg/mL。最后,以硫酸奎宁溶液为参比,测量了Glu-FCN在不同激发波长下的荧光量子产率,在最佳激发波长338 nm处的荧光量子产率高达51.5%,适合作为荧光标记物使用。
关键词 :谷氨酸钠,FCN,pH特性,荧光标记物

1. 引言
荧光碳纳米粒子(Fluorescent Carbon Nanoparticle, FCN)是近十年来发现的一种新型荧光纳米材料。2004年Xu等人 [1] 在分离纯化由电弧放电制备的单壁碳纳米管(Single Walled Carbon Nanotubes, SWCNTs)时,首次发现了能够发出荧光的碳纳米粒子,但其荧光量子产率很低,提纯困难。直到2006年,Sun等人 [2] 用激光消融碳靶物结合有机试剂钝化的方法,制备出了荧光性能较好的碳纳米粒子,并首次称其为FCN (Carbon Dots, CDs)。FCN作为新型的荧光碳纳米材料,具有良好的发光性能与小尺寸特性,而且还具有很低的生物毒性与无光眨眼性质。因此,在细胞成像、标记及检测等领域有着良好的应用前景,是替代量子点和传统标记物的良好选择。
目前,FCN的合成方法包括自上而下 [3] [4] 和至下而上 [5] [6] 两类。自上而下的方法包括:电弧放电法、激光灼烧法、电化学法、机械粉碎、球磨或化学氧化。自下而上的方法包括:灰烬的氧化或腐蚀法、热解有机物法、微波合成法、超声法及掺杂法等。荧光材料的光学性能是其各种应用的基础,本论文以高温热解谷氨酸钠得到的荧光碳纳米颗粒(Glu-FCN)为研究对象,而它的荧光性质目前还尚未研究过。本文首次针对Glu-FCN的荧光光谱、pH特性、时间稳定性以及荧光产率等荧光性质做出了非常细致地研究。
2. 实验
2.1. 试剂与仪器
试剂:无水乙醇、浓盐酸、氢氧化钠、硫酸皆为分析纯;谷氨酸钠(国药集团化学试剂有限公司,纯度99.28%);硫酸奎宁(国药集团化学试剂有限公司,纯度99%);Glu-FCN自制;去离子水用于整个试验过程。
仪器:高速冷冻离心机CR21GII (Hitachi);紫外–可见光分光光度计V-530 (日本分光株式会社);荧光光度计F-4500 (日立公司);868型pH/ISE测试仪(Orion);透射电子显微镜JEM-2100 (日本电子)。
2.2. 实验方法
2.2.1. Glu-Na的制备
如图1所示:称取2.0 g谷氨酸钠(Glu-Na)放入马弗炉中,N2保护下10℃/min升温至400℃,煅烧0.5 h。煅烧后将样品研磨充分,然后将得到的黑色粉末溶解于15 mL蒸馏水中,4℃ 10,000 rpm/min高速离心30 min,得上清液,即为含有FCN的水溶液。烘干后无水乙醇萃取,干燥,研磨,得到FCN粉末。
2.2.2. 硫酸奎宁参比溶液以及Glu-FCN溶液的配制
硫酸奎宁以0.050 mol·L−1硫酸溶液配成1.00 × 10−3 mol·L−1标准溶液,使用时以0.050 mol·L−1硫酸溶液适当稀释。Glu-FCN用去离子水配置成1.00 mg/mL的标准溶液,使用时适当稀释。
2.2.3. 测试方法
在25 mL容量瓶中,分别加入Glu-FCN溶液或硫酸奎宁溶液分别用蒸馏水和配置的硫酸溶液稀释至刻度,摇匀。用紫外–可见光分光光度计及荧光分光光度计分别扫描相应的光谱。为了准确计算荧光量子产率,在测量荧光光谱之前,首先用罗丹明B光量子计和散射光板对F-4500荧光分光光度计的激发光谱和发射光谱进行校正。
3. 结果和讨论
3.1. Glu-FCN在不同酸度下的荧光光谱与荧光强度
固定Glu-FCN溶液的浓度为1.00 mg/mL,改变pH值,测量Glu-Na稀溶液在不同酸度下的荧光光谱。稀释溶液到0.10 mg/mL,测试此溶液的基本荧光性质(bandpasses of slits: 2.5/5 nm)。图2中不带标记的黑
色实线为Glu-FCN的基本性质荧光光谱。可以看出荧光发射峰λEM位于391 nm,荧光最佳激发峰λEX位于338 nm处。图2中带标记的曲线为不同pH条件下Glu-FCN溶液在最佳激发波长338 nm处的荧光光谱。可以看出Glu-FCN在不同pH环境下的发射峰位置很稳定,基本没有变化。而发射峰的强度随着pH的不同而改变。这就表明了,Glu-FCN存在着一定的pH依耐性。从而,对不同pH下Glu-FCN溶液的荧光光谱发射峰强度做统计,并绘制处发射峰强度与环境pH的关系,得到图3。从图3中可以看出,在pH小于3.0或者pH大于12.0时荧光强度较弱;当pH在3.0到9.0之间时它的荧光强度最强。Glu-FCN的这项特性使它可以在大范围pH变化的环境中使用。
3.2. Glu-FCN的时间稳定性
取一定量Glu-FCN标准溶液稀释到0.30 mg/mL。将样品置于四面光石英比色皿中,用荧光分光光度计进行荧光时间扫描(Time-scan, response: 0.5 s, bandpasses of slits: 2.5/5 nm),得到图4。从图4中可以看
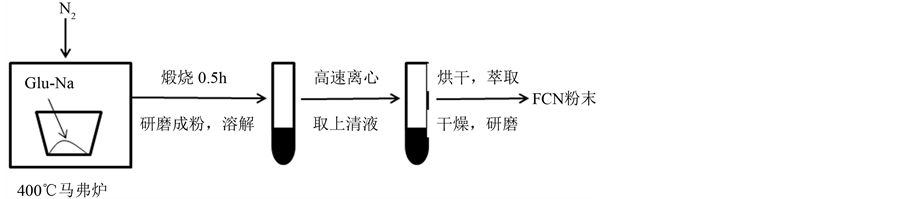
Figure 1. Preparation of Glu-FCN
图1. Glu-FCN的制备
 (带标记曲线为不同pH下的荧光光谱对应右边纵坐标,不带标记曲线为基本荧光性质光谱对应左边纵坐标)
(带标记曲线为不同pH下的荧光光谱对应右边纵坐标,不带标记曲线为基本荧光性质光谱对应左边纵坐标)
Figure 2. Fluorescence spectrum of Glu-FCN and those under different pHs
图2. 不同pH下Glu-FCN及其基本荧光性质荧光光谱

Figure 3. Relationship of the intensity at the Glu-FCN’s emission peak and pH
图3. 环境pH与Glu-FCN发射峰的强度关系图
出,Glu-FCN稀溶液在氙灯338 nm条件照射下连续照射,Glu-FCN的荧光强度基本没有变化,没有漂白和猝灭的现象。表明极其稳定。Glu-FCN的荧光稳定性极强,可以满足长时间实时的应用要求。
3.3. Glu-FCN稀溶液浓度与荧光强度的关系
在中性条件下,不同浓度的Glu-FCN稀溶液的荧光发射光谱见图5所示(bandpasses of slits: 5/5 nm)。从图中可以看出,Glu-FCN稀溶液浓度越大相应的荧光发射峰越高,荧光强度越强。统计不同浓度下Glu-FCN稀溶液的发射峰强度,可以得出图6。从图6中可以看出,在一定浓度范围内(0.2~50 μg/mL) Glu-FCN稀溶液浓度与发射峰荧光强度呈良好的线性关系,回归直线的相关系数为0.9982。超出了最大值,由于荧光物质自吸收和浓度效应的影响,线性关系不佳;低于最小值时,F-4500荧光分光光度计检测效果不佳。发射峰的位置非常稳定,基本没有变化。
3.4. Glu-FCN荧光量子产率的测量
量子产率的定义是荧光物质吸光后发射的光子数与吸收的激发光的光子数之比。它是衡量一种荧光
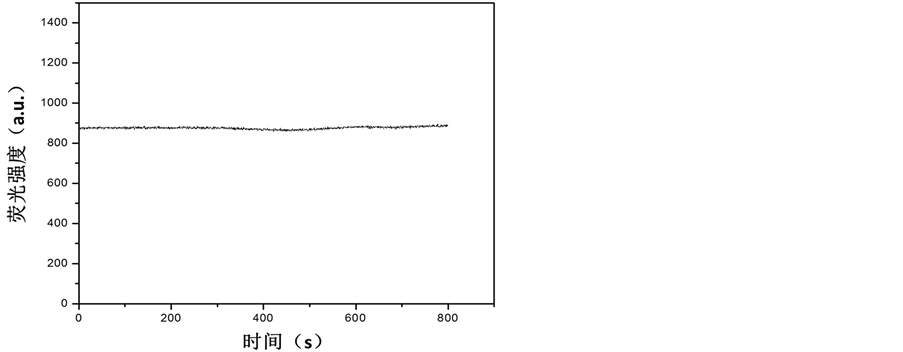
Figure 4. Fluorescence stability of Glu-FCN irradiated with 338 nm xenon lamp
图4. Glu-FCN在氙灯338 nm照射下光稳定性测试
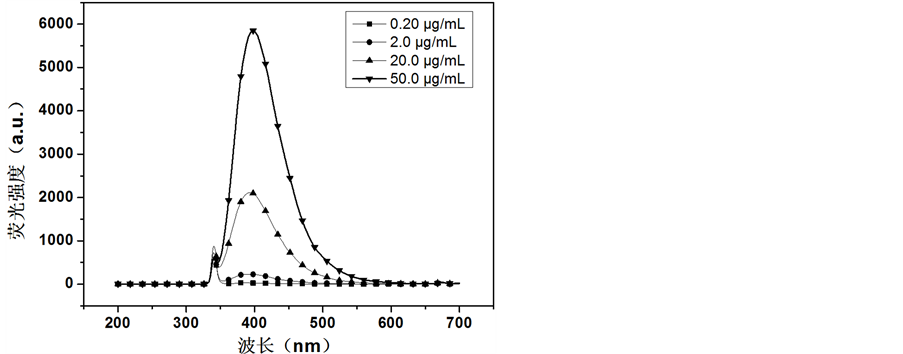
Figure 5. Fluorescence spectra of Glu-FCN with different concentrations
图5. 不同浓度Glu-FCN稀溶液的荧光光谱
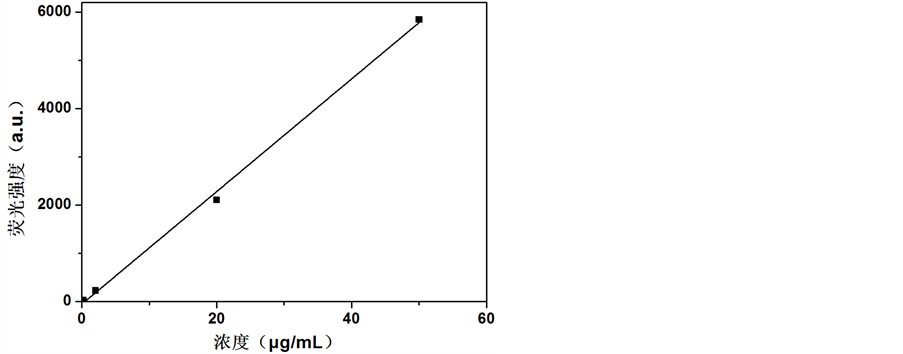
Figure 6. Diagram of different concentration of Glu-FCN and intensity of emission peak
图6. Glu-FCN稀溶液浓度与发射峰荧光强度的关系
物质荧光效率的重要指标,表示物质的荧光发射特性。量子产率的高低直接影响FCN的性能优劣。它的数值通常小于1,QY值越大,则该物质荧光越强。选用硫酸奎宁作为参比物质,然后测量FCN溶液和参比物质溶液在相同激发波长下的荧光发射峰面积和该激发波长对应的吸光度。然后按照以下公式(1)计算量子产率: [7] [8]
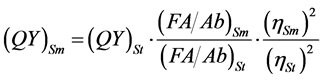 (1)
(1)
其中,FA表示荧光发射峰面积,Ab表示激发波长下的吸光度,QY表示量子产率。下标sm表示样品,st表示参比物质,η代表溶液的折射率。由于此浓度下硫酸奎宁溶液和FCN溶液的折射率都接近水的折射率,因此大致相等。
将一定量的硫酸奎宁溶解于配制好的浓度为0.05 mol/L硫酸中制备成一定浓度的标准硫酸奎宁溶液,作为标准参比物质。然后,测量FCN溶液和硫酸奎宁溶液在对应激发波长下的吸光度,分别用去离子水和硫酸溶液稀释直至这两种溶液在对应的波长下吸光度都小于0.05 (吸光度要小于0.05,以防止溶液“自吸收”带来的影响)如图7所示。接着测量上述FCN溶液和硫酸奎宁溶液在一定激发波长313 nm和338 nm下的荧光强度,并得到荧光峰半峰高积分面积,各样品荧光曲线如图8所示。以在激发波长313 nm下硫酸奎宁的荧光量子产率0.55为标准,按照式(1)计算得FCN溶液和硫酸奎宁的荧光量子产率,列于表1。由表1可知:338 nm激发波长下Glu-FCN的荧光量子产率为51.5%。
3.5. Glu-FCN的TEM表征
使用了高分辨率的TEM对Glu-FCN进行了表征,结果如图9所示,可见,Glu-FCN颗粒呈规整的晶格纹分布,颗粒尺寸均匀。
4. 结论
本论文通过以高温热解谷氨酸钠得到的荧光碳纳米颗粒(Glu-FCN)为实验对象。通过对Glu-FCN荧光光谱、pH依耐性、时间稳定性以及荧光量子产率的研究,得出Glu-FCN荧光性质非常优异。一方面,Glu-FCN的发射峰半峰宽较窄,单色性较好;环境pH和自身浓度均不影响发射峰位置;发光强度高。
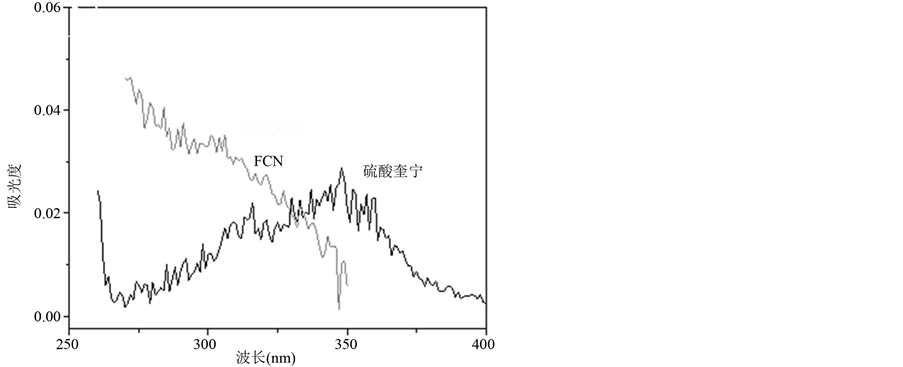
Figure 7. Absorption spectra of quinine sulfate and FCN (CFCN: 53 µg/mL, CQS: 2 × 10−6 mol/L)
图7. 硫酸奎宁和FCN溶液吸收光谱(CFCN: 53 µg/mL, CQS: 2 × 10−6 mol/L)
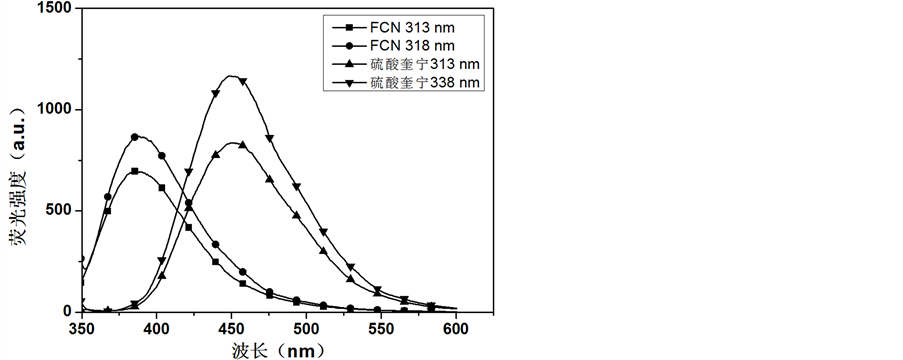
Figure 8. Fluorescence spectrum of FCN and quinine sulfate under different excitation wavelengths (CFCN: 53 µg/mL, CQS: 2 × 10−6 mol/L)
图8. FCN与硫酸奎宁溶液在不同波长下激发的荧光光谱(CFCN: 53 µg/mL, CQS: 2 × 10−6 mol/L)

Figure 9. TEM image of FCN
图9. FCN的高分辨率TEM图
Table 1. Photo-quantum yield of Glu-FCN and quinine sulfate
表1. Glu-FCN和硫酸奎宁荧光量子产率计算表
另一方面,Glu-FCN极其稳定,存在pH依赖性,可以弱酸弱碱的环境中稳定应用;荧光稳定性很高,不发生光漂白以及自猝灭。最后,对Glu-FCN荧光量子产率的计算表明其高达51.5%,说明Glu-FCN是一种强荧光碳纳米材料。Glu-FCN优异的荧光性质、极好稳定性、具备pH稳定性以及量子产率如此之高都更加证明了Glu-FCN具备作为荧光标记物使用的良好前景。
致谢
在论文完成之际,我要特别感谢我的指导老师周兴平老师的热情关怀和悉心指导。在我撰写论文的过程中,周老师倾注了大量的心血和汗水,无论是在论文的构思和资料的收集方面,还是在论文的研究方法以及成文定稿方面,我都得到了周老师悉心细致的教诲和无私的帮助,特别是他广博的学识、深厚的学术素养、严谨的治学精神和一丝不苟的工作作风使我终生受益,在此表示真诚地感谢和深深的谢意。在论文的写作过程中,也得到了许多同学的宝贵建议,同时还得到许多在工作过程中许多同事的支持和帮助,在此一并致以诚挚的谢意。感谢所有关心、支持、帮助过我的良师益友。最后,向在百忙中抽出时间对本文进行评审并提出宝贵意见的各位专家表示衷心地感谢!
文章引用
郑楠楠,楚险峰,潘立志,毕森林,丁 莎,周兴平. 谷氨酸钠碳纳米颗粒的荧光光谱及量子产率测定
Measurement of Fluorescence Spectra and Quantum Yield of Carbon Nanoparticles Made from Monosodium Glutamate[J]. 物理化学进展, 2016, 05(03): 75-82. http://dx.doi.org/10.12677/JAPC.2016.53008
参考文献 (References)
- 1. Xu, X.Y., Ray, R., Gu, Y.L., et al. (2004) Electrophoretic Analysis and Purification of Fluorescent Single-walled Carbon Nanotube Fragments. Journal of the American Chemical Society, 126, 12736-12737. http://dx.doi.org/10.1021/ja040082h
- 2. Sun, Y.P., Zhou, B., Lin, Y., et al. (2006) Quantum-sized Carbon Dots for Bright and Colorful Photoluminescence. Journal of the American Chemical Society, 128, 7756-7757. http://dx.doi.org/10.1021/ja062677d
- 3. Shi, Y.L. and Gao, Z.Q. (2014) Carbon Quantum Dots and their Applications. Chemical Society Reviews, 44, 362-381.
- 4. Jayasmita, J., Mainak, G. and Tarasankar, P. (2015) Intriguing Cysteine Induced Improvement of the Emissive Property of Carbon Dots with Sensing Applications. Physical Chemistry Chemical Physics (PCCP), 17, 2394-2403. http://dx.doi.org/10.1039/C4CP04982A
- 5. Liu, R.L., Wu, D.Q, Liu, S.H., et al. (2009) An Aqueous Route to Multi-color Photoluminescent Carbon Dots Using Silica Spheres as Carriers. Angewandte Chemie, 12, 4668-4671. http://dx.doi.org/10.1002/ange.200900652
- 6. Barman, M.K., Jana, B., Bhattacharyya, S., et al. (2014) Photophysical Properties of Doped Carbon Dots (N, P, and B) and Their Influence on Electron/Hole Transfer in Carbon Dots–Nickel (II) Phthalocyanine Conjugates. The Journal of Physical Chemistry C, 118, 20034-20041. http://dx.doi.org/10.1021/jp507080c
- 7. Wei, Y.J., Li, N. and Qin, S.J. (2004) Fluorescence Spectra and Fluorescence Quantum Yield of Sulfosalicylic Acid. Spectroscopy and Spectral Analysis, 24, 647-651.
- 8. Xu, M.H., He, G.L., Li, Z.H., He, F.J., Gao, F., Su, Y.J., et al. (2014) A Green Heterogeneous Synthesis of N-doped Carbon Dots and Their Photolumi-nescence Applications in solid and Aqueous States. Nanoscale, 6, 10307-10315. http://dx.doi.org/10.1039/C4NR02792B
