Water pollution and treatment
Vol.06 No.01(2018), Article ID:23587,8
pages
10.12677/WPT.2018.61011
Study on Adsorption of Heavy Metal Ions by Citron Peel Activated Carbon
Yuyang Xu1, Peirong Qi2, Shifeng Wang2
1Guangdong Meixian Dongshan High School, Meizhou Guangdong
2Technological and Higher Education Institute of Hong Kong, New Territories Hong Kong

Received: Dec. 23rd, 2017; accepted: Jan. 22nd, 2018; published: Jan. 29th, 2018

ABSTRACT
This paper uses agricultural waste grapefruit skin as raw material to prepare activated carbon (PC-AC), which was successfully used as an adsorbent for removal of Mn(II) ion in waste water. This work investigates the best adsorption conditions, and fits the corresponding kinetic and thermodynamic models. From the results, adsorption capacity of adsorbent (PC-AC) for Mn(II) depends on the initial concentration of manganese ion, the amount of adsorbent, the adsorption temperature, and the adsorption time. Activated carbon adsorption dynamics model accords with the second reaction kinetics model and the thermodynamic models follows Langmuir model. PC- AC as adsorption removes Mn(II) ion in waste water under relatively broad conditions, and the heavy metal wastewater needn’t pretreatment, which can effectively solves the problem of energy consumption.
Keywords:Manganese Ion-Containing Waste Water, Grapefruit Skin, Activated Carbon
柚子皮活性炭对重金属锰离子吸附的研究
徐宇炀1,祁佩荣2,王世锋2
1广东梅县东山中学,广东 梅州
2香港高等教育科技学院,香港 新界
收稿日期:2017年12月23日;录用日期:2018年1月22日;发布日期:2018年1月29日

摘 要
本文用农业废弃物柚子皮制备了一种柚子皮活性炭(PC-AC),并成功将其作为吸附剂用于去除废水中的Mn(II)离子。研究考察了最佳的吸附条件,并拟合其相应的动力学和热力学模型。结果表明,影响吸附剂(PC-AC)对于Mn(II)的吸附能力的因素包括锰离子的初始浓度,吸附剂投入量,吸附温度和吸附时间;活性炭吸附锰离子的动力学模型为二级反应动力学模型,热力学模型满足Langmuir吸附模型。柚子皮活性碳能够在较为广泛的条件下吸附重金属锰离子,且对重金属废水无需进行预处理,能够有效解决能耗问题。
关键词 :含锰离子废水,柚子皮,活性炭

Copyright © 2018 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
近年来,中国经济持续中高速发展的同时,水污染问题频繁出现,严重影响人们的生活质量和生活品质。工业废水中含有大量的重金属离子,如果处理不当,会造成严重的污染事故。从环境污染角度来说,重金属主要包括汞、镉、铅等毒性显著的重金属元素,也指具有一定毒性的一般重金属,如锌、铜、钴、锰等。重金属污染的最大特点是污水中的重金属在环境中降解困难,只能被迁移,并且重金属容易在生物体内聚积。当重在生物体内积聚到一定量后就会使生物体致畸或导致突变,对人体健康和自然环境都会产生大量危害。毫无疑问,重金属是否超标与人们身心健康息息相关 [1] 。
目前处理水体重金属污染的方法主要有化学法:中和沉淀法、硫化物沉淀法、铁氧化沉淀法和钡盐沉淀法等;物理化学法:离子交换法、吸附法、膜分离技术、吸附法和溶剂萃取法等;生物化学法:生物絮凝法、生物吸附法和植物修复法 [2] 。目前,吸附方法被认为是这些方法中过程最简单,成本较低且适合大规模废水处理的一种方法。常用到的吸附剂是活性炭、凹凸棒、浮石、整合树脂、麦饭石、蛇纹石、大洋多结合矿和硅藻土等。活性炭吸附法处理重金属离子可以无差别的除去各种重金属、节能和高效,同时活性炭来源广泛,种类繁多,产量大,因此在净化重金属废水领域有很大的潜力 [3] 。
柚子是我国主要水果之一,在南方许多地区大量种植。柚子皮占到全重的55%~54%。通常柚子皮未被利用就丢弃了,造成极大浪费。研究表明,柚皮表面白色絮状物中含有大量的孔隙和纤维素 [4] ,其纤维组织结构类似于椰子壳和玉米秸秆,可将其制备成一种具有较丰富的内部孔隙结构和较高的比表面积的优质活性炭。
这部分工作中,我们用农业废弃物柚子皮作为碳源,制备了活性炭,并将它用在含重金属的废水处理中。并对碳材料进行SEM,XRD表征。为了模拟活性炭吸附重金属离子的规律,实验室用模拟重金属废水为含锰离子的水溶液。
2. 实验
2.1. 样品制备
柚皮活性炭的制备:实验时将新鲜的柚子皮剪切成小块,用去离子水多次洗涤干净,然后在130℃温度下干燥24 h后,用粉碎机少量多次粉碎至100目以下,置于干燥器中备用。将粉碎后的柚子皮粉末在管式炉中氩气气氛下400℃煅烧0.5 h,再升温至800℃恒温5 h进行炭化。将炭化后的柚子皮粉末与KOH以质量比3:1的配比物理混合,在管式炉中氩气气氛下800℃活化1 h,得到柚子皮活性炭(PC-AC)。
2.2. 活性炭表征
柚皮活性炭(PC-AC)的结构通过X-射线衍射仪(XRD,Bruker D8 Advance X-射线衍射仪)测量,X射线源为Cu Kα辐射(λ = 1.5406 Å),电流电压分别为40 mA和40 mV,扫描角度范围20˚~90˚。柚皮活性炭(PC-AC)的微观形貌,采用扫面电子显微镜(SEM,Hitachi SU8010)表征,加速电压为0.5~30 kV。吸收过重金属离子的活性炭用X射线光谱仪(EDX,1800ROHS)测定锰元素的相对含量。
2.3. 吸附试验
模拟重金属废水的制备:称取一定量的氯化锰(MnCl2∙4H2O)作为模拟废水中的重金属离子源,用容量瓶准确配制一定浓度的含Mn离子的水溶液,作为模拟重金属离子废水。
研究PC-AC吸附锰离子的影响因素时,通过单因素的实验进行考察。实验时,用移液管移取50 ml一定浓度的Mn(II)溶液放入一组150 mL锥形瓶,加入相应质量的PC-AC,然后在不同温度条件下置于恒温振荡器中往复振荡。用抽滤法得到处理后的模拟废水滤液和吸附剂活性炭,用火焰原子吸收光度法(FAAS)测试剩余的滤液中离子的浓度。根据不同吸附条件,分别探索了锰离子的初始浓度,吸附剂投入量,吸附温度和吸附时间对PC-AC吸附锰离子的影响。
吸附量(qe,mg)由以下方程计算:
(1)
其中C0和Ce是金属离子的初始浓度及吸附后浓度(mg/L);V是模拟重金属离子溶液的体积(L);m是吸附剂的质量(g)。
Mn(II) 的去除率(Re%),由以下方程计算:
(2)
吸附实验的数据处理主要进行了一级反应动力学模型与二级反应动力学模型拟合。
一级反应动力学模型由以下方程计算:
(3)
二级反应动力学模型由以下方程计算:
(4)
(5)
采用Langmuir 方程和 Freundlich方程拟合柚子皮活性炭对废水中锰离子的等温吸附过程。
方程(6)为Langmuir模型方程,方程(7)为分离因子方程:
(6)
(7)
KL是朗格缪尔常数,表示吸附能量(L/mg);qmax表示重金属离子的最大吸附量。RL分离因子,值在0~1之间,表示吸附的难易程度。
Freundlich热力学模型,由以下方程计算:
(8)
KF与结合能有关 [5] 。
3. 结果与讨论
3.1. 吸附反应的影响因素
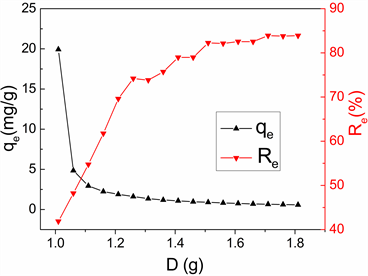
影响PC-AC活性炭吸附效果的因素很多,由图1(a)可知,随着吸附剂加入量的增加,锰离子的去除率逐渐上升。锰离子浓度一定时,去除率逐渐增加,吸附量逐渐降低。当PC-AC活性炭加入量为1.5 g时,吸附量qe和Mn(II)的去除率Re均趋于平衡,吸附达到饱和。这说明,吸附剂投入量加大可以增大可吸附比表面积,使吸附位点增加,锰离子与吸附剂的结合几率增大 [6] 。从图1(b)中可以看出,随着时间的延长,吸附量qe和Mn(II)的去除率Re逐渐增大。模拟废水中初始的锰离子含量一定,随着吸附反应的进行,空缺的吸附位点逐渐变少,Mn离子浓度逐渐变小,5 h以后,吸附量qe和Mn(II)的去除率Re
 (a)
(a)
 (b)
(b)
 (c)
(c)
 (d)
(d)
Figure 1. The influence factors on adsorption capacity: (a) the amount of adsorbent; (b) the adsorption time; (c) the adsorption temperature; (d) initial concentration of manganese ion
图1. (a) PC-AC投入量对Mn(II)吸附效果的影响;(b) 吸附时间对Mn(II)吸附效果的影响;(c) 温度对Mn(II)吸附效果的影响;(d) Mn(II)的起始浓度对吸附效果的影响
均趋于平衡,吸附达到平衡 [7] 。图1(c)为温度对吸附性能的影响,由图可知,吸附量qe和Mn(II)的去除率Re随温度的升高而增加,在35℃左右达到吸附最大值。继续升高温度,吸附量qe和Mn(II)的去除率Re均出现下降趋势。这是因为,Mn(II)的热运动随着温度的升高而增加,从而与PC-AC接触的机会增多。同时,由于吸附反应是放热反应,温度太高不利于吸附的进行,因此我们认为35℃为吸附最佳温度 [8] 。从图1(d)中可以看出随着Mn(II)初始浓度的增大吸附量增大,去除率减小。这是因为锰离子的增多使分子间碰撞加剧,从而使PC-AC更好的接触,但是由于PC-AC表面的吸附位点有限,因此浓度过高反而会使Mn(II) 的去除率Re降低 [9] 。
3.2. 吸附的动力学模型
为了更好地了解活性炭(PC-AC)的吸附过程,我们对吸附反应进行动力学计算,如图2所示。当温度一定时,增加模拟废水中重金属离子Mn(II)浓度,一级反应动力学模型中ln(qe − qt)随着吸附时间的延长逐渐下降,相关性系数为0.6448~0.8553。当模拟废水中重金属离子Mn(II)浓度一定时,增加反应温度,一级反应动力学模型中t/qt逐渐增加,相关性系数为0.7799~0.9522,因此活性炭(PC-AC)吸附重金属离子Mn(II)过程的动力学模型满足二级反应动力学模型 [10] [11] 。
3.3. 吸附的热力学模型
PC-AC活性炭吸附模拟废水中的锰离子的热力学模型分析,如图3所示。图3(a)为Langmuir吸附模型,随着Ce的增大,Ce/qe呈线性增长,同时,升高温度Ce/qe明显下降,郎格缪尔系数约为0.72~0.975。图3(b)为Freundlich模型,随着lnCe的增加,lnqe逐渐上升,并且随着温度的升高出现下降趋势,Freundlich系数为0.813~0.9395。从图中可以看出,2种等温模型都能够很好的描述柚皮粉末活性炭对锰离子的吸附,其线性相关系数均大于0.9。但Langmuir方程的线性相关系数更接近于 =1,能够更好的描述柚皮粉末活性炭对锰离子的吸附过程,结果表明PC-AC活性炭吸附模拟废水中的锰离子的吸附热力学的模型满足Langmuir模型 [10] [12] 。
3.4. PC-AC的结构与形貌
从图4(a)中PC-AC的SEM结果可以看出,在PC-AC活性炭表面存在大量的小颗粒凸起分布,并且存在丰富的孔道结构。这主要是来自于柚皮本身孔隙和纤维素碳化,其次,植物本身含有的微量金属盐
 (a)
(a) (b)
(b)
Figure 2. The corresponding kinetic (a) First order reaction kinetics model; (b) Second order reaction kinetics model
图2. (a) 一级反应动力学模型;(b) 二级反应动力学模型
 (a)
(a)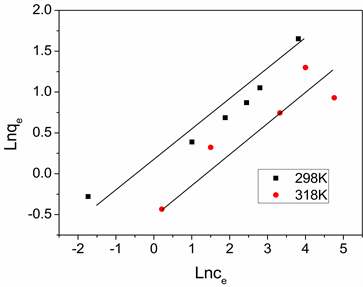 (b)
(b)
Figure 3. The thermodynamic models: (a) Langmuir model; (b) Freundlich model.
图3. (a) 吸附锰离子Langmuir吸附模型;(b) 吸附锰离子Freundlich模型

Figure 4. The results of SEM (a) and XRD (b) of PC-AC
图4. (a) PC-AC的SEM图;(b) PC-AC的XRD图
与KOH相互作用生成灰分,随着高温活化排出,达到造孔效果,增大了PC-AC活性炭的比表面积。PC-AC活性炭的较大比表面积可以增加活性炭表面的空缺吸附位点数量,微孔数量增多,可以增大PC-AC活性炭的吸附力。
PC-AC活性炭吸附模拟废水中重金属离子Mn(II)达到饱和以后,过滤,干燥。从图4(b)中可以看出,在吸附后的PC-AC活性炭XRD谱图中没有观察到明显的锰的化合物衍射峰,这主要是由于吸附锰离子进入孔道中,活性炭的衍射峰覆盖了微小的锰化合物衍射峰。也有可能是负载的锰化合物含量较少且尺寸太小,在吸附剂活性炭表面以无定型锰离子存在,超出XRD仪器检测范围,无法被扫描 [13] 。
为了更好地了解Mn(II)在活性炭表面的吸附状态,用PC-AC活性炭吸附模拟废水中重金属离子Mn(II),达到饱和以后,过滤,干燥。然后对得到的碳材料进行EDX分析。如图5所示,在AC/MnOx表面大量分布着C,O元素,并且在AC/MnOx材料表面观察到明显的Mn元素均匀分布。
4. 结论
本文利用碱活化法将农业废弃物柚子皮制成柚子皮活性炭(PC-AC),并成功将其用作吸附剂,用于吸

Figure 5. The results of (a) SEM of AC/MnOx; (b) EDX of C element; (c) EDX of O element; (d) EDX of Mn element
图5. (a) AC/MnOx的SEM图;(b) C元素的EDX扫描图;(c) O元素的EDX扫描图;(d) Mn元素的EDX扫描图
附工业废水中重金属离子。实验探索出最佳吸附Mn(II)的条件是温度为35℃、金属离子初始浓度为10 mg/L、吸附剂投加量为20 g/L、吸附饱和时间为5 h。PC-AC吸附锰离子的动力学模型为二级反应动力学模型,热力学模型满足Langmuir吸附模型。柚子皮活性碳由于较好的吸附性能可是使其作为吸附重金属废水中锰离子的优良吸附剂。柚子皮活性碳能够在较为广泛的条件下吸附重金属锰离子,且对重金属废水无需进行预处理,能够有效解决能耗问题。
文章引用
徐宇炀,祁佩荣,王世锋. 柚子皮活性炭对重金属锰离子吸附的研究
Study on Adsorption of Heavy Metal Ions by Citron Peel Activated Carbon[J]. 水污染及处理, 2018, 06(01): 87-94. http://dx.doi.org/10.12677/WPT.2018.61011
参考文献 (References)
- 1. 熊安晗, 莫文龙, 王君华, 等. 蛭石对模拟废水中镍离子的吸附研究[J]. 合成材料老化与应用, 2015, 44(3): 79-81.
- 2. Demiral, H., Demiral, İ., Tümsek, F., et al. (2008) Adsorption of Chromium (VI) from Aqueous Solution by Activated Carbon Derived from Olive Bagasse and Applicability of Different Adsorption Models. Chemical Engineering Journal, 144, 188-196.
https://doi.org/10.1016/j.cej.2008.01.020 - 3. Esfandiar, N., Nasernejad, B. and Ebadi, T. (2014) Removal of Mn(II) from Groundwater by Sugarcane Bagasse and Activated Carbon (a Comparative Study): Application of Response Surface Methodology (RSM). Journal of Industrial and Engineering Chemistry, 20, 3726-3736.
https://doi.org/10.1016/j.jiec.2013.12.072 - 4. 张军强, 李随勤. 柚子皮的利用研究[J]. 西部皮革, 2016, 38(8): 282.
- 5. Kumar, P.S., Ramalingam, S., Kirupha, S.D., et al. (2011) Adsorption Behavior of Nickel (II) onto Cashew Nut Shell: Equilibrium, Thermodynamics, Kinetics, Mechanism and Process Design. Chemical Engineering Journal, 167, 122-131.
https://doi.org/10.1016/j.cej.2010.12.010 - 6. Wang, J., Pan, K., He, Q., et al. (2013) Polyacrylonitrile/Polypyrrole Core/Shell Nanofiber Mat for the Removal of Hexavalent Chromium from Aqueous Solution. Journal of Hazardous Materials, 244-245, 121-129.
- 7. Chávez-Guajardo, A.E., Medina-Llamas, J.C., Maqueira, L., et al. (2015) Efficient Removal of Cr (VI) and Cu (II) Ions from Aqueous Media by Use of Polypyrrole/Maghemite and Polyaniline/Maghemite Magnetic Nanocomposites. Chemical Engineering Journal, 281, 26-36.
https://doi.org/10.1016/j.cej.2015.07.008 - 8. Swain, B., Mishra, C., Park, J.L., et al. (2015) Treatment of Indium-Tin-Oxide Etching Wastewater, Recovery of Semiconductor Grade Indium and Copper Nanopowder: A Commercial Hybrid Green Process. The Asia Pacific Conference on Sustainable Energy & Environmental Technologies, July 2015, University of Seoul, Seoul.
- 9. Anirudhan, T.S. and Sreekumari, S.S. (2011) Adsorptive Removal of Heavy Metal Ions from Industrial Effluents Using Activated Carbon Derived from Waste Coconut Buttons. Journal of Environmental Sciences, 23, 1989-1998.
https://doi.org/10.1016/S1001-0742(10)60515-3 - 10. Dada, O.A., Adekola, F.A. and Odebunmi, E.O. (2015) Kinetics and Equilibrium Models for Sorption of Cu(II) onto a Novel Manganese Nano-Adsorbent. Journal of Dispersion Science and Technology, 37, 119-133.
https://doi.org/10.1080/01932691.2015.1034361 - 11. Shi, P. and Liu, C.-J. (2009) Characterization of Silica Supported Nickel Catalyst for Methanation with Improved Activity by Room Temperature Plasma Treatment. Catalysis Letters, 133, 112-118.
https://doi.org/10.1007/s10562-009-0163-0 - 12. Arulkumar, M., Thirumalai, K., Sathishkumar, P., et al. (2012) Rapid Removal of Chromium from Aqueous Solution Using Novel Prawn Shell Activated Carbon. Chemical Engineering Journal, 185-186, 178-186.
- 13. Liu, W., Zhang, J., Zhang, C., et al. (2012) Preparation and Evaluation of Activated Carbon-Based Iron-Containing Adsorbents for Enhanced Cr(VI) Removal: Mechanism Study. Chemical Engineering Journal, 189-190, 295-302.