Open Journal of Nature Science
Vol.04 No.03(2016), Article ID:18409,8
pages
10.12677/OJNS.2016.43040
Preparation of Titanium Nitride Film Electrode and Its Application for Determination of Dopamine
Linling Wang, Liyao Kong, Gang Wen, Fengming Zhao, Chun’an Ma*
College of Chemical Engineering, Zhejiang University of Technology, Hangzhou Zhejiang

Received: Aug. 4th, 2016; accepted: Aug. 23rd, 2016; published: Aug. 26th, 2016
Copyright © 2016 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
A roughened titanium nitride (TiN) film is fabricated on a polished Ti substrate through anodic oxidation process and subsequent nitridation in ammonia atmosphere. The composition and morphology were characterized by XRD, SEM and EDS. The results indicate that, after the nitriding process annealed at 850˚C, the surface of TiN film is of flower convex structure, with Ti2N and TiN as the main nitride phase, and the content of N element (Atom%) reached 32.14%. Experiments have conducted to explore the electrochemical behavior of dopamine (DA) at TiN film. It is found that TiN film has good electrocatalytic activity for dopamine. Chronoamperometry and differential pulse voltammetry (DPV) were used to determine the detection limit of DA in 0.1 M phosphate buffer solution. The detection limits by two methods were calculated to be 1.3 μM and 0.33 μM. And the detection limit of DA in the presence of 100 μM ascorbic acid was calculated to be 0.56 μM. Furthermore, TiN film exhibits a good repeatability with the relative standard deviation (RSD) of 3.97% for 5 parallel detections in 25 μM dopamine using a single TiN electrode, and the RSD of 4 new electrodes is 4.2%.
Keywords:Anodic Oxidation, Titanium Nitride, Dopamine, Detection

氮化钛膜电极的制备及对多巴胺的检测
王琳玲,孔丽瑶,闻刚,赵峰鸣,马淳安*
浙江工业大学化学工程学院,浙江 杭州

收稿日期:2016年8月4日;录用日期:2016年8月23日;发布日期:2016年8月26日

摘 要
采用阳极氧化法在抛光后的钛片表面制备了粗糙的TiO2膜电极,经氨气氮化还原后将前驱体TiO2转化为氮化钛(TiN)。XRD、SEM和EDS表征分析发现,850℃氮化处理后,氮化钛电极表面具有花状凸起结构,氮化钛的主要成分为Ti2N和TiN,N元素的含量达到了32.14%。实验研究了多巴胺在该电极的电化学行为,发现TiN电极对多巴胺有良好的电催化作用。在0.1 M磷酸缓冲溶液中,采用计时电流法和差分脉冲伏安法测定了TiN电极对多巴胺的检出限,分别为1.3 μM和0.33 μM。在100 μM抗坏血酸存在下,TiN电极对多巴胺的检出限为0.56 μM。TiN电极具有较好的重现性。单个电极对25 μM DA重复测定5次,相对标准偏差(RSD)为3.97%;新制的4根膜电极在含25 μM DA的溶液中测试所得的相对标准偏差为4.2%。
关键词 :阳极氧化,氮化钛,多巴胺,检测

1. 引言
多巴胺(4-(2-氨基乙基)-1,2-苯二酚,DA)是一种天然存在的儿茶酚胺,在哺乳动物体内作为一种重要的神经传递为物质,对中枢神经、荷尔蒙分泌及心血管系统具有重要意义 [1] [2] 。脑内多巴胺含量的失调可能直接引发人体的一些疾病,如导致帕金森氏症神经分裂症、社交恐惧症等 [3] [4] 。因此,多巴胺的定量检测具有重要的意义。当前,多巴胺的检测方法包括了色谱法 [5] 、化学发光法 [6] 、比色法 [7] 等,这些方法一般需要复杂的前处理过程。而电化学方法对检测物的响应速度快、灵敏度高,设备廉价且操作简单,在检测方面应用广泛。
氮化钛是一种过渡金属氮化物,具有良好的导电性、导热性和化学稳定性 [8] 。Carolina Nunes Kirchner等 [9] 指出氮化钛薄膜在电分析方面,特别是对可逆的氧化还原物质的检测占优势。目前,氮化钛已用于双氧水 [10] 、金属离子 [11] 、氯霉素 [12] 等电化学传感器的构建,而对多巴胺的电化学检测却鲜有报道。本文通过阳极氧化法和氨气氮化还原法 [13] [14] 在钛片表面制备了粗糙化的氮化钛电极。利用X射线衍射(XRD)、扫描电子显微镜(SEM)和能谱(EDS)对制备的氮化钛进行表征,循环伏安法探究多巴胺在TiN电极上的电化学行为,并以TiN电极为工作电极,采用计时电流法和差分脉冲伏安法(DPV)对DA进行检测分析。
2. 实验部分
2.1. 仪器和试剂
Vertex型IVIUM 电化学工作站(荷兰,IVIUM公司);X’ Pert PRO 型X射线衍射仪(荷兰PNAlytical公司);S-4700型电子扫描显微镜(日本Hitachi公司);Thermo Noran Vanstage ESI型能谱仪(美国Thermo Fisher Scientific公司);雷磁PHS-3C精密pH计(上海精密科学仪器有限公司)。
盐酸多巴胺(DA)、抗坏血酸(AA)购买于阿拉丁试剂公司。0.1 M磷酸缓冲溶液用0.1 M KH2PO4配置,并用H3PO4和KOH调节溶液pH,作为电化学测试的电解质溶液。实验所用试剂均为分析纯,所有用水均为二次去离子水。实验所用的DA溶液每日新配。
2.2. 氮化钛电极的制备
氮化钛(TiN)电极的制备主要分为2个过程。(1) 阳极氧化处理,制备TiO2薄膜电极。(2) 氨气氮化还原,将TiO2氮化生成TiN。实验将钛片(纯度>99.6%)化学抛光处理 [15] 后,在1.0 M H2SO4溶液中,20 V电压下阳极氧化1.5 h,制备TiO2薄膜电极 [16] 。而后将预先制备的TiO2电极放置在管式炉中,N2保护下,以10℃/min的升温速率升温至450℃,恒温1 h。而后更换气体,在NH3氛围中,以5℃/min的升温速率加热至850℃并恒温2 h进行氮化,制备TiNx电极。
TiO2在管式炉中经NH3高温氮化反应方程式如下:
 (1)
(1)
2.3. 测试方法
电化学测试采用三电极体系,以氮化钛电极为工作电极(10 mm × 10 mm),Pt片为辅助电极,Ag/AgCl(饱和KCl)电极为参比电极,室温下,在磷酸缓冲溶液中进行测试。将氮化钛电极在电解液中浸渍60 s后,在−0.3~0.8 V电位范围内,采用循环伏安法进行测试。计时电流法是在不断搅拌的磷酸缓冲溶液中,连续滴加一定浓度的多巴胺溶液,通过拟合响应电流与溶液中DA浓度的线性关系,计算其检测限。差分脉冲法是在0~0.8V电位范围内,对含一定浓度DA的缓冲溶液进行测试。测试条件是50 mV的脉冲宽度,200 ms的脉冲时间,扫描速率是20 mV/s。
3. 结果与讨论
3.1. 氮化钛电极的表征
实验对抛光处理后的钛片,阳极氧化制备的TiO2薄膜电极和氮化后的TiN电极进行SEM分析,结果如图1。
从图中可以看出,化学抛光处理后的Ti片(a)表面较为光滑。经阳极氧化处理制备的TiO2薄膜电极(b),表面呈现出凸起的向日葵状结构,这些颗粒状的凸起,大小不一,在一定层度上增大了电极的表面粗糙度。氮化处理后,TiN薄膜电极(c)的形貌较好地保留了其前驱体TiO2电极的形貌,表面花心部分的直径约有1.3 mm。图1(d)是TiN薄膜电极的EDS分析图。EDS分析发现,TiN薄膜电极表面的元素组成仅有Ti、N两种。其中N元素的含量达到了电极表面元素总量(Atom%)的32.14%。
图2是TiN膜电极的X射线衍射曲线。从图中可以看出,氮化钛电极表面氮化物的组成为Ti2N和TiN。其中,2θ等于34.66˚,39.28˚,51.06˚,61.03˚,64.26˚,67.31˚,73.13˚分别属于Ti2N (101),(111),(211),(002),(301),(311),(202)晶面。而位于42.77˚的衍射峰属于TiN(200)晶面的衍射。分析未发现属于钛的氧化物的衍射峰,这一结果与EDS分析结果相一致。说明,在850℃氮化2 h后,TiO2已经完全氮化,转化为了氮化钛。
3.2. DA在TiN电极上的电化学行为
图3是DA在TiN电极上的循环伏安图。从图中可以看出,TiN电极在不含DA的溶液中,循环伏安扫描不出现任何氧化还原峰,说明该电极在−0.3~0.8 V电位范围内相对稳定。当溶液中含有DA时,循环伏安扫描时出现了一对氧化还原峰。其氧化峰电位为0.56 V,氧化峰电流为60.9 μA,还原峰电位为−0.02 V,还原峰电流为44 μA,电位之差ΔEp = 0.58 V。循环伏安扫描结果表明DA在TiN膜电极上的氧化还原是一个不可逆的反应过程。

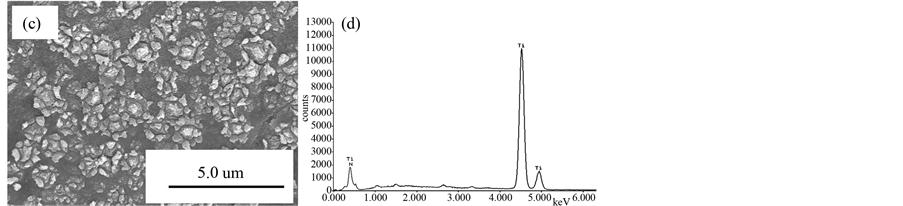
Figure 1. SEM images of polished Ti sheet (a), TiO2 film electrode (b), TiN film electrode (c), and EDS analysis of TiN film electrode (d)
图1. 抛光后的Ti(a),TiO2薄膜电极(b),TiN电极(c)的扫描电镜图以及TiN电极的能谱分析(d)

Figure 2. XRD pattern of TiN electrode
图2. TiN电极的XRD图形
图4是DA在TiN电极上,不同扫描速率下的循环伏安图。在扫描速率为10~150 mV/s范围内,DA的氧化峰电流(Ipa)和还原峰电流(Ipc)与扫速的二分之一次方(V1/2)成正比,线性方程:R = 0.9931 ,R = 0.9910。实验结果表明,DA在TiN电极上的电催化过程是扩散控制的。
溶液PH对电催化有较大的影响。实验发现,DA的氧化峰电位随着PH值增大而负向偏移。在PH3-7范围内,氧化峰电流随PH值增大表现为先增大后减小的趋势,在PH为6时氧化峰电流达到最大值,因此,我们选取缓冲溶液PH6.0作为后期实验的优化PH值。
3.3. TiN电极对DA的检测分析
采用计时电流法,在0.6 V外加电位,磁力搅拌下,连续滴加一定量的DA于缓冲溶液中,测定TiN

Figure 3. Cyclic voltammograms of TiN electrode in 0.1 M PBS (pH 6.0) containing 0 mM and 1.0 mM DA, respectively
图3. TiN电极在含0 mM和1.0 mM DA的PBS (pH 6.0)中的循环伏安曲线
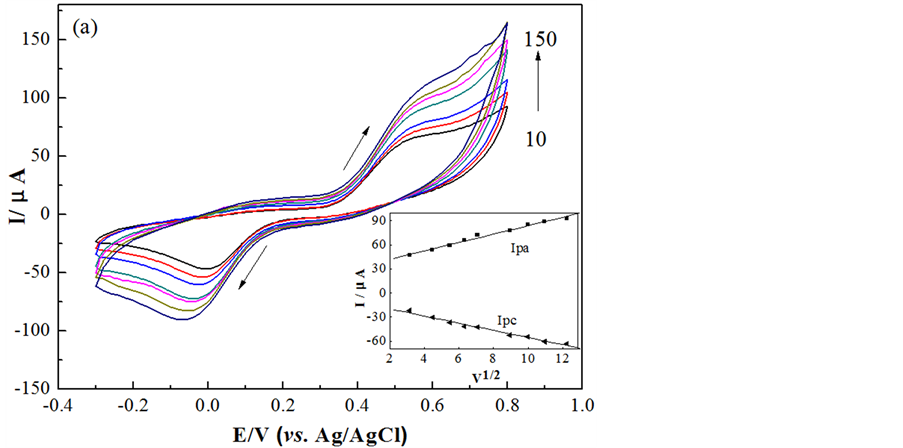
Figure 4. Cyclic voltammograms of TiN electrode in 0.1 M PBS (pH 6.0) and 1.0 mM DA with different scan rate
图4. 不同扫描速率下DA在TiN电极上的循环伏安曲线
电极对DA的响应曲线,结果如图5(a)。从图中可以看出,每次滴入DA,TiN膜电极的响应电流均会明显上升,且在5 s内达到稳定。在DA浓度为12.5~1128.8 μM范围内,DA浓度与响应电流呈现良好的线性关系(图4(a)插图),线性相关系数R = 0.9997。在信噪比为3的情况下(S/N = 3),计算可得其检测限(LOD)为1.3 μM。
差分脉冲伏安法(DPV)可以减小背景电流的影响,将法拉第电流放大。如图5(b),在DA浓度为1.0~47.8 μM范围内,TiN膜电极对DA的氧化峰电流与其浓度呈良好的线性关系(如插图所示),线性方程,线性相关系数R = 0.9937。在性噪比为3的情况下,计算得出检测限为0.33 μM。

Figure 5. (a) Amperometric response of TiN film electrode to the successive injection of DA in 0.1 M PBS (pH 6.0) under stirring. Insert: the calibration curve. (b) Differential pulse voltammetry (DPV) of TiN film electrode in 0.1 M PBS with different concentration of DA
图5. (a) 磁力搅拌下TiN膜电极在连续滴加DA的PBS中的安培响应曲线;(b) TiN膜电极在含不同浓度DA的缓冲溶液中(pH 6.0)的差分脉冲曲线
对比两种检测方法发现,采用计时电流法时,TiN电极对DA的灵敏度较高(0.0805 μA·μM−1)。但差分脉冲伏安法减小了背景电流的影响,在空白试样中测试所得的标准偏差较小,使得检测限较低。
3.4. 干扰和重现性分析
采用计时电流法,在PH6.0的磷酸缓冲溶液中依次加入的多巴胺(DA, 300 μM)、葡萄糖(Glucose, 500 μM)、抗坏血酸(AA, 500 μM)、双氧水(H2O2, 500 μM),探究TiN电极的抗干扰性能。如图6(A),加入DA后,TiN膜电极的响应电流明显上升;后继加入葡萄糖和双氧水后,响应电流没有明显的变化;加入抗坏血酸后,响应电流增大了12.90%。实验结果表明,TiN电极对葡萄糖和双氧水具有较好的抗干扰性能,而抗坏血酸对多巴胺的检测存在一定的干扰。
实验采用循环伏安法探究了抗坏血酸在TiN电极上的电化学行为。从图6(B)-a可以看出,TiN电极对抗坏血酸(浓度为500 μM)没有明显的电催化性能。对比仅有DA存在时的伏安曲线(b),在AA和DA(各500 μM)的混合溶液中,循环伏安扫描只出现一个氧化峰,而氧化峰电流有所增长,还原峰电流减小(c)。这可能是由于TiN电极对抗坏血酸没有直接的电化学氧化性能,但存在响应电流,而抗坏血酸本身的氧化性能使得多巴胺的还原受限,还原峰电流下降。实验采用线性扫描法,进一步探究了50μM DA存在下,不同浓度的抗化血酸(AA)对TiN膜电极电催化DA的影响,结果如表1所示。从表中可以看出,随着AA浓度的增大,TiN膜电极对反应体系的响应电流明显逐渐增大。在AA浓度为100 μM时,电流增长率达到了14.95%。
实验在100 μM AA存在下,探究了TiN膜电极对多巴胺的检测限,结果如图6(C)。在DA浓度为1.0~33.5 μM范围内,氧化峰电流与DA浓度的线性方程为,线性相关系数R = 0.9957,计算得出检测限为0.56 μM。对比相同测试条件下仅含DA的DPV测试结果(图5(b)),实验发现,在AA存在下,膜电极对DA的响应峰型很宽,根据Florian Ponzio [17] 关于氧化的多巴胺溶液的相关分析,我们推测这个峰型极有可能是电极的吸附作用造成的。抗坏血酸的氧化性使得DA的在电极表面的还原性能进一步减弱。在DPV扫描过程中生成了聚多巴胺并附着于电极表面,而聚多巴胺对溶液中的小分子具有吸附作用,当电极表面聚合的聚多巴胺覆盖率较大时,DPV扫描时出现了吸附峰。
重现性分析:单个TiN膜电极在含25 μM DA的缓冲溶液中,采用计时电流法重复测定5次,相对
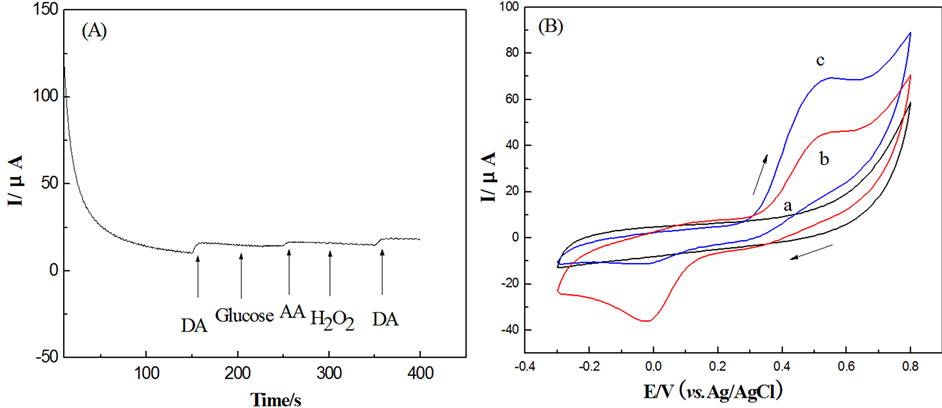
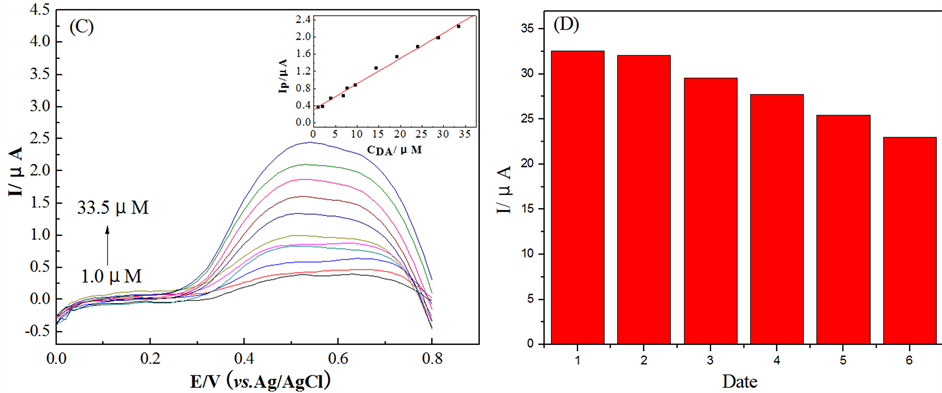
Figure 6. (A) Interference of glucose, AA and H2O2 to the detection of DA at TiN film electrode. (B) Cyclic voltammogram of TiN film electrode in the solution containing 500 μM AA(a), 500 μM DA(b) and 500 μM AA+DA(c), respectively. (C) DPV of TiN film electrode in 0.1 M PBS containing 100 μM AA with different concentration of DA (1.0, 2.0, 3.90, 5.8, 7.7, 9.6, 14.4, 19.2, 24.0, 28.8, 33.5 μM). (D) Current responses of successive 6 days tests in 100 μM DA
图6. (A) 葡萄糖、抗坏血酸、双氧水(浓度各为500 μM)对DA (300 μM)检测的干扰探究。(B) TiN电极在AA(a)、DA(b)和AA + DA混合溶液(浓度各为500 μM)中的循环伏安图。(C) TiN膜电极在100 μM AA存在下,不同DA浓度下的差分脉冲曲线。(D) TiN膜电极对100 μM DA连续6天的伏安响应电流
Table 1. Effects of response current for dopamine (50 mM) in the different concentration of ascorbic acid
表1. 不同浓度的抗坏血酸对多巴胺(50 μM)响应电流的影响
标准偏差(RSD)为3.97%;新制的4根膜电极在25 μM的DA溶液中进行测试,其相对标准偏差为4.2%。实验结果表明,TiN膜电极对DA的检测具有较好的重现性。
稳定性分析:采用循环伏安法,在DA浓度为100 μM的溶液中,连续测定6天(DA每天新配),响应峰电流的变化如图6(D)。从图中可以看出,TiN膜电极对DA的响应峰电流逐天下降。在测试的前3天,响应电流下降了9.3%。6天后,响应电流下降了29.5%。结果表明,TiN膜电极在应用后的前3天具有较好的稳定性。
4. 结论
本文通过阳极氧化法和氨气氮化还原法制备了粗糙化的TiN膜电极,并对其进行了表征分析。通过电化学测试发现TiN膜电极对多巴胺有较好的电催化活性。采用差分脉冲法测得TiN膜电极对多巴胺的检测限为0.33 μM,说明该电极在多巴胺检测方面具有一定的应用前景。
文章引用
王琳玲,孔丽瑶,闻 刚,赵峰鸣,马淳安. 氮化钛膜电极的制备及对多巴胺的检测
Preparation of Titanium Nitride Film Electrode and Its Application for Determination of Dopamine[J]. 自然科学, 2016, 04(03): 338-345. http://dx.doi.org/10.12677/OJNS.2016.43040
参考文献 (References)
- 1. Wang, C.Q., Du, J., Wang, H.W., et al. (2014) A Facile Electrochemical Sensor Based on Reduced Graphene Oxide and Au Nanoplates Modified Glassy Carbon Electrode for Simultaneous Detection of Ascorbic Acid, Dopamine and Uric Acid. Sensors Actuators B: Chemical, 204, 302-309. http://dx.doi.org/10.1016/j.snb.2014.07.077
- 2. Ye, F.Y., Feng, C.Q., Fu, N., et al. (2015) Application of Graphene Oxide/Lanthanum-Modified Carbon Paste Electrode for the Selective Determination of Dopamine. Applied Surface Science, 357, 1251-1259. http://dx.doi.org/10.1016/j.apsusc.2015.09.177
- 3. Yusoff, N., Pandikumar, A., Ramaraj, R., et al. (2015) Gold Nanoparticle Based Optical and Electrochemical Sensing of Dopamine. Microchimial Acta, 182, 2091-2114. http://dx.doi.org/10.1007/s00604-015-1609-2
- 4. 何凤云, 柳闽生, 朱子丰, 等. 多巴胺在氧化锌纳米棒嵌入石墨修饰电极上的电化学行为及测定[J]. 应用化学, 2011, 28(3): 320-325.
- 5. Tufi, S., Lamoree, M., de Boer, J., et al. (2015) Simultaneous Analysis of Multiple Neurotransmitters by Hydrophilic Interaction Liquid Chromatography Coupled to Tandem Mass Spectrometry. Journal of Chromatography A, 1395, 79-87. http://dx.doi.org/10.1016/j.chroma.2015.03.056
- 6. Stewart, A.J., Hendry, J. and Dennany, L. (2015) Whole Blood Electrochemiluminescent Detection of Dopamine. Analytical Chemistry, 87, 11847-11853. http://dx.doi.org/10.1021/acs.analchem.5b03345
- 7. Palanisamy, S., Zhang, X.H. and He, T. (2015) Fast, Sensitive and Selective Colorimetric Gold Bioassay for Dopamine Detection. Journal of Materials Chemistry B, 3, 6019-6025. http://dx.doi.org/10.1039/C5TB00495K
- 8. 于仁红, 蒋明学. TiN的性质, 用途及其粉末制备技术[J]. 耐火材料, 2005, 39(5): 386-389.
- 9. Kirchner, C.N., Hallmeier, K.H., Szargan, R., et al. (2007) Evaluation of Thin Film Titanium Nitride Electrodes for Electroanalytical Applications. Electroanalysis, 19, 1023-1031. http://dx.doi.org/10.1002/elan.200703832
- 10. Xie, Z., Liu, X.X., Wang, W.P., et al. (2014) Fabrication of TiN Nanostructure as a Hydrogen Peroxide Sensor by Oblique Angle Deposition. Nanoscale Research Letters, 9, 105. http://dx.doi.org/10.1186/1556-276X-9-105
- 11. 普勖琳, 王立平, 肖丹. 基于氮化钛的银离子选择电极的研制[J]. 化学传感器, 2004, 24(3): 23-25.
- 12. Kong, F.Y., Chen, T.T., Wang, J.Y., et al. (2016) UV-Assisted Synthesis of Tetrapods-Like Titanium Nitride-Reduced Graphene Oxide Nanohybrids for Electrochemical Determination of Chloramphenicol. Sensors and Actuators B, 225, 298-304. http://dx.doi.org/10.1016/j.snb.2015.11.041
- 13. Kamiya, K. and Nishijima, T. (1990) Nitridation of the Sol-Gel-Derived Titanium Oxide Films by Heating in Ammonia Gas. Journal of American Ceramic Society, 73, 2750-2752. http://dx.doi.org/10.1111/j.1151-2916.1990.tb06758.x
- 14. Wang, G.Q. and Liu, S.M. (2015) Porous Titanium Nitride Microspheres on Ti Substrate as a Novel Counter Electrode for Dye-Sensitized Solar Cells. Materials Letters, 161, 294-296. http://dx.doi.org/10.1016/j.matlet.2015.08.110
- 15. 张霄炎, 骆小平, 张洁. 钛(TA2)化学抛光工艺的实验研究[J]. 口腔材料器械杂志, 2005, 14(2): 69-72.
- 16. 马淳安, 赵峰鸣. 一种Ti/TiO2膜电极原位化学制备方法[P]. 中国专利, 200820122146. 2009-04-15.
- 17. Ponzio, F. and Ball, V. (2014) Persistence of Dopamine and Small Oxidation Products There of Inoxygenated Dopamine Solutions and in “Polydopamine” Films. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 443, 540-543. http://dx.doi.org/10.1016/j.colsurfa.2013.12.027
