Material Sciences
Vol.1 No.1(2011), Article ID:69,3 pages DOI:10.4236/ms.2011.11002
Preparation and Characterization of Triangle Silver Nanoparticles
1College of Physics and Electronic Information, Huaibei Normal University, Huaibei
2Suzhou Institute of Nano-Tech and Nano-Bionics, Chinese Academy of Sciences, Suzhou
Email:daikai940@163.com; lhlu2007@sinano.ac.cn
Received: Feb. 28th, 2011; revised: Mar. 6th, 2011; accepted: Mar. 21st, 2011.
ABSTRACT:
Triangle silver (Ag) nanoparticles have been successfully prepared by an easy and large scale productive liquid phase reduction method. The nanosize silver particles were characterized by using transmission electron microscopy (TEM), Selected-area electron diffraction (SAED), UV-Vis absorption spectroscopy and X-ray diffraction (XRD). The results show that the nanosize silver particles produced by this method are pure and spherical with uniform and narrow-dispersed size distribution, the length of a side is about 60 - 100 nm. The growth mechanism of triangle Ag nanoparticles is discussed at last.
Keywords: Triangle; Silver; Preparation; Characterization
三角形纳米银粒子的制备及其表征
代 凯1*,朱光平1,刘忠良1,刘亲壮1,芦露华2*,陈 征2
1淮北师范大学物电学院,淮北
2中国科学院苏州纳米技术与纳米仿生研究所,苏州
Email:daikai940@163.com; lhlu2007@sinano.ac.cn
摘 要:
采用简单液相还原法制备出三角形纳米银粒子。利用透射电子显微镜,选区电子衍射,紫外-可见吸收光谱和X射线衍射对纳米银粒子进行表征。结果表明,该法制备的三角形纳米银粒子杂质含量低,粒度分布集中,颗粒均匀一致,边长约为60~100 nm。最后对三角形纳米银的生长机理进行了探讨。
收稿日期:2011年2月28日;修回日期:2011年3月6日;录用日期:2011年3月21日
关键词:三角形;银;制备;表征
1. 引言
纳米材料具有一些特殊的性质,如小尺寸效应、表面效应、量子尺寸效应和宏观量子隧道效应等,它在催化、医药、电学、磁介质及新材料方面有着广阔的应用前景[1-3]。而贵金属纳米材料因其在微电子学领域的潜在应用前景及其特有的光电磁和催化特性一直是纳米材料科学领域的热点之一[4,5]。其中的纳米银粒子由于高的传热导电性、耐腐蚀性和抗氧化性,可用于照相制版、建筑材料、润滑剂、光吸收材料、涂料、传感器、表面增强拉曼光谱的基质及多种反应的催化剂,并且在其表面等离子振荡吸收峰附近具有超快的非线性光学响应,因而是一种最有前途的贵金属材料,正在受到广泛的重视[6-8]。由于金属纳米材料的这些性质和应用强烈依赖于纳米颗粒的尺寸和形貌[9],通过控制纳米颗粒的尺寸和形貌可以使其物理和化学特性可控可调,因此对纳米颗粒尺寸和形貌的控制研究非常有意义。本文采用及其简单的工艺方法制备出三角形结构纳米银,并用带电子衍射的透射电子显微镜(TEM)、X射线衍射(XRD)和紫外可见吸收光谱(UV-Vis)对所制得的纳米银粒子进行了表征。
2. 实验部分
2.1. 原料
硝酸银(分析纯,中国上海试剂一厂);
聚氧乙烯十二烷基醚(分析纯,国药集团化学试剂有限公司);
柠檬酸钠(分析纯,国药集团化学试剂有限公司);
硼氢化钠(分析纯,国药集团化学试剂有限公司);
无水乙醇(分析纯,上海凌峰化学试剂有限公司);去离子水(自制)。
2.2. 纳米银粒子的制备
0.1 mol/LAgNO3和0.15 mol/L柠檬酸钠充分混合后加入0.01 mol/L无水乙醇和0.25 mol/L聚氧乙烯十二烷基醚混合物强烈混合10 min,然后注入0.2 mol/L NaBH4搅拌5 min,放入避光水浴48 h后抽滤便制得所需样品。最后将样品置于40度真空环境中干燥,待用。
2.3. 表征方法
采用带选区电子衍射的日本JEM-200CX型透射电镜观察纳米银粒子形貌;
采用日本分光公司V-570紫外/可见分光光度计研究纳米银粒子的结构性能;
采用日本理学Rigaku D/maX-2400型X射线衍射仪(XRD)检测分析纳米银粒子的晶型结构。
3. 结果与讨论
3.1. 纳米银粒子的形貌分析
三角形纳米银粉的TEM图谱及选区电子衍射图谱如图1所示。从TEM图谱上可以发现纳米银粉几乎全部为等边三角形,且尺度分布较为均匀,边长在60~100 nm左右。从电子衍射图表明该样品的确为多晶纳米银颗粒。
3.2. 纳米银粒子的XRD分析
样品的XRD分析如图2所示,由图2可发现,纳米银的X射线衍射峰十分清晰,其结晶程度好,图中的(111),(200),(220)和(311)峰的出现同JCPDS标准卡片中编号为04-0783峰型完全一致,并结合图1中选区电子衍射谱图,因此可以断定产物是单质银,并且制备的纳米银为面心立方晶型结构。
3.3. 纳米银粒子的紫外——可见光谱分析
金属胶体在紫外可见光区有吸收带或者吸收区,

Figure 1. TEM and SAED images of Ag nanoparticle
图1. 纳米银粉的TEM图谱及选区电子衍射图谱
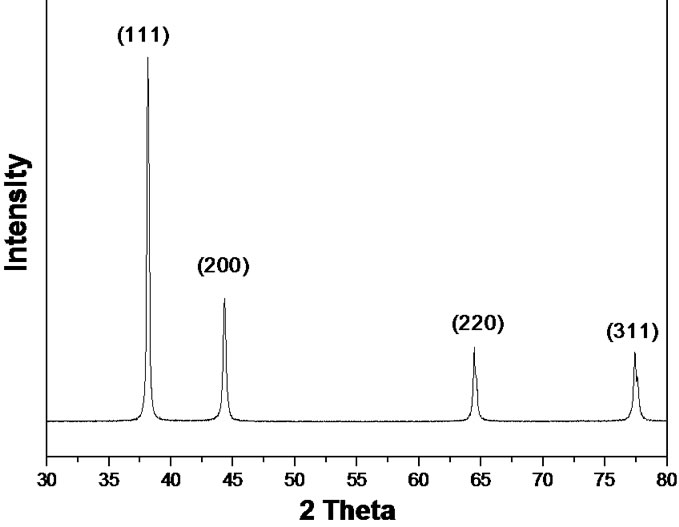
Figure 2. Powder X-ray diffraction (XRD) pattern of Ag nanoparticle
图2. 纳米银的XRD图谱
这是由于等离子共振激发或者带间跃迁形成的,由于银在可见区有着很强的吸收,因此观查银纳米结构的光学现象是非常有意义的[10,11],其吸收与粒子大小、形状和团聚状态有关。本实验制备的纳米银粒子的紫外—可见光谱如图3所示,从图3中可以发现纳米银的吸收峰在420波数左右的一段狭窄的波段内,因此认为该种方法制备的纳米银粒度均匀,纯度较高。
3.4. 生长机理探讨
在实验过程中,银原子通过硝酸银在乙醇溶液中被硼氢化钠还原而制得。反应分为3个阶段:(1) 预成核期(即诱导期);(2) 成核阶段;(3) 生长阶段。首先银柠檬酸钠诱导作用下形成晶核。然后随着反应的进行,溶液中Ag晶核数目不断增大,导致超过饱和浓度而进入过饱和状态。当达到成核浓度时,反应即由诱导期进入爆发式成核阶段,此阶段时间很短,随即
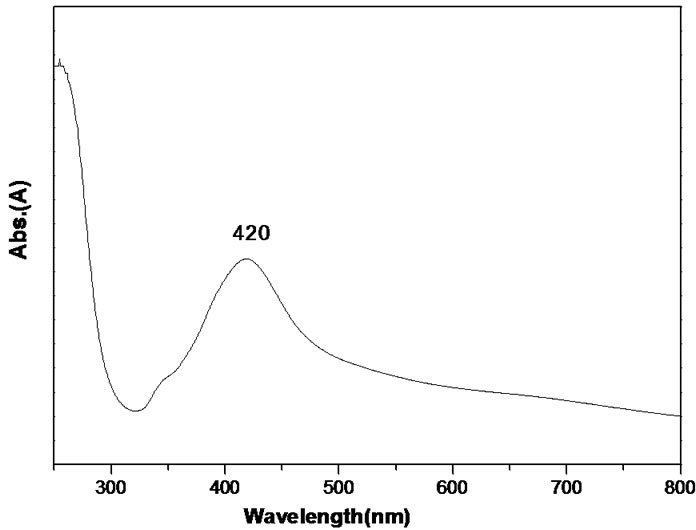
Figure 3. UV-vis absorption spectrum of Ag nanoparticle
图3. 纳米银的紫外——可见光谱吸收图谱
开始颗粒生长。乙醇溶液在本反应中作为一种溶剂,同时又作为一种较弱的还原剂,在柠檬酸钠、聚氧乙烯十二烷基醚作用下,以小银颗粒为“成核点”,硼氢化钠将硝酸银在小银颗粒上不断还原。其中,柠檬酸钠、聚氧乙烯十二烷基醚由于其结构有着特殊性,对纳米粒子生长起着非常重要的作用,起到配位、机械阻聚的作用,可以包覆颗粒表面防止所形成的银粒子发生团聚,从而控制银纳米粒的生长;另一方面柠檬酸钠、聚氧乙烯十二烷基醚共同作用使得银离子会选择性地吸附在特定的晶面上,导致这个晶面的生长速率慢于其它晶面,从而起到控制形貌的作用,最终形成了三角形纳米银结构。
4. 结论
用该法制备的纳米银性能稳定,在长时间放置不变色。利用透射电子显微镜,选区电子衍射,紫外–可见吸收光谱和X射线衍射等现代检测仪器测试表明该法制备的三角形纳米银粒子纯度较高,粒度分布集中,颗粒均匀一致,边长约为60~100 nm。最后通过机理研究解释了三角形纳米银的生长机理。
5. 致谢
该项目得到国家自然基金(编号:11004071,20803051),江苏省自然科学基金(编号:BK2010258),淮北师范大学校青年基金(编号:2011xqxm08)等资助,在此表示感谢!
参考文献 (References)
[1] Y. J. Kim, T. S. Shin, and H. D. Choi, et al. Electrical conductivity of chemically modified multiwalled carbon nanotube/epoxy composites. Carbon, 2005, 43(1): 23-30.
[2] M. Yu, H. H. Funke, and J. L. Falconer, et al. Gated ion transport through dense carbon nanotube membranes. Journal of the American Chemical Society, 2010, 132(24): 8285-8290.
[3] 代凯, 施利毅, 方建慧等. 导电胶粘剂的研究进展[J]. 材料导报, 2006, 20(3): 116-118.
[4] K. K. Hong, S. B. Cho, and J. S. You, et al. Mechanism for the formation of Ag crystallites in the Ag thick-film contacts of crystalline Si solar cells. Solar Energy Materials and Solar Cells, 2009, 93(6-7): 898-904.
[5] S. C. Wu, C. F. Chen, and W. C. Chao. Collective optical behavior in complementary wire arrays with Au nanoparticles. Microelectronic Engineering, 2005, 77(3-4): 277-284.
[6] Y. H. Kim, D. K. Lee, and Y. S. Kang. Synthesis and characterization of Ag and Ag–SiO2 nanoparticles. Colloids and Surfaces A: Physicochem. Eng. Aspects, 2005, 257-258(5): 273-276.
[7] R. B. Matthew, A. G. Antonio, and A. H. Steven. A comparison of silver ion to streptavidin coated microplates. Journal of Microbiological Methods, 2001, 44(2): 113-120.
[8] R. Z. Chen, D. S. Xu, and G. L. Guo, et al. Electrodeposition of thin films and single-crystalline nanowires of Ag7Te4 . Chemical Physics Letters, 2003, 377(1-2): 205-209.
[9] Q. Zhang, W. Y. Li, and C. Moran, et al. Seed-Mediated Synthesis of Ag Nanocubes with Controllable Edge Lengths in the Range of 30-200 nm and Comparison of Their Optical Properties. Journal the American Chemical Society, 2010, 132(32): 11372-11378.
[10] A. Filankembo, M. P. Pileni. Shape control of copper nanocrystals. Applied Surface Science, 2000, 164(1-4): 260-267.
[11] A. I. Lukman, B. Gong, and C. E. Marjo, et al. Facile synthesis, stabilization, and anti-bacterial performance of discrete Ag nanoparticles using Medicago sativa seed exudates. Journal of Colloid and Interface Science, 2011, 353(2): 433-444.