Advances in Clinical Medicine
Vol.
13
No.
11
(
2023
), Article ID:
75698
,
9
pages
10.12677/ACM.2023.13112536
尼妥珠联合放化疗治疗非小细胞肺癌的疗效和安全性的Meta分析
张超贻1*,戎彪学2#,李俏苒2,陈晨2,赵悦3,宋陈晨3,梁天赐3
1西安医学院研工部,陕西 西安
2西安医学院第一附属医院肿瘤内科,陕西 西安
3西安医学院第一附属医院心血管内科,陕西 西安
收稿日期:2023年10月21日;录用日期:2023年11月14日;发布日期:2023年11月21日

摘要
目的:系统评价尼妥珠联合放化疗对比单纯放化疗治疗非小细胞肺癌的疗效及安全性。方法:计算机检索中国期刊全文数据库(CNKI)、万方数据库、维普全文数据库(VIP)、PubMed、Medline、EMBase中关于尼妥珠联合放化疗对比单纯放化疗治疗非小细胞肺癌的随机对照试验(RCT),检索时限均从建库至2023年6月。由2名研究者按照纳入排除标准独立筛选文献、提取资料和质量评价后,采用RevMan5.4软件进行Meta分析。主要结局指标包括疾病控制率、客观缓解率、骨髓抑制、腹泻、皮疹、肝肾损伤,使用固定效应模型或随机效应模型计算具有95%置信区间的风险比。结果:纳入9个RCT,共838例患者。Meta分析结果显示,与单纯放化疗治疗非小细胞肺癌相比,尼妥珠联合放化疗可以提高非小细胞肺癌患者的疾病控制率[RR = 1.11, 95% CI (1.02, 1.20), P = 0.01]和客观缓解率[RR = 1.30, 95% CI (1.14, 1.49), P = 0.0001],在安全性方面,两组骨髓抑制、腹泻、皮疹、肝肾功能损伤,差异均无统计学意义(均P > 0.05)。结论:尼妥珠联合放化疗对非小细胞肺癌的治疗具有一定的优越性,可显著提高疾病控制率、客观缓解率,具有良好的安全性。由于纳入研究的质量和数量有限,降低了本系统评价的证据强度,故本系统评价的结论仅供临床实践和研究参考。
关键词
肺癌,非小细胞肺癌,尼妥珠,Meta分析

A Meta Analysis of the Efficacy and Safety of Nimotuzumab Combined with Radiotherapy or Chemotherapy in the Treatment of Non-Small Cell Lung Cancer
Chaoyi Zhang1*, Biaoxue Rong2#, Qiaoran Li2, Chen Chen2, Yue Zhao3, Chenchen Song3, Tianci Liang3
1Research and Engineering Department, Xi’an Medical University, Xi’an Shaanxi
2Department of Oncology, The First Affiliated Hospital of Xi’an Medical University, Xi’an Shaanxi
3Department of Cardiovascular Medicine, The First Affiliated Hospital of Xi’an Medical University, Xi’an Shaanxi
Received: Oct. 21st, 2023; accepted: Nov. 14th, 2023; published: Nov. 21st, 2023

ABSTRACT
Objective: To systematically evaluate the efficacy and safety of nimotuzumab combined with radiotherapy and chemotherapy compared to radiotherapy and chemotherapy alone in the treatment of non-small cell lung cancer. Methods: CNKI, Wanfang Database, VIP Database, PubMed, Medline and EMBase were searched by computer to collect randomized controlled studies on the comparing nimotuzumab combined with radiotherapy or chemotherapy to radiotherapy or chemotherapy alone in the treatment of non-small cell lung cancer. The search period was from the establishment of the databases to June 2023. Two researchers independently screened literature, extracted data, and evaluated quality based on inclusion and exclusion criteria, and conducted meta-analysis using RevMan5.4 software. The main outcome measures include disease control rate, objective response rate, bone marrow suppression, diarrhea, rash, liver and kidney injury, and the risk ratio with a 95% confidence interval was calculated using fixed or random effects models. Result: Nine RCTs were included, with a total of 838 patients. The meta-analysis results showed that compared with simple radiotherapy or chemotherapy for non-small cell lung cancer, the combination of nimotuzumab and radiotherapy or chemotherapy can improve the disease control rate [RR = 1.11, 95% CI (1.02, 1.20), P = 0.01] and objective response rate [RR = 1.30,95% CI (1.14, 1.49), P = 0.0001] in non-small cell lung cancer patients. In terms of safety, there was no statistically significant difference between the two groups in terms of bone marrow suppression, diarrhea, rash, and liver and kidney function damage (both P > 0.05). Conclusion: Nimotuzumab combined with radiotherapy or chemotherapy has certain advantages in the treatment of non-small cell lung cancer, which can significantly improve the disease control rate, objective response rate, and has good safety. Due to the limited quality and quantity of included studies, the evidence strength of this system evaluation has been reduced. Therefore, the conclusions of this system evaluation are only for clinical practice and research reference.
Keywords:Lung Cancer, Non-Small Cell Lung Cancer, Nimotuzumab, Meta-Analysis

Copyright © 2023 by author(s) and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY 4.0).
http://creativecommons.org/licenses/by/4.0/


1. 引言
在世界范围内,肺癌是癌症相关死亡的主要原因 [1] ,在中国,肺癌是发病率和死亡率较高的原发性癌症类型。由于缺乏典型临床表现,大多数非小细胞肺癌(NSCLC)患者错过了最佳治疗时机 [2] ,确诊时多为晚期,已失去手术机会,临床只能通过放化疗等方法延长患者生存期。但是,放化疗不良反应严重且效果并非十分理想。尼妥珠单抗是治疗恶性肿瘤的功能性单抗,是治疗头颈部恶性肿瘤的常见靶向药物,其能特异性结合表皮生长因子受体(EGFR),促进肿瘤细胞的凋亡 [3] 。近年来研究发现 [4] ,尼妥珠对肺癌也有效,但大多数研究结果存在差异。本文拟通过收集相关尼妥珠联合放化疗治疗NSCLC的随机对照试验(RCT),采用Meta分析的方法系统评价尼妥珠单抗治疗肺癌的有效性与安全性,供临床用药和研究参考。
2. 资料与方法
2.1. 纳入与排除标准
2.1.1. 研究类型
随机对照试验(RCT)。
2.1.2. 研究对象
纳入1) 经病理或细胞学检查证实的非小细胞肺癌患者;2) 肝肾功能及周围血象正常,无放化疗禁忌症;3) 不限制年龄与性别;4) 预期生存时间 ≥ 2个月;5) 至少有一个可测量的临床或影像学观察指标。排除1) 样本量过小;2) 非随机对照试验;3) 无可测量的临床或影像学指标。
2.1.3. 干预措施
试验组采用尼妥珠联合放化疗方案,对照组采用单纯放化疗方案。两组的其他辅助治疗措施完全相同。
2.1.4. 结局指标
1) 近期疗效:完全缓解率(CR)、部分缓解率(PR)、疾病控制率(DCR)、客观缓解率(ORR);2) 安全性指标:骨髓抑制、腹泻、皮疹、肝肾功能损害。
2.2. 检索策略
计算机检索中国期刊全文数据库(CNKI)、万方数据库、维普全文数据库(VIP)、PubMed、Medline、EMBase中关于尼妥珠联合放化疗对比单纯放化疗治疗非小细胞肺癌的随机对照试验(RCT),检索时限均从建库至2023年6月。中文检索词为“肺癌”、“肺肿瘤”、“非小细胞肺癌”、“尼妥珠”。英文检索词为“Lung Cancer”、“Lung Neoplasms”、“Nimotuzumab”。检索采用目标疾病与干预措施相结合的方式,并根据具体数据库调整检索词。
2.3. 文献筛选和资料提取
由2名研究者按照纳入排除标准独立筛选文献、提取资料并交叉核对,如遇分歧讨论或参考第三位研究者意见决定。提取数据主要内容包括:① 一般资料:标题、作者、出版日期;② 研究特征:研究对象的一般情况、基线可比性、各组患者的干预措施和疗效及不良反应评价标准;③ 结局指标。如报告不详或资料缺乏,则尝试通过邮件联系作者以进一步获取未发表数据。
2.4. 质量评价
采用Cochrane评价手册5.1.0提供的RCT方法学质量评价标准进行质量评价,评价内容包括① 具体随机分配方法;② 分配方案隐藏;③ 是否采用盲法;④ 结果数据的完整性;⑤ 选择性报告研究结果;⑥ 其他偏倚来源。质量评价由2位研究者独立进行并交叉核对,如遇分歧通过讨论或参考第三位研究者意见决定。
2.5. 统计学方法
采用Cochrane协作网提供的RevMan5.4软件进行Meta分析。计数资料采用相对危险度(RR)及其95% CI表示。各纳入研究结果间的异质性采用χ2检验。如各研究间有统计学和临床同质性(P > 0.1, I2 < 50%),则采用固定效应模型进行Meta分析;如各项研究结果间存在统计学异质性(P < 0.1, I2 ≥ 50%),则采用随机效应模型进行Meta分析。当数据变量存在异质性时,首先分析异质性产生的原因,并用敏感性分析处理,如果仍然无法消除异质性,若其具有临床一致性,则采用随机效应模型合并分析。
3. 结果
3.1. 文献检索结果
初筛获得286篇文献后,依次阅读摘要和全文进行筛选,获得15个RCT,进一步阅读全文,排除研究案例少、低质量研究及结局指标不完整,最终纳入9个RCT,其中英文文献4篇,中文文献5篇,共838例患者,文献筛选流程图见图1。
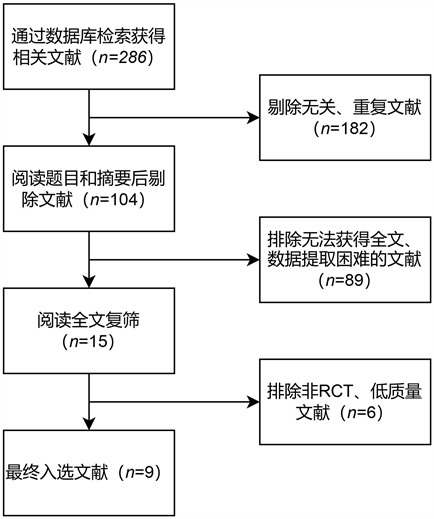
Figure 1. Results and process of literature screening
图1. 文献筛选结果及流程
3.2. 纳入研究的基本特征及质量评价
纳入的9个研究中患者均经病理诊断为NSCLC,其中实验组415例,对照组423例。文献发表时间为2012~2022年,所有纳入研究的基线均可比,纳入研究9篇文献的基本特征见表1;纳入研究的质量评价见表2。
Table 1. Basic features of the included literature
表1. 纳入文献的基本特征
NA,未提供;N,例数。
Table 2. Quality assessment of included studies
表2. 纳入文献的质量评价
3.3. Meta分析结果
3.3.1. 疾病控制率
7个研究报告了尼妥珠联合放化疗与单纯放化疗之间的疾病控制率,各研究间同质性较好(P = 0.32, I2 = 14%),采用固定效应模型进行Meta分析,结果显示尼妥珠联合放化疗组的疾病控制率显著高于单纯放化疗组,其差异具有统计学意义(RR = 1.11, 95% CI: 1.02~1.20, P = 0.01) (图2)。
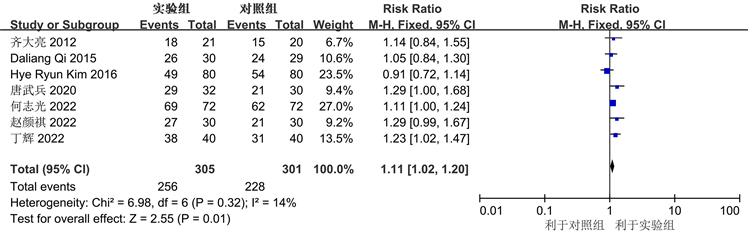
Figure 2. Forest plot comparing disease control rates between the two groups
图2. 两组疾病控制率比较的森林图
3.3.2. 客观缓解率
9个研究报告均报告了尼妥珠联合放化疗与单纯放化疗之间的客观缓解率,各研究间同质性较好(P = 0.32, I2 = 13%),采用固定效应模型进行Meta分析,结果显示尼妥珠联合放化疗组的客观缓解率显著高于单纯放化疗组,其差异具有统计学意义(RR = 1.30, 95% CI: 1.14~1.49, P = 0.0001) (图3)。
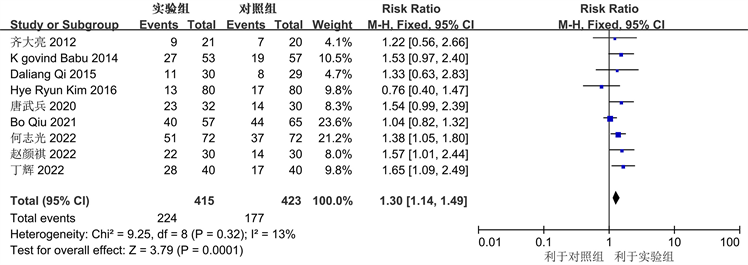
Figure 3. Forest plot comparing objective response rates between the two groups
图3. 两组客观缓解率比较的森林图
3.3.3. 不良反应发生率
分别对骨髓抑制、腹泻、皮疹、肝肾损等不良反应进行Meta分析(图4)。纳入的7个研究报道了骨髓抑制情况,各研究间同质性较好(P = 0.50, I2 = 0%),采用固定效应模型进行Meta分析,结果显示尼妥珠联合放化疗组与单纯放化疗组骨髓抑制发生率,其差异无统计学意义(RR = 1.10, 95% CI: 0.94~1.27, P = 0.24)。5项研究报告了腹泻情况,各研究间同质性较好(P = 0.72, I2 = 0%),采用固定效应模型进行Meta分析,结果显示尼妥珠联合放化疗组与单纯放化疗组的腹泻发生率差异无统计学意义(RR = 0.94, 95% CI: 0.74~1.20, P = 0.62)。5项研究报告了皮疹情况,各研究间同质性较好(P = 0.63, I2 = 0%),采用固定效应模型进行Meta分析,结果显示尼妥珠联合放化疗组与单纯放化疗组的皮疹发生率差异无统计学意义(RR = 1.20, 95% CI: 0.87~1.65, P = 0.27)。4项研究报告了肝肾损情况,各研究间同质性较好(P = 0.55, I2 = 0%),采用固定效应模型进行Meta分析,结果显示尼妥珠联合放化疗组与单纯放化疗组的肝肾损发生率差异无统计学意义(RR = 0.99, 95% CI: 0.65~1.50, P = 0.96)。
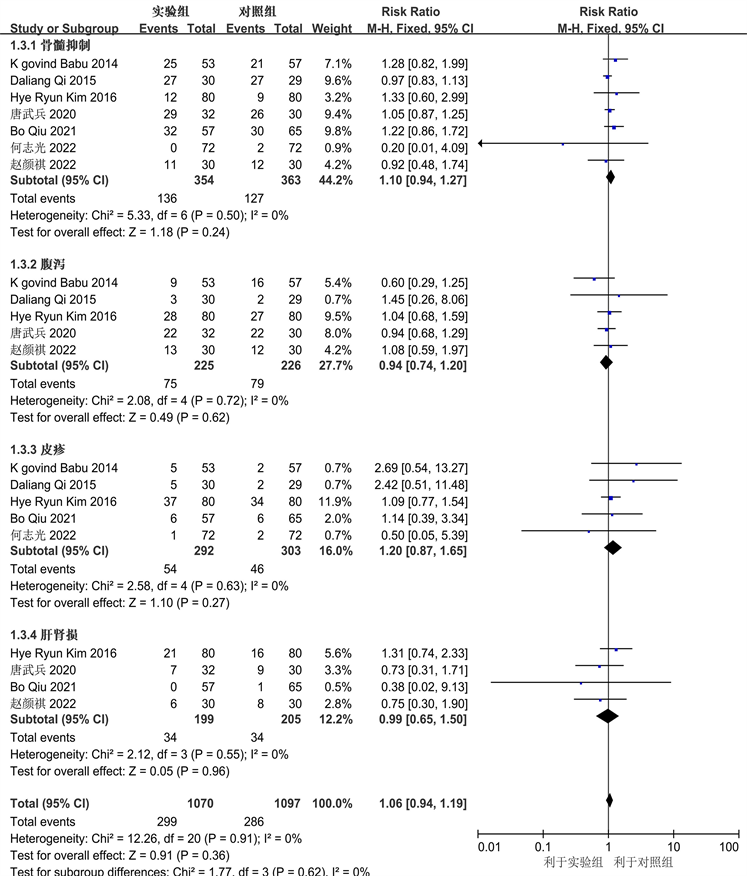
Figure 4. Forest plots comparing the incidence of adverse reactions between the two groups
图4. 两组不良反应发生率比较的森林图
3.4. 发表偏倚
在本研究中,客观缓解率在每项研究中均有报道,而其它指标报告不完整,因此我们以客观缓解率为指标,绘制漏斗图进行发表偏倚的定性评估,结果显示,两侧的分布大致对称,说明发表偏倚对研究结果的影响较低,见图5。
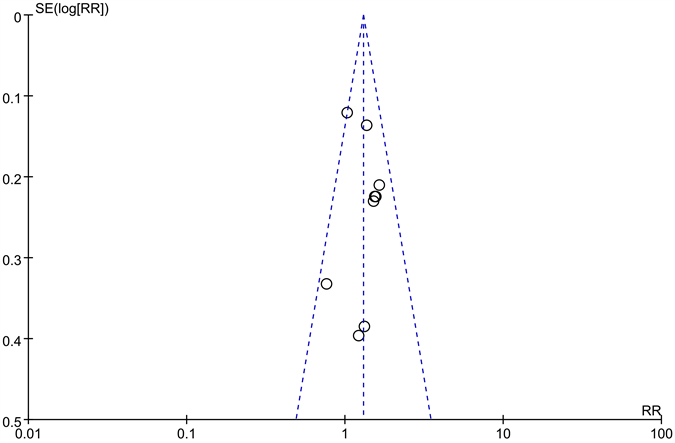
Figure 5. Funnel plots of objective response rates
图5. 客观缓解率的漏斗图
4. 讨论
NSCLC是肺癌最常见的组织类型,多数患者在确诊时已为晚期,此期患者可选择的治疗手段少,预后较差。因此,我们亟需寻找一种更为有效的治疗措施 [14] 。尼妥珠单抗是一种人源化抗EGFR单克隆抗体,能与有关配体和EGFR结合使得在非小细胞肺癌发生发展过程中发挥作用的EGFR受阻 [15] 。研究显示,使用尼妥珠单抗结合放化疗方式治疗非小细胞肺癌,不但可以通过阻碍EGFR的方式使得癌细胞恶性生物学行为得到抑制,而且可以增强肿瘤细胞对化疗药物的敏感性 [16] 。尼妥珠单抗具有半衰期长、高选择性等特点,其在多种实体肿瘤的治疗中已被证明可以提高抗肿瘤免疫力,且有着较高的组织特异性和抗肿瘤活性 [17] [18] [19] [20] 。目前尼妥珠单抗已被用于治疗鼻咽癌、结肠癌和宫颈癌等,均取得了一定的临床疗效,但尼妥珠单抗治疗非小细胞肺癌的临床证据相对缺乏。
本Meta分析结果显示:与单纯放化疗组相比,尼妥珠联合放化疗可以提高非小细胞肺癌患者的疾病控制率和客观缓解率。采取尼妥珠单抗联合放化疗治疗肺癌能产生较好的临床疗效,且患者耐受性好,两组间骨髓抑制、腹泻、皮疹、肝肾功能受损等无明显差异。各结局指标纳入研究间统计学异质性小,漏斗图示发表偏倚较小。
本研究的局限性包括:① 部分纳入文献质量不高,且样本量较小,部分研究结局指标差异无统计学意义;② 各临床试验之间的纳入排除标准和治疗措施不尽相同,存在一定的临床异质性,可能会对结果造成一定影响;③ 因缺乏充足的临床数据,无法对生活质量、长期疗效做出确定的评价;④ 纳入研究近期疗效评价标准不同,可能降低检验效能。综上所述,各种原因降低了本系统评价的证据强度,故本系统评价的结论仅供临床实践与研究参考。
综上所述,现有证据表明,尼妥珠单抗联合放化疗对非小细胞肺癌的治疗具有一定的优越性,可提高近期疗效,且具有良好的安全性,但尚缺乏长期疗效相关证据。
基金项目
陕西省科技计划(面上)项目(No. 2021JM-491);西安市科技计划项目(No. 20YXYJ0001-8)。
文章引用
张超贻,戎彪学,李俏苒,陈 晨,赵 悦,宋陈晨,梁天赐. 尼妥珠联合放化疗治疗非小细胞肺癌的疗效和安全性的Meta分析
A Meta Analysis of the Efficacy and Safety of Nimotuzumab Combined with Radiotherapy or Chemotherapy in the Treatment of Non-Small Cell Lung Cancer[J]. 临床医学进展, 2023, 13(11): 18058-18066. https://doi.org/10.12677/ACM.2023.13112536
参考文献
- 1. Leiter, A., Veluswamy, R.R. and Wisnivesky, J.P. (2023) The Global Burden of Lung Cancer: Current Status and Future Trends. Nature Reviews Clinical Oncology, 20, 624-639. https://doi.org/10.1038/s41571-023-00798-3
- 2. Chen, P., Liu, Y., Wen, Y., et al. (2022) Non-Small Cell Lung Cancer in China. Cancer Communications, 42, 937-970. https://doi.org/10.1002/cac2.12359
- 3. 郭宏果, 乔松, 程才, 等. 尼妥珠单抗联合同期放化疗治疗表皮生长因子受体阳性局部晚期非小细胞肺癌患者的疗效和安全性分析[J]. 癌症进展, 2023, 21(2): 166-168.
- 4. 肖聃. 尼妥珠单抗联合TP方案对Ⅲa-Ⅳ期非小细胞肺癌的疗效及免疫功能分析[J]. 中国药物与临床, 2021, 21(23): 3878-3880.
- 5. 齐大亮, 王华庆, 李燕, 等. 尼妥珠单抗联合紫杉醇脂质体和卡铂方案治疗晚期非小细胞肺癌的近期疗效与毒副反应[J]. 中华肿瘤杂志, 2012, 34(2): 152-155.
- 6. Babu, K.G., Prabhash, K., Vaid, A.K., et al. (2014) Nimotuzumab plus Chemotherapy versus Chemotherapy Alone in Advanced Non-Small-Cell Lung Cancer: A Multicenter, Randomized, Open-Label Phase II Study. OncoTargets and Therapy, 7, 1051-1060. https://doi.org/10.2147/OTT.S63168
- 7. Qi, D., Cui, Y., Wang, Q., et al. (2015) A Clinical Trial on Docetaxel and Carboplatin Therapy with or without Nimotuzumab for the Treatment of Advanced Nonsmall Cell Lung Cancer. Journal of Cancer Research and Therapeutics, 11, S32-S37. https://doi.org/10.4103/0973-1482.163836
- 8. Kim, H.R., Jang, J.S., Sun, J.M., et al. (2017) A Randomized, Phase II Study of Gefitinib Alone versus Nimotuzumab plus Gefitinib after Platinum-Based Chemotherapy in Advanced Non-Small Cell Lung Cancer (KCSG LU12-01). Oncotarget, 8, 15943-15951. https://doi.org/10.18632/oncotarget.13056
- 9. 唐武兵, 陈永发, 潘兴喜, 等. 尼妥珠单抗联合同期放化疗一线治疗局部晚期非小细胞肺癌临床观察[J]. 中华肿瘤防治杂志, 2020, 27(13): 1075-1080+1093.
- 10. Qiu, B., Wang, D.Q., Li, Q.W., et al. (2021) Concurrent Chemoradiation Therapy with or without Nimotuzumab in Locally Advanced Squamous Cell Lung Cancer: A Phase 2 Randomized Trial. International Journal of Radiation Oncology Biology Physics, 111, 917-925. https://doi.org/10.1016/j.ijrobp.2021.06.032
- 11. 何志光, 姜乐, 许学宗, 等. 尼妥珠单抗联合紫杉醇和卡铂对晚期肺癌患者免疫功能的影响[J]. 西北药学杂志, 2022, 37(6): 124-128.
- 12. 赵颜祺, 焦鹏飞. 尼妥珠单抗联合调强放疗及同期化疗一线治疗表达表皮生长因子受体局部晚期非小细胞肺癌的临床观察[J]. 肿瘤基础与临床, 2022, 35(5): 374-376.
- 13. 丁辉. 观察尼妥珠单抗靶向治疗联合常规化疗方案治疗晚期非小细胞肺癌的临床效果[J]. 新疆医学, 2022, 52(8): 904-906+956.
- 14. 马进元, 于鹏, 祝毓琳, 等. 晚期或转移性非小细胞肺癌全身治疗进展[J]. 中国实用内科杂志, 2013, 33(S1): 164-166.
- 15. 肖宇, 曹宝山, 梁莉. 尼妥珠单抗对不同化疗药物在肺癌PC9细胞中敏感性的影响及其机制[J]. 中国肺癌杂志, 2015, 18(2): 98-103.
- 16. 李文斌, 陈静, 赵艳杰, 等. 尼妥珠单抗联合术后同步放化疗治疗华人恶性胶质瘤的Ⅰ期临床试验[J]. 中国肿瘤临床, 2013, 40(23): 1455-1459.
- 17. 朱秋霞, 张振勇. 尼妥珠单抗联合多西他赛和顺铂一线治疗复发或转移性头颈部鳞癌疗效观察[J]. 肿瘤防治研究, 2021, 48(6): 631-634.
- 18. 陈杰, 曹元杰, 朱莉, 等. 尼妥珠单抗联合同步放化疗治疗局部晚期宫颈癌的临床观察[J]. 中华医学杂志, 2021, 101(8): 597-601.
- 19. Wang, L., Zhuang, H., Xu, X., et al. (2023) Efficacy and Survival Analysis of Nimotuzumab Combined with Concurrent Chemoradiotherapy in the Treatment of Locally Advanced Nasopharyngeal Carcinoma. Frontiers in Oncology, 13, Article ID: 1129649. https://doi.org/10.3389/fonc.2023.1129649
- 20. Teng, F., Cui, G., Qian, L., et al. (2023) Changes of T Lymphocyte Subsets in Peripheral Blood of Patients with Intermediate and Advanced Cervical Cancer before and after Nimotuzumab Combined with Chemoradiotherapy. International Archives of Allergy and Immu-nology, 184, 85-97. https://doi.org/10.1159/000525487
NOTES
*第一作者。
#通讯作者。
