Advances in Environmental Protection
Vol.
09
No.
03
(
2019
), Article ID:
30985
,
9
pages
10.12677/AEP.2019.93062
Preparation of Polydopamine/Sodium Alginate (SA-PDA) Gel Ball and Its Adsorption of Cu2+ in Water
Jianyi Tang, Niannian Yang, Lei Guo, Dinghao Zhai, Yafei Ren, Runzhen Wang*
School of Chemistry and Chemical Engineering, Shanghai University of Engineering Science, Shanghai

Received: June 5th, 2019; accepted: June 20th, 2019; published: June 27th, 2019

ABSTRACT
The poly-dopamine/sodium alginate gel ball was prepared for studying the adsorption efficiency of Cu2+ in water environment. It was observed that the adsorption process could be affected by pH, adsorption time and ionic strength. The characterization of the sample was conducted with Fourier Transform infrared spectroscopy (FTIR) test and scanning electron microscope (SEM) test, showing the best adsorption condition of the experiment: pH = 6, adsorption equilibrium time 1600 min. SA-PDA had a better adsorption efficiency than PDA under the same experiment condition. This process could be fitted much better with the pseudo-second-order reaction kinetics than that with the pseudo-first order, suggesting that the adsorption rate was dominated by chemical reaction. According to the R2 value of fitted Langmuir and Freundlich model, the monolayer adsorption was investigated and the maximum adsorption capacity of Cu2+ was 116.14 mg/g by SA-PDA, remarkably higher than that by the simple PDA (23.78 mg/g).
Keywords:Alginate, Poly-Dopamine, Adsorption, Cu2+
聚多巴胺/海藻酸钠(SA-PDA)凝胶球的制备 及其对水中Cu2+的吸附研究
唐健毅,杨念念,郭磊,忻丁豪,任亚飞,王润锴*
上海工程技术大学化学化工学院,上海

收稿日期:2019年6月5日;录用日期:2019年6月20日;发布日期:2019年6月27日

摘 要
本研究制备了聚多巴胺/海藻酸钠(SA-PDA)凝胶球,用以研究其在水环境中对Cu2+的吸附影响,分别考察了pH、吸附时间和离子强度对Cu2+的吸附效果。对样品进行了傅立叶变换红外线光谱(FTIR)测试和扫描电子显微镜(SEM)的表征观察。研究显示,实验最佳的吸附条件为:pH值为6,吸附平衡时间为1600 min。SA-PDA在同等实验条件下的吸附效果明显优于PDA。此过程更符合准二级动力学方程,表明该吸附速率是由化学反应速率控制。通过Langmuir和Freundlich吸附等温式拟合,计算出SA-PDA凝胶球对水中Cu2+的最大吸附量为116.14 mg/g,吸附行为单分子层吸附,显著高于相同条件下单纯PDA对Cu2+约23.78 mg/g的吸附量。
关键词 :海藻酸钠,聚多巴胺,吸附,Cu2+

Copyright © 2019 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
在水体环境中,铜元素通常以正二价的离子形态出现。近年来,随着科学技术的不断进步,冶金、电镀行业以及铜矿的开采会排放大量的含铜废水。而铜离子作为一种重金属离子,在自然界食物链的作用下,逐渐沉积在动植物的体内,并最终危害人体健康,破坏生态平衡。因此,在全球范围内,铜离子的消除研究持续受到关注。在现有技术下,较成熟的方法有沉淀法 [1] 、离子交换法 [2] 、萃取法 [3] 、吸附法 [4] 等。在吸附法中,常用的吸附剂有离子交换树脂、海藻酸钠 [5] 、活性炭 [6] 等。寻找新吸附材料的实验,也一直是研究热门。
海藻酸钠是一种天然生物大分子 [7] ,具有黏附性、生物相容性、可生物降解性等特性,被大量使用在生物技术、食品、载药等领域。多巴胺能在弱碱性的溶液中自聚,并最终被氧化成聚多巴胺,包覆于其他物质表面。聚多巴胺作为多巴胺的氧化聚合物,根据其丰富的基团,及亲水性、粘附性和生物相容性,人们已将其广泛应用于能源、环境、光电传感领域等 [8] 。
基于上述两种材料的特征,本研究将聚多巴胺与海藻酸钠混合,简单地制备出一种高效、亲环境、能高效吸附水体中Cu2+的全新材料。利用傅立叶变换红外线光谱仪及扫描电子显微镜对材料进行了表征,并对材料的吸附动力学、热力学及pH影响进行了研究。
2. 实验部分
2.1. 材料和仪器
2.2. 吸附剂的制备
2.2.1. 聚多巴胺球(PDA)的制备
将90 mL蒸馏水和40 mL无水乙醇混合,加入1 mL氨水(25%~28%),并缓慢搅拌30 min。随即加入10 mL 5% (w/v)的盐酸多巴胺溶液,于室温下反应36 h,可观察到混合液的颜色从无色变为棕色再至黑色。待反应结束后进行抽滤,用蒸馏水清洗5遍,置于80℃烘箱内真空干燥12 h。取出的深褐色产物即为聚多巴胺球,用玛瑙研钵研磨成粉末状以备后续之用。
Table 1. Message of experimental materials
表1. 实验材料信息
Table 2. Message of experimental apparatus
表2. 实验仪器信息
2.2.2. 聚多巴胺/海藻酸钠凝胶球(SA-PDA)的制备
配制100 mL 0.02% (W/V)海藻酸钠溶液,溶解后投入0.2 g的PDA球粉末,磁力搅拌后超声,使之均匀分散。采用直接滴加法,将上述海藻酸钠溶液逐滴加入250 mL 1% (w/v)氯化钙溶液中,在缓慢搅拌的条件下固化,持续2 h,得到SA-PDA黑色凝胶球。将产物用蒸馏水清洗若干遍,以除去剩余Ca2+,置于60℃烘箱中干燥待用。
2.3. 吸附实验
移取20 mL 50 mg/L的Cu2+溶液,加入0.01 g SA-PDA凝胶球,超声分散。根据实验需要,用0.1 mol/L NaOH或0.1 mol/L HCl调节pH值,室温下磁力搅拌3 h。随后离心分离,并取上清液,用电感耦合等离子体发射光谱仪(ICP-OES)测定溶液中剩余Cu2+的浓度,即可计算已吸附Cu2+的量Q。
可用如下公式计算SA-PDA对Cu2+的吸附量Q (mg/g):
(1)
其中,M为吸附剂的质量,g;C0表示Cu2+溶液的初始浓度,mg/L;Ct表示t时刻的Cu2+浓度,mg/L;V是溶液的体积,L。
3. 结果与讨论
3.1. SA-PDA凝胶球的表征
分析SA-PDA凝胶球的结构性能及其对铜离子的吸附影响,需对样品进行傅里叶红外光谱图(FTIR)和电子扫描显微镜(SEM)分析的表征。
3.1.1. 傅立叶红外光谱(FTIR)分析
图1为SA、PDA和SA-PDA的红外光谱图,主要特征峰归属如下:SA谱线中C=O对称和非对称伸缩振动出现在1608 cm−1和1430 cm−1,C-O和-OH的伸缩振动峰为1045 cm−1分别为3436 cm−1,2923 cm−1处归属为中C-H伸缩振动 [9] 。PDA谱线中,分子间氢键(O-H)伸缩振动或芳香族仲胺N-H伸缩振动引起3000~3500 cm−1之间的宽带 [10] ,1600 cm−1处和1511 cm−1处的吸收峰归属于苯环的伸缩振动和变形振动 [11] 。1280 cm−1处的峰则是由C-N弯曲振动所引起。
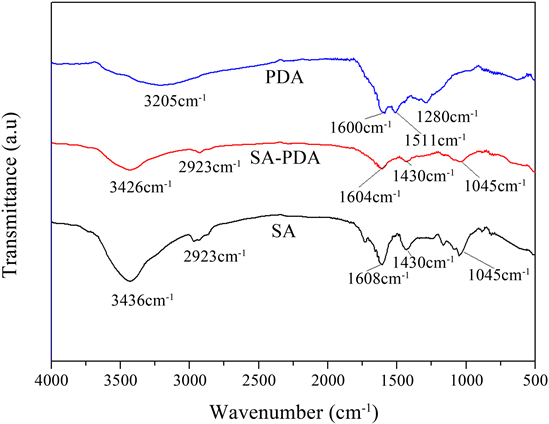
Figure 1. FT-IR spectra of SA, PDA and SA-PDA
图1. SA、PDA和SA-PDA的红外图谱
通过比较可观察到,在SA-PDA的红外光谱图中3426 cm−1、1430 cm−1、1045 cm−1以及1604 cm−1同时出现了SA和PDA两者的特征吸收峰,分别与之相似。故可做出判断,聚多巴胺成功包覆在海藻酸钠表面,经SEM测试可进一步辨别。
3.1.2. 电子扫描显微镜(SEM)分析
为确认SA-PDA的结构特征,经扫描电子显微镜测试,两者形态如图2清晰显示:聚多巴胺微球远小于海藻酸钠,粒径均一,约为40 nm,在海藻酸钠分子表面分散均匀,层叠聚集。结合傅立叶红外光谱(FTIR)分析,海藻酸钠已成功被聚多巴胺包覆。

Figure 2. The SEM images of the PDA (A and B) and SA-PDA (C and D)
图2. PDA球(A和B)及SA-PDA凝胶球(C和D)的扫描电镜图
3.2. 影响SA-PDA凝胶球吸附因素的考察
3.2.1. pH的影响
溶液的pH值在吸附实验中扮演着重要的角色,它会同时影响吸附剂表面带电情况、质子化程度,甚至可能改变重金属离子的存在状态 [12] 。在不同pH下,SA-PDA凝胶球对Cu2+的吸附量如图3所示。结果显示,吸附剂SA-PDA凝胶球对Cu2+的吸附能力随着pH的增大(2~6)而逐渐增大,在pH为6时达到最大吸附量97.46 mg/g。原理是低pH时吸附剂表面的质子化会阻碍吸附反应的进行;当pH逐渐升高,OH−离子增多,降低吸附剂表面的质子化率;且带有正电荷的Cu2+产生静电吸引,同时促进了SA-PDA凝胶球对Cu2+的吸附 [13] 。

Figure 3. Effect of pH on the adsorption of Cu2+
图3. pH对吸附Cu2+的影响
3.2.2. 吸附时间的影响
吸附时间对Cu2+有着重要的影响。如图4所示,考察了PDA和SA-PDA凝胶球在不同时间下对Cu2+的吸附影响。结果表明,PDA和SA-PDA凝胶球对Cu2+的吸附量均随着时间的增长而提升,并最终稳定在吸附平衡状态且SA-PDA的吸附量远远大于PDA。在吸附初始阶段,大量Cu2+易于同吸附剂的活性位点接触并被吸附;经过一段时间后位点饱和,吸附量几乎不再增大,可判断已达到吸附平衡。本实验条件下,经1600 min达到吸附平衡,吸附量为79.34 mg/g。
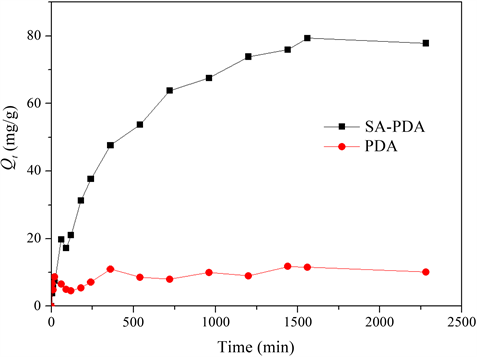
Figure 4. Effect of time on the adsorption of Cu2+ by PDA and SA-PDA
图4. 吸附时间对PDA和SA-PDA吸附Cu2+的影响
3.2.3. 离子浓度的影响
离子的存在对吸附量的影响不可忽视。采用NaCl溶液,在其浓度为0、0.01、0.05、0.1、0.5和1.0 mol/L的条件下,分别研究了SA-PDA凝胶球对Cu2+的吸附量,数据如图5所示。结果显示,当没有外部离子干扰时,能达到最大吸附量80.74 mg/g。

Figure 5. The effect of different ion concentrations on the adsorption of Cu2+ by PDA and SA-PDA
图5. 离子浓度对SA-PDA吸附Cu2+的影响
3.3. 吸附机理分析
3.3.1. 吸附动力学分析
依据准一级动力学方程和准二级动力学方程(颗粒间扩散的数学模型),考察SA-PDA凝胶球对Cu2+吸附动力学过程。分别对方程进行线性拟合,求得k。并通过比较相关系数(R2),确定方程的拟合效果。表3和图6显示,准二级动力学方程的R2较大,k较小。表明该实验条件下,液膜扩散不是控制吸附过程的唯一步骤 [14] 。吸附过程以化学吸附为基础,主要受活性位数量的影响,而非溶液浓度 [15] 。采用准二级动力学线性方程拟合曲线的R2更高,说明该吸附过程更符合准二级动力学方程。
Table 3. The parameters of adsorption kinetic equation
表3. 吸附动力学方程拟合参数

Figure 6. First order adsorption kinetics curve and second order adsorption kinetics curve
图6. 准一级吸附动力学曲线和准二级吸附动力学曲线
3.3.2. 吸附等温线分析
通过研究Langmuir和Freundlich两种吸附等温模型,确定SA-PDA凝胶球对Cu2+吸附曲线符合的类型。实验条件为室温,pH值为6,吸附时间为1600 min,离子强度为0。Langmuir吸附等温式假定,游离的分子被吸附于固体表面一定数目未被占据的吸附位。当分子在固体表面形成紧密吸附层时,即为吸附最大值(吸附上限) [16] 。Langmuir吸附等温式描述来理想吸附体系下,单层吸附平衡体系的吸附关系。Freundlich模型以Langmuir模型作为基础推导而来,描述非理想吸附体系下,单层吸附平衡体系下的吸附关系。由两个模型的拟合数据,如表4和图7所示,比较相关系数(R2),确定两者的拟合效果。
Table 4. Fitted results of Langmuir/Freundlich adsorption isotherm
表4. Langmuir和Freundlich吸附等温模型拟合结果

Figure 7. Langmuir/Freundlich adsorption isotherm
图7. Langmuir和Freundlich吸附等温模型
如表4中参数所示,Freundlich吸附等温模型更加准确得揭示了SA-PDA对水中Cu2+的吸附规律,表明该吸附过程为单分子层吸附过程。根据模型,显示了SA-PDA凝胶球对Cu2+的最大吸附量为116.14 mg/g,远大于PDA对Cu2+的吸附量(约23.78 mg/g)。
4. 结论
本研究成功制备了聚多巴胺/海藻酸钠(SA-PDA)凝胶球,相比于纯聚多巴胺(PDA)球,对水体中Cu2+的吸附能力明显提升。主要结论有:
1) SA-PDA凝胶球可作为一种新型吸附材料,其合成方法简便,安全无毒,稳定性好,具有可观的开发前景。
2) SA-PDA凝胶球最佳吸附条件为:pH值为6,吸附平衡时间为1600 min,离子强度为0。
3) SA-PDA凝胶球对水体中Cu2+吸附动力学过程更符合准二级动力学方程,以Freundlich吸附等温模型描述更加准确,属于单分子层吸附。
文章引用
唐健毅,杨念念,郭 磊,忻丁豪,任亚飞,王润锴. 聚多巴胺/海藻酸钠(SA-PDA)凝胶球的制备及其对水中Cu2+的吸附研究
Preparation of Polydopamine/Sodium Alginate (SA-PDA) Gel Ball and Its Adsorption of Cu2+ in Water[J]. 环境保护前沿, 2019, 09(03): 449-457. https://doi.org/10.12677/AEP.2019.93062
参考文献
- 1. 李新颖, Francis Ruzagiliza Innocent, 陈泉源, 薛罡. 沉淀法处理含铜废水及其沉淀产物的表征[J]. 化工环保, 2011, 31(4): 298-303.
- 2. 刘冰扬, 赵建民. 离子交换法处理含铜废水的实验研究[J]. 南京理工大学学报, 1995, 19(2): 184-188.
- 3. 刘利民, 曾立华, 肖国光. 液膜萃取法处理含铜废水的研究[J]. 矿冶工程, 2009, 29(5): 86-89.
- 4. 张剑波, 王维敬, 祝乐. 离子交换树脂对有机废水中铜离子的吸附[J]. 水处理技术, 2001, 27(1): 29-32.
- 5. 朱一民, 沈岩柏, 魏德洲. 海藻酸钠吸附铜离子的研究[J]. 东北大学学报, 2003, 24(6): 589-592.
- 6. 洪惠, 陈浩传, 姬海燕, 范晓丹. 活性炭对重金属离子的吸附研究[J]. 天津化工, 2013, 27(2): 1-3+7.
- 7. 李红兵. 海藻酸钠理化性质研究和特种品种制备[D]: [博士学位论文]. 天津: 天津大学, 2005.
- 8. 李晓燕, 徐强, 冯瑞雪, 张升晓, 罗浩, 韩富富. 基于聚合多巴胺的磁性碳材料的制备及其对甲基绿的吸附[J]. 环境科学学报, 2016, 36(11): 3986-3993.
- 9. 熊诚. 海藻酸钠的疏水改性及其在药物控释中的应用[D]: [硕士学位论文]. 无锡: 江南大学, 2008.
- 10. 乔丽英, 姚艳, 王勇, 赖宁, 王维朗. 纯镁表面聚多巴胺膜的制备及表征[J]. 华南理工大学学报(自然科学版), 2018, 46(7): 16-23.
- 11. 韩睿. 聚多巴胺基功能材料的制备与研究[D]: [硕士学位论文]. 上海: 上海师范大学, 2013.
- 12. Sari, A., Tuzen, M., Citak, D., et al. (2007) Equilibrium, Kinetic and Thermodynamic Studies of Adsorption of Pb (II) from Aqueous Solution onto Turkish Kaolinite Clay. Journal of Hazardous Materials, 149, 283-291. https://doi.org/10.1016/j.jhazmat.2007.03.078
- 13. 李鹏莉, 于树玲, 石家华. 聚多巴胺改性碳纳米管对Pb~(2+)的吸附性能[J]. 河南大学学报(自然科学版), 2014, 44(4): 416-420.
- 14. 骆欣, 杨怡心, 徐东耀, 阮金钊. 铝盐改性活性炭对水中Cr(VI)的吸附[J]. 工业安全与环保, 2019, 45(2): 69-72+82.
- 15. Dural, M.U., Cavas, L., Papageorgiou, S.K. and Katsaros, F.K. (2010) Methylene Blue Adsorption on Activated Carbon Prepared from Posidonia oceanica (L.) Dead Leaves: Kinetics and Equilibrium Studies. Chemical Engineering Journal, 168, 77-85. https://doi.org/10.1016/j.cej.2010.12.038
- 16. Langmuir, I. (1916) The Constitution and Fundamental Properties of Solids and Liquids. Part I. Solids. Journal of the American Chemical Society, 38, 2221-2295. https://doi.org/10.1021/ja02268a002
NOTES
*通讯作者。
