Nuclear Science and Technology
Vol.06 No.02(2018), Article ID:24510,8
pages
10.12677/NST.2018.62005
Preparation of Enriched Elemental B-10
Xiaofei Hu, Jing Zeng, Nanlin Xiao, Shilin Hu
Engineering Department of Special Materials, China Institute of Atomic Energy, Beijing

Received: Mar. 27th, 2018; accepted: Apr. 18th, 2018; published: Apr. 25th, 2018

ABSTRACT
Boron has a strong neutron absorption capacity as 10B has a larger neutron absorption cross-section. Enriched B-10 is widely used in radiation protection, fuel element manufacturing, neutron detection and other fields, which ensures it with a great research value. Due to the boron isotope separation process, the production of enriched B-10 isotope products requires the use of 10BF3 as a starting material. In this paper, we have compared the preparation method of natural abundance elemental boron, proposed several possible processes of preparing enriched elemental B-10, and analyzed the advantages and disadvantages of the various methods.
Keywords:Enriched Elemental B-10, Mg-Thermal Reduction, Fused Salt Electrolysis, Hydrogenous Reduction
富集B-10单质的制备
胡小飞,曾静,肖楠林,胡石林
中国原子能科学研究院,特种材料工程部,北京

收稿日期:2018年3月27日;录用日期:2018年4月18日;发布日期:2018年4月25日

摘 要
硼具有很强的中子吸收能力,这种能力来自于10B较大的中子吸收截面。富集B-10在辐射防护、燃料元件制造、中子探测等领域应用广泛,具有较大的研究价值。受限于硼同位素分离工艺,生产富集B-10同位素产品需要以10BF3为起始原料。本文主要结合天然丰度元素硼的制备方法,提出了制备富集B-10单质的工艺路线,并对制备富集10B单质硼的各种方法的优势和不足进行了分析和说明。
关键词 :富集10B,镁热还原,熔盐电解,氢气热还原

Copyright © 2018 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
硼具有10B和11B两种天然的同位素,其丰度分别为19.78%和80.22%。10B对热中子的吸收截面为3837靶,而11B仅为0.005靶,天然丰度的硼对热中子的吸收截面约为750靶,10B对热中子的吸收截面是自然丰度硼的5倍多。除了吸收截面大,与其它常见的中子吸收材料Gd和Cd等相比,10B还具有吸收频谱较宽,吸收后不产生γ射线,价格相对廉价,无毒不致癌等优点 [1] [2] [3] 。由于上述优点,B或者富集10B及其化合物被广泛应用于辐射防护、中子探测、军事装备及放射性治疗等领域 [4] [5] [6] [7] 。例如,富集10B可作为制造涂硼正比计数管的原料,用于中子探测领域 [8] ;在核工业,富集10B也可作为生产硼化锆的原料,涂敷在燃料芯块表面,以解决核电站初始运行阶段的过度反应性问题 [9] ;10B也可用于生产硼不锈钢,用作辐射屏蔽材料,在辐射防护领域发挥作用。总之,10B的用途广泛,制备富集10B的硼单质具有较大的研究价值。
要得到富集10B的元素硼,首先需要对B进行同位素分离。目前,硼同位素分离的方法有低温化学交换精馏法 [10] 、离子交换色谱法 [11] [12] [13] 、激光法 [14] [15] 等,在当前的科技水平下,上述方法中只有低温化学交换精馏能实现工业化大规模生产。化学交换精馏法分离硼同位素的原料通常有BF3-甲醚络合物、BF3-乙醚络合物、BF3-苯甲醚络合物等,在经过化学交换精馏后,10B以络合物的形式在气相中被富集,而11B则在液相中被富集。富集10BF3-醚的络合物通常需要在分解塔中进行裂解,以BF3-苯甲醚体系为例,分解塔顶部温度大于158℃、中部和底部温度为190℃时,分解效果最佳,得到的10BF3丰度可达92.5% [16] 。
受到硼同位素分离工艺的限制,目前,含富集10B的化工产品主要大都是由10BF3进行化学转化得到,因而,选择合适的工艺路线,是由10BF3制取富集10B硼粉的重点。天然丰度的硼粉的生产方法有金属热还原法、熔盐电解法、硼烷裂解法、氢气还原卤化硼等 [17] [18] [19] [20] [21] ,这些方法对于生产富集10B硼粉有一定的参考价值。上述方法和工艺对B粉的纯度、粒径、晶型有较大影响,其收率、成本和生产规模也有较大差异,这也是本文讨论的重点。
2. 制备路线
2.1. 金属热还原法
天然丰度的硼粉通常由金属热还原法制得,其主要原理为:以B2O3为硼源,以较活泼的金属,通常是Mg或Al,作为还原剂,将原料混合后在惰性气体的保护下放入高温炉中(700℃~900℃)发生强烈的氧化还原反应,从而得到硼粉。以镁热还原法为例,涉及的主要化学反应方程式为:
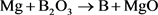 (1)
(1)
富集10B单质的制备也可以借鉴这种方法,但首先需要用10BF3制取10B2O3,目前,尚无以10BF3制取10B2O3的相关报道,参考核电用的富集硼-10硼酸的制取,可以先由10BF3制取H310BO3,在此方面,天津大学等单位取得了较多的研究成果,其由10BF3制取H310BO3的主要方法有机酯化法和无机水解法两种。有机酯化法 [22] 是指以甲醇作为反应介质,使三氟化硼与甲醇钠(或甲醇钙)反应,生成硼酸三甲酯,如图1所示;硼酸三甲酯极易水解,可在纯水中水解成硼酸和甲醇,此后通过降温结晶等手段即可以得到硼酸,该方法产品纯度 > 99.5%,收率可达95.2%。无机水解法是指在水相中,采用无机碳酸盐(碳酸
钙、碳酸锂)作为脱氟剂,将三氟化硼通入体系中,氟离子与钙离子或锂离子紧密结合生成难溶于水的氟化物,得到硼酸,反应,该方法产品纯度 > 99.2%,收率 > 95% [23] 。将得到的H310BO3脱水、造粒即可得到纯度大于99%的10B2O3。
在以10BF3制取10B2O3的基础上,采用金属热还原法可制取无定形的富集10B单质。目前,关于金属热还原法从B2O3制取无定形硼粉的研究较多,特别是以镁作为还原剂的镁热还原法,如图2所示。除了在惰性气体保护下将氧化硼和镁粉混合加热直接反应外,金属热还原法多用高能球磨机或者自蔓延反应装置进行。反应装置的不同对反应物的接触状态和反应体系温度分布等有较大影响,从而会影响产物的粒径和纯度。
1996年,黄菊林等 [24] 采用在惰性气体保护下将氧化硼和镁粉混合加热的方式制备了无定形硼粉,通过采用不同浓度的盐酸溶液加热浸取热还原产物、热分解镁等方式提高无定形硼粉的纯度。黄研究了不同反应物配比、保温时间、反应物粒度、热分解温度、热分解时间等条件对产物纯度的影响,所得到的无定形硼纯度的主要杂质相为Mg3(BO3)2,主要杂质元素为Mg (0.7%)、O (4%)和Fe (0.29%)等。
在黄菊林等人研究的基础上,伍继君等 [25] 采用自蔓延冶金法制备了无定形硼粉。自蔓延高温还原合成技术是在高真空或介质气氛中点燃原料,产生化学反应,化学反应放出的生成热使得临近的物料温度骤然升高,而引起新的化学反应并以燃烧波的形式蔓延至整个反应物,当然烧波推行前移的时候反应物变成生成物产品。B2O3和Mg反应是强烈放热的反应,与常规的镁热还原法相比,自蔓延高温合成在燃烧合成过程中,燃烧波的传递是呈层状的,使反应完的物料不与未反应的物料继续反应,从而大大避免了副反应生成硼镁化合物的可能性。采用这种方式,得到的硼粉纯度为94%,其平均粒径约为0.6 μm,还原过程中生成的酸不溶物MgB6、BxO、Mg2SiO4、FeB49是影响硼粉纯度的主要杂质。Zhihe Dou等 [26] 采用高能球磨法制备无定形硼,制备的无定形硼的粒径小于30 nm,具有很高的反应活性,其纯度为92.86%。2014年,彭超 [27] 等对自蔓延冶金法制备无定形棚粉中夹杂物及其去除机制进行了分析和研究,采用最优的酸浸工艺条件酸浸除杂后,制备出的高活性无定形硼粉中杂质镁含量仅为3.5%,平均粒径小于300 nm。
纯度较低是金属热还原法制备硼粉的最大缺点 [28] ,其中主要杂质元素为Mg和O;杂质的存在形式为未反应完全的B2O3、反应生成的MgO、副反应生成的MgB2、MgB4、MgB2O6等。采用自蔓延高温合成法,通过酸浸提纯,其纯度依然小于95%。造成金属热还原法制备的硼粉纯度较低的主要原因在于:所发生的化学反应为固-固反应,反应物难以混合均匀,导致局部发生副反应,生成的硼也不会脱离反应
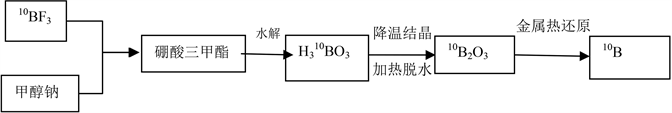
Figure 1. Preparation of 10B by indirect hydrolysis and magnesium thermal reduction
图1. 间接水解-镁热还原法制备10B的流程图
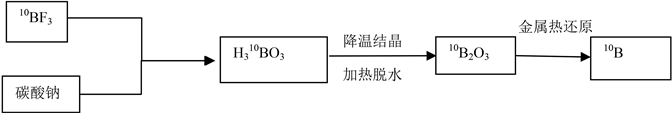
Figure 2. Preparation of 10B by direct hydrolysis and magnesium thermal reduction
图2. 直接水解-镁热还原法制备10B的流程图
体系,从而继续与镁反应生成MgB2、MgB4等副产物;Mg和B2O3的反应会放出巨大的热量,体系的温度难以控制,副反应难以避免。
提升产物纯度是金属热还原法制备硼粉的研究重点和难点,除改进反应装置和优化制备工艺条件外,考虑通过在粗硼中加入锌粉 [29] 等其它还原剂进行二次反应进行提纯也是一种思路。目前金属热还原法仍是生产天然丰度无定型硼的主要方法,其主要优点有工艺简单、能耗低、能大规模生产等。对于制备富集10B的无定型硼而言,由于硼同位素富集工艺的成本较高,保证硼的转化率对于制备富集10B单质的经济性有重大意义。镁热还原法首先需要制备10B2O3,其整个工艺流程较长,过程中硼的损失较多,这必将降低其经济性,且这种方法引入的杂质元素较多,难以满足一些尖端领域的要求,如何提高这种方法的经济性和产物纯度仍然需要继续研究。
2.2. 熔盐电解法
熔盐电解法也是制备天然丰度的单质硼的主要方法之一,其基本原理是通过电解含氧化硼或卤化硼的高温熔盐体系,硼在电解装置的阴极被还原,取出阴极产物,经过酸洗等处理后就可以得到无定型硼,如图3。1809年,Davy最早采用电解法制备元素硼 [30] 。两个世纪以来,对熔盐电解法制备元素硼的研究主要集中在:熔盐体系的选取、电解装置的优化、电解工艺的探索等方向。目前熔盐体系主要有氯盐体系(如NaCl-KCl-B2O3)、氟盐体系(如NaF-KF-KBF4-B2O3)、混合体系(如KF-KCl-KBF4-B2O3)等 [31] [32] [33] ,在选取电解体系时,通常需要从电解体系的融化温度、电导率、对硼前驱体的溶解度、腐蚀性弱等方面进行考虑。在电解装置上,最重要的是阴极、阳极和用于盛装熔盐的坩埚,电极和坩埚都需要具有很强的耐高温熔盐腐蚀的能力。阴极材料一般有硼棒、石墨、金属、导电陶瓷等;阳极材料通常为石墨,或者直接将石墨坩埚作为阳极;坩埚通常是石墨。电解工艺主要从电解温度、电流密度、电解时间等方面对电流效率、产物的纯度等产生影响。
与镁热还原法相比,熔盐电解法制得的硼的纯度较高,可达99.6% [34] ,其主要杂质元素通常为C、O、Fe等。其中,C主要来自于石墨坩埚、O来自于空气或未电解的氧化硼,Fe则主要来自于电极材料 [35] 。除了含有少量杂质元素以外,熔盐电解法在高温下进行,会产生BCl3、BF3等有毒气体,增加了操作难度的同时也降低了B的收率。由于持续电解会导致电解体系成分的改变,电解效率下降,副产物增多,因此如何实现连续生产也是这种方法需要解决的问题。随着材料领域的发展,一旦解决坩埚和电极材料的问题,并通过优化生产工艺实现连续生产,熔盐电解法必将成为制备高纯元素硼的最主要方法。

Figure 3. A schematic diagram of a device for preparing elemental boron by fused salt electrolysis
图3. 熔盐电解法制备元素硼的装置示意图
对于采用电解法制备10B而言,目前的思路有两种,一种是按前文所述的方法将10BF3先转化成10B2O3,以10B2O3作为前驱体再进行电解得到10B;另一种是将10BF3先转化为可用于电解的K10BF4进行电解,或直接向溶液体系中通入10BF3进行电解得到10B。其中第一种方法依旧存在工艺流程长,10B的收率低,经济性差的问题;第二种方法流程短,硼的收率高,经济性好,具有较大的研究价值。
2.3. 氢气还原卤化硼法
硼位于元素周期表中的第III主族,其化学性质与其同主族的其他元素相差较大,更接近于其对角线上的硅元素。目前,高纯多晶硅通常采用改良西门子法 [36] 生产,其主要过程是将粗硅用HCl气体氯化后产生三氯氢硅(SiHCl3),之后采用化学气相沉积法(CVD),利用氢气还原三氯氢硅,采用这种方法可以得到纯度高达99.9999999% (9N)。鉴于此,生产高纯元素硼也可能采取氢气还原卤化硼法进行。相较于金属热还原法和熔盐电解法,目前对于氢气还原卤化硼法制备高纯硼的研究较少,按照硼沉积位置分类,其大体可以分为热丝法、热管炉法;按照加热源,又可分为常规热源加热法、等离子体法 [37] 和激光法 [38] 等。
早在1959年,David [39] 就对氢气还原卤化硼法制备元素硼做了一些研究,其目的为制备纯度较高的晶体硼。David对采用H2还原三种卤化硼(BF3, BCl3, BBr3)的自由能进行分析,认为H2还原BBr3最容易发生,需要的温度较低,但考虑到经济性,由于BCl3最为廉价,David认为BCl3是三者中最理想的生产高纯硼的原料。其反应方程式为:
 (2)
(2)
David制取硼的方法为热丝法:将H2、BCl3、通入到容器中,用热丝(钼、钽、石墨、钛等)对体系进行加热,反应结束后取出热丝,收集热丝上附着的元素硼。热丝法制取硼过程中,热丝在高温下会渗入到硼中,造成硼纯度的降低,在上述几种热丝中,钛被认为是被认为是最佳材料,因为渗入到硼中的钛可以在300℃~350℃下用氯气除去,在此温度下,硼不与氯气发生反应。David采用热丝法制取的硼的纯度高达99%,但其产量较低,每小时仅能生产数克高纯硼。
2015年,Mary Anne White [40] 采用热管炉法用H2还原BCl3得到了ɑ-型晶体硼,其主要装置为石英管,石英管两端塞有石英棉,石英管置于高温炉中,石英管两端分别为气体的入口和出口,如图4。工作时,将H2、BCl3和Ar的混合通入石英管,加热并保持温度为850℃,反应持续90分钟,在石英管中收集到30 mg硼。通过EDS分析,硼粉纯度超过99.9%,通过XRD和拉曼光谱分析,产物为ɑ-型晶体硼。
以BCl3作为硼源,采用H2在高温还原制取高纯硼通常存在产率较低、反应温度高、能耗大、产量小等缺点,而制取富硼-10的硼粉,最优先考虑的是硼粉的纯度和收率,鉴于此,国内外开始研究用BBr3代替BCl3作为硼源,通过H2还原生产高纯硼。夏雯 [41] 发明了一种以工业硼粉为原料制备高纯硼粉的方法和装置。将工业硼粉溴化、除溴、分馏得到高纯的BBr3,在将BBr3和H2通入高温炉中进行反应得到

Figure 4. A schematic diagram of a device for preparing elemental boron by a tube furnace
图4. 热管炉法制备硼单质的装置示意图
高纯的硼粉。这种方法可用于硼粉的提纯,生产出的高纯硼粉杂质少,纯度高,可达到99.99995% (6N)以上,以溴化硼计产率达到80%以上。
等离子体法和激光法制备元素硼的化学原理与常规热源法相同。等离子体法温度较高,生产流程短,制备的硼纯度在99%以上;激光法利用反应物分子对激光的选择性吸收,大大降低了反应能耗。这两种方法都能制备纯度较高、粒径较小的元素硼,但难以大规模应用的问题。
由于H2还原10BF3反应的所需温度较高,转化率较低,采用氢气还原卤化硼法制备高纯硼时,可以先将10BF3转化为更容易被还原的10BBr3 [42] ,再利用H2还原10BBr3得到10B。
采用H2还原卤化硼制备法制备10B的流程较短,所得的10B纯度高,粒径小,但这种方法能耗大,生产效率低,10B的转化率低,目前这种方法多用于实验室规模制备少量元素硼或在很小的尺度下制备硼纳米线和硼薄膜材料,如何将其应用于工业规模还需要进一步研究。
2.4. 其它方法
制备元素硼的其它方法还有热分解法、硼烷裂解法等 [43] [44] [45] 。热分解发一般是通过分解BI3得到硼,硼烷裂解法通过高温裂解乙硼烷得到硼。乙硼烷是剧毒易爆气体,操作困难,在高温下容易生成其它硼烷,裂解过程中需要严格控制反应温度。硼烷裂解法生产元素硼的纯度较高,可以达到99.99%以上 [46] ;就制备富集10B的硼单质而言,用三氟化硼乙醚溶剂通过氢化锂还原的方法将10BF3转化为10B2H6是可行的 [47] ,但乙硼烷裂解效率和收率都较低,危险性也较大。
3. 结论与展望
富集硼-10单质应用广泛,有较大的研究价值,其生产方式主要有金属热还原法、电解法、氢气热还原法、硼烷裂解法等。金属热还原法工艺简单,可大规模生产无定型10B,但是用于制备富集B-10流程太长,收率难以保证,且纯度低的问题难以解决。氢气热还原法生产10B的流程短,产品纯度高,但其转化率较低,能耗高,经济性有待提高。硼烷裂解法效率和收率都较低,危险性也较大。熔盐电解法能制备无定型的富集B-10,其流程短,10B的转化率高,生产规模较大,主要存在的问题是设备材料腐蚀的问题,这些问题相对容易解决,因而是制备富集B-10较为可行的方法。
文章引用
胡小飞,曾静,肖楠林,胡石林. 富集B-10单质的制备
Preparation of Enriched Elemental B-10[J]. 核科学与技术, 2018, 06(02): 35-42. https://doi.org/10.12677/NST.2018.62005
参考文献
- 1. 郑学家. 核工业用硼化物[M]. 北京: 化学工业出版社, 2015: 116.
- 2. Chadwick, M.B., Herman, M., Obložinský, P., et al. (2011) Nuclear Data for Science and Technology: Cross Sections, Covariances, Fission Product Yields and Decay Data. Nuclear Data Sheets, 112, 2887-2996. https://doi.org/10.1016/j.nds.2011.11.002
- 3. Wang, L. (2000) The Position of Boron Carbide in Neutron Absorbing Materials and Its Properties Relation to Nuclear Applications. Materials Science & Engineering of Powder Metallargy, 5, 113-120.
- 4. Arnaldi, R., Chiavassa, E., Colla, A., et al. (2006) Thermal Neutron Detection with Resistive Plate Chambers via the 10B(n, α)7 Li Reaction. Nuclear Physics B—Proceedings Supplements, 158, 177-181. https://doi.org/10.1016/j.nuclphysbps.2006.07.021
- 5. Zheng, H., Ramalingam, B., Mukherjee, S., et al. (2016) Neutron Detection with Integrated sub-2 nm Pt Nanoparticles and 10B Enriched Dielectrics—A Direct Conversion Device. Sensing and Bio-Sensing Research, 9, 1-6. https://doi.org/10.1016/j.sbsr.2016.03.006
- 6. 厉井钢, 卢皓亮, 张洪, 等. 硼化锆在CPR1000核电厂1/4换料燃料管理中的应用研究[J]. 核动力工程, 2012, 33(5): 1-5.
- 7. 罗全勇, 朱瑞森. 硼中子俘获治疗[J]. 同位素, 2004, 17(3): 174-177.
- 8. Lintereur, A.T., Ely, J.H., Kouzes, R.T., et al. (2012) Boron-10 Lined Proportional Counter Model Validation. Nuclear Science Symposium and Medical Imaging Conference, Springfield, June 2012, 4290-4295.
- 9. Li, J.-G., Lu, H.-L., Zhang, H., et al. (2012) Study on Application of Zirconium Diboride(ZrB2) in CPR1000 Quarter-Core Fuel Management. Nuclear Power Engineering, 33, 1-5.
- 10. 于景阳, 韩莉果, 张卫江, 等. 化学交换反应法分离硼同位素的数学模型[J]. 同位素, 2005, 18(4): 216-219.
- 11. Huang, Y., Cheng, S., Xu, J., et al. (2011) Research on Chemical Exchange Process of Boron Isotope Separation. Procedia Engineering, 18, 151-156. https://doi.org/10.1016/j.proeng.2011.11.024
- 12. Itoh, S., Aida, M., Okamoto, M., et al. (2008) Boron Isotope Separation by Ion Exchange Chromatography Using Weakly Basic Anion Exchange Resin. Isotopenpraxis Isotopes in Environmental & Health Studies, 21, 204-208.
- 13. Zhou, F., Zhang, J., Bai, P., et al. (2016) Theoretical Calculation of Boron Isotopic Separation Factors in Ion-Exchange Chromatography. Journal of Chemical & Engi-neering Data, 62, 525-531.
- 14. Lyakhov, K. and Lee, H.J. (2015) New Experimental Setup for Boron Isotopes Separation by the Laser Assisted Retardation of Condensation Method. Journal of Nanoscience & Nanotechnology, 262, 579-587. https://doi.org/10.1166/jnn.2015.11467
- 15. Lyakhov, K.A., Lee, H.J. and Pechen, A.N. (2017) Some Issues of Industrial Scale Boron Isotopes Separation by the Laser Assisted Retarded Condensation (SILARC) Method. Separation & Purification Technology, 176, 402-411. https://doi.org/10.1016/j.seppur.2016.12.021
- 16. 李建平. 硼同位素分离工艺与生产技术[J]. 同位素, 2014, 27(2): 87-92.
- 17. Dou, Z.H. and Zhang T.A. (2004) Preparation of Boron Powder by Self-Propagating High Temperature Synthesis Metallurgy. Chinese Journal of Nonferrous Metals, 14, 2137-2143.
- 18. 喇培清, 卢学峰, 申达, 等. 铝热还原法制备硼粉[J]. 粉末冶金材料科学与工程, 2012, 17(6): 748-753.
- 19. Peng, C., Chen, S., Wu, Y., et al. (2010) Preparation of Boron Powder by Molten Salt Electrolysis. Chinese Journal of Rare Metals, 34, 264-270.
- 20. 张慧敏. 熔融电解法制备硼-10粉[J]. 辽宁化工, 1993(6): 33-36.
- 21. White, M.A., Cerqueira, A.B., Whitman, C.A., et al. (2015) Determination of Phase Stability of Elemental Boron. Angewandte Chemie, 54, 3626-3629. https://doi.org/10.1002/anie.201409169
- 22. Zhang, L., Zhang, W. and Xu, J. (2015) Preparation of Boric-10 Acid Applied in Nuclear industry. Transactions of Tianjin University, 21, 172-177. https://doi.org/10.1007/s12209-015-2390-3
- 23. Zhang, W., Liu, T. and Xu, J. (2016) Preparation and Characterization of 10B Boric Acid with High Purity for Nuclear Industry. Springerplus, 5, 1202. https://doi.org/10.1186/s40064-016-2310-6
- 24. 黄菊林. 金属镁热还原法制备非晶硼粉的研究[J]. 矿冶, 1996(3).
- 25. 伍继君, 杨斌, 马文会, 等. 超细高能燃料无定形硼粉的自蔓延制备与表征[J]. 功能材料, 2007, 38(12): 2073-2076.
- 26. Dou, Z.H., Zhang, T.A., Shi, G.Y., et al. (2014) Preparation and Characterization of Amorphous Boron Powder with High Activity. Transactions of Nonferrous Metals Society of China, 24, 1446-1451. https://doi.org/10.1016/S1003-6326(14)63211-8
- 27. 彭超. 自蔓延冶金法制备无定形硼粉中夹杂物分析及去除机制[D]: [硕士学位论文]. 沈阳: 东北大学, 2014.
- 28. Neelameggham, N.R. (2012) Elemental Boron and Magnesium Boride Synthesis. Journal for Manufacturing Science & Production, 12, 155-160. https://doi.org/10.1515/jmsp-2012-0014
- 29. Tilekar, K.V., Gajbhiye, V.P., Prasanth, H., et al. (2005) Preparation of High Purity Amorphous Boron Powder. Defence Science Journal, 55, 471-475. https://doi.org/10.14429/dsj.55.2009
- 30. 彭程, 陈松, 吴延科, 等. 熔盐电解法制备硼粉的研究[J]. 稀有金属, 2010, 34(2): 000264.
- 31. Mehra, R. (2013) High Pressure Synthesis and Investigation of Single Crystals of Metastable Boron Phases. High Pressure Research, 33, 673-683. https://doi.org/10.1080/08957959.2013.806500
- 32. 彭程, 陈松, 王力军, 等. 一种熔盐电解制备硼粉的方法及电解装置[P]. 中国专利, 2012.
- 33. Copper, H.S. (1951) Electrolytic Method of Making Boron. US Patent No. 2572248.
- 34. Alvin Uchiyama, A., et al. () (1960) Electrorefining of Elemental Boron. WO Patent No. 2940911.
- 35. Copper, H.S. (1959) Production of Boron by Fused Salt Bath Electrolysis. US Patent No. 2918417.
- 36. 徐华毕, 沈辉, 梁宗存. 太阳能级多晶硅生产与发展概况[J]. 材料导报, 2008, 22(9): 86-90.
- 37. Tsai, C.C. (1979) Characterization of Amorphous Semiconducting Silicon-Boron Alloys Prepared by Plasma Decomposition. Physical Review B, 19, 2041-2055. https://doi.org/10.1103/PhysRevB.19.2041
- 38. Song, Z.F., Ye, S.Z., Chen, Z.Y., et al. (2011) Study on Boron-Film Thermal Neutron Converter Prepared by Pulsed Laser Deposition. Applied Radiation & Isotopes Including Data Instrumentation & Methods for Use in Agriculture Industry & Medicine, 69, 443-447. https://doi.org/10.1016/j.apradiso.2010.09.017
- 39. Stern, D.R. and Lynds, L. (1958) High Purity Crystalline Boron. Journal of the Electrochemical Society, 105, 676-682. https://doi.org/10.1149/1.2428689
- 40. White, M.A., Cerqueira, A.B., Whitman, C.A., et al. (2015) Determination of Phase Stability of Elemental Boron. Angewandte Chemie International Edition, 127, 3697-3700. https://doi.org/10.1002/ange.201409169
- 41. 夏雯, 等. 一种高纯硼粉的制备方法及装置[P]. 中国专利, 201510780933.1, 2015-11-13.
- 42. 夏雯, 刘淑凤, 蒋文全, 等. 高纯三溴化硼的制备[J]. 化学试剂, 2014, 36(6): 000569.
- 43. Pickering, A.L., Mitterbauer, C., Browning, N.D., et al. (2007) Room Temperature Synthesis of Sur-face-Functionalised Boron Nanoparticles. Chemical Communications, 6, 580. https://doi.org/10.1039/b614363f
- 44. Si, P.Z., Zhang, M., You, C.Y., et al. (2003) Amorphous Boron Nanoparticles and BN Encapsulating Boron Nano-Peanuts Prepared by Arc-Decomposing Diborane and Nitriding. Journal of Materials Science, 38, 689-692. https://doi.org/10.1023/A:1021832209250
- 45. Parakhonskiy, G. (2012) Synthesis and Investigation of Boron Phases at High Pressures and Temperatures.
- 46. Oleksandr, O., Kurakevych, Y.G., Hammouda, T., et al. (2012) Comparison of Solid State Crystallization of Boron Polymorphs at Ambient and High Pressures. High Pressure Research, 32, 30-38. https://doi.org/10.1080/08957959.2011.635145
- 47. 韩美, 朱心才. 乙硼烷的制备方法[J]. 低温与特气, 1998(2): 35-38.