Advances in Analytical Chemistry
Vol.
09
No.
03
(
2019
), Article ID:
31842
,
7
pages
10.12677/AAC.2019.93024
Detection of Gatifloxacin in Drugs by Fluorescence Probe Method
Yaxin Zhao, Ziran Zhou, Yue Zhai, Peng Lin, Yuqing Cheng, Chang Zhao, Qiang Guo, Yuguang Lv*
College of Pharmacy, Jiamusi University, Jiamusi Heilongjiang

Received: Jul. 28th, 2019; accepted: Aug. 16th, 2019; published: Aug. 23rd, 2019

ABSTRACT
A fluorescent probe (DCDHF-2-V) was designed by synthesizing the new three cyanide two hydrofuran (DCDHF-2-V) electron acceptor. A new method of measuring the content of a new type of tricyanodihydrofuran and gatifloxacin was established. At the same time, the sensitivity was increased in the wavelength range, and the principle was studied and the best conditions for the experiment were discussed. The fluorescence intensity of the charge transfer complex was the highest when it was reacted for 30 minutes at 30˚C, and a new electron acceptor tricyanodihydrofuran was synthesized. A new fluorescence probe for the new three cyanohydrofuran derivatives and gatifloxacin was developed, which opened up a new idea of the new drug fluorescent probe. The best synthesis conditions were determined by experiments. The results show that the concentration of gatifloxacin in a specific range has a linear relationship with the fluorescence intensity, and the fluorescence characteristics of the complex are obviously stronger than that of the single gatifloxacin.
Keywords:Tricyanodihydrofuran, Gatifloxacin, Complex, Fluorophotometry
采用荧光探针法检测药物中加替沙星
赵雅欣,周子冉,翟月,林鹏,程雨晴,赵畅,郭强,吕玉光*
佳木斯大学药学院,黑龙江 佳木斯

收稿日期:2019年7月28日;录用日期:2019年8月16日;发布日期:2019年8月23日

摘 要
通过合成三氰基二氢呋喃(DCDHF-2-V)电子受体,设计了(DCDHF-2-V)荧光探针。创建了一种三氰基二氢呋喃衍生物与加替沙星进行反应形成的多种荷移络合物为其进行含量检测的新方法,同时测定在波长范围内可以达到增加灵敏度,并研究其原理,探讨实验进行的最佳条件。在30℃下反应30 min时,所形成的荷移络合物的荧光强度最高,合成了新型电子受体–新型三氰基二氢呋喃。通过对三氰基二氢呋喃衍生物与加替沙星药物形成的络合物进行荧光探针,开辟了新型药物荧光探针的新思路。通过实验的方式确定了各自最佳的合成条件。研究表明络合物在特定的范围内加替沙星的浓度与荧光强度直接存在一定程度的线性关联,而且络合物的荧光特性明显强于单个加替沙星的荧光特性。
关键词 :三氰基二氢呋喃,加替沙星,络合物,荧光分光光度法

Copyright © 2019 by author(s) and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
随着世界的发展,对于抗菌药的使用也越来越广泛,天然抗生素与半合成化合物是抗菌领域的主要抗菌药物,喹诺酮类药品从开始治疗尿路感染发展到现在成为一类重要的抗菌药品,仅在1997,全球销售量的销售额就超越24亿元。随着喹诺酮类药物的迅速发展,新型合成结构得到了越来越广泛的应用。同时,喹诺酮类药物的有效检测方法也越来越重要。因此,本文选用口服吸收效果好、无交叉耐药、临床应用广泛的氟喹诺酮类药物——加替沙星为研究对象 [1] [2] [3] 。
加替沙星(Gat ifloxacin)是由日本杏林制药株式会社研究出来的,在诺氟沙星、氟罗沙星之后研制的新型合成抗菌剂它是第四代氟喹诺酮类广谱抗菌药物,它不仅对革兰阳性菌及厌氧菌抗菌作用有所加强,还降低了会引起的光毒性作用。喹诺酮类药物——加替沙星具有很多优点包括抗菌谱广泛、强抗菌性、进药方便、产生不良反应小等,加替沙星对细菌DNA旋转酶及拓普异构酶有较高的选择性 [4] - [9] ,抑制和杀灭细菌,几乎不影响正常的细胞代谢活动,这就是为什么它的抗菌活性突出和氟喹诺酮类抗生素差异明显的原因,而且在慢性呼吸道感染的临床疗效和复杂的尿路感染之间的所有方面都显示出了优越的抗菌效果。众所周知,加替沙星具有与环丙沙星和氧氟沙星相同的优点,具有良好的广谱特性。加替沙星有非常显著的效果。而且加替沙星是通过口服方式进行吸收,口服方式方便快捷,吸收特别快分布的也很广泛,使它在血清蛋白结合率表现的很低,它伴有轻微的不良反应和基本不伴有潜在的光敏反应,而且用药很安全,所以在临床上使用效率特别高。尤其是对慢性复杂性呼吸道感染方面起到的灭菌作用已经达到了喹诺酮类中上市药物的佼佼者,它可以对细菌起到94.7%的抗菌活性 [10] - [16] 。因此,目前的临床研究表明,加替沙星有可能成为治疗各种传染病的常用药物之一,并被广泛应用于临床实践。三氰基二氢呋喃(DCDHF-2-V)是一种有机材料,它具有非线性光学活性。三氰基二氢呋喃衍生物是一个含有特殊结构的电子受体,它对于二阶微观非线性光学系数来说有很高的系数,是具有良好应用前景的小分子物质。本课题研究主要以第四代喹诺酮类药物加替沙星为主,作为研究对象,构建了由三种氰基二氢呋喃衍生物与加替沙星组成的新的络合物并进行分析研究,研究一种的检测手段 [17] - [22] 。
2. 仪器、试剂和材料
2.1. 仪器
2.2. 试剂和材料
3. 实验方法
3.1. 三氰基二氢呋喃衍生物合成
三氰基二氢呋喃衍生物合成如图1所示。
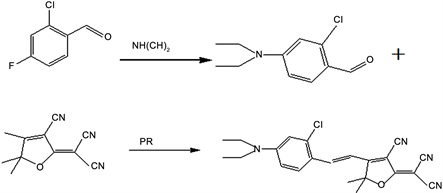
Figure 1. Synthesis of tricyanodihydrofuran derivatives
图1. 三氰基二氢呋喃衍生物合成过程
3.2. 储备液的配制
采用干燥的称量纸精密称量5 mg三氰基二氢呋喃衍生物,量取后放入规格为5 mL的具塞试管中,首先,用少量丙酮溶解,并在规模线上添加更多的丙酮。制备了1 × 103 mg/L的标准溶液,充分震荡,贮存冰箱备用。逐渐稀释到所需浓度。
3.3. 加替沙星溶液的配制
按照实验方案准备若干规格为10 mL及5 mL的具塞比色管,然后将实验所需的玻璃仪器洗净放置120℃的恒温干燥箱中干燥30 min,待放冷后备用。取一定量的加替沙星低温烘干去除结晶水后,用干燥的称量纸精密称取其中的0.1 mg,溶解在少量无水甲醇中,然后放入规格为5 mL的试管中,将更多的甲醇稀释至标度线,完全摇晃成标准的4 × 102 mg/L的溶液,储存在冰箱中以防止标准溶液变劣质。
3.4. 三氰基二氢呋喃衍生物最佳浓度的测定
对1 × 103 mg/L三氰基二氢呋喃衍生物的保留溶液进行了逐步稀释,得到浓度为0.1 mg/mL、0.01 mg/mL、0.005 mg/mL、0.001 mg/mL、0.0005 mg/mL的三氰基二氢呋喃衍生物溶液,在激发波长593 nm条件下检测其荧光发射光谱。实验结果如图2所示,浓度为0.005 mg/L是三氰基二氢呋喃衍生物检测最佳浓度。
加替沙星的最佳浓度的测定,将已经制备好的浓度为0.4 mg/ mL加替沙星保留溶液进行逐步稀释,得到浓度为0.2 mg/mL、0.1 mg/mL、0.05 mg/mL、0.025 mg/mL、0.0125 mg/mL的加替沙星溶液,在激发波长为362 nm的条件下测定了荧光发射光谱,故选用加替沙星浓度0.05 mg/mL为最佳浓度。
根据实验方案,准备不同规格的5 L比色管,并用甲醇溶液提前清洗,将其干燥。在比色管中加入2.5 mL三氰基二氢呋喃衍生物工作液,加入适量的加替沙星工作液并稍稍摇晃,然后用无水甲醇定容至比色管的刻度线。比色管放置在恒温水浴中。温度控制在30℃,加热30 min。反应结束后放冷至室温。将2.5 mL样品置于荧光比色管中。在激发波长为232 nm时,电荷转移复合物的荧光强度为471 nm。空白试验以同样的方式进行。

Figure 2. The relationship between concentration and intensity of gatifloxacin
图2. 加替沙星浓度与强度的关系
4. 结果与讨论
4.1. 加替沙星荷移反应前后的荧光激发和发射光谱
对加替沙星和三氰基氢呋喃衍生物形成的络合物分别进行荧光激发和发射扫描,络合物是完全反应2.5 mL容量。并对加替沙星工作液2.5 mL和三氰基二氢呋喃2.5 mL进行了研究。在相同条件下,将两种液体的荧光激发波长和发射光波长作为对照组。
结果如图3所示。三氰基二氢呋喃衍生物(1)加替沙星(2)加替沙星–三氰基二氢呋喃衍生物(3)。从图谱上看,加替沙星溶液本身具有一定程度的荧光特性。当加替沙星和三个氰氢呋喃衍生物相互作用形成电荷转移络合物时,所形成的配合物的激发光谱和发射光谱与加替沙星单独的特征峰没有位置变化,因此位移没有变化,加替沙星–三氰基氢呋喃衍生物配合物的光强显著增加,表明加替沙星成功地形成了三氰基二氢呋喃衍生物的电荷转移络合物。

Figure 3. Fluorescence excitation and emission spectra of gatifloxacin before and after charge transfer reaction
图3. 加替沙星荷移反应前后的荧光激发和发射光谱
4.2. 探讨加替沙星荷移络合物生成的影响因素
将2 mL加替沙星溶液添加到6个比色管中,然后分别将三氰氢呋喃工作液0.1~0.6 mL加入2 mL加替沙星工作液中。轻度震荡后,将无水甲醇定容刻度使溶液与无水甲醇完全反应,加到恒温水浴中,温度控制在30℃,30 min后。取出并放却至室温。测定了一定体积的溶液在471 nm处的荧光强度。实验结果表明,电荷转移络合物形成的最佳剂量是三氰基二呋喃的量控制在0.3 mL,低浓度导致不完全反应,高浓度的超强浓度会降低配合物的荧光特性。
将0.3 mL三氰氢呋喃溶液添加到5个比色管中,然后分别将加替沙星工作液1~5 mL加入3 mL三氰氢呋喃溶液中。轻度震荡后,将无水甲醇定容刻度使溶液与无水甲醇完全反应,加到恒温水浴中,温度控制在30℃以内,30 min后。取出并放却至室温。测定了一定体积的溶液在471 nm处的荧光强度。实验结果表明,最佳的电荷转移复合物需要控制加替沙星在2 mL的剂量。
加替沙星哌嗪基氮原子具有一对电子,可作为电子供体,可与强电子受体试剂进行反应。其在一定条件下能与强电子受体发生荷移反应而生成荷移络合物。三氰氢呋喃为强电子受体试剂,可与加替沙星以1:1的比例形成p-π体系的络合物,使荧光强度增强,波长向长波方向移动,提高药物检测的灵敏度。
致谢
感谢黑龙江省大学生创新项目(项目号201910222024),大力支持。
基金项目
国家自然科学基金项目(21346006),黑龙江省自然科学基金项目(B2017015),黑龙江省大学生创新项目(201910222024),黑龙江省教育科学“十二五”规划重点项目(GBB1212070),佳木斯大学国家培育项目(JMSUJCGP 2016-003)。
文章引用
赵雅欣,周子冉,翟 月,林 鹏,程雨晴,赵 畅,郭 强,吕玉光. 采用荧光探针法检测药物中加替沙星
Detection of Gatifloxacin in Drugs by Fluorescence Probe Method[J]. 分析化学进展, 2019, 09(03): 179-185. https://doi.org/10.12677/AAC.2019.93024
参考文献
- 1. 丁兆猛, 栾雨. 高效液相色谱法同时测定加替沙星滴眼液中加替沙星和羟苯乙酯的含量[J]. 中国药物经济学, 2017, 12(12): 32-33+39.
- 2. Wakabays, H.E. and Mitsuhas, H.S. (1994) In Vitro Antibacterial Activity of AM-1155, Novel 6-Fluoro-8-Methoxy Quinolone. Antimicrobial Agents and Chemotherapy, 38, 594-601.
https://doi.org/10.1128/AAC.38.3.594 - 3. 李家泰, 刘健, 王彤等. 盐酸加替沙星(Gatifloxacin)体外抗菌作用[J]. 中国临床药理学杂志, 2001, 17(6): 403-409.
- 4. Ta Kei, M., Fukuda, H., Yasue, T., Hosaka, M. and Oomori, Y. (1998) Inhibitory Activities of Gatifloxacin (AM- 1155), a New Developed Fluoroquinolone, against Bacterial and Mammalian Type Ⅱ Topoisomerases. Antimicrobial Agents and Chemotherapy, 42, 2678-2681.
https://doi.org/10.1128/AAC.42.10.2678 - 5. Shen, Y., Du, X., Zhang, W., et al. (2013) Spaceresolved Extreme Ultraviolet Spectrometer System for Impurity Behavior Research on Experimental Advanced Superconducting Tokamak. Nuclear Instruments and Methods in Physics Research Section A: Accelerators, Spectrometers, Detectors and Associated Equipment, 700, 25-27.
https://doi.org/10.1016/j.nima.2012.10.070 - 6. Ael-Said, W., Yoon, J.H. and Choi, J.W. (2018) Nanostructured Surfaces for Analysis of Anticancer Drug and Cell Diagnosis Based on Electrochemical and SERS Tools. Nano Convergence, 5, 46-49.
https://doi.org/10.1186/s40580-018-0143-4 - 7. Pan, Z.Y., Peng, J.D., Peng, H.J., et al. (2017) High-Performance Liquid Chromatography Study of Gatifloxacin and Sparfloxacin Using Erythrosine as Post-Column Resonance Rayleigh Scattering Reagent and Mechanism Study. Luminescence: The Journal of Biological and Chemical Luminescence, 12, 23-24.
- 8. Pornprasert, S. and Punyamung, M. (2015) Detection of Compound Heterozygous of the Constant Spring and by Capillary Electrophoresis and High Performance Liquid Chromatography. Indian Journal of Hematology & Blood Transfusion, 31, 229-232.
https://doi.org/10.1007/s12288-014-0411-3 - 9. Jacqueline, G., Alfonso, D., Denis, L., et al. (2016) Nearing the Cold-Arid Limits of Microbial Life in Permafrost of an Upper Dry Valley, Antarctica. The ISME Journal, 10, 68-69.
https://doi.org/10.1038/ismej.2015.239 - 10. 黄其春. 紫外分光光度法测定加替沙星的含量[J]. 海峡药学, 2002, 14(2): 34-35.
- 11. 李一峻, 常子栋, 何锡文. 电化学分析的进展及应用[J]. 分析试验室, 2007, 26(10): 107-122.
- 12. 赵东江, 马松艳. 电化学分析法在食品安全检测中的应用[J]. 绥化学院学报, 2016, 36(2): 141-144.
- 13. 赵云芳, 张晓丽. 加替沙星的电化学特性及其应用[J]. 山西农业大学学报(自然科学版), 2009, 29(4): 370-373.
- 14. Wang, H., Lu, Z., Lord, S.J., et al. (2006). The In-fluence of Tetrahydroquinoline Rings in Dicyanome Thylenedihydrofuran (DCDHF) Single-Molecule Fluorophores. Tetrahedron, 10, 103-114.
https://doi.org/10.1016/j.tet.2006.10.044 - 15. 朱斌, 蒋受军, 胡昌勤. 高效毛细管电泳法测定加替沙星含量[J]. 药物分析杂志, 2002, 22(5): 397-400.
- 16. 刘鹏, 马仕洪, 戴翚等. 加替沙星微生物限度检查方法的建立[J]. 药物分析杂志, 2007, 27(6): 881-884.
- 17. 翟海云, 李江梅, 陈缵光, 等. 微芯片毛细管电泳快速测定加替沙星注射液中加替沙星的含量[J]. 分析试验室, 2012, 31(3): 36-38.
- 18. 连宁, 孙春燕, 赵慧春. 加替沙星的荧光光度法测定[J]. 分析测试学报, 2002, 21(1): 79-81.
- 19. 敖登高娃, 陶玉龙, 樊海燕. 荷移荧光光谱法测定加替沙星[J]. 光谱学与光谱分析, 2007, 27(8): 1615-1618.
- 20. 何立芳, 林丹丽, 李耀群, 等. 同步荧光分析法的应用及其新进展[J]. 化学进展, 2004, 16(6): 879-885.
- 21. Pearce, D.A., Jotterand, N., Carrico, I.S. and Imperiali, B. (2001) Derivatives of 8-Hydroxy-2-Methyl Quinoline Are Powerful Prototypes for Zinc Sensors in Biological Systems. Journal of the American Chemical Society, 123, 5160-5161.
https://doi.org/10.1021/ja0039839 - 22. Tan, J.H., Li, G.R., Yang, H.X., Wang, Y.S. and Zhou, D.J. (2013) Determination of Gatifloxacin in Milk and Biological Fluids by Inhibitory Resonance Fluorescence Spectrometry. Analytical Letters, 46, 72-74.
https://doi.org/10.1080/00032719.2012.723228
NOTES
*通讯作者。