Hans Journal of Nanotechnology
Vol.1 No.2(2011), Article ID:228,4 pages DOI:10.4236/nat.2011.12009
Preparation and Antimicrobial Activity of Cd1–xMxO Composite Oxides
College of Chemistry & Life Science, Zhejiang Normal University, Jinhua
Email: sky52@zjnu.cn
Received: Jun. 26th, 2011; revised: Jul. 25th, 2011; accepted: Jul. 27th, 2011.
ABSTRACT:
Cd1–xMxO composite oxides (M = Cu,Cr; x = 0.02,0.04,0.06,0.08,0.10) were prepared by sol-gel method. The X-ray powder diffraction (XRD) and scanning electron microscope (SEM) were employed to characterize the crystal structure and morphology of the samples. The results indicated that the Cd1–xMxO nanoparticles presented an irregular hexagonal shape and the their size is about 50~80 nm. Antibacterial testing showed that the Cd1–xMxO had excellent antibacterial activity than pure CdO against Staphylococcus aureus, Escherichia coli and Candida albicans. The Cd0.94Cu0.06O and Cd0.94Cu0.08O had the best antibacterial effect on Escherichia coli and Candida albicans in a series of samples doped with Cu, respectively; and the antibacterial activity of samples increased with increase of Cr content in a series of ones doped with Cr.
Keywords: CdO; Doped; Sol-Gel Method; Antimicrobial Activity
Cd1–xMxO复合氧化物的制备及抗菌活性
孙檬茜,梁效锡,陈耀斌,李良超*
浙江师范大学化学与生命科学学院,金华
Email: sky52@zjnu.cn
摘 要:
用溶胶–凝胶法制备了Cd1–xMxO复合氧化物(M为Cu、Cr,x = 0.02,0.04,0.06,0.08,0.1)。用XRD、SEM表征了样品的物相结构和形貌。结果表明Cd1–xMxO纳米粒子为不规则的六角形貌,晶粒尺寸约为50~80 nm。抗菌测试表明Cd1–xMxO对金黄色葡萄球菌、大肠杆菌、白色念珠菌的抗菌活性明显优于纯的CdO。在掺Cu系列中,Cd0.94Cu0.06O和Cd0.94Cu0.08O样品分别对大肠杆菌和白色念珠菌的抗菌效果最佳;在掺Cr系列样品中,随Cr掺杂浓度增加对金黄色葡萄球菌的抑菌作用增强。
收稿日期:2011年6月26日;修回日期:2011年7月25日;录用日期:2011年7月27日
关键词:CdO;掺杂;溶胶–凝胶法;抗菌活性
1. 引言
21世纪,人们的生活受到了病原菌的威胁。日本的病原性大肠杆菌“O-15”、英国的“疯牛病”、“9·11”事件后的“炭疽菌”和SARS病毒的袭击使人们充分认识到生存环境和微生物环境的恶化给地球和人类健康带来的危害。抗菌材料的应用能使人们脱离微生物对生存环境的影响,生活质量得以提高。抗菌材料按其抗菌机理可以分为以Ag、Cu、Zn等金属离子为代表的溶出型抗菌材料和以ZnO、TiO2为代表的具有光催化活性类抗菌材料。溶出型抗菌材料在使用过程中,抗菌剂缓慢释放出来的金属离子能破坏细菌的细胞膜或细胞原生质活性酶的活性而具有抗菌效果;光催化活性类抗菌材料是在光的作用下,抗菌剂与水或空气作用,生成活性氧O2–和OH·,具有很强的氧化还原作用,产生持久的抗菌效果。
纳米CdO在太阳能电池、电池阴极材料、传感器、透明电极、光学晶体管和二极管等领域有着广泛的应用前景[1-3]。CdO是一种重要的半导体功能材料,具有独特的光学、光电子学和催化性能等,可以作为一种催化活性抗菌材料;同时,镉具备一定的生物毒性,纳米CdO对微生物具有抑菌作用,也可以作为一种溶出型抗菌材料。CdO的制备通常有溶胶–凝胶法[4]、水热法[5]、湿化学法[6]、喷雾热解法[7]、溅射法[8]等方法。在众多制备方法中,溶胶–凝胶工法具有均匀性好、化学计量比容易控制、工艺简单和安全性较高等特点,是制备纳米氧化物较常用的方法。
据报道,Cu2+的抗菌性好、毒性小、成本低,是一种广谱抗菌材料[9];Cr3+具有优良的抗菌性能,但毒性较大,其应用受到了限制。如果将Cu2+和Cr3+掺杂到CdO中,是否会产生更好的抗菌性能呢?基于此设想,本文用柠溶胶–凝胶法制备了Cu2+、Cr3+掺杂的Cd1–xMxO复合氧化物,研究了Cu2+和Cr3+掺杂量对纳米CdO抗菌性能的影响,并对样品的抗菌机理做了初步的探讨。
2. 实验
2.1. 试剂
柠檬酸、硝酸镉、硝酸铜、硝酸铬、氨水、葡萄糖、氯化钠、氢氧化钠等都是分析纯试剂;牛肉膏、蛋白胨、琼脂等为生化试剂。
2.2. Cd1–xMxO复合氧化物的制备
用柠檬酸溶胶–凝胶法[4]制备纳米Cd1–xMxO复合氧化物(M = Cu、Cr,x = 0.02、0.04、0.06、0.08、0.1)。称取一定量的硝酸镉、硝酸铜(硝酸铬)和柠檬酸,加入适量去离子水溶解后,磁力搅拌下滴加氨水(25 ~28 wt%),有沉淀物生成;继续滴加氨水至pH ≈ 9,沉淀溶解得均一透明溶液。70℃下恒温蒸发水分形成湿凝胶,干燥得干凝胶。将干凝胶在空气中350℃煅烧2 h (升温速率10℃/min),自然冷却至室温的掺Cu和掺Cr纳米CdO样品,研磨后备用。同样方法制备纯纳米CdO。
2.3. 样品表征及抗菌性能评价
2.3.1. 样品表征
用Philps-Pw 3040/60型X-射线粉末衍射仪(XRD),Cu Kα 辐射(λ = 0.154056 nm),工作电压为40 kV,工作电流为40 mA,扫描范围2θ = 20˚~80˚,扫描速率4˚/min分析样品的物相和结构;用Hitachi S-4800扫描电子显微镜(SEM)观察样品的表面形貌,操作电压为50 kV。
2.3.2. 培养基制备
按文献[10]制备牛肉膏蛋白胨液体培养基、牛肉膏蛋白胨固体培养基、沙堡氏液体培养基和沙堡氏固体培养基。牛肉膏蛋白胨培养基用于细菌的培养(金黄色葡萄球菌、大肠杆菌),沙堡氏培养基用于真菌的培养(白色念珠菌)。
2.3.3. 菌悬液制备
供试菌种为细菌类的大肠杆菌(ATCC25923)、金黄色葡萄球菌(ATCC25922)和真菌类的白色念珠菌(ATCC10231),以上菌株由浙江师范大学生物技术专业实验室提供。取菌种划平板分离得单菌落,然后用接种环挑取培养的菌株接种到无菌培养基中,置于震荡箱中,恒重37℃,100 r/min振荡24 h,然后加无菌生理盐水稀释成1×105~9×105 cfu/mL浓度的菌悬液,摇匀后备用。
2.3.4. 抑菌圈实验
按文献[11]方法进行抑菌圈实验。用游标卡尺测量抑菌圈直径的大小,每个测试样品平行测试3次,取平均值。
3. 结果与讨论
3.1. XRD
图1为CdO(a),Cr0.04Cd0.96O1.02(b),Cu0.04Cd0.96O(c) 样品的XRD图谱。从图1中发现2θ = 34˚,39˚,55˚,66˚,69˚,82˚处出现了CdO的特征峰,与CdO的标准谱图(JCPDS Card No.75-576)完全一致。根据Scherrer公式[12]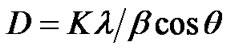 (其中D为晶粒尺寸(nm);λ为X射线入射波长(0.154056 nm);K为Scherrer常数,其值取0.89;β为积分半高宽度;θ为布拉格衍射角)计算出样品的晶粒尺寸为80~100 nm,且掺杂样品的晶粒尺寸比母体CdO的略小。其可能原因是Cr3+,Cu2+半径均小于Cd2+半径,它们进入CdO晶格形成固溶体导致CdO晶胞发生局部收缩,使得晶粒尺寸略有减小。
(其中D为晶粒尺寸(nm);λ为X射线入射波长(0.154056 nm);K为Scherrer常数,其值取0.89;β为积分半高宽度;θ为布拉格衍射角)计算出样品的晶粒尺寸为80~100 nm,且掺杂样品的晶粒尺寸比母体CdO的略小。其可能原因是Cr3+,Cu2+半径均小于Cd2+半径,它们进入CdO晶格形成固溶体导致CdO晶胞发生局部收缩,使得晶粒尺寸略有减小。
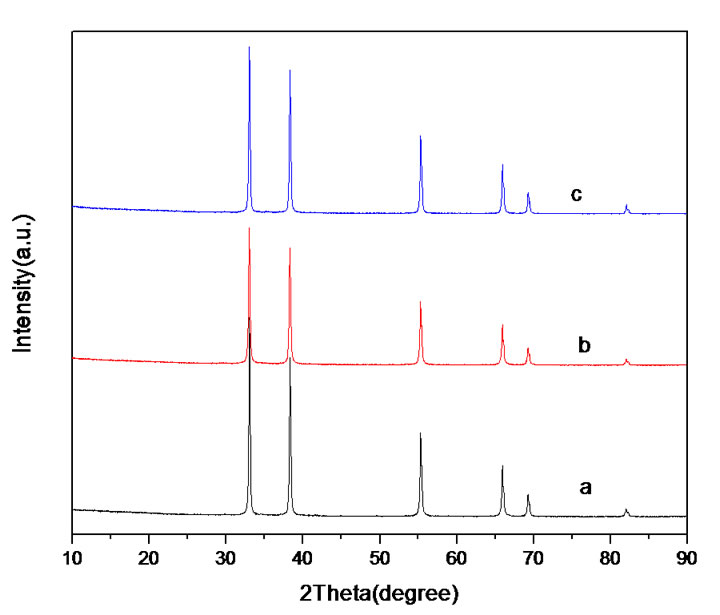
Figure 1. Powder X-Ray diffraction patterns of CdO(a), Cr0.04Cd0.96O1.02(b) and Cu0.04Cd0.96O(c)
图1. CdO(a), Cr0.04Cd0.96O1.02(b), Cu0.04Cd0.96O(c)的XRD衍射图
3.2 微观形貌
图2为CdO、Cu0.04Cd0.96O和Cr0.04Cd0.96O样品的SEM照片。从图中可以看出CdO晶粒为准六角形貌,尺寸在50~100 nm范围,粒子的分布不大均匀;而Cu0.04Cd0.96O和Cr0.04Cd0.96O样品均呈不规则六角形貌,粒子分布比较均匀。掺Cr样品的晶粒尺寸比掺Cu的略小,但程度的团聚略大,这可能与前者是异价置换,有较大的晶格缺陷的缘故。掺杂样品的晶粒尺寸比CdO的大,与XRD的结果基本一致。
3.3. 抗菌性能
3.3.1. Cd1–xMxO复合氧化物的抗菌性能
在普通日光灯照射条件下,考察Cu2+和Cr3+ 掺杂量对大肠杆菌、金黄色葡萄球菌、白色念珠菌的抑菌性能的影响,其结果示于表1和表2。由表获悉,随着Cr3+和Cu2+掺杂量的增加,样品对大肠杆菌、白色念珠菌的抑菌能力呈先增强后减弱的变化趋势。Cu2+掺杂量x = 0.06, 0.04和0.08的样品分别对大肠杆菌、金黄色葡萄球菌和白色念珠菌具有最强的抗菌作用,其最大抑菌直径分别达到29.2 mm、26.7 mm和28.7 mm。相对于纯CdO的抗菌性能都有显著地增强,说明适量Cu2+掺杂能提高Cd1–xCuxO的抗菌性能;当掺杂量过大时,抗菌性能反而减弱。因为适量Cu2+取代CdO晶胞中Cd2+的位置,在晶体的内部乃至表面产生了晶格缺陷,使表面活性位增多,有利于金属粒子溶出,从而增强抗菌性能;随着Cu2+掺杂量的增加,Cu2+取代Cd2+有一个极限,过多的CuO覆盖在CdO表面上,影响金属粒子的溶出,导致其抗菌性能反而减弱。Cr3+掺杂量x = 0.06, 0.1和0.08的样品分别对白色念珠菌、大肠杆菌和金黄色葡萄球菌的抑菌能力最强;掺Cr3+样品的抑菌能力总体上比纯CdO的强,且随着Cr3+掺杂浓度的增加,对金黄色葡萄球菌的抑菌能力逐渐增强。



Figure 2. SEM images of CdO (a), Cu0.04Cd0.96 (b) and Cr0.04Cd0.96(c)
图2. CdO (a)、Cu0.04Cd0.96 (b)和Cr0.04Cd0.96 (c)的SEM照片
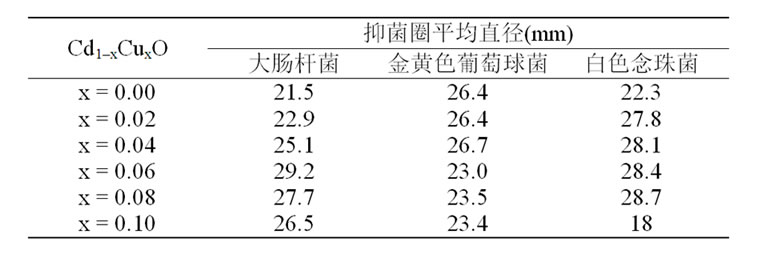
Table 1. Average diameter (mm) of inhibition zone for Cd1–xCuxO composites
表1. Cd1-xCuxO复合氧化物的抑菌圈平均直径(mm)
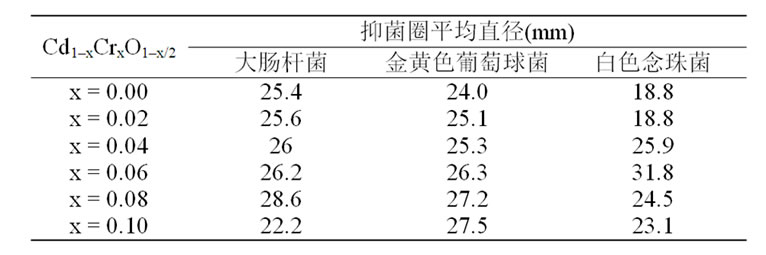
Table 2. Average diameter (mm) of inhibition zone for Cd1–xCrxO1+x/2 composites
表2. Cd1–xCrxO1+x/2复合氧化物的抑菌圈平均直径(mm)
3.3.2. Cd1–xMxO复合氧化物的抗菌机制
Cd1–xMxO复合氧化物的光催化抑菌原理与CdO的相同。CdO是一种N-型宽禁带半导体,它的禁带宽度是2.3 eV[13]。在Cd1–xMxO复合氧化物中,Cu2+、Cr3+取代Cd2+生成活性更大的固溶体,降低了掺杂样品的禁带宽度。因此Cd1–xMxO复合粉末的抗菌机制主要来自两个方面:1) Cd1–xMxO纳米粒子具备特殊的表面效应和高氧化活性,尤其是在紫外光照条件下,在水和空气中会分解出自由移动的电子(e–),同时留下带正电的空穴(h+)。带正电的空穴具有很强的氧化作用,能激发产生活性氧,与大多数有机化合物发生氧化反应,从而能够将细菌等微生物杀死,达到杀菌的作用;2) 游离出来的Cr3+、Cu2+ 和Cd2+ 接触细菌等微生物时,能与细菌体内的氧化代谢酶(-SH)结合,使其失去活性而导致细菌窒息死亡。Cr3+、Cu2+和Cd2+从死亡细菌体内游离出来后可继续杀死其他的细菌,从而达到持久抗菌的作用。
4. 结论
1) 用柠檬酸–溶胶凝胶法制备了Cd1–xMxO复合氧化物。Cr3+和Cu2+掺入导致Cd1–xMxO样品的晶粒尺寸减小。
2) Cd1–xMxO纳米复合氧化物对大肠杆菌、金黄色葡萄球菌和白色念珠菌都有良好的抑制作用。Cu适量掺杂能提高Cd1–xCuxO的抗菌性能,当掺杂量过大时,抗菌性能反而减弱;掺Cr3+样品的抑菌能力总体上比纯CdO强,Cr3+掺杂量x = 0.06, 0.08和 0.1的样品分别对白色念珠菌、大肠杆菌和金黄色葡萄球菌具有最佳抑菌作用。
5. 致谢
本文得到了国家自然科学基金(21071125)和浙江省大学生新苗人才计划项目(2010R404013)的资助,特此致谢!
参考文献 (References)
[1] H. Zhang, X. Y. Ma, Y. J. Ji, et al. Synthesis ofcadmium hydroxide nanoflake and nanowisker by hydrothermal method. Materials Letters, 2005, 59(1): 5625-5658.
[2] M. Ristic, S. Popovic, and S. Music. Formation and properties of Cd(OH)2 and CdO particles. Materials Letters, 2004, 58(20): 2494-2499.
[3] S. Motupally, M. Jain, V. Srinivasan, et al. The role of oxygen at the second discharge plateau of nickel hydroxide. Journal of the Electrochemical Society, 1998, 145(1): 3423-2429.
[4] 李晓娥, 祖庸, 马沛. 溶胶–凝胶法合成纳米二氧化钛中催化剂的研究[J]. 河北化工, 1997, 2: 10-12.
[5] Z. X. Yang, W. Zhong,Y. X. Yin, et al. Controllable synthesis of single-crystalline CdO and Cd(OH)2 nanowires by a simple hydrothermal approach. Nanoscale Research Letters, 2010, 5(6): 961-965.
[6] 邸云萍, 徐利华, 刘明等. 钛精矿湿化学法合成Fe2TiO5/TiO2复合纳米粉[J]. 人工晶体学报, 2008, 37(6): 1365-1369.
[7] 赵俊亮, 李效民, 边继明等. 喷雾热解法生长N掺杂ZnO薄膜机理分析[J]. 无机材料学报, 2005, 20(4): 959-964.
[8] 潘峰, 郭颖, 陈长乐, 文军. 磁控溅射法生长ZnO薄膜的结构和表面形貌特性[J]. 陕西理工学院学报(自然科学版), 2010, 26(4): 58-62.
[9] I. Perelshtein, G. Applerot, N Perkas, et al. CuO-cotton nanocomposite: Formation, morphology, and antibacterial activity. Surface and Coatings Technology, 2009, 204(1-2): 54-57.
[10] 孙爱兰, 谭天伟, 朱中伟. 几种抑菌材料对化妆品中腐败菌的抑制作用比较[J]. 日用化学工业, 2005, 35(2): 84-87.
[11] 张昭, 王向东, 曾光远等. 含银无机抗菌剂的研制和抗菌性能初探[J]. 稀有金属, 2002, 26(5): 401-404.
[12] 郭金玲, 沈岳年. 用Scherrer公式计算晶粒度应注意的几个问题[J]. 内蒙古师范大学学报(自然科学汉文版), 2009, 38(3): 357-358.
[13] 季振国, 吴秋红, 毛启楠. 射频磁控溅射法沉积透明柔性导电CdO薄膜[J]. 半导体技术, 2010, 35(12): 1170-1173.