Bioprocess
Vol.1 No.1(2011), Article ID:270,4 pages DOI:10.4236/bp.2011.11001
Determination of Selenium in ChitooligosaccharideSelenium and Selenium Carboxymethyl-Chitosan#
1College of Life Science, Dalian Nationalities University, Dalian
2College of Life Science, Jinan University, Guangzhou
3Yantai Entry-Exit Inspection and Quarantine Bureau, Yantai
Email: jlm@dlnu.edu.cn
Received: Sep. 12th, 2011; revised: Sep. 21st, 2011; accepted: Sep. 25th, 2011.
ABSTRACT:
Sodium selenite and chitooligosaccharide, carboxymethyl-chitosan, respectively, were used to synthesize chitooligosaccharide-selenium and selenium carboxymethyl-chitosan in this experiment by chemical method. The contents of selenium were tested by o-phenylenediamine and diaminobenzidine spectrophotometric methods. The results showed the consistence of the two methods. The contents of selenium in chitooligosaccharide-selenium were 9.02 mg/g, 8.82 mg/g, respectively. The contents of selenium in selenium carboxymethyl-chitosan were 20.50 mg/g, 20.24 mg/g, respectively.
Keywords: Chitooligosaccharide-Selenium; Selenium Carboxymethyl-Chitosan; O-Phenylenediamine Spectrophotometric; Diaminobenzidine Spectrophotometric
硒化壳寡糖和硒化羧甲基壳聚糖中硒含量的测定#
全文颖1,覃仙玲1,曹 鹏2,3,齐小辉1,范圣第1,金黎明1*
1大连民族学院,生命科学学院,大连
2暨南大学生命科学学院,广州
3烟台出入境检验检疫局,烟台
Email: jlm@dlnu.edu.cn
摘 要:
分别以亚硒酸钠与壳寡糖、羧甲基壳聚糖为原料,合成硒化壳寡糖和硒化羧甲基壳聚糖。分别用邻苯二胺分光光度法和二氨基联苯胺分光光度法测定其中的硒含量,两种方法测定的结果较为一致,测得硒化壳寡糖中硒含量分别为9.02 mg/g、8.82 mg/g,测得硒化羧甲基壳聚糖中硒含量分别为20.50 mg/g、20.24 mg/g。
收稿日期:2011年9月12日;修回日期:2011年9月21日;录用日期:2011年9月25日
关键词:硒化壳寡糖;硒化羧甲基壳聚糖;邻苯二胺分光光度法;二氨基联苯胺分光光度法
1. 引言
壳聚糖(chitosan)是甲壳素(chitin)的N-脱乙酰基的产物,因其良好的生物相容性、无毒性和可降解性被广泛应用于生物医药和保健等诸多领域。壳聚糖的缺点是难溶于水,限制了其应用。壳寡糖(chitooligosaccharide)是壳聚糖的水解产物,具有相对分子量小,可溶性高,生物活性高等优点,在提高人体免疫力,抗癌,降低血压、血脂、血糖,促进钙以及其他微量元素吸收等方面有显著的功效。羧甲基壳聚糖(carboxymethyl-chitosan)是壳聚糖经化学改性得到的水溶性衍生物,其溶解性好、络合金属离子能力强,可作为水处理的絮凝剂,化妆品保湿剂,果蔬的保鲜剂,植物的生长促进剂,药物辅料等[1]。
硒(selenium)是人体所必需的微量元素之一,由于其本身具有极高的抗氧化能力,因此它在延缓衰老、抗癌、增强人体免疫力等方面具有明显的功效,甚至被人赞誉为“抗癌之王”。但是,大多数无机硒化合物毒性比较大,最低致死量相对较小,因此应用受到极大的限制[2]。所以,寻找生物活性相对较高且毒性相对较低的有机硒替代品就成为给机体补硒的首要任务。目前已有研究表明,有机硒多糖作为补硒剂不仅稳定性好,溶出性高,而且释放出硒后配体多糖不会对机体产生毒副作用,是理想的补硒产品[3,4],而对硒化壳聚糖的研究也引起了广泛的关注[5,6]。但是,对硒化壳寡糖(chitooligosaccharide-selenium)、硒化羧甲基壳聚糖(selenium carboxymethyl-chitosan)的研究较少。
本实验分别以亚硒酸钠和壳寡糖、羧甲基壳聚糖为原料,合成了硒化壳寡糖和硒化羧甲基壳聚糖,并用邻苯二胺分光光度法和二氨基联苯胺分光光度法测定其中的硒含量。
2. 实验部分
2.1. 试剂与仪器
试剂:壳寡糖、羧甲基壳聚糖,中国海洋大学海洋生命学院提供。亚硒酸钠,无水乙醇,冰乙酸,盐酸,硝酸,甲苯,邻苯二胺盐酸盐,3,3’-二氨基联苯胺,EDTA-2Na,硒粉,氢氧化钠等,均为国产分析纯试剂。
仪器:370DTGS型红外光谱仪(美国Thermo公司);DF-101S型恒温磁力搅拌器(巩义市英峪于华仪器厂);DHG-9070A型真空干燥箱(上海精宏实验设备有限公司);Seven Easy 型PH计(上海梅特勒-托利多仪器有限公司);UV-2100型分光光度计(上海尤尼柯仪器有限公司)。
2.2. 实验方法
2.2.1. 硒化壳寡糖和硒化羧甲基壳聚糖的合成
准确称取壳寡糖(羧甲基壳聚糖)1.0 g,加入49 mL的去离子水和1 mL 1%的冰乙酸,搅拌溶解至澄清。将1.33 g亚硒酸钠溶于10 mL的去离子水中,缓慢加入到壳寡糖(羧甲基壳聚糖)溶液中,混匀后放置2 h,使其充分反应。加入3倍体积的无水乙醇,室温条件下过夜醇析,抽滤,再用无水乙醇洗涤2次,冷冻干燥即得硒化壳寡糖(硒化羧甲基壳聚糖)样品[4]。
2.2.2. 红外光谱法表征
将少量的壳寡糖、硒化壳寡糖、羧甲基壳聚糖和硒化羧甲基壳聚糖用KBr压片,进行红外光谱测定,测定范围为400~4000 cm–1。
2.2.3. 硒含量的测定
1) 邻苯二胺分光光度法[7]
硒标准溶液的配制:准确称取0.100 g硒粉置于具塞试管中,加入5 mL的浓硝酸使硒粉溶解,用10%的硝酸溶液定容至100 mL,此即为贮备液。取0.4 mL贮备液加水定容至100 mL,得4 µg/mL的硒标准溶液。
硒标准曲线的绘制:取7个具塞的玻璃瓶,编号为0~7。分别取0、1、2、3、4、5、6 mL的硒标准溶液于玻璃瓶中,加去离子水至24 mL。用1:1的HCl调其pH为2左右,再加入2 mL 1%的邻苯二胺溶液,振荡,放置黑暗处1 h后取出,加入10 mL甲苯,振荡30 s,静置10 min后取甲苯萃取层(上层),以甲苯为参比,于335 nm波长处测其吸光值。绘制标准曲线。
硒含量的测定:称取0.010 g样品,溶于50 mL水中,配制成0.2 mg/mL的样品溶液。取1 mL样品溶液置于玻璃瓶中,加水至25 mL,其后的操作同硒标准曲线绘制相同,测其吸光值。根据标准曲线计算样品中硒含量。
2) 二氨基联苯胺分光光度法[8]
硒标准溶液的配制:准确称取0.100 g硒粉于具塞试管中,加入2 mL浓硝酸使硒粉溶解,转入100 mL容量瓶中,用1:1 HCl定容,得1 mg/mL的硒溶液。再取上述溶液50 µL于50 mL容量瓶中,加去离子水定容,得1 µg/mL硒标准液。
硒标准曲线的绘制:取6个具塞玻璃瓶,编号为1~6。分别加入硒标准溶液0、1、2、4、6、8 mL,加水稀释至25 mL。再分别加入5%的EDTA-2Na溶液1 mL,用1:1HCl调pH至2~3。加入0.5% 3,3’-二氨基联苯胺4 mL,摇匀后在暗处放置20 min。用10%的 NaOH调pH至中性,然后加入10 mL的甲苯,振荡2 min,静置10 min后取甲苯萃取层,以甲苯为参比,于波长420 nm处测吸光值。绘制标准曲线。
硒含量的测定:同1)。
3. 结果与讨论
3.1. 硒化壳寡糖和硒化羧甲基壳聚糖的合成
得到的硒化壳寡糖为无定形的黄色粉末,产率为37.26%。得到的硒化羧甲基壳聚糖为无定形的白色粉末,产率为44.78%。
3.2. 红外图谱
从图1~图4可以看出,硒化后壳寡糖的氨基(-NH2)的剪式振动吸收峰由1627.92 cm–1移动到1629.85 cm–1;壳寡糖分子中的羟基(-OH)的变角振动吸收峰由1033.85 cm–1移动到1035.77 cm–1。羧甲基壳聚糖1627 cm–1处的-COOH反对称吸收峰在硒化羧甲基壳聚糖中红移至1599 cm–1;1119 cm–1 处的C-O伸缩振动在硒化羧甲基壳聚糖中红移至1064 cm–1。此外,在硒化壳寡糖和硒化羧甲基壳聚糖的红外光谱中都有位于800 cm–1左右的Se = O双键振动峰。由此可见,硒化壳寡糖和硒化羧甲基壳聚糖制备成功,亚硒酸根连在C2和C6位。

Figure 1. IR spectra of chitooligosaccharide
图1. 壳寡糖的红外吸收光谱图
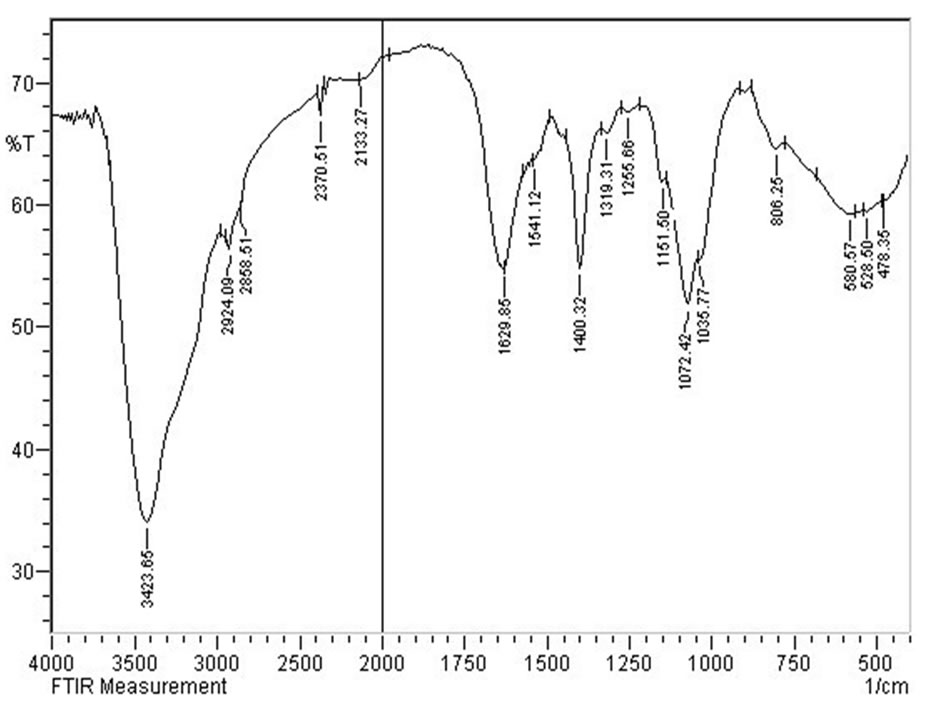
Figure 2. IR spectra of chitooligosaccharide-selenium
图2. 硒化壳寡糖的红外吸收光谱图

Figure 3. IR spectra of carboxymethyl-chitosan
图3. 羧甲基壳聚糖的红外吸收光谱图
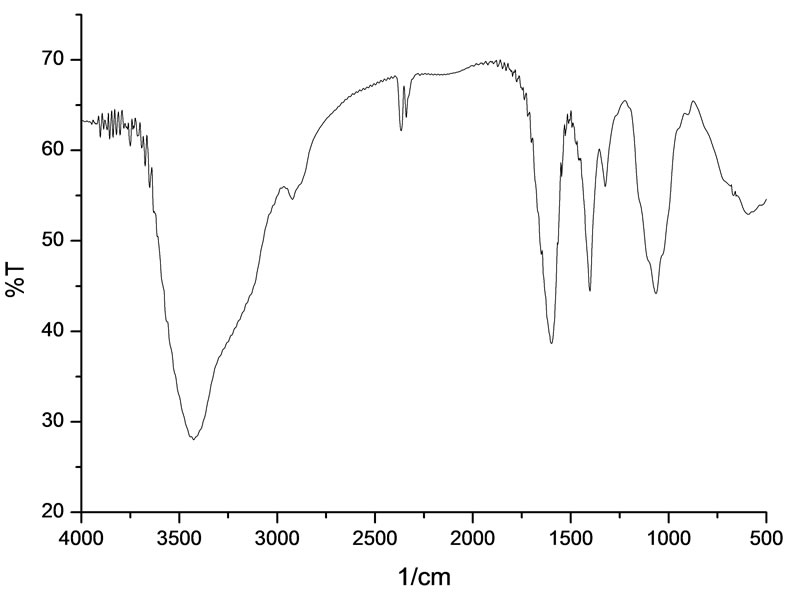
Figure 4. IR spectra of selenium carboxymethyl-chitosan
图4. 硒化羧甲基壳聚糖的红外吸收光谱图
3.3. 硒含量的测定
应用邻苯二胺分光光度法和二氨基联苯胺分光光度法中,得到的硒标准曲线见图5、图6。由标准曲线计算可得,硒化壳寡糖中硒含量分别为9.02 mg/g、8.82 mg/g,硒化羧甲基壳聚糖中硒含量分别为20.50 mg/g、20.24 mg/g。
邻苯二胺和3,3’-二氨基联苯胺在酸性条件下都可以与四价硒反应生成络合物,此络合物分别在335 nm、420 nm波长处有最大吸收,络合物用甲苯萃取,可根据有机层显色程度,进行分光光度法测定。
目前,硒的测定方法主要有荧光分光光度法、原子吸收光谱法、发射光谱法、火焰光度法、中子活化法、火花源质谱法、气相色谱法、阳极溶出伏安法、催化极谱法、氢化物原子荧光光谱法等[9]。但有些方法存在操作繁琐、线性范围窄、灵敏度低、仪器昂贵等缺点,应用受到了限制。本文采用的两种方法仪器易得、操作简单、重复性较好,且两种方法测得的结
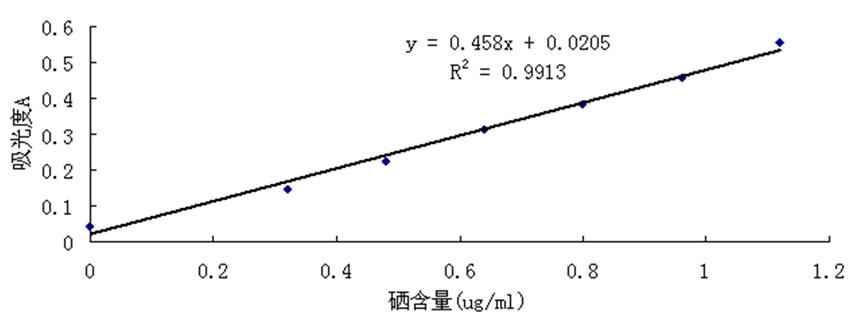
Figure 5. Standard curve of selenium (o-phenylenediamine spectrophotometric)
图5. 硒标准曲线(邻苯二胺分光光度法)

Figure 6. Standard curve of selenium (diaminobenzidine spectrophotometric)
图6. 硒标准曲线(二氨基联苯胺分光光度法)
果较为一致。
4. 结论
本实验分别以亚硒酸钠和壳寡糖、羧甲基壳聚糖为原料,成功合成了硒化壳寡糖和硒化羧甲基壳聚糖,产率分别为37.26%和44.78%。红外光谱分析表明,硒化壳寡糖和硒化羧甲基壳聚糖制备成功,亚硒酸根是连在C2和C6位。
应用邻苯二胺分光光度法和二氨基联苯胺分光光度法测得硒化壳寡糖中硒含量分别为9.02 mg/g、8.82 mg/g,测得硒化羧甲基壳聚糖中硒含量分别为20.50 mg/g、20.24 mg/g。两种方法的测定结果较为一致。
5. 致谢
本实验由国家自然科学基金(21172028),大连民族学院“太阳鸟”项目资助。特此感谢。
参考文献 (References)
[1] 王海青. 壳聚糖及其衍生物的开发及应用[J]. 日用化学工业, 2003, 12(5): 18-22.
[2] 孔涛, 曲韵笙, 朱连勤等. 壳聚糖硒的合成及其理化性质[J]. 安徽农业科学, 2007, 35(1): 21.
[3] 尚德静, 李庆伟, 崔乔等. 灵芝多糖SeGLP-1抗氧化与抗肿瘤作用的研究[J]. 营养学报, 2002, 24(3): 249-251.
[4] 张宏莲, 傅中滇, 陈婉蓉. 硒云芝多糖对小鼠脏器组织及全血抗氧化能力的影响[J]. 上海交通大学学报(农业科学版), 2001, 19(3): 192-194.
[5] 徐春兰, 钦传光, 朱卫宁等. 硒化壳聚糖的制备及其体外抗氧化活性研究[J]. 化学与生物工程, 2009, 26(9): 45-48.
[6] 曲韵笙, 朱连勤. 壳聚糖硒对小鼠的抗氧化作用研究[J]. 青岛农业大学学报(自然科学版), 2009, 26(1): 12-14.
[7] 刘有芹, 杨庆辉, 黄函等. 紫外分光光度法测定枸杞子、陈皮、生姜中硒含量[J]. 理化检验(化学分册), 2010, 46(3): 329-330.
[8] 冯海, 周玲, 汤湛. 硒化壳聚糖中硒含量测定的研究[J]. 饲料广角, 2011, 1: 38-40.
[9] 史丽英. 微量元素硒的测定方法综述[J]. 微量元素与健康研究, 2007, 24 (4): 63-65.
NOTES
#基金项目:国家自然科学基金(21172028);大连民族学院“太阳鸟”项目。