Hans Journal of Chemical Engineering and Technology
Vol.
09
No.
01
(
2019
), Article ID:
28316
,
9
pages
10.12677/HJCET.2019.91001
Effect of Different Salt Solutions on the Conformation of Polyethylene Oxide
Zhihua Meng1,2, Zhihui Zhao2,3*, Yanzhi Xia2,3,4, Lili Wang2,3, Yali Li1,2, Haoliang Zang1,2
1College of Materials Science and Engineering, Qingdao University, Qingdao Shandong
2State Key Laboratory of Bio-Fibers and Eco-Textiles, Qingdao Shandong
3Institute of Marine Biobased Materials, Qingdao University, Qingdao Shandong
4Collaborative Innovation Center of Shandong Marine Biobased Fibers and Ecological Textiles, Qingdao Shandong

Received: Dec. 8th, 2018; accepted: Dec. 22nd, 2018; published: Dec. 29th, 2018

ABSTRACT
The influence of salt concentration on the conformation of poly (ethylene oxide) in dilute solution was studied by using gel permeation chromatograph (TDA-GPC) coupled with differential light scattering and viscosity three detector coupled with dynamic light scattering (DLS) and polyoxyethylene standard sample (PEO-24K) as the research object. By comparing the physical parameters such as intrinsic viscosity (h), hydrodynamic radius (Rh) and Mark-Houwink exponent (a) in different concentration of salt solution, the conformational changes of PEO were obtained: in lower concentration of salt solution, the typical random conformation of PEO was formed; with the increase of salt concentration, the molecular chain of PEO in solution gradually developed. The size of the coil decreases as the coil aggregates, shrinks and collapses, and the conformational change from random coil to densely packed collapse ball occurs. Meanwhile, the solution viscosity increases. This conformational change is mainly due to the reduction of solvation of PEO chains due to the competition between salt molecules in solution and water in PEO solution. The effect of temperature on the conformation of PEO has also been studied. When the temperature decreases, the molecular chain of PEO shrinks from random coils to collapsed spheres.
Keywords:TDA-GPC, DLS, Polyethylene Oxide, Conformation Transition, Solvation
溶液中盐浓度对聚氧化乙烯构象的影响
孟知华1,2,赵志慧2,3*,夏延致2,3,4,王莉莉2,3,李亚莉1,2,臧昊良1,2
1青岛大学材料科学与工程学院,山东 青岛
2生物多糖纤维成形与生态纺织国家重点实验室,山东 青岛
3海洋纤维新材料研究院,山东 青岛
4海洋生物基纤维与生态纺织技术协同创新中心,山东 青岛

收稿日期:2018年12月8日;录用日期:2018年12月22日;发布日期:2018年12月29日

摘 要
采用带有示差、光散射和粘度三检测器联用的凝胶色谱仪(TDA-GPC)和动态光散射(DLS)联用的方法,以聚氧化乙烯标样(PEO-24K)作为研究对象,研究了稀溶液中盐浓度对聚氧化乙烯构象的影响。通过比较在不同浓度的盐溶液中的特性粘数([h])、流体力学半径(Rh)和Mark-Houwink指数(a)等物理参数的大小,得出了PEO的构象变化:在较低盐浓度溶液中,PEO形成典型的无规线团构象;随着盐浓度的增加,溶液中的PEO分子链逐渐发生聚集、收缩、坍塌,线团尺寸减小,并发生由无规线团逐渐向密堆积的坍塌球转变的构象变化,同时溶液黏度增大。这种构象变化主要是由于溶液中的盐分子与PEO竞争溶液中的水分,使得PEO链段的溶剂化程度减少造成的。本文还研究了温度对PEO构象的影响:当温度降低时,PEO分子链发生收缩,由无规线团逐渐收缩为坍塌球。
关键词 :TDA-GPC,DLS,聚氧化乙烯,构象转变,溶剂化

Copyright © 2019 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
聚氧化乙烯(PEO)作为一种传统的聚合物,是一种良好的水溶性聚合物,具有黏度高、絮凝性好和润滑性好的特点 [1] 。人们对PEO稀溶液的构象进行了研究,赵文杰和刘勇刚等人测定了不同分子量的PEO在凝胶色谱中的扩展效应,结果显示PEO的扩展效应随分子量增加而增大,表明长链PEO在水溶液中由于排除体积效应采取溶胀的无规线团构象 [2] 。程熔时等 [3] 研究了PEO水溶液反复冷冻过程的溶剂化效应,发现溶剂化溶剂分子与高分子链结合在一起运动,在色谱过程中与周围的自由溶剂分子相互分离。经查阅大量文献 [4] [5] ,PEO作为表面活性剂等被广泛研究,目前还没有研究报道PEO的构象是否会受到溶液盐浓度的影响。
近年来,随着科学技术的发展,各种测试仪器功能不断完善。凝胶色谱仪(GPC)被广泛应用于高分子的绝对分子量、分子量分布的测定以及稀溶液构象的研究,Guo [6] 等人通过GPC测试了可溶微生物多糖的分子和溶液性质,并通过研究发现GPC测定多糖分子量和特性粘数的有效办法。同时跟传统分子量测试方法相比,GPC操作简单,测试结果更加准确,不用做传统的校正,只需通过一种标准物质对仪器参数进行校正即可进行测试,所以标准样品的稳定性对测试结果显得尤为重要。对于水相,一般采用PEO作为标样,通常水相测试条件是在0.1 mol/L NaNO3中进行,但对于不同样品可能需要不同溶解条件,例如不同盐溶液的浓度。在研究中我们发现,PEO-24K标样的构象会受到溶液盐浓度的影响。另外,动态光散射(DLS)是测定粒径与分布的重要手段。通过DLS测试 [7] [8] [9] [10] 研究了样品浓度对粒径测试的影响,结果显示由于多重散射和颗粒间相互作用的存在,样品浓度对于测试结果有较大的影响,可通过不同样品浓度下的检验、加入适量电介质盐、线性回归法等方法来消除样品浓度对测量结果的影响。本文通过带有示差、黏度和光散射三检测器的GPC (TDA-GPC)与DLS联用研究PEO-24K标样在不同盐溶液中的粒径大小和分布情况,并根据测试结果对其构象进行了分析。
2. 实验部分
2.1. 试剂与仪器
聚氧化乙烯标样(PEO-24K),购自于英国Malvern公司,Mw为23,850,Mn为23,533,IV为0.404。硝酸钠(NaNO3)和硫酸钠(Na2SO4),分析纯,国药集团化学试剂有限公司。溶液均由净水机制备的超纯水(18.2 MΩ∙cm)配制。凝胶色谱与多检测器联用系统由英国Malvern公司的独特的内置进样泵、自动进样器、7˚ (小角)/90˚ (直角)光散射检测器、黏度检测器及示差折光检测器组成,所用色谱柱为Malvern公司的A7 Guard,Aq Guard Col (50 mm × 8.0 mm) 1根和A6000M,General Mixed Aq (300 mm × 8.0 mm) 2根,流动相为质量分数0.1 mol/L NaNO3水溶液,并经过0.22 μm尼龙滤膜过滤,测试时流动相流速为0.7 ml/min。英国Malvern公司纳米粒度仪Zetasizer nano ZSE,激光器的波长为633 nm。阿贝折光仪型号为WYA-2WAJ。乌氏粘度计型号为宁波天恒仪器厂的WSN-1,毛细管为0.4~0.5 mm。
2.2. 实验过程
2.2.1. TDA-GPC
先用0.1 mol/L NaNO3溶液溶解已知分子量和分子量分布的PEO-24K标样,待样品溶解后经0.22 μm滤膜过滤后进样测试,进样量为100 μL。用软件(Malvern Omni SEC 5.12版本)进行数据处理,计算各检测器的仪器常数。分别用0.1 mol/L Na2SO4和0.2 M Na2SO4来溶解PEO-24K标样,保持相同的溶液浓度。对各样品进行测试,每个样品测试两次。测试温度设定为45℃。
2.2.2. DLS
在使用仪器测试过程中需知溶剂的折光指数(RI)、黏度等参数。我们通过阿贝折光仪测定了0.1 mol/L NaNO3,0.1 mol/L Na2SO4和0.2 mol/L Na2SO4等三种溶液的RI,每个样品测试三遍取平均值,结果列入表1。通过乌氏粘度计测定三种溶液的黏度,结果列入表1,每个样品测试三遍取平均值。
Table 1. Refractive index and viscosity of three solvents
表1. 三种溶液的折光指数和黏度
将分别用0.1 mol/L NaNO3,0.1 mol/L Na2SO4和0.2 mol/L Na2SO4溶解的溶液经0.22 μm的滤膜过滤后,注入样品池进行测试。测试温度分别为25℃,35℃和45℃。每次测试之间需要平衡3~5 min,以使温度稳定。数据的收集和处理使用的是Malvern的Zetasizer software版本。
3. 结果与讨论
TDA-GPC
为了精确研究溶液的盐浓度对PEO-24K构象的影响,实验中用分子量分布小于1.02的PEO-24K标样来排除分子量分布对构象的影响,并分别用0.1 mol/L NaNO3,0.1 mol/L Na2SO4和0.2 mol/L Na2SO4作为溶剂来改变溶液的盐浓度(虽然0.1 mol/L NaNO3和0.1 mol/L Na2SO4浓度一致,但0.1 mol/L Na2SO4中的钠离子浓度更大,我们认为其盐浓度增大)。首先对TDA-GPC测试的可靠性进行了验证。图1给出溶解在0.1 mol/L NaNO3中的PEO-24K两次进样的示差折光检测器(RI)曲线,可以看出,两次测试曲线几乎完全重合,说明TDA-GPC测试具有良好的重复性,数据可靠。
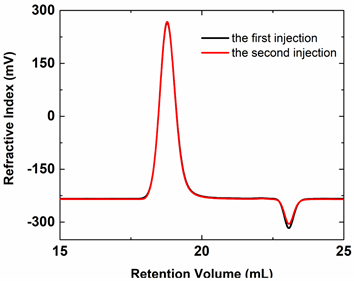
Figure 1. The RI curves of PEO dissolved 0.1 mol/L NaNO3 by repeated injections in by TDA-GPC
图1. 由TDA-GPC两次测得的溶解在0.1 mol/L NaNO3中的PEO标样的RI曲线
同样,两次进样的黏度检测器(DP)、小角光散射检测器(LALS)和直角光散检测器(RALS)的测试曲线也是完全重合的,本实验中所有的TDA-GPC测试样品都是两次进样,且测试结果都具有同样的重复性。
将PEO-24K分别溶解在0.1 mol/L NaNO3、0.1 mol/L Na2SO4和0.2 mol/L Na2SO4中,PEO的浓度保持一致。图2给出三种溶液经由TDA-GPC不同检测器的信号曲线,横坐标表示样品的保留体积(VR),纵坐标表示各检测器信号强度大小。由图2可以看出,在不同溶剂中溶解的PEO的RV值发生了明显变化,且由不同检测器测得的信号曲线展现出了相似的规律:即随着盐浓度的增加,VR值逐渐增大。以RI曲线为例,PEO在0.1 mol/L NaNO3中的出峰位置最早,大约为18 mL,在VR为18.776 mL时达到峰值;在0.1 mol/L Na2SO4中,PEO出峰位置较0.1 mol/L NaNO3略迟,约为18.1 mL,并在VR为18.919 mL时达到峰值。在盐浓度增幅最大的0.2 mol/L Na2SO4中,VR值也出现了较大偏移,19.5 mL时开始出峰,峰值出现在20.8 mL。需要特别注意的是,在0.2 mol/L Na2SO4溶解样品的RI曲线中,PEO的信号峰与在22 mL时开始出现的溶剂信号峰发生部分重叠,这将导致RI积分面积不准,影响各物理量的计算结果。
根据GPC色谱柱的分离原理,高分子在色谱柱填料孔中和孔隙之间分配,尺寸越小的分子更容易进入微孔,在流出色谱柱时其洗脱液的累积体积VR更大。可以推断,造成VR值发生改变的主要原因是不同溶液中PEO的线团尺寸发生了变化。由于所用的PEO为窄分布标样,可以排除分子量分布对线团尺寸变化的影响,因此,我们认为溶液中盐浓度的增大,造成PEO的线团尺寸逐渐减小。
除VR值外,不同样品的信号强度也发生了规律性变化。表2给出图2中各检测器信号峰的积分面积。从表2可以看出,所有检测器的峰面积均随着溶液中盐浓度的增加呈现降低的趋势。其中,RI检测器的峰面积计算公式如下:
(1)
其中KRI为RI检测器的仪器常数,通过标样校正计算得到精确数值;c为溶液浓度,V为溶液的体积,在本实验中均为定值。因此,造成峰面积变化的因素为PEO在溶液的折光指数增量dn/dc。表1结果表明,这三种溶剂的折光指数是递增的,因此,同一个聚合物在这三种溶剂中的折光指数增量应该是递减的,进而造成ARI的逐渐降低。
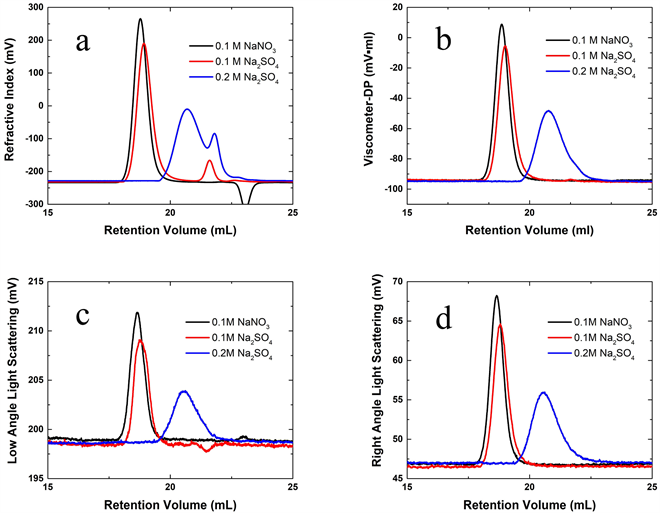
Figure 2. Different detector signal curves of PEO dissolved in three solutions by TDA-GPC, a: signal curve of the RI detector; b: signal curve of viscosity detector; c: the low angle signal curve of the light scattering detector; d: the right angle signal curve of the light scattering detector
图2. PEO溶解在三种溶液中时由TDA-GPC测试得到的不同检测器信号,a:示差检测器信号;b:黏度检测器信号;c:小角光散射检测器信号;d:直角光散射检测器信号
Table 2. Peak area of different signals
表2. 不同信号的峰面积
同理,由光散射信号的计算公式:
(2)
式中,KLS为LS检测器的仪器常数,可以得出造成光散射峰面积降低的因素同样是样品dn/dc的差异。
通过多个检测器的联用,可以计算得到大分子的流体力学半径Rh、Mark-Houwink指数a等跟大分子构象相关的参数。但是0.2 mol/L Na2SO4溶液无法得到计算结果。
TDA-GPC对Rh的计算公式如下:
(3)
其中M为绝对分子量,由RI和LS检测器联用测得;NA为阿伏伽德罗常数。对Rh的计算结果列在表4中。
DLS是测试溶液中颗粒流体力学粒径的更方便快捷的方法。DLS通过检测颗粒的布朗运动速度,记录做布朗运动的颗粒造成的散射光波动随时间的变化,通过累积距法拟合得到颗粒的布朗运动速度,即扩散系数D。然后根据Stokes-Einstein方程 [11] 得到颗粒的粒径信息。计算公式如下:
(4)
其中 为玻尔兹曼常数,T为绝对温度,η为溶液黏度,d为颗粒的流体力学直径。表3给出DLS的计算结果,为方便比较,将测定的直径d转化为半径Rh。DLS测试结果的PDI为0.220左右,结果具有参考性。
Table 3. Rh of PEO in three solvents by DLS and TDA-GPC
表3. 由DLS和TDA-GPC测得PEO溶解在三种溶液中时的Rh值
Table 4. The calculation results of PEO in three different solvents by TDA-GPC
表4. PEO溶解在不同溶液中的TDA-GPC计算结果
由表中看出在不同溶剂中的粒径虽然接近,但是由图2中信号出峰前后可以得出PEO-24K标样溶解在不同溶液中的粒径是不同的,计算结果的差异并不是系统误差,粒径差别是真实存在的。由表4可以看出,TDA-GPC和DLS的计算结果是完全一致的,且每个样品均经过多次重复实验,结果呈现相同的规律性。随着盐浓度的增加,PEO的粒径呈减小趋势。在0.1 mol/L NaNO3和0.1 mol/L Na2SO4中溶解PEO的粒径比较接近,而0.2 mol/LNa2SO4中溶解的PEO的粒径要明显小于前两个溶液,与图2的测试结果一致,Rh的减小对应着图2中样品VR值的增大;且图2中,前两个样品的信号峰的出峰位置也是明显要早于最后一个样品的信号峰的。
溶液黏度信息是了解大分子溶液构象的重要手段。TDA-GPC计算结果中的DP信号强度与溶液黏度有关。TDA-GPC中黏度检测器是通过微分粘度计来检测黏度信号,DP为微分压力传感器测量桥路中点的压力差,IP为入口与出口之间的压力差。由DP和IP可以计算溶液的增比黏度:
(5)
对于低浓度的TDA-GPC样品,根据Huggins-Kramer方程,可以由增比黏度来推算特性黏数[h]:
(6)
该公式的计算过程需要用RI来得到溶液的瞬时浓度,而由于0.2 mol/L Na2SO4溶液的RI与溶剂峰重叠,故而无法进行计算。其它两个溶液的计算结果列在表5中。
用 作图,得到样品的Mark-Houwink曲线(图3),并根据方程:
(7)
得到a值。其中M为绝对分子量,K为Mark-Houwink常数,直线斜率即为a,列在表5中。
Table 5. The particle size of PEO solved in 0.1 M NaNO3 at different temperatures by DLS
表5. 由DLS测得在不同温度下PEO溶解在0.1 M NaNO3得粒径分布
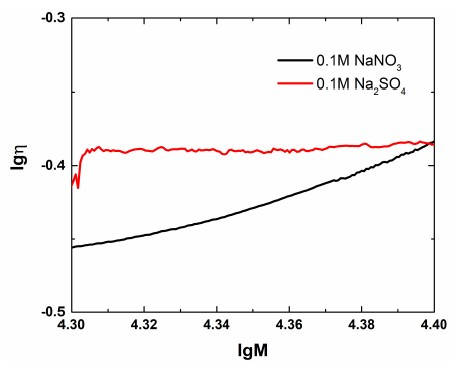
Figure 3. Mark-Houwink curves of PEO dissolved in two solutions by TDA-GPC
图3. 由TDA-GPC测得PEO溶解在不同溶液中的Mark-Houwink曲线
由图3可以看出,两个样品的Mark-Houwink曲线具有较大的差异,说明两个样品的构象差别较大。从图3和表4都可以看出,在低盐溶液中,溶液的[h]值较小,a值则较大;高盐浓度的溶液中,[h]值增大,a值则明显减小。特性黏数[h]代表浓度增加到一定程度时溶液黏度的增加。一般来说,分子量越大,则特性黏数越大。而对于给定的分子链,其特性黏数的变化说明溶液中的分子链构象发生了变化。聚电解质的[h]受到溶液盐浓度的影响 [12] 这一点被广为人知。对于聚电解质来说,在低盐浓度下,随着盐浓度的增大,聚电解质上的电荷部分被屏蔽,由电荷间的静电排斥带来的链伸展逐渐减少,导致其特性黏数逐渐降低。而在我们的实验中,PEO-24K的分子链上不带电荷,且随着盐浓度的增大,PEO的特性黏数明显发生了增大,与聚电解质的变化规律截然相反,因此,其构象变化也应该与聚电解质不同。我们可以通过a值的变化来推断分子链的构象变化:a值可以反映稀溶液中分子链的刚柔性。根据Haug提出的构象三角定律 [13] ,所有大分子的构象都处于密堆积的坍塌球、刚性棒和无规线团这三种极端构象其中的两者之间,而根据Harding等 [14] 提出的构象指数定律,可以通过a值来判断大分子构象,其中坍塌球的a值为0,刚性棒的a值为1.8,无规线团的a值则为0.5~0.8。0.1 mol/L NaNO3中溶解的样品a值为0.764,而0.1 M Na2SO4中溶解的样品a值仅为0.143。因此,我们可以推测,在0.1 M NaNO3中,PEO呈现出典型的无规线团构象;而在0.1 mol/L Na2SO4中,PEO的构象则介于无规线团和密堆积球之间。也就是说,随着盐浓度的增加,溶液中的PEO分子链逐渐发生聚集、收缩、坍塌。
线团到坍塌球的转变往往跟溶剂的溶解性变差有关。聚合物的溶解过程存在溶剂化效应,溶剂扩散到高分子之间,分子链发生解缠解,表现为溶胀,在溶剂分子渗透到一定程度,溶剂和大分子链的相互作用力与大分子链之间的相互作用力达到平衡时,表现为溶解。在水溶液中的大分子链,其四周包裹了一层溶剂化的水分子层,它是溶液中大分子链的实际组成部分。当溶液中的盐浓度逐渐增大时,盐分子与大分子之间发生竞争,浓度逐渐增大的盐分子会结合更多的水分子,使大分子能结合的溶剂化水分子数目减少。Guo等 [15] 报道过聚电解质多糖在高盐浓度的溶液中随盐浓度的增大而发生聚集。PEO是典型的柔性链,在与充足的水分子结合的情况下,其构象表现为无规线团;随着盐浓度的增大,分子链与水的相互作用力逐渐减小,PEO分子链间的相互作用力占主导因素,使得分子链发生聚集,构象由无规线团转变为密堆积的坍塌球,同时,由于分子链周围溶剂化水分子层的减少,使线团Rh减小,VR增大,溶液粘度增大。
接下来,我们还用DLS研究了温度对马尔文PEO标样构象的影响。我们测试了PEO-24K的0.1 mol/L NaNO3溶液在不同温度下的粒径变化,测试结果如图4和表5所示。
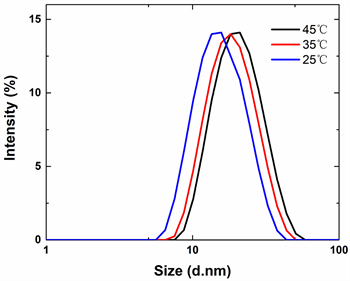
Figure 4. Particle size of PEO solved in 0.1 M NaNO3 at different temperatures by DLS
图4. 由DLS测得在不同温度下PEO溶解在0.1 M NaNO3得粒径分布
测试结果显示,随着温度的降低,PEO的粒径有明显的减小。在35℃时,线团直径(13.3 nm)就已经小于PEO在0.2 mol/L Na2SO4中线团直径(15.51 nm,见表4)。而在25℃时,线团尺寸收缩到10.59 nm。说明PEO分子链随温度下降而发生收缩,由无规线团逐渐收缩为坍塌球。这与传统研究 [16] 的结果是一致的。
4. 结论
采用带有示差、光散射和黏度三检测器联用的凝胶色谱仪(TDA-GPC)和动态光散射(DLS)联用,表明PEO-24K标样在不同浓度的盐溶液中时,它的构象存在明显的差异。随着盐浓度的增加,PEO分子链与水的相互作用力逐渐减小,PEO分子链间的相互作用力占主导因素,使得分子链发生聚集,分子链尺寸减小,溶液粘度增大。PEO在0.1 mol/L NaNO3呈现出典型的无规线团构象,随着盐浓度增加,PEO分子链逐渐发生聚集、收缩、坍塌,在0.1 mol/L Na2SO4中时,PEO的构象则介于无规线团和密堆积球之间。通过DLS测试说明当温度降低时,PEO分子链发生收缩,由无规线团逐渐收缩为坍塌球。
文章引用
孟知华,赵志慧,赵志慧,夏延致,王莉莉,李亚莉,臧昊良. 溶液中盐浓度对聚氧化乙烯构象的影响
Effect of Different Salt Solutions on the Conformation of Polyethylene Oxide[J]. 化学工程与技术, 2019, 09(01): 1-9. https://doi.org/10.12677/HJCET.2019.91001
参考文献
- 1. Luo, Y., Bai, C.K. and Jiang, X.D. (2008) Study of Solution Polymerization of Polyethylene Oxide. Fine Chemicals.
- 2. 赵梓良, 李琦, 薛彦虎, 等. 定量体积排除色谱测定高分子双水相系统的组成和分子量分布[J]. 高等学校化学学报, 2016, 37(1): 167-173.
- 3. 李文波, 薛锋, 程鎔时. 聚乙烯醇水溶液反复冷冻过程中的溶剂化效应[J]. 高分子学报, 2008, 1(12): 1198-1203.
- 4. Werzer, O., Warr, G.G. and Atkin, R. (2011) Conformation of Poly(Ethylene Oxide) Dissolved in Ethylammonium Nitrate. Journal of Physical Chemistry B, 115, 648. https://doi.org/10.1021/jp110216k
- 5. 王冉, 梅花, 任文坛, 等. PEO类聚合物基体的改性及其高性能电解质材料研究的新进展[J]. 材料导报, 2016, 30(11): 63-67.
- 6. Guo, Q. and Chang, S. (2017)Tetra-Detector Size Exclusion Chromatography Characterization of Molecular and Solution Properties of Soluble Microbial Polysaccharides from an Anaerobic Membrane Bioreactor. Frontiers of Environmental Science & Engineering, 11, 16. https://doi.org/10.1007/s11783-017-0922-x
- 7. 左矩. 激光散射原理及在高分子科学中的应用[M]. 郑州: 河南科学技术出版社, 1994.
- 8. 娄本浊, 王少清, 张华东, 等. 光纤式动态光散射系统综述[J]. 光学仪器, 2007, 29(1): 89-94.
- 9. 章宇斌, 齐崴, 苏荣欣, 等. 动态光散射分析不同物化条件下酪蛋白的聚集行为及其胶束尺寸[J]. 分析化学, 2007, 35(6): 809-813.
- 10. 刘俊杰, 国凯. 样品浓度对动态光散射法测量颗粒粒径的影响及分析[J]. 计量技术, 2014(8): 10-13.
- 11. Zhao, C., Chao, Z. and Kang, H. (2017) Gelation of Na-Alginate Aqueous Solution: A Study of Sodium Ion Dynamics via NMR Relaxometry. Carbohydrate Polymers, 169, 206-212. https://doi.org/10.1016/j.carbpol.2017.03.099
- 12. 郁彩红, 虞大红, 秦原, 等. NaCl在聚电解质溶液中活度系数的实验测定[J]. 化工学报, 2001, 52(8): 738-741.
- 13. Harding, S.E., Abdelhameed, A.S. and Morris, G.A. (2010) Molecular Weight Distribution Evaluation of Polysaccharides and Glycoconjugates Using Analytical Ultracentrifugation. Macromolecular Bioscience, 10, 714-720. https://doi.org/10.1002/mabi.201000072
- 14. Fiebrig, I., Vårum, K.M. and Harding, S.E. (1997) Colloidal Gold and Colloidal Gold Labelled Wheat Germ Agglutinin as Molecular Probes for Identification in Mucin/Chitosan Complexes. Carbohydrate Polymers, 33, 91-99. https://doi.org/10.1016/S0144-8617(97)00028-3
- 15. Qian, G., Cui, S.W. and Wang, Q. (2009) Microstructure and Rheological Properties of Psyllium Polysaccharide Gel. Food Hydrocolloids, 23, 1542-1547. https://doi.org/10.1016/j.foodhyd.2008.10.012
- 16. Bauer, D.R. and Ullman, R. (1980) Contraction of Polystyrene Molecules in Dilute Solution below the θ Temperature. Macromolecules, 13, 392-396. https://doi.org/10.1021/ma60074a036
附录
说明:因为在实验中使用的GPC标样价格较贵,且一次配制的样品(10 ml)可以进行多次测试(每次测试只需2 ml),测试结果的重复性好,规律如文中所述。而且在通常测试GPC时会使用0.1 mol/L NaNO3,配制多个浓度的会造成标样浪费。
NOTES
*通讯作者。
