Journal of Advances in Physical Chemistry
Vol.3 No.02(2014), Article ID:13583,5 pages
DOI:10.12677/JAPC.2014.32002
Research on Properties of o-Hydroxyaniline on Copper as Inhibitor
Zhenyu Li1, Yanli Lv1, Mingjun Shan2, Yanqiu Wang1, Wenlin Cao1, Yuandong Chen1
1University of Science and Technology Liaoning, Anshan
2Beijing Normal University, Beijing
Email: 244843538@qq.com
Copyright © 2014 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



Received: Apr. 10th, 2014; revised: May 10th, 2014; accepted: May 17th, 2014
The properties of copper corrosion research were studied by method of adjacent amino phenol in 1 mol/L HCL solution, discussed the dosage, temperature and time on the corrosion performance, and studied the inhibition mechanism of the compound by polarization curves and scanning electron microscopy.
Keywords:o-Hydroxyaniline, Corrosion Inhibitor, Copper

邻氨基苯酚对铜的缓蚀性能研究
李振宇1,吕艳丽1,单明军2,王艳秋1,曹文林1,陈元栋1
1辽宁科技大学,鞍山
2北京师范大学,北京
Email: 244843538@qq.com
收稿日期:2014年4月10日;修回日期:2014年5月10日;录用日期:2014年5月17日

本文通过失重法研究了邻氨基苯酚在1 mol/L盐酸溶液中对铜的缓蚀性能的研究,讨论了用量、温度、时间对缓蚀性能的影响,并通过极化曲线和扫描电镜研究了该化合物的缓蚀机理。
邻氨基苯酚,缓蚀剂,铜

铜合金广泛应用于电子、太阳电池、结构材料、工艺品、货币、工业生产中的热循环系统等领域[1] -[3] 。通常情况下,由于铜合金本身形成的氧化膜,使铜的耐蚀性较好,但在含氧的水、氧化性酸、高浓度Cl−及含有CN−、NH4+的溶液中可形成配位离子,产生较严重的腐蚀[4] -[6] 。资料表明:目前仅海洋工业一项,每年就消耗铜合金10万吨以上,特别是随着电力工业的发展,铜在循环冷却水系统中的应用越来越广泛[7] -[10] 。但铜制换热设备在使用一段时间后,除了服役环境会对其造成一定的腐蚀之外,表面沉积的污垢也会引起腐蚀、阻塞管道,进而降低换热效率。所以,需要对换热设备进行定期的清洗以提高其工作效率[11] -[14] 。所用清洗液一般为酸液,而酸液又会对铜制设备造成严重的侵蚀[15] 。铜设备腐蚀导致的工业生产率下降给人类生活带来极大的危害。因此,对铜防腐蚀方法及其机理进行系统的研究就显得极有必要。
邻氨基苯酚的制备方法主要有:本文采用Pd/C催化下,用水合肼还原邻硝基苯酚制备邻氨基苯酚(反应原理见图1)。
3.1. 实验介质及缓蚀剂浓度
实验介质为1 mol/L盐酸溶液。缓蚀剂浓度分别为0.2 mol/L、0.4 mol/L、0.6 mol/L、0.8 mol/L、1.0 mol/L。同时,以空白进行对比实验。
3.2. 缓蚀效率的测定
缓蚀效率的测定采用失重法。将已称重的试片分别用尼龙细线悬挂于腐蚀介质中,使试片的顶部浸没的缓蚀液面以下,实验的温度为30℃,反应时间为4 h。实验过程中不蒸发,不排污,不补药,用补水的方式维持液面。实验后,用去离子水冲洗试片表面,持续15 s,然后用滤纸擦干其表面的水渍,用橡皮轻轻擦试片表面,去除试片的表面的粘附物质。接下来依次用去离子水、无水乙醇、丙酮分别擦拭试片表面,用吹风机冷风吹干,将其置于干燥器干燥24小时后称重,称重精确到0.0001 g。
4.1. 邻氨基苯酚用量对其缓蚀性能的影响
在30℃,浸入时间4 h,不同浓度的邻氨基苯酚对铜的缓蚀性能实验结果。为便于比较不同缓蚀剂浓度对铜的缓蚀效率的影响,将缓蚀剂浓度和缓蚀效率的关系作图,见图2。缓蚀剂的缓蚀效率采用如下公式计算:
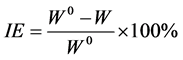
其中W、W0分别为铜在有缓蚀剂和空白盐酸溶液中浸泡4小时后铜因腐蚀造成的质量损失。
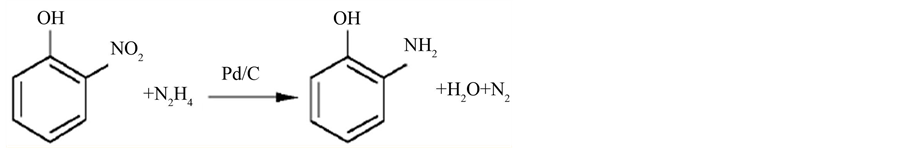
Figure 1. Hydrazine reduction nitrophenol preparation of o-aminophenol reaction principle
图1. 水合肼还原邻硝基苯酚制备邻氨基苯酚反应原理
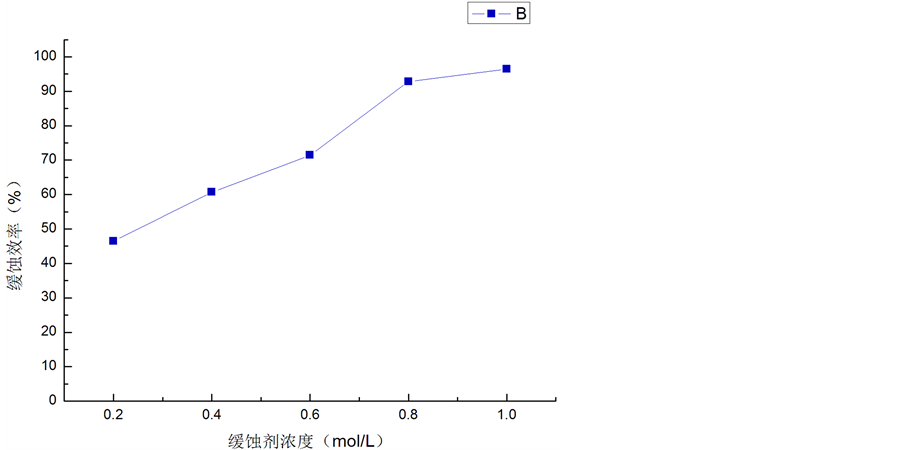
Figure 2. Inhibition efficiency in different corrosion’s concentrations
图2. 不同缓蚀剂浓度下的缓蚀效率
由图2我们可以清晰的看出,温度相同,浸入时间相同,缓蚀剂浓度对铜试样的缓蚀效果影响很大。随着缓蚀剂浓度的增高,铜的腐蚀程度越来越低,缓蚀剂的缓蚀效率依次升高。当邻氨基苯酚浓度达到1 mmol/L时缓蚀效率最高,可达96.55%。
4.2. 时间对其缓蚀性能的影响
在温度30℃、同一缓蚀剂浓度1 mmol/L、不同的浸入时间,邻氨基苯酚作为缓蚀剂对铜的缓蚀性能实验结果。为明确时间对缓蚀效率的影响,反应时间与缓蚀效率的关系见图3。
由图3可以知道,随着反应时间的延长,缓蚀剂的缓蚀效率越来越高,反应6个小时时,缓蚀效率达到最高,最高可达97.73%,但是随着时间的延长,缓蚀剂被消耗完,铜继续跟溶液中的盐酸反应,导致铜的质量减少,根据以上计算公式可知,时间过长将会导致缓蚀效率降低,所以,当时间超过6个小时时,缓蚀剂的效率开始下降。因此,在实际生产过程中若时间超过6小时,应及时向盐酸介质中添加一定量的缓蚀剂,确保生产的正常进行。
4.3. 温度对缓蚀性能的影响
在相同反应时间4 h、缓蚀剂浓度1 mmol/l,不同反应温度下,缓蚀剂对铜的缓蚀效率。为了更好的反应温度对缓蚀效率的影响,将不同温度下的缓蚀效率作图,见图4。
由图4可以看出,随着温度的升高,缓蚀效率逐渐降低。温度升高,铜的腐蚀速率加剧,通常认为
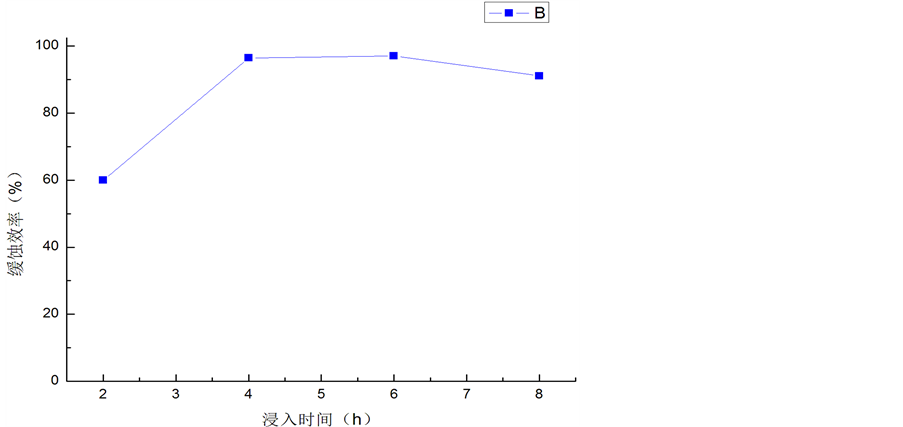
Figure 3. Inhibition efficiency in different time
图3. 不同时间对应的缓蚀效率

Figure 4. Relationship with the inhibition efficiency of the reaction temperature
图4. 反应温度与缓蚀效率的关系
这是缘于温度的升高使得腐蚀的Cu2+由于分子的热运动加剧加速了脱离铜表面进入到腐蚀介质中,缓蚀剂在铜表面的吸附减少,增大了腐蚀介质与金属作用的表面积,从而使得腐蚀速率加快,腐蚀环境温度的升高使得缓蚀剂效率降低,温度对缓蚀剂的影响也取决于缓蚀剂的品种。
4.4. 腐蚀形貌分析
铜试片在盐酸中浸泡前已经进行实验前处理。
处理后的试片样品在没有添加缓蚀剂的1 mol/L盐酸以及添加1 mmol/L邻氨基苯酚的盐酸溶液中同时恒温浸泡4小时。利用扫描电镜观察其表面的腐蚀情况,见图5。
 (a)
(a) (b)
(b) (c)
(c)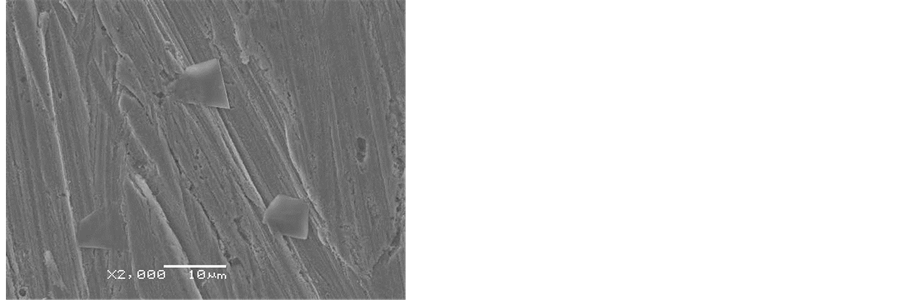 (d)
(d)
Figure 5. The surface morphology of copper what is immersed in the solution of 1 mol/L HCl after 4 hours; (a) and (b) are rot surface topography which copper without inhibitor; (c) and (d) are rot surface topography which copper in O-aminophenol
图5. 浸泡在1mol/L盐酸溶液中腐蚀4小时后的表面形貌;(a),(b)为未添加缓蚀剂的空白盐酸溶液中的腐蚀形貌;(c),(d)为添加邻氨基苯酚后的腐蚀形貌
从图5(a),图5(b)中发现,铜表面形貌已被严重腐蚀,且其表面呈现出无规则的蚀坑,从表面的粗糙程度来看铜表面发生了的典型均匀腐蚀现象,这表明浸泡在空白盐酸溶液中4小时后的铜试片表面发生了剧烈的腐蚀反应使得试样表面受到非常严重的腐蚀。而浸没在1 mmol/L邻氨基苯酚中的铜试片与空白盐酸中的腐蚀4小时的表面形貌相比较,添加了缓蚀剂的溶液中铜试片基体未发生严重的腐蚀,表面加工打磨的痕迹仍然清晰可见,试样表面平整有光泽。同腐蚀体系中未加缓蚀剂的腐蚀试样表面相比其腐蚀程度已大大减缓,说明加入的缓蚀剂邻氨基苯酚分子在盐酸介质中在铜表面形成了一层致密的缓蚀剂吸附层,从而使得铜试样表面和腐蚀介质盐酸的接触点减少,抑制了铜溶解反应的活性点,提高了反应活化能位垒,从而很好的抑制了铜试样的腐蚀,起到了非常好的保护效果。
1) 邻氨基苯酚缓蚀剂在1 mmol/L盐酸介质中对金属铜具有良好的缓蚀性能。
2) 邻氨基苯酚在酸性介质中缓蚀时间可以达到6小时。
3) 通过Langmuir吸附等温线分析,邻氨基苯酚在铜的表面符合Langmuir吸附;通过ΔG0的计算,邻氨基苯酚在铜表面属于化学吸附;扫描电镜的结果与失重法具有一致性。
- [1] Ravichandran, R., Nanjundan, S. and Rajendran, N. (2004) Effect of benzotriazole derivatives on the corrosion of brass in NaCl solutions. Applied Surface Science, 236, 241-250.
- [2] 董泉玉, 张强, 李锐等 (2003) 国内铜缓蚀剂的最新发展现状. 全面腐蚀控制, 17, 19.
- [3] Ravichandran, R., Nanjundan, S., et al. (2005) Corrosion inhibition of brass by benzotriazole derivatives in NaCl solution. Anti-Corrosion Methods and Materials, 52, 226.
- [4] Ravichandran, R. and Rajendran, N. (2005) Influence of benzotriazole derivatives on the dezincificationof 65-35 brass in sodium.
- [5] 赵永生等 (2002) 咪唑及其衍生物作为铜的盐酸酸洗缓蚀剂的量子化学研究. 北京化工学学报, 29, 53.
- [6] 付占达, 芮玉兰, 周坤 (2007) 含盐体系中有机铜缓蚀剂及缓蚀机理研究进展. 化工生产与技术, 14, 38.
- [7] 张秀娟, 刘瑞泉, 王献群 (2008) 碱性介质中POTAS和PDTAS对铜的缓蚀作用. 物理化学学报, 24, 338-344.
- [8] 王献群, 刘瑞泉, 朱丽琴等 (2007) 碱性介质中BIT, BIOHT和BIMMT对铜的缓蚀性能和吸附行为. 物理化学学报, 23, 21-26.
- [9] 付占达, 王海涛, 苗玉兰等 (2007) 国外海水及模拟海水中铜缓蚀剂的最新研究进展. 清洗世界, 23, 21-26.
- [10] 于静敏, 陈学清, 付占达 (2007) 海水及模拟海水介质中铜缓蚀剂缓蚀机理的研究进展. 清洗世界, 23, 5-11.
- [11] 徐杰群, 刘小华, 刘月丽等 (2001) Na2WO4和BTA复配对铜缓蚀性能的研究. 腐蚀与防护, 22, 424-425.
- [12] 张娟, 李周, 陈畅等 (2008) BTA及其复配铜缓蚀剂的研究进展. 材料导报, 22, 83-85.
- [13] 张万友, 王冰, 廖强强等 (2001) BTA系列Cu缓蚀剂的电化学行为. 腐蚀科学与防护技术, 13, 263-266.
- [14] 徐杰群, 周国定, 陆柱等 (1998) 交流阻抗法对几种铜缓蚀剂比较研究. 华东理工大学学报, 24, 324-328.
- [15] 贾艳霞, 谷宁, 李春梅 (2008) 硫酸溶液中聚天冬氨酸对铜的缓蚀作用. 河北北方学院学报, 24, 39-42.