Asian Case Reports in Veterinary Medicine
Vol.05 No.03(2016), Article ID:18044,5
pages
10.12677/ACRPVM.2016.53004
Establishment of Skin Scald Model in Mice
Jingjing Kang, Zhe Jiao, Bowei Su, Jinhua Zhang, Huiping Li
Department of Veterinary Medicine, Henan University Animal Husbandry and Economy, Zhengzhou Henan

Received: Jun. 30th, 2016; accepted: Jul. 15th, 2016; published: Jul. 22nd, 2016
Copyright © 2016 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
To establish an animal model in mice for the drug development with skin scald. After the anesthetization BABL/c mice were scalded in a 1 cm-diameter circle area on the dorsum by boiling water at contact time 10 s. The mice were sacrificed at 1, 7, 14 and 21 days after scald. The skin samples were collected and analyzed by histopathological examinations. Histological observation showed a II degree injury involving full-thickness skin in the 1 d mice group. Tissue necrosis and inflammatory reaction were observed in the 7 d mice group. Granulation tissue hyperplasia began to appear in the 14 d and 21 d mice group. All the results showed that a mice skin scald model was successfully established which is stable and can be used on the drug development for the damaged skin in future research.
Keywords:Mice, Skin, Scald, Animal Model

小鼠皮肤烫伤模型的建立
康静静,焦哲,苏博威,张金花,李慧平
河南牧业经济学院(龙子湖校区)动物医学院,河南 郑州

收稿日期:2016年6月30日;录用日期:2016年7月15日;发布日期:2016年7月22日

摘 要
建立用于皮肤烫伤修复药物研发的动物模型。将20只实验组BALB/c小鼠麻醉后,分别用沸水(接触时间为10 s)在小鼠背部烫出直径1 cm的圆形烫伤区,烫伤后1、7、14和21 d处死小鼠,取其损伤皮肤进行组织学的观察。组织学观察发现烫伤1 d的小鼠皮肤全层组织细胞发生水肿,符合Ⅱ度烫伤特点,7 d时小鼠皮肤组织细胞发生坏死并出现炎性反应,14 d和21 d时烫伤皮肤处开始出现增生肉芽组织。所有数据均表明本研究采用简单的方法成功制作出较为稳定的皮肤烫伤模型,从而为后续进行皮肤烫伤药物的开发奠定了一定的理论基础。
关键词 :小鼠,皮肤,烫伤,动物模型

1. 引言
临床实际中,为了研发一种效果良好的皮肤烫伤修复药物,必须要先弄清楚皮肤烫伤的发生发展过程。已知皮肤烫伤是临床医学实践中常见的一类皮肤损伤 [1] ,因此建立一个稳定、简便、重复性良好且经济的实验性皮肤烫伤动物模型,就有助于评价所研发药物对烫伤皮肤的修复效果。目前,用于建立皮肤烫伤模型的动物多为大鼠、豚鼠、犬、猪和灵长类等,关于小鼠烫伤模型的描述则相对较少 [2] 。本研究拟通过克服既往皮肤烫伤模型的一些不足,建立一种能够控制烫伤面积和烫伤程度的简单易操作的小鼠皮肤烫伤模型,并对其病理变化做出描述,从而为皮肤烫伤修复药物的研发及药效评价提供重要的临床材料和理论基础。
2. 材料与方法
2.1. 实验动物及分组
BALB/c小鼠25只,购自郑州大学实验动物中心[SCXK(豫)2010-0002],雌雄随机,体重为18~20 g,清洁级饲养。按实验设计需将小鼠分为皮肤烫伤组和正常对照组,其中烫伤组20只,正常对照组5只,其中再按烫伤后观察时间将皮肤烫伤组分为烫伤后1、7、14、和21 d 4个亚组,每组5只小鼠。将小鼠编号后,按照分组设计每5个编号为一组,每组放入一个鼠笼喂养,再将鼠笼编号为1、2、3、4、5,其中1号笼为正常对照组,2~5号笼为皮肤烫伤组的4个亚组。本研究经河南牧业经济学院实验动物伦理委员会批准进行。
2.2. 皮肤烫伤模型的制作
参照任鹏等 [1] 研究中所用的实验方法,我们根据现有实验条件稍加改良,具体如下:剪去小鼠背部皮肤毛发(注意在此过程中不伤及皮肤),乙醚浅麻醉后,将其四肢固定在操作板上,暴露背部皮肤,并保持平坦。室温下,将两端无堵头、内直径为1 cm的中空塑料管直立于小鼠背部,其一端与小鼠备皮处皮肤紧密接触(接触压力保证水不流出且不对皮肤造成机械损伤),另一端用预热后的注射器快速向塑料管内注入100℃的沸水(2 mL)。沸水与皮肤持续接触10 s (经检测,水温基本无变化)后,迅速将操作板及小鼠连同中空管翻转,将热水从塑料管上口倒出,此时可见烫伤区域为直径l cm的圆形。伤后小鼠分笼饲养,保证垫料干燥清洁,通风良好,给予充足的饲料和饮水。对照组小鼠背部皮肤剪毛后,用室温蒸馏水代替沸水,按损伤组操作步骤处理。
2.3. 组织病理学观察
按预先设定时间分别将皮肤烫伤组小鼠和实验对照组小鼠麻醉后处死,取背部烫伤部位及周边区域1.5 cm × 1.5 cm大小皮肤,固定于10%福尔马林中,然后按照常规石蜡切片制作方法进行切片制作,切片厚度为4 μm,H&E染色后,在显微成像系统下观察烫伤小鼠皮肤的组织病理学变化,以及烫伤后不同时间小鼠烫伤皮肤的愈合情况。
3. 组织学观察结果
3.1. 对照组小鼠皮肤的组织学结构
皮肤全层完好,角质层存在,棘细胞层结构清晰,真皮内胶原纤维排列整齐,毛囊及皮脂腺结构清晰(见图1)。
3.2. 烫伤组小鼠皮肤的组织学结构
烫伤后1 d,烫伤部位表皮细胞发生坏死,毛囊、皮脂腺等皮肤附属结构坏死,真皮胶原纤维明显肿胀,排列紊乱,血管扩张明显且充血,由于细胞崩解坏死而出现空泡,无明显炎性细胞浸润(图2(a))。
烫伤后7 d,烫伤创面出现较薄的肉芽组织层,其中有少量新生毛细血管和成纤维细胞,表皮细胞增殖不活跃,真皮内有坏死组织,有炎性细胞浸润(图2(b));
烫伤后14 d,烫伤创面处的肉芽组织迅速增殖,创面边缘开始收缩,并出现再上皮化,烫伤交界处可见多量炎性细胞浸润,创面中间部位也可见较多的新生毛细血管和排列整齐的成纤维细胞,但尚未出现上皮样结构(图2(c));
烫伤后21 d,可见烫伤创面平直,边缘部分已基本修复完全,被覆复层鳞状上皮,角化明显,表皮下为排列整齐的成纤维细胞和胶原纤维,有少量炎性细胞浸润(图2(d))。
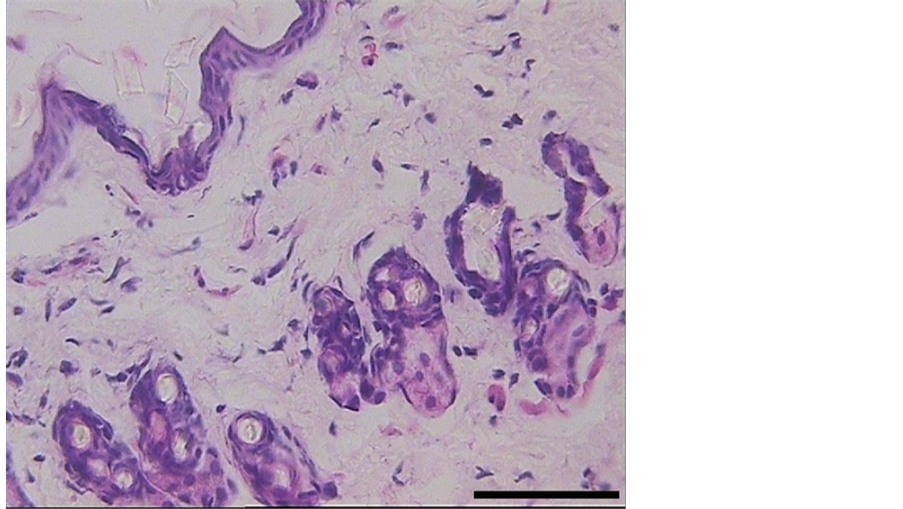
Figure 1. Histological structure of skin in control group mice (H&E) Scale bar = 100 μm
图1. 对照组小鼠皮肤组织学结构(H&E)标尺 = 100 μm
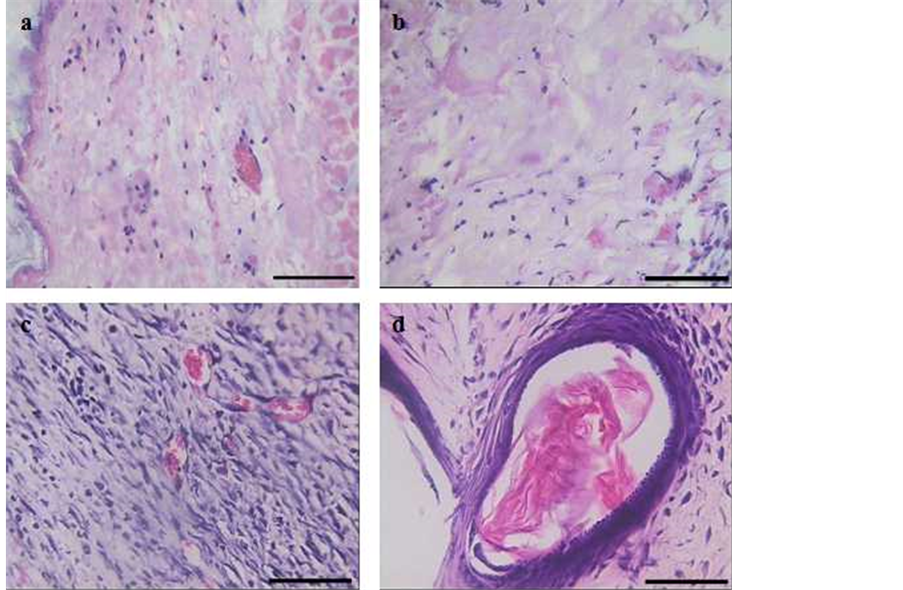
Figure 2. Histological structure of skin damage mice (H&E) Scale bar = 100 μm
图2. 烫伤组小鼠皮肤组织学结构(H&E)标尺 = 100 μm
4. 结论与讨论
临床实践中要想客观地评价和比较皮肤烫伤药物的修复作用,皮肤烫伤动物模型的建立是一个至关重要的环节。目前已知的比较理想的烫伤药物评价模型是II度烧烫伤动物模型 [3] ,因为II度烫伤所造成的损伤程度适中,损伤可达真皮乳头层,损伤部分网状层及皮肤附件,愈合周期在20 d左右,能够明显区分皮肤损伤药物的疗效。经过病理组织学的观察发现,本研究所建立的小鼠烫伤皮肤模型完全符合II度烫伤的组织学特点,能够用于后续的烫伤药物评价试验。
皮肤烫伤动物模型能否成功建立,取决于皮肤烫伤面积的大小和造成烫伤的时间长短是否一致。除此之外,还与使用的烫伤方法、烫伤物质、烫伤物与皮肤接触的压力等因素有关。过往的研究者曾经使用混合固体燃料或酒精涂抹皮肤点燃烧伤建立烫伤动物模型 [2] [4] 或使用预热的金属进行烫伤 [5] 。但是,上述方法所建立的皮肤烫伤模型存在一定的缺陷,比如燃料烧灼皮肤的温度不恒定且无法测量,烫伤时间和烫伤面积不易控制等,而这些缺陷都会直接影响烫伤药物修复作用的评价结果。本研究采用沸腾的蒸馏水作为烫伤物质 [6] 制作小鼠皮肤烫伤模型,利用秒表控制烫伤的时间,利用中空塑料管保证烫伤面积的一致性,通过控制注入中空塑料管内热水的高度保证烫伤物与皮肤接触压力的恒定。为了保证烫伤模型的成功建立,制作模型时需要在温度较为恒定的实验室进行,随着损伤时间的延长,热水的温度会略有降低,从而对损伤结果有所影响。在剪毛过程中,为了避免损伤毛囊等附属器和表皮结构的完整性,尽量使用小剪刀剪短小鼠背部毛发。
总之,采用本方法所建立的小鼠皮肤烫伤模型具有烫伤程度和烫伤面积稳定,重复性好,操作简便等优点。通过观察模型中小鼠皮肤的组织学结构变化特点,掌握了皮肤烫伤以后的自然修复过程,从而为进一步研发皮肤烫伤药物及评价药物的修复作用提供了理论依据。
基金项目
河南牧业经济学院大学生科技创新项目(KJCX201409)。
文章引用
康静静,焦 哲,苏博威,张金花,李慧平. 小鼠皮肤烫伤模型的建立
Establishment of Skin Scald Model in Mice[J]. 亚洲兽医病例研究, 2016, 05(03): 15-19. http://dx.doi.org/10.12677/ACRPVM.2016.53004
参考文献 (References)
- 1. 任鹏, 官大威, 赵锐, 等. 小鼠皮肤烫伤模型的建立[J]. 法医学杂志, 2012, 28(2): 92-94.
- 2. 褚锋, 刘建国, 唐帆, 等. 小鼠烧伤模型的复制及皮肤病理形态改变的动态观察[J]. 中国实验动物学报, 2009, 17(3): 10-12.
- 3. 蔡斌, 范尚坦, 张勇, 等. 深Ⅱ度兔子烫伤模型的建立[J]. 中国比较医学杂志, 2010, 20(7): 10-12.
- 4. 侯敏娜, 平大地. 混合燃料建立大鼠火焰烧伤模型的实验研究[J]. 云南中医中药杂志, 2010, 31(8): 67-68.
- 5. Singer, A.J., McClain, S.A., Romanov, A., et al. (2007) Curcumin Reduces Burn Progression in Rats. Academic Emergency Medicine, 14, 1125-1129. http://dx.doi.org/10.1111/j.1553-2712.2007.tb02330.x
- 6. Lee, J.A., Jeong, H.J., Park, H.J., et al. (2011) Acupuncture Acce-lerates Wound Healing in Burn-Injured Mice. Burns, 37, 117-125. http://dx.doi.org/10.1016/j.burns.2010.07.005