Hans Journal of Chemical Engineering and Technology
Vol.
12
No.
06
(
2022
), Article ID:
58383
,
10
pages
10.12677/HJCET.2022.126055
钯基催化制备具有活性基团取代的苯基硼酸
魏开举*,伍敏志,陈重铭,任明秀
中国科学技术大学苏州高等研究院,江苏 苏州
收稿日期:2022年10月17日;录用日期:2022年11月21日;发布日期:2022年11月28日

摘要
活性基团取代的苯基硼酸是新型电子材料、医药和农药的重要中间体,其制备研究既具备重要的科学意义,又具备实际的工业生产价值。本文基于Suzuki-Miyaura交叉偶联反应,以活性取代苯为原料,实现了在CH3COOK为碱,[(C6H5)3P]2PdCl2为催化剂的条件下与联硼酸频那醇酯在适宜溶剂协同作用下,获得高收率活性基团取代的苯硼酸频那醇酯,并进一步水解获得对应硼酸化合物,该催化反应特别是对硝基、羰基、酯基的催化效果极好,产品收率可达90%以上。该催化反应是一类优异的准备芳基硼酸衍生物的方法。
关键词
偶联反应,钯催化,芳基硼酸

Palladium-Catalyzed Preparation of Phenylboric Acid with Active Groups
Kaiju Wei*, Minzhi Wu, Chongming Chen, Mingxiu Ren
Suzhou Institute for Advanced Research, University of Science and Technology of China, Suzhou Jiangsu
Received: Oct. 17th, 2022; accepted: Nov. 21st, 2022; published: Nov. 28th, 2022

ABSTRACT
Phenylboric acid substituted by active groups is an important intermediate of new electronic materials, medicine and pesticides. Its preparation has important scientific significance and practical industrial production value. In this paper, based on the Suzuka-Miyaura cross-coupling reaction, with active substituted benzene as raw material, under the condition of CH3COOK as base, [(C6H5)3P]2PdCl2 as catalyst and biboratefenalyl ester under the synergic action of suitable solvent, the high yield of active group substituted fenalyl phenyl ester was obtained. The boric acid was further hydrolyzed to obtain the corresponding boric acid compound. The catalytic reaction, especially for nitro group, carbonyl group and ester group, was very good, and the yield of the product could reach more than 90%. This catalytic reaction is an excellent method for preparing arylboric acid derivatives.
Keywords:Coulping Reaction, Palladium Catalyst, Phenylboric Acid

Copyright © 2022 by author(s) and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY 4.0).
http://creativecommons.org/licenses/by/4.0/


1. 引言
活性基团取代的苯基硼酸是一类具有容易参加化学反应的官能团取代的芳基硼酸衍生物,如氰基、酯基、硝基取代苯硼酸,其是新型电子材料、医药和农药的重要中间体 [1] [2],如硝基苯硼酸,氰基苯硼酸 [3] 合成联苯衍生物 [4]。与惰性基团取代芳基硼酸相比,活性基团可以更直接、更方便地引入到目标产物中,在某些特殊化合物的应用中具有重要意义。取代苯基硼酸(或其酯)通常采用有机锂 [5] 或Grignard [6] 试剂和催化硼化法制备 [7]。然而,传统的硼酸制备方法不适合于活性基团取代芳基硼酸的合成,因为有机锂或格氏试剂很容易与活性基团发生反应,产生大量副反应的存在。另一方面,传统有机锂或格氏试剂方法一般需要在低温下进行,局限性较大,且设备和原材料成本昂贵,操作风险高 [8],其适用于实验研究,大规模工业生产显然没有优势。
通过邻硝基苯硼酸的合成研究,探索适合工业化生产的制备方法,并进一步拓展到一系列活性基团取代的苯基硼酸衍生物的制备。不同于发烟硝酸直接硝化苯硼酸 [9] 或通过格氏试剂交换 [10] 制备,本论文的研究是基于钯催化硼化的方法,通过催化剂的筛选与协同试剂与溶剂的作用,先制备邻硝基苯硼酸频哪醇酯(见图1),然后水解得到硼酸产物(见图2)。以邻溴硝基苯和双(频哪醇合)二硼为原料,详细地对催化剂、溶剂、碱进行筛选,并进一步优化其参数:反应温度、反应时间、摩尔比例等,形成了极具工业生产价值的合成方法,并将其方法拓展到类似化合物的制备中。
2. 实验部分
2.1. 仪器和试剂
常规制备设备,安捷伦HPLC1260高效液相色谱仪。
甲苯,1,4-二氧六环,石油醚,DMF,IPA,CH2Cl2,(CH3)2O,CH3(CH2)4CH3,Et2O,EtOAc,Pd/C (10%),PdCl2,PdCl2(pddf),[(C6H5)3P]2PdCl2,TBAB,邻溴硝基苯,邻氯硝基苯,邻碘硝基苯,双(频哪醇合)二硼,对碘苯乙酮,对溴苯甲腈,对碘苯甲酸甲酯,2,4-二硝基氯苯,邻溴苯胺,对溴苯甲酸均购于阿拉丁试剂有限公司。K3PO4,K2CO3,CH3COOK均购于国药基团。以上试剂均为分析纯。
2.2. 邻硝基苯硼酸频哪醇酯的合成

Figure 1. Synthesis of o-nitrophenylboronic acid pinacol ester
图1. 邻硝基苯硼酸频哪醇酯的合成
在10 mL的Schlenk管中,将邻溴硝基苯0.202 g (1.0 mmol)、双(频哪醇合)二硼0.330 g (1.3 mmol)、[(C6H5)3P]2PdCl2 0.0035 g (0.5% mmol)、CH3COOK 0.294 g (3.0 mmol)、TBAB (四丁基溴化铵) 0.0645 g (0.2 mmol)和干燥的1,4-二氧六环(2 mL)置于氮气气氛下。将反应混合物在油浴中加热至规定温度,持续搅拌4小时,然后冷却至室温。反应混合物在烧结过滤漏斗中通过硅藻土塞过滤,然后用EtOAc洗涤。有机相采用无水MgSO4干燥,减压脱除溶剂得到粗产物,以CH3(CH2)4CH3和EtOAc为洗脱剂,以5:1的比例分别用硅胶柱层析纯化。获得产物邻硝基苯硼酸频那醇酯。
2.3. 2-硝基苯硼酸频哪醇酯两步脱保护步骤
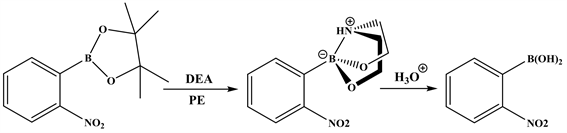
Figure 2. Two step deprotection of 2-nitrophenylboronic acid pinacol ester
图2. 2-硝基苯硼酸频哪醇酯两步脱保护步骤
在10 mL的Schlenk管中,将邻硝基苯硼酸频那醇酯0.249 g (1.0 mmol)、乙二醇胺0.315 g (3 mmol)、石油醚(5 mL)置于氮气气氛下。室温持续搅拌5小时,然后冷却至室温。用2N HCl调节至pH为弱酸性,除去溶剂获得产物邻硝基苯硼酸(见图2)。
3. 结果与讨论
3.1. 催化剂及其用量对偶联反应影响的研究
Table 1. Investigation of catalysts and its dosage effects on the coupling reaction
表1. 催化剂及其用量对偶联反应影响的研究
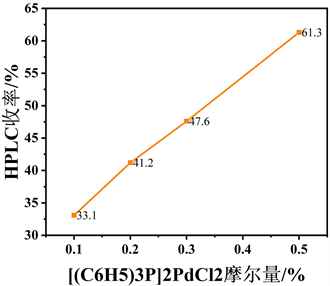
Figure 3. [(C6H5)3P]2PdCl2 molar quantity comparison diagram
图3. [(C6H5)3P]2PdCl2摩尔量对比图
催化剂是反应体系的核心研究内容,通过使用多种催化剂的实验研究:如,Pd/C (10%),PdCl2,PdCl2(pddf)和[(C6H5)3P]2PdCl2进行了催化剂性能筛选研究(见表1)。观察到0.2 mol%的[(C6H5)3P]2PdCl2 (见表1路径5)与1 mol%的PdCl2 (pddf) (见表1路径3)的产率近乎相同,较高的转化,是一种较好的催化剂,显然助催化剂的作用在偶联反应体系较传统无机盐催化效率明显较好,因为[(C6H5)3P]2PdCl2的富电子体系对此反应的催化效果更佳 [11]。通过0.1、0.2、0.3、0.5 mol%等不同用量下的平行反应(见图3),生成产物邻硝基苯硼酸频那醇酯的产率分别为33%、41.2%、47%和61% (见表1)。显然催化剂越多转化效果越好,但并不是线性关系,综合经济成本因素,0.5 mol %的[(C6H5)3P]2PdCl2用量较为合适。
3.2. 碱和相转移催化剂TBAB对偶联反应影响的研究
Table 2. Investigation of base and TBAB effects on the coupling reaction
表2. 碱和TBAB对偶联反应影响的研究
基于以上反应,进一步研究碱、相转移催化剂TBAB的作用(见表2)。通过磷酸钾、碳酸钾、乙酸钠、乙酸钾(见图4)的实验,CH3COOK在当量(见表2路径1、2、3、5、8)和产率方面明显优于其它碱,在无水体系效果更为明显,其转化反应可以达到90%以上。另一方面,由于体系是非均相反应,相转移催化剂的加入非常重要,在该类反应中采用TBAB作为相转移催化剂。当反应在无TBAB时,生成邻硝基苯
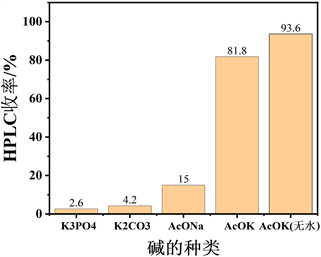
Figure 4. Effect of the type of base on the reaction
图4. 碱的种类对反应的影响
硼酸频那醇酯酯的产率较差(见表2路径6)。当TABA的数量从0.1当量增加到0.2当量时,分别获得60.7%和81.8%的产率(见表2路径7、8)。当使用无水CH3COOK作为反应的碱时,反应产率更是达到93.6% (见表2路径8、9)。故应使用3当量无水CH3COOK作为碱,0.2当量的TBAB作为相转移催化剂来进行此步反应。
3.3. 溶剂及其用量对偶联反应的影响
Table 3. Effect of solvent and its dosage on the coupling reaction
表3. 溶剂及其用量对偶联反应的影响
 (a)
(a)
 (b)
(b)
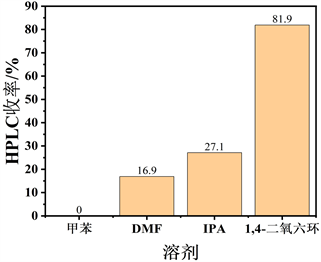
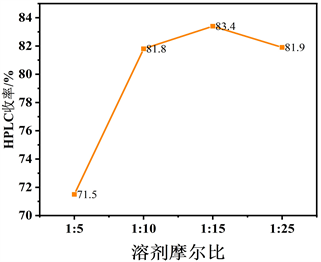
Figure 5. Influence of solvent and molar ratio on coupling reaction
图5. 溶剂及其摩尔比对偶联反应的影响
催化反应是个综合系统作用,为了探究溶剂的影响,采用各种不同极性溶剂对反应效果进行研究(见图5):如甲苯、DMF、IPA、1,4-二氧六环等在CH3COOK (无水)下进行偶联反应(见表3)。当反应在甲苯中进行时,反应几乎不能进行(见表3路径1)。使用极性溶剂DMF、IPA和1,4-二氧六环,反应产率分别为16.9%、27.1%和81.9% (见表3路径2、3、4)。显然,1,4-二氧六环是较好的选择。进一步,优化了底物与溶剂的摩尔比例为1:5~1:25 (见图5)。研究发现,在1:10到1:25之间(见表3路径4~6),溶剂的变化量对反应结果影响不大,但在1:10以下,反应结果急剧下降。因此,在已选择的体系中,该反应的最佳溶剂体系为1,4-二氧六环,底物与溶剂摩尔比为1:15为宜,这也再次证明了反应体系的系统性催化的协同作用,不仅仅是一个溶剂。
3.4. 双(频哪醇合)二硼、反应温度和反应时间对偶联反应的影响
Table 4. Investigation of B2Pin2, reaction temperature and reaction time effects on the coupling reaction
表4. 双(频哪醇合)二硼、反应温度和反应时间对偶联反应的影响
 (a)
(a)
 (b)
(b)
 (c)
(c)
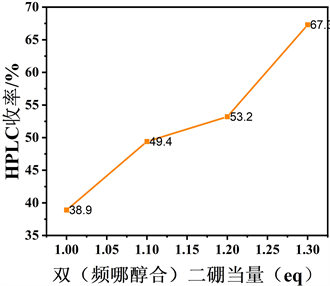
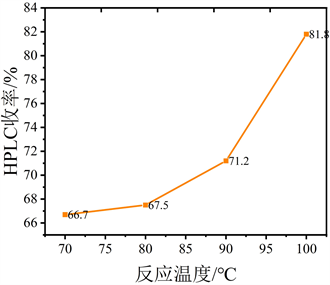
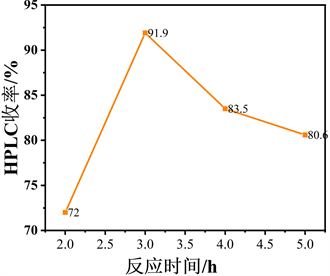
Figure 6. Investigation of B2Pin2 equivalent, reaction temperature and reaction time effects on the coupling reaction
图6. 双(频哪醇合)二硼当量、反应温度和反应时间对偶联反应的影响
为了确定双(频哪醇合)二硼的适宜浓度、最佳温度和反应时间,我们进行了一系列对照实验(见图6)。研究发现,当双(频哪醇合)二硼的量增加到1.3当量时,邻溴代苯可以完全反应(见表4路径1~4)将所得结果应用于最优条件,得到了相同的结论。此外,随着反应温度从70℃升高到100℃产物产率逐渐增加(66.7%到81.8%) (见表4路径5~8)。此外,反应时间对产率影响不大,4 h为最佳(见表4路径9~12)。
3.5. 溶剂、二乙醇胺当量、反应时间对2-硝基苯硼酸频哪醇酯两步脱保护步骤的影响
Table 5. Effects of solvent, diethanolamine and reaction time on two-step deprotection of 2-nitrophenyl borate
表5. 溶剂、二乙醇胺、反应时间对2-硝基苯硼酸频哪醇酯两步脱保护步骤的影响
需要指出的是,2-硝基苯硼酸频那醇酯在硼酸频哪醇酯的制备过程中通常与邻溴硝基苯、双(频哪醇合)二硼分离困难,所以采用2-硝基苯硼酸频那醇酯脱保护的两步方案制备邻硝基苯硼酸(图2)。几种脱保护方法如酸性水解 [12]、高碘酸钠氧化裂解 [13]、碱性水解 [14]。然而,通过烷基硼酸盐与二乙醇胺反应可以制备烷烃产物中间体 [15],并且中间体易于水解。
 (a)
(a)
 (b)
(b)
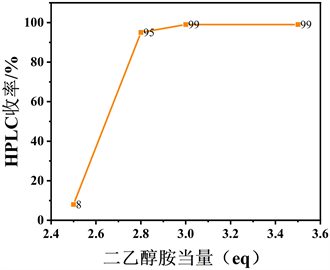
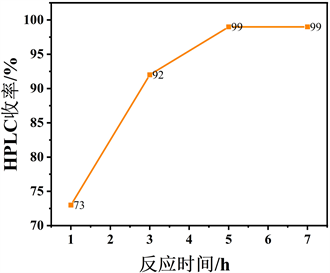
Figure 7. Effects of diethanolamine and reaction time on two-step deprotection of 2-nitrophenyl borate
图7. 二乙醇胺、反应时间对2-硝基苯硼酸频哪醇酯两步脱保护步骤的影响
在研究中,我们尝试将此方法应用于芳族硼酸盐,并对反应条件进行了优化(见图7)。从表5的结果可以看出,极性较小的溶剂如CH3(CH2)4CH3、CH3OCH3、O(CH2CH3)2、石油醚等对反应的影响较好,而CH2Cl2相对较差。从经济成本来看,石油醚无疑是最好的(见表5路径1~5)。用二乙醇胺对2-硝基苯硼酸频哪醇酯的转化率进行了优化,结果表明,在3当量二乙醇胺,室温下5小时条件下转化率可达99% (见表5路径5~11)。
3.6. 具有活性基团的频哪醇芳基硼酸盐的制备
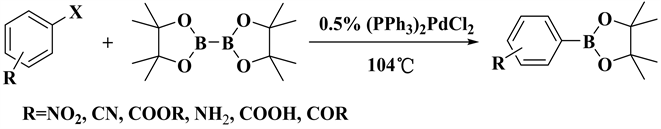
Figure 8. Preparation of pinacol arylboronates with active groups
图8. 具有活性基团的频哪醇芳基硼酸盐的制备
在10 mL的Schlenk管中,将芳基卤化物(1.0 mmol)、双(频哪醇合)二硼(1.3 mmol)、[(C6H5)3P]2PdCl2 (0.5% mmol)、CH3COOK (3.0 mmol)、TBAB (0.2 mmol)和干燥的1,4-二氧六环(2 mL)置于氮气气氛下。将反应混合物在油浴中加热至规定温度,持续搅拌4 h,然后冷却至室温。反应混合物在烧结过滤漏斗中通过硅藻土塞过滤,然后用EtOAc洗涤。有机相采用无水MgSO4干燥,减压脱除溶剂得到粗产物,以CH3(CH2)4CH3和EtOAc为洗脱剂,以5:1的比例分别用硅胶柱层析纯化。
为了评估优化反应条件1的普遍性,我们将多种具有活性基团的卤代芳烃与双(频哪醇合)二硼反应(见图8)。从表6中可以看出,具有活性基团如硝基、酯基、羰基、氰基和氨基的卤代芳烃在优化过程中是相容的。特别是对硝基、羰基、酯基的催化效果极好,产品收率可达90%以上(表6路径1, 3, 4, 6)。
Table 6. Preparation of a variety of pinacol arylboronates with active groups
表6. 多种具有活性基团的频哪醇芳基苯硼酸盐的制备
4. 结论
研究了一种温和、简单的方法,以0.5%当量[(C6H5)3P]2PdCl2为催化剂,0.2当量TBAB为相转移催化剂,3.0当量CH3COOK (无水)为碱,在与底物摩尔比为1:15的1,4-二氧六环中制备有活性基团的1.0当量芳基卤化物和1.3当量双(频哪醇合)二硼偶联反应的取代苯基硼酸,然后对目标产物进行二乙醇胺脱保护。该方法具有底物范围广、操作简单、操作简便、反应时间短、产率高等优点。
基金项目
苏州科学技术项目(Nos. SYG201624,SYG202017)资助;江苏省自然科学基金(No. BK20151238)资助。
文章引用
魏开举,伍敏志,陈重铭,任明秀. 钯基催化制备具有活性基团取代的苯基硼酸
Palladium-Catalyzed Preparation of Phenylboric Acid with Active Groups[J]. 化学工程与技术, 2022, 12(06): 424-433. https://doi.org/10.12677/HJCET.2022.126055
参考文献
- 1. Khurana, L., Fu, B.Q., Duddupudi, A.L., et al. (2017) Pyrimidinyl Biphenylureas: Identification of New Lead Compounds as Allosteric Modulators of the Cannabinoid Receptor CB1. Journal of Medicinal Chemistry, 60, 1089-1104. https://doi.org/10.1021/acs.jmedchem.6b01448
- 2. 徐剑霄. 一种2-硝基苯硼酸频那醇酯的合成方法[P]. 中国, 110964046. 2020-04-07.
- 3. Oikawa, A., Kindaichi, G., Shimotori, Y. and Hoshi, M. (2016) First Synthesis of both 1-aryl-4-[(E)-alk-1-enyl]-1H-1, 2,3-Triazoles and 1-aryl-4-[(Z)-1-(trimethylsilyl)alk-1-enyl]-1H-1,2,3-triazoles: Assembly of π-Extended 1,2,3-Triazoles Using a Cross-Coupling/Click Reaction Sequence. Tetrahedron, 72, 4205-4213. https://doi.org/10.1016/j.tet.2016.05.055
- 4. Fang, H., Kaur, G., Yan, J. and Wang, B. (2005) An Efficient Synthesis of Sterically Hindered Arylboronic Acids. Tetrahedron Letters, 46, 1671-1674. https://doi.org/10.1016/j.tetlet.2005.01.064
- 5. Stones, D., Manku, S., Lu, X.S. and Hall, D.G. (2004) Modular Solid-Phase Synthetic Approach to Optimize Structural and Electronic Properties of Oligo-Boronic Acid Receptors and Sensors for the Aqueous Recognition of Oligosaccha-Rides. Chemistry—A European Journal, 10, 92-100. https://doi.org/10.1002/chem.200305400
- 6. 张永强, 贺全国, 蒋欢妹, 邓燕, 等. 2,6-二甲基苯硼酸制备方法的改进[J]. 应用化学, 2007, 24(10): 1216-1218.
- 7. Ando, S., Matsunaga, H. and Ishizuka, T. (2015) A Bicyclic N-Heterocyclic Carbene as a Bulky but Accessible Ligand: Application to the Copper-Catalyzed Borylations of Aryl Halides. Journal of Organic Chemistry, 80, 9671-9681. https://doi.org/10.1021/acs.joc.5b01721
- 8. Leermann, T., Leroux, F.R. and Colobert, F. (2011) Highly Efficient One-Pot Access to Functionalized Arylboronic Acids via Noncryogenic Bromine Magnesium Exchanges. Organic Letters, 13, 4479-4481. https://doi.org/10.1021/ol2016252
- 9. Appukkuttan, P., Dehaen, W. and Van, D.E. (2007) Microwave-Assisted Transition-Metal-Catalyzed Synthesis of N-Shifted and Ring-Expanded Buflavine Analogues. Chemistry—A European Journal, 13, 6452-6460. https://doi.org/10.1002/chem.200700177
- 10. Collibee, S.E. (2005) A Facile and Convenient Synthesis of Func-tionalized Ortho-Nitrophenylboronic Acids. Tetrahedron Letters, 46, 4453-4455. https://doi.org/10.1016/j.tetlet.2005.04.129
- 11. Lu, J., Guan, Z. and Gao, J. (2011) An Improved Procedure for the Synthesis of Arylboronates by Palladium-Catalyzed Coupling Reaction of Aryl Halides and Bis(pinacolato)diboron in Polyethylene Glycol. Applied Organometallic Chemistry, 25, 537-541. https://doi.org/10.1002/aoc.1799
- 12. Martin, R. and Jones, J.B. (1995) Rational Design and Synthesis of a Highly Effective Transition State Analog Inhibitor of the RTEM-1 β-Lactamase. Tetrahedron Letters, 36, 8399-8402. https://doi.org/10.1016/0040-4039(95)01799-N
- 13. Norsikian, S., Soule, J.F., Cannillo, A., Guillot, R., Dau, M.E.T.H. and Beau, J.M. (2012) Remarkable Stereoselectivity in Intramolecular Borono-Mannich Reactions: Synthesis of Conduramines. Organic Letters, 14, 544-547. https://doi.org/10.1021/ol203162s
- 14. Snow, R.J., Bachovchin, W.W., Barton, R.W., et al. (1994) Studies on Proline Boronic Acid Dipeptide Inhibitors of Dipeptidyl Peptidase IV: Identification of a Cyclic Species Containing a B-N Bond. Journal of the American Chemical Society, 116, 10860-10869. https://doi.org/10.1021/ja00103a002
- 15. Sun, J., Perfetti, M.T. and Santos, W.L. (2011) A Method for the Deprotection of Alkylpinacolyl Boronate Esters. Journal of Organic Chemistry, 76, 3571-3575. https://doi.org/10.1021/jo200250y
NOTES
*通讯作者。
1典型实验步骤:在10 mL的Schlenk管中,将芳基卤化物(1.0 mmol)、双(频哪醇合)二硼(1.3 mmol)、[(C6H5)3P]2PdCl2 (0.5% mmol)、CH3COOK (3.0 mmol)、TBAB (0.2 mmol)和干燥的1,4-二氧六环(2 mL)置于氮气气氛下。将反应混合物在油浴中加热至规定温度,持续搅拌4 h,然后冷却至室温。反应混合物在烧结过滤漏斗中通过硅藻土塞过滤,然后用EtOAc洗涤。有机相采用无水MgSO4干燥,减压脱除溶剂得到粗产物,以CH3(CH2)4CH3和EtOAc为洗脱剂,以5:1的比例分别用硅胶柱层析纯化。
