Material Sciences
Vol.
13
No.
12
(
2023
), Article ID:
78242
,
12
pages
10.12677/MS.2023.1312125
CO2氧化丙烷催化剂研究进展
洪广
成都大学,机械工程学院,四川 成都
收稿日期:2023年11月15日;录用日期:2023年12月21日;发布日期:2023年12月28日

摘要
由于丙烯需求的快速增长和含丙烷页岩气的勘探,丙烷脱氢制取丙烯工艺越来越受到人们关注,丙烷直接脱氢制丙烯(DHP)提供了较高的丙烷收率,但由于焦炭的形成容易导致催化剂快速失活。CO2辅助丙烷脱氢(CO2-ODHP)是一种很有前景的实现高量产丙烯和CO2利用的技术。近年来对CO2-ODP反应的探索结果表明反应机理限制、CO2利用率低、快速失活仍是限制金属氧化物基催化剂发展的主要因素。金属基催化剂因其独特的性能可以通过催化剂设计调控丙烷脱氢复杂的反应偏向,是未来采用丙烷催化制备丙烯,解决焦炭和烧结问题,提高丙烷脱氢制丙烯产率的一种重要手段。
关键词
丙烷,丙烯,金属催化剂,二氧化碳

Advances in Catalysts for CO2 Oxidation of Propane
Guang Hong
College of Mechanical Engineering, Chengdu University, Chengdu Sichuan
Received: Nov. 15th, 2023; accepted: Dec. 21st, 2023; published: Dec. 28th, 2023

ABSTRACT
Due to the rapid growth of propylene demand and the exploration of propane-containing shale gas, the process of propane dehydrogenation to propylene has received increasing attention. Direct dehydrogenation of propane to propylene (DHP) provides high propane yields but is prone to rapid catalyst deactivation due to coke formation. CO2-assisted dehydrogenation of propane (CO2-ODHP) is a promising technology to achieve high volume production of propylene and CO2 utilization. The results of exploring the CO2-ODHP reaction in recent years indicate that reaction mechanism limitation, low CO2 utilization, and rapid deactivation are still the main factors for the development of metal oxide-based catalysts. Metal-based catalysts, due to their unique properties, can be used to modulate the complex reaction bias of propane dehydrogenation through the design of catalyst, which is an important means to solve the coke and sintering problems and increase the yield of propylene from propane dehydrogenation in the future by using propane catalytic preparation of propylene.
Keywords:Propane, Propylene, Metal Catalysts, Carbon Dioxide

Copyright © 2023 by author(s) and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY 4.0).
http://creativecommons.org/licenses/by/4.0/


1. 引言
丙烯是三大合成材料最基本的原材料之一,用于制备工业聚丙烯、环氧丙烷等重要化学产品。传统的丙烯生产工艺主要依靠于石油资源的催化裂化(FCC)和蒸汽裂化(SC) [1] [2] ,随着丙烯需求的日益增加,石油资源的过度消耗,寻找新的丙烯生产技术迫在眉睫 [3] [4] [5] 。全球页岩气的开发为众多增值化学品提供了原材料,其中丙烷(页岩气的主要成分) DHP已成功工业化 [6] ,各类铬基和铂基催化剂被广泛研究和报道。由于丙烷C-H键的化学惰性和DHP反应本质上的无氧化脱氢,致使工业化的丙烷脱氢制丙烯需要在高压高温(600℃以上)条件下才能得到较高的转化率,反应实际温度过高往往带来丙烷深度热解和脱氢等副反应,同时高温有利于焦炭的形成,严重影响催化剂活性 [7] [8] 。丙烷催化氧化脱氢(ODHP)加入氧组分可以大大降低丙烷脱氢的反应能耗,由于目标产物丙烯的双键键能低于丙烷C-H键键能,使其在反应过程中更容易被活性氧攻击,进一步氧化生成CO、CO2等物种,导致丙烯选择性和产率下降 [9] [10] 。改用较温和的CO2作氧化剂,通过多相催化技术将丙烷转化为丙烯则可以避免上述问题 [11] [12] 。对于CO2氧化丙烷脱氢制取丙烯反应体系中,目前研究广泛的金属基催化剂(Pt)和金属氧化物催化剂如CrOx或Vox等 [4] [5] [13] [14] ,大多的金属氧化物催化剂因其催化剂特性都表现出较差的CO2转化效率。相比之下金属基催化剂在不降低丙烷活化能力的前提下还能表现出较高的CO2转化率而被广泛研究,其中贵金属Pt基催化剂因其对C-H键断裂的高活性成为主要的研究对象 [15] [16] [17] 。各类第二相第三相助剂也用于调控Pt基催化剂对CO2-ODP反应和与之平行的副反应之间的优先性 [18] [19] [20] 。
2. 金属氧化物催化剂
金属氧化物是低碳烷烃脱氢反应的重要催化剂之一,催化活性与其在载体上的负载量和载体性质有关。载体既可以增强催化剂的机械强度和热稳定性,同时改变金属氧化物在载体表面的存在形式,产生合适的活性位点。常见的金属氧化物有CrOx、Vox、Ga2O3、Fe2O3 [6] [21] [22] [23] [24] 等。表1总结了不同金属氧化物基催化剂和金属基催化剂在CO2-ODP反应中的反应性能。
从1933年Frey和Huppke发现Cr2O3催化剂具有优秀的低碳烷烃脱氢性能后 [25] ,负载铬氧化物(CrOx)基催化剂是脱氢领域中应用较为广泛的一类负载型催化剂,目前已在工业化的Lummus公司的Catofin工艺中使用。后面被各课题组引入CO2氛围下的丙烷脱氢 [25] [26] [27] [28] [29] 。Takahar [29] 等人以Al2O3,活性炭和SiO2负载的几种Cr2O3催化剂为研究对象,仅在SiO2上负载的催化剂观察到了CO2对丙烷脱氢的促进作用,提高丙烯收率并抑制了催化剂失活,原因在于CO2存在下帮助了Cr2O3/SiO2表面维持部分
Table 1. Propane conversion rate and selectivity of different catalysts in CO2-ODP reaction
表1. 不同催化剂在CO2-ODP反应中丙烷转换率和选择性
氧化。5 wt%Cr负载在SiO2催化剂,在823 K时具有9.1%的丙烯收率。Kocon [30] 等人用浸渍法制备了负载量为3.4%的Cr2O3/Al2O3,进一步证明了CO2在丙烷脱氢过程中改变了CrOx/Al2O3催化剂的酸碱度。在873 K条件下反应0.2 h,取得了29.7%丙烷转化率和80.5%的丙烯选择性。但上述催化剂均在反应初期快速失活,之后的稳定性也只能维持6~7 h,这源于CrOx用于丙烷脱氢的反应机理的限制(图1)。CrOx结构复杂,在煅烧后通常含有Cr6+、Cr5+、Cr3+三种不同的氧化态,含有Cr=O双键的高氧化态物种在丙烷脱氢的氛围下很容易还原为Cr3+物种,CrOx基催化剂在CO2氛围下丙烷的脱氢反应遵循晶格氧机理(Mars-Van-Krevelen)。高价的孤立Cr-O作为活性位点促进丙烷分子脱氢,同时Cr6+/Cr5+被还原成Cr3+物种。CO2又将低价的Cr3+物种重新氧化成Cr6+/Cr5+,但CO2的反应惰性使这一步骤相对缓慢,由此导致丙烷脱氢的活性位点Cr6+/Cr5+数量减少,催化剂逐渐失活。为了进一步了解CrOx活性位点对C3H8和CO2的吸附与活化,表面吸附物种和CrOx的结构演变及相关机理,Wang [28] 等采用浸渍法将少量的CrOx负载在分子筛载体上用于CO2-ODP,采用传统表征与原位光谱相结合确认CrOx结构在CO2-ODP反应中的演变。结果表明聚合态Cr6+氧化物比孤立态Cr6+物种对催化CO2-ODP具有更高的反应活性和丙烯选择性,这是由于反应物C3H8和产物C3H6强吸附在聚合态Cr6+氧化物上,随反应的持续发生焦炭的累计,整个反应由快速失活阶段过渡到稳定阶段。在催化活性上表现出降低C3H8转换率和提高C3H6选择性的双重作用。主要原因在于CO2作为弱氧化剂很难将低价的Cr全部氧化为活性高价Cr,除活性位点减少引起的催化剂失活外,反应过程中焦炭的产生会覆盖活性位点也会导致催化剂失活,需要频繁对催化剂进行再生,而且Cr具有毒性。
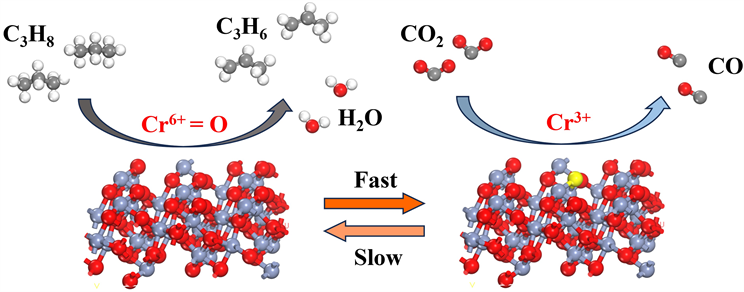
Figure 1. Mechanism of CO2 oxidative dehydrogenation of propane to propylene on CrOx based catalysts
图1. CrOx基催化剂上CO2氧化丙烷脱氢生成丙烯反应机理
最近,一类新型的Ga2O3催化剂逐渐从丙烷的芳构化反应中被引入丙烷脱氢反应,其脱氢活性竟高于传统的Cr2O3催化剂 [31] [32] [33] [34] [35] 。随着研究的深入进行人们发现Ga2O3基催化剂对丙烷脱氢反应并非如Cr2O3和V2O5等催化剂一般遵循Mars-Van-Krevelen机理,而是与其表面吸附活化H原子能力有关,其活化能力的强弱取决于Gaδ+-H化学键形成的难易程度。Ga2O3催化剂符合两步法脱氢机理,Gaδ+-H作为中间步骤为脱氢的第一步,临位氧对*C3H7的脱氢并形成H2脱附(图2),随后产生的H2与CO2在气相中发生水逆煤气转变生成H2O和CO。之后的研究表明Gaδ+的分散和Lewis酸位点强度显著地影响了丙烷活化的能力。Xu [34] 等将Ga2O3负载于不同载体上(TiO2、Al2O3、ZrO2、SiO2和MgO)用于CO2辅助丙烷脱氢反应,发现Ga2O3/TiO2、Ga2O3/Al2O3和Ga2O3/ZrO2是更好的脱氢反应催化剂,这是因为催化剂表面有更多的酸性位点。CO2对Ga2O3/TiO2的脱氢活性有促进作用,对Ga2O3/ZrO2和Ga2O3/Al2O3有负向影响。这些不同的载体效应可能源于催化剂不同的H2吸附能力和酸碱性质,这可能是由氧化镓和载体之间的不同相互作用引起的。XPS研究表明,Ga2O3/TiO2表面有丰富的还原镓原子(45%),这可能解释了该催化剂在CO2存在下脱氢反应中独特的催化行为。Xiao [35] 等用水热合成法将Ga2O3负载于Al2O3,通过改变热液条件改善表面镓的分散和分布。这一过程暴露更多的Ga3+位点并促进Lewis酸性位点的形成。此外,水热处理也有利于改善催化剂表面积和增加孔体积,Ga2O3/Al2O3催化剂在反应9 h后,通过空气再生也能得到很好的恢复,优选的Ga2O3-Al2O3催化剂上丙烷的最高转化率为35.35%。Liu [36] 等采用PH控制的等体积浸渍法合成了不同Ga负载量的Ga2O3/SiO2催化剂。发现CO2的引入可以消除DHP过程中产生的Ga氢化合物,原位漫反射红外傅里叶变换(DRIFT)光谱显示,CO2可以有效地消除Gaδ+-Hx再生成Ga3+-O,同时减少积碳提高催化剂性能。尽管上述的研究提高了Ga2O3催化剂的对丙烷脱氢的各项性能,但其稳定性仍有待提高,上述体系的催化剂均在数小时后有明显的活性下降。
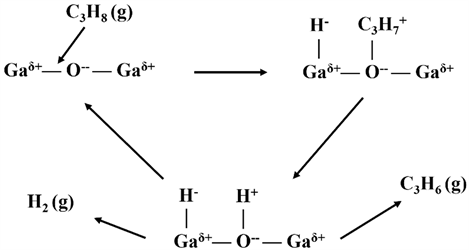
Figure2. Process diagram of propane dehydrogenation using Ga2O3 catalyst
图2. Ga2O3催化剂丙烷脱氢流程图
金属氧化物催化剂CO2-ODP反应机理可以概括为氧化还原活性金属位点与丙烷反应生成丙烯,同时将高氧化态的活性位点还原为低氧化态,然后由CO2将被还原的活性中心再次氧化为原始状态。由于这个反应机制催化剂往往由于以下原因面临失活:1) 高氧化态活性位点缺乏;2) CO2活化能力低;3) 焦炭难以去除,金属氧化物催化剂在使用过程中不断被氧化和还原,极容易积碳失活,尽管再生周期非常短,但频繁的再生会导致催化剂结构被破坏,从而永久性地失去活性;4) 碱性位点对CO2的吸附活性强。这些固有的缺点表明需要寻找更有利的反应路径进行CO2氛围下的丙烷脱氢反应。金属基催化剂可以通过改变活性组分、添加多相助剂、调控活性组分与载体之间的协同关系等等手段促使丙烷脱氢反应往有利的方面进行。
3. 金属基催化剂
金属基催化剂对于CO2-ODP反应从反应机理上会比金属氧化基催化剂更具设计性。通过调控金属活性位点尺寸大小、形貌构型,或是添加第二相金属或多相金属与主要活性金属形成金属间化合物,从电子效应、几何效应、立体效应、有序效应等方面调控活性金属催化性能 [48] [49] [50] [51] [52] 。尤其是Co、Ni、Cu等过渡金属的加入可以促进CO2的捕获和还原,弥补金属氧化催化剂对CO2吸附和还原的调控能力不足 [53] [54] ;而Ga、In、Sn等惰性金属虽然自身不作为反应的活性位点,却可以起到分散主活性位点和调控电子密度的作用,同时引发的集团效应也可以使催化剂稳定性提高和延长寿命;CO2-ODP反应区别于DHP反应是因为引入了弱氧化剂CO2,相对应地对催化剂载体也有了更高的要求,CeO2因为其自身的碱性和优秀的氧释放能力被广泛应用于CO2-ODP研究 [55] [56] [57] [58] (图3)。
3.1. 单金属催化剂
单金属在身成为丙烷脱氢活性位点,往往有较强的C-H键活化能力同时也有较强的C-C键断裂能力,这往往有利于丙烷的干重整而不是脱氢反应。Solymosi [37] 等通过浸渍法将Rh负载在Al2O3、SiO2、TiO2、MgO上用于CO2-ODP反应,发现即使在很低的温度下(256 K~300 K),丙烷仍能与Rh相互作用生成丙烯和亚丙基。引入CO2后丙烷的反应路径发生变化,丙烷脱氢产物丙烯与CO2迅速反应生成合成气CO和H2。

Figure 3. Modification of Pt based catalysts and mechanism of propane dehydrogenation reaction
图3. Pt基催化剂改性以及丙烷脱氢反应机理
考虑到可以通过调控载体与活性金属之间的协同关系控制反应走向,Pradhan [38] 等将贵金属Rh负载在CeO2和ZrO2上研究了载体不同的氧释放能力对催化剂CO2-ODP反应的影响,结果表明CeO2具有更强的氧迁移能力用于CO2的捕获和还原,使整个反应氧化性增加,但这仅限于增强了反应的干重整活性。
金属氧化物载体强氧释放能力会增强丙烷的干重整反应,同时也给到提示可以通过载体的改性调控CO2-ODP反应。Nowicka [39] 等人研制了一种Pd/CeZrAlOx催化剂,并在CO2氛围下表现出长期的稳定性和C3H6选择性。Pd相比于Rh更有利于C-H键断裂而C-C键活化能则需要更高,这抑制了丙烷的干重整反应,Ce、Zr混合氧化物作为载体有利于CO2的捕获和活性氧的迁移使反应向有利的方向进行的同时,帮助了焦炭的燃烧延长催化剂寿命。
Pt基催化剂因其优异的反应性能广泛地应用于丙烷脱氢反应中,一般认为,丙烷脱氢位点为金属态的Pt,其形式为单原子或者团簇,但传统的Pt基催化剂在CO2-ODP反应中往往表现出较差的丙烯选择性,这主要是因为Pt在裂解、氢解和干重整反应中都具有较高的活性 [59] [60] 。其中丙烯脱附困难进而发生深度脱氢是CO2-ODP反应中丙烯选择性低的主要原因。巩金龙 [61] 等用溶胶–凝胶法将TiO2分散到Al2O3上以改变Pt的负载形式。结果表明部分还原的TiOx(x < 2)会向Pt原子转移电子,表面Pt电子密度增加后会削弱丙烯吸附。NH3-TPD结果表明TiO2的掺杂会使得载体表面的酸性位点数量增加,这会产生更多的焦炭,通过调节TiO2的掺杂量以协调Pt与载体之间的电子转移效应和酸性位点之间的作用。
一般认为,在丙烷脱氢反应中,Pt团簇的结构大小会直接影响催化剂活性。较小的Pt团簇在减少副反应的同时能暴露更多的丙烷脱氢位点。Zhang [40] 等通过简单浸渍法制备一系列Al2O3负载的原子、亚纳米团簇和纳米团簇。原子分散Pt/Al2O3催化剂的转换频率(TOF)分别比亚纳米簇和纳米颗粒高约3倍和7倍,与纳米颗粒相比,亚纳米尺寸的团簇对丙烯选择性具有相反的尺寸依赖性。原子分散的Pt和大纳米颗粒的Pt都具有较高的丙烯选择性,而且原子分散的Pt因为电荷密度的增加减弱了丙烯的吸附,阻止丙烯的深度脱氢。此外分散的Pt可以有效地抑制丙烷的深度脱氢(C-C键断裂),提高丙烯选择性和稳定性。Pt负载量为0.05%时,丙烯选择性能达到95%。
Sun [62] 等采用第一性原理计算研究了丙烷在氮化硼纳米片中氮和硼空位上Pt单原子的脱氢反应。结果表明在Bvac(Pt-Bvac)上Pt原子比在Nvac(Pt-Nvac)的Pt原子对丙烷和丙烯具有更高的吸附能,对C-H键的活化也更具活性。然而,Pt-Bvac的高反应性也阻碍了丙烯的脱附,这可能导致副反应深度脱氢和裂解。C-H活化能力和丙烯脱附的反应平衡是提高丙烯收率的必要条件,由此,氮空位上的Pt原子被认为是高效的丙烷脱氢催化剂。
基于DFT对单原子Pt上丙烷脱氢反应机理的探究,Pt颗粒尺寸大小、分散情况对丙烷脱氢活性的影响。充分认识到了CO2-ODP是个复杂的反应,高效的CO2氧化丙烷脱氢制丙烯催化剂必须具备较好的C-H键活化能力和C-C键活化惰性以抑制丙烷的过度裂解。能较好地解吸目标产物丙烯防止深度脱氢,保证丙烯选择性。同时具备较好的CO2捕获还原能力,CO2的活化可以改变丙烷脱氢的反应平衡,加快丙烷的脱氢频率,氧组分的加入可以抑制焦炭的形成保证催化剂的稳定性。故此,一般要对Pt基催化剂加以修饰和改性来控制CO2-ODP反应向理想的方向进行。
3.2. 双金属催化剂
为使丙烷脱氢生成丙烯反应往有利的方向进行,在金属催化剂设计时通常将第二金属与主活性金属结合来调控活性金属的电子密度和几何结构(金属间化合物的集团效应) [63] [64] [65] 。稀释主活性金属从而抑制多余的副反应,如丙烷热解和重整反应。将贵金属Pt或Pd与非贵金属Fe、Co、Ni组合,二者之间的协同效应使得催化剂有着更高的催化性能。
Comez [41] 等使用CeO2负载双金属Fe3Ni、Fe3Pt、Ni3Pt用于CO2-ODP反应制取丙烯,作者通过XANES发现在反应条件下,Ni和Pt是以单质形式存在,而Fe在Fe3Ni催化剂中则是以氧化态存在的。在活性测试中虽然单独的Fe3对于反应没有催化效果,但是Fe3Ni双金属催化剂表现出了良好的催化活性及选择性(丙烯选择性58.2%),而贵金属Pt与过渡金属Fe、Ni的组合却更有利于丙烷干重整生成CO和H2,其中Ni3Pt/CeO2有较高的催化活性(丙烷转化率11.6%),Fe3Pt/CeO2有较高的丙烯选择性(32%)。建立了一个双金属催化剂库,用于确定对DRP或CO2-ODP的固有活性,并可用于未来提高活性、稳定性和选择性的努力。该小组之后的研究继续了这个理念 [66] ,将Pt基和Pd基金属催化剂与Fe、Co、Ni过渡金属组合以及不同原子组成的非贵金属组合形成双金属催化剂,探究CO2-ODP反应中生产合成气和丙烯不同的反应路径,结果表明,Pt基双金属在质量转化率和位点特异性TOF值方面均优于Pd基催化剂。在与过渡金属的组合中,Ni3在CO2转化率方面优于Fe3和Co3。而非贵双金属Ni3和Co3组合不仅活性更高,而且稳定性更强,相比之下,FexNiy催化剂对CO2-ODP表现出更高的丙烯选择性。
Bian [42] 通过精细调控双金属纳米颗粒的结构进一步理解丙烷脱氢反应中结构-活性关系,发现PtFe双金属催化剂中过量的Fe物种会促进焦炭累积,导致较低的C3H6选择性,通过调整CO2与丙烷的进气关系,当CO2/C3H8的摩尔比为0.20时,在不改变PtFe合金催化表面结构的情况下将Fe0活性位点选择性氧化,Pt1Fe7/S-1催化剂表现出最高的丙烯产率,积碳量也从18.8 wt%降低到了1.0 wt%,而焦炭的抑制并不是因为反向Boudouard反应发生,而是将过量的非合金铁Fe0有效地氧化。这项工作为在反应条件下调节PtFe双金属催化剂的结构和提高PDH反应的性能提供了一种有前途的策略。
Wang [43] 等在Beta分子筛上负载直径为1~2.5 nm的双金属PtCo纳米颗粒,通纳米Beta分子筛脱铝后形成的硅羟基作为锚定位点增强了PtCo纳米颗粒的分散性。Co的引入进一步促进了Pt的分散均匀,并得到了更小的双金属纳米。Pt/Co的比例也显著影响了丙烷催化反应(脱氢或干重整)的路径,优化Pt/Co比例,Pt1Co1-SiBeta催化剂在550℃时丙烷和CO2的转换率分别高达51.8%和30.6%。过渡金属Co引入用于增加CO2的捕获和还原,但相比PtNi双金属组合有着更高的丙烯选择性,这除了3 d晚期过渡金属之间的差异外,载体的差异也对丙烷的脱氢或干重整反应有很重要的作用。有意思的是CO2-ODP反应众多金属基催化剂都是基于CeO2载体,其氧空位能够活化丙烷的C-H键和CO2的C=O键 [67] 。
Sn是目前应用最为广泛的Pt基催化剂改性助剂,在DHP反应中,由于Sn自身的化学反应惰性,又能与贵金属Pt形成双金属合金,从而引起的几何效应和电子效应共同提高Pt基催化剂的活性和稳定性 [68] [69] 。Mata-Martinez [44] 等研究了Sn的比例对Pt/KIT-6催化剂在PDH反应中的影响。结果表明在随Sn比例的提升,目标产物丙烯选择性先增加后减小。这是由于Sn的逐步加入会优先形成Pt:Sn = 1:1的合金,过量的Sn则会使合金尺寸增大并阻碍活性位点。Wang [45] 等将Sn掺杂到CeO2负载Pt(Pt/Sn-CeO2)催化剂,一方面通过形成PtSn合金,增加Pt的电子密度,促进丙烷的吸附和碳氢键解离。另一方面Sn的掺杂提高了CeO2载体的氧空位浓度,促进了CO2的解离。在550℃反应4 h后,0.1 wt%Pt/1.0 wt%Sn-CeO2催化剂仍能达到15.1%的丙烷转化率和63.9%的丙烯选择性。研究通过原位红外跟踪了反应过程中丙烷和CO2的演变,发现了MvK机制在反应过程中的作用。后续该课题通过改变Sn/Pt摩尔比,阐明了SnOx物种对CO2-ODP反应中Pt催化活性和丙烯选择性的影响 [46] 。当比值增加时,丙烷转化率逐渐降低,而丙烯选择性增加。Sn物种的增加了Pt分散性的同时增加了Pt的电子密度,使丙烷C-H键活化更为容易而不是断裂C-C键发生干重整反应,从而逐渐抑制CO2-RP、丙烷裂解和焦炭积累。原位拉曼证明了还原的PtSn/CeO2表面氧缺陷可以与CO2反应生成Pt-O-Ce键,作为CO2-ODP反应的循环位点,其中Pt-O-Ce键与丙烷反应生成丙烯和水,然后形成的氧缺陷从CO2分子中摄取氧气生成CO。
近期,Zhai等 [47] 采用浸渍法制备了SiO2负载的Pt-M (M = Sn, In, Zn)双金属催化剂用于CO2-ODP反应,实验结果显示,Pt-M双金属催化剂对丙烷裂解/氢解副产物如甲烷、乙烷、乙烯等选择性较低,且在CO收率/CO2转换率比值接近于1,这意味着干重整反应的贡献并不显著。之后,研究人员进一步研究了Pt/SiO2、Sn1.5/SiO2和PtSn1.5/SiO2样品的催化性能,结果显示,Pt/SiO2催化剂有着最高的CO2转换率,而Sn1.5/SiO2几乎没有活性,意味着Sn的加入使得CO2转换率下降,同时抑制了高丙烷转化率下CO2-ODP中这些副反应(裂解、氢解、重整和甲烷化),大大提高了丙烯的选择性。DFT计算结果表明,双金属基催化剂上的CO2-ODP反应分两步进行,第一步以丙烷脱氢为主,第二步为丙烷脱氢与逆水煤气转变反应偶联,并且整个反应动力学受限于逆水煤气转变。PtSn合金化形成的独特的Pt3Sn-SnOx界面使得Sn0、Pt0和SnO2之间能够协同作用,导致Pt3Sn-SnOx界面成为提高丙烯选择性和收率的活性中心。
3.3. 多金属催化剂
高效的CO2-ODP催化剂,需要考虑C-H键断裂和CO2活化能力同时抑制丙烷过渡氢解和过渡氧化等副反应。双金属催化剂的成功给到我们启示可以通过多相金属的加入调控CO2-ODP相关的平行反应。Xing [12] 等设计了一种Pt-Co-In三元合金催化剂,Pt作为断裂C-H键的主要活性金属,过渡金属Co、Ni在费米能级附近的高密度状态,降低了CO2的还原能垒,惰性金属Sn、In合金的集团效应增强催化剂稳定的同时提高了丙烯的选择性。三元合金强大的活性与CeO2载体的放氧能力结合,提高CO2的利用率,极大地提高了催化剂的稳定性。在CO2-ODP催化活性上,Pt/CeO2和Pt-M(M=Co、In和Sn)催化剂初始转化率较高(52%~68%),但在5~10小时内快速失活,其中Pt-Sn和Pt-In的组合都具有较高的丙烯选择性。而Pt/CeO2和Pt-Co/CeO2在反应刚开始时,丙烯选择性只有35%和27%。这是因为发生了不希望的副反应生成了C1和C2碳氢化合物,物质平衡的偏离(比如Pt/CeO2,CxHy:0.71,Cox:1.31),说明在很大程度上发生了丙烷向CO的干重整反应。相比之下,Pt-Co-In/CeO2在20小时内保持了较高的丙烷转化率(50%),丙烯选择性最高(95%),CxHy和Cox中碳平衡接近统一,也表明了干重整对三元合金催化剂的贡献很小。对于CO2转化稳定性,只有三元合金催化剂表现出了良好的稳定性,其余催化剂的CO2转化率趋势顺序为Pt-Co > Pt,Pt-Sn,Pt-Co-In>>Pt-In。这一结果表明Co金属如预期一样增强了CO2的捕获和还原,单独的In合金化降低了这种能力。因此Pt、Co和In的组合可以中和In对CO2还原的负面影响,重新促进对二氧化碳的转化。DFT计算结果表明Pt-Co-In三元催化剂上CO2-ODP反应的速度决定步骤(RDS)是CO2活化,将Co掺入Pt-In后,CO2活化能(EA)显著降低。
该组进一步研发了基于高熵合金金属化合物(HEI)的新型催化剂 [70] ,由XAFS分析表明了HEI结构与金属间化合物PtSn类似,其中Pt、Co、Ni、Sn和In均被还原到零价态,而Ga物种大部分被氧化,其中Pt和Sn部分位点分别被Co/Ni和In/Ga部分取代。显著提高了抗焦性和催化剂的稳定性,此外,熵效应增加合金纳米团簇的热稳定性,还可以防止纳米颗粒的烧结。在600℃的CO2-ODP测试中HEI/CeO2催化剂在前20 h仍保持较高的丙烷转化率(约30%)较高的丙烯选择性(95%),并在反应进行50 h后仍具有较高的稳定性。将重复使用的HEI/CeO2催化剂在600℃下通入CO2,然后进行H2还原,再生的催化剂的C3H8和CO2转化率都完全恢复。因此,HEI/CeO2催化剂在CO2-ODP中表现出优异的稳定性、可再生性和抗焦炭性。金属表面的积碳能够被CeO2晶格氧燃烧,HEI的燃烧温度低于Pt-Co-In,表明HEI/CeO2的积碳燃烧能力优于Pt-Co-In/CeO2。这项工作不仅展示了优异的催化性能,而且为CO2-ODP反应的催化剂设计理念开辟了新的领域。
4. 结论与展望
用较为温和的CO2辅助丙烷脱氢制取丙烯,在反应上可以消耗H2、去除焦炭和解吸丙烯,同时CO2作为反应物的工业利用可以有效地保护环境。目前的工艺仍未达到工业化水平,除提高催化剂性能外,焦炭的形成和烧结问题都需要进一步地改进。近年来,无论是金属氧化物基催化剂还是金属基催化剂在CO2-ODP反应上的进展,都表明了设计多功能催化剂调控反应平衡的重要性。同时增强的是对CO2活化的理解,进一步发展CO2的捕集和再利用,提高温室气体CO2的利用率,这也是达成碳达峰碳中和目标的重中之重。CO2-ODP自身复杂的反应体系随催化剂设计的偏向不同,因此为了更好的设计高效催化剂,应该充分结合活性位点与反应机制之间的复杂关系,例如各种常规表征,原位表征以及第一性原理计算与分子动力学计算。
文章引用
洪 广. CO2氧化丙烷催化剂研究进展
Advances in Catalysts for CO2 Oxidation of Propane[J]. 材料科学, 2023, 13(12): 1124-1135. https://doi.org/10.12677/MS.2023.1312125
参考文献
- 1. 马文明. 丙烷脱氢制丙烯技术研究进展[J]. 现代化工, 2023, 43(5): 20-24, 30.
- 2. 杨瑞云. 丙烷催化脱氢制丙烯技术研究进展[J]. 中国石油和化工标准与质量, 2023, 43(6): 164-166.
- 3. Hu, Z.P., Yang, D., Wang, Z., et al. (2019) State-of-the-Art Catalysts for Direct Dehydrogenation of Propane to Propylene. Chinese Journal of Catalysis, 40, 1233-1254. https://doi.org/10.1016/S1872-2067(19)63360-7
- 4. Al-Ghamdi, S.A. and De Lasa, H.I. (2014) Pro-pylene Production via Propane Oxidative Dehydrogenation over VOx/γ- Al2O3 Catalyst. Fuel, 128, 120-140. https://doi.org/10.1016/j.fuel.2014.02.033
- 5. Song, C., Park, H., Choi, W.C., et al. (2022) Initial Catalytic Be-havior of Chromium Oxide during Induction Period of fluidized Dehy-Drogenation of Propane. Chemical Engineering Journal, 440, Article ID: 135860. https://doi.org/10.1016/j.cej.2022.135860
- 6. Sun, Y., Tao, L., You, T., et al. (2014) Effect of Sulfation on the Performance of Fe2O3/Al2O3 Catalyst in Catalytic Dehydrogenation of Propane to Propylene. Chemical Engineering Journal, 244, 145-151. https://doi.org/10.1016/j.cej.2014.01.047
- 7. Karimipourfard, D., Kabiri, S. and Rahimpour, M.R. (2014) A Novel Integrated Thermally Double Coupled Configuration for Methane Steam Reforming, Methane Oxidation and Dehydro-genation of Propane. Journal of Natural Gas Science and Engineering, 21, 134-146. https://doi.org/10.1016/j.jngse.2014.06.018
- 8. Saerens, S., Sabbe, M.K., Galvita, V.V., et al. (2017) The Positive Role of Hydrogen on the Dehydrogenation of Propane on Pt(111). ACS Catalysis, 7, 7495-7508. https://doi.org/10.1021/acscatal.7b01584
- 9. Fattahi, M., Kazemeini, M., Khorasheh, F., et al. (2014) An Investi-gation of the Oxidative Dehydrogenation of Propane Kinetics over a Vanadium-Graphene Catalyst Aiming at Minimizing of the COx Species. Chemical Engineering Journal, 250, 14-24. https://doi.org/10.1016/j.cej.2014.04.002
- 10. Grant, J.T., Carrero, C.A., Love, A.M., et al. (2015) Enhanced Two-Dimensional Dispersion of Group V Metal Oxides on Silica. ACS Catalysis, 5, 5787-5793. https://doi.org/10.1021/acscatal.5b01679
- 11. Atanga, M.A., Rezaei, F., Jawad, A., et al. (2018) Oxidative Dehy-drogenation of Propane to Propylene with Carbon Dioxide. Applied Catalysis B: Environmental, 220, 429-445. https://doi.org/10.1016/j.apcatb.2017.08.052
- 12. Xing, F., Nakaya, Y., Yasumura, S., et al. (2022) Ternary Plati-num-Cobalt-Indium Nanoalloy on Ceria as a Highly Efficient Catalyst for the Oxidative Dehydrogenation of Propane Using CO2. Nature Catalysis, 5, 55-65. https://doi.org/10.1038/s41929-021-00730-x
- 13. Nakaya, Y., Hirayama, J., Yamazoe, S., et al. (2020) Sin-gle-Atom Pt in Intermetallics as an Ultrastable and Selective Catalyst for Propane Dehydrogenation. Nature Communica-tions, 11, Article No. 2838. https://doi.org/10.1038/s41467-020-16693-9
- 14. Sim, S., Gong, S., Bae, J., et al. (2017) Chromium Oxide Sup-ported on Zr Modified Alumina for Stable and Selective Propane Dehydrogenation in Oxygen Free Moving Bed Process. Molecular Catalysis, 436, 164-173. https://doi.org/10.1016/j.mcat.2017.04.022
- 15. 刘杰, 刘昌呈, 马爱增, 等. Pt系催化剂在丙烷脱氢反应中的研究进展[J]. 石油学报(石油加工), 2015(5): 1218-1231.
- 16. 李修仪, 周金波, 黄剑锋, 等. 丙烷催化脱氢制丙烯Pt系催化剂研究进展[J]. 石油炼制与化工, 2019, 50(12): 102-108.
- 17. 谢继阳, 王红琴, 安霓虹, 等. 丙烷脱氢制丙烯中铂基催化剂研究进展[J]. 贵金属, 2020, 41(1): 70-76, 84.
- 18. Xiong, H., Lin, S., Goetze, J., et al. (2017) Thermally Stable and Regenerable Platinum-Tin Clusters for Propane Dehydrogenation Prepared by Atom Trapping on Ceria. Angewandte Chemie International Edition, 56, 8986-8991. https://doi.org/10.1002/anie.201701115
- 19. Yang, M.L., Zhu, Y.A., Zhou, X.G., et al. (2012) First-Principles Calculations of Propane Dehydrogenation over PtSn Catalysts. ACS Catalysis, 2, 1247-1258. https://doi.org/10.1021/cs300031d
- 20. Kaichev, V.V., Chesalov, Y.A., Saraev, A.A., et al. (2019) A Mechanistic Study of Dehydrogenation of Propane over Vanadia-Titania Catalysts. The Journal of Physical Chemistry C, 123, 19668-19680. https://doi.org/10.1021/acs.jpcc.9b04991
- 21. Zhang, F., Wu, R., Yue, Y., et al. (2011) Chromium Oxide Sup-ported on ZSM-5 as a Novel Efficient Catalyst for Dehydrogenation of Propane with CO2. Microporous and Mesopo-rous Materials, 145, 194-199. https://doi.org/10.1016/j.micromeso.2011.05.021
- 22. Xie, Y., Hua, W., Yue, Y., et al. (2010) Dehydrogenation of Propane to Propylene over Ga2O3 Supported on Mesoporous HZSM‐5 in the Presence of CO2. Chinese Journal of Chemistry, 28, 1559-1564. https://doi.org/10.1002/cjoc.201090265
- 23. De, M. and Kunzru, D. (2004) Oxidative Dehydrogenation of Propane on V2O5/ZrO2 Catalyst. Catalysis Letters, 96, 33-42. https://doi.org/10.1023/B:CATL.0000029526.50161.3e
- 24. Jibril, B.Y. (2004) Propane Oxidative Dehydrogena-tion over Chromium Oxide-Based Catalysts. Applied Catalysis A: General, 264, 193-202. https://doi.org/10.1016/j.apcata.2003.12.054
- 25. Frey, F.E. and Huppke, W.F. (1933) Equilibrium Dehydrogena-tion of Ethane, Propane, and the Butanes. Industrial & Engineering Chemistry, 25, 54-59. https://doi.org/10.1021/ie50277a013
- 26. Agafonov, Y.A., Gaidai, N.A. and Lapidus, A.L. (2014) Influence of the Preparation Conditions for Catalysts CrOx/ SiO2 on Their Efficiency in Propane Dehydrogenation in the Presence СО2. Russian Chemical Bulletin, 63, 381-388. https://doi.org/10.1007/s11172-014-0441-x
- 27. Jin, R., Easa, J., Tran, D.T., et al. (2020) Ru-Promoted CO2 Acti-vation for Oxidative Dehydrogenation of Propane over Chromium Oxide Catalyst. Catalysis Science & Technology, 10, 1769-1777. https://doi.org/10.1039/C9CY01990A
- 28. Wang, J., Song, Y.H., Liu, Z.T., et al. (2021) Active and Selective Nature of Supported CrOx for the Oxidative Dehydrogenation of Propane with Carbon Dioxide. Applied Catal-ysis B: Environmental, 297, Article ID: 120400. https://doi.org/10.1016/j.apcatb.2021.120400
- 29. Takahara, I., et al. (1998) Promoting Effects of CO2 on Dehy-drogenation of Propane over a SiO2-Supported Cr2O3 Catalyst. Studies in Surface Science and Catalysis, 114, 419-422. https://doi.org/10.1016/S0167-2991(98)80785-4
- 30. Kocoń, M., Michorczyk, P. and Ogonowski, J. (2005) Effect of Supports on Catalytic Activity of Chromium Oxide-Based Catalysts in the Dehydrogenation of Propane with CO2. Catalysis Letters, 101, 53-57. https://doi.org/10.1007/s10562-004-3749-6
- 31. Zheng, B., Hua, W., Yue, Y., et al. (2005) Dehydrogenation of Propane to Propene over Different Polymorphs of Gallium Oxide. Journal of Catalysis, 232, 143-151. https://doi.org/10.1016/j.jcat.2005.03.001
- 32. Michorczyk, P. (2003) Dehydrogenation of Propane to Propene over Gallium Oxide in the Presence of CO2. Applied Catalysis A: General, 251, 425-433. https://doi.org/10.1016/S0926-860X(03)00368-5
- 33. Michorczyk, P., Kuśtrowski, P., Kolak, A., et al. (2013) Ordered Mesoporous Ga2O3 and Ga2O3-Al2O3 Prepared by Nanocasting as Effective Catalysts for Propane Dehydro-genation in the Presence of CO2. Catalysis Communications, 35, 95-100. https://doi.org/10.1016/j.catcom.2013.01.019
- 34. Xu, B., Zheng, B., Hua, W., et al. (2006) Support Effect in De-hydrogenation of Propane in the Presence of CO2 over Supported Gallium Oxide Catalysts. Journal of Catalysis, 239, 470-477. https://doi.org/10.1016/j.jcat.2006.02.017
- 35. Xiao, H., Zhang, J., Wang, P., et al. (2016) Dehydrogena-tion of Propane over a Hydrothermal-Synthesized Ga2O3-Al2O3 Catalyst in the Presence of Carbon Dioxide. Catalysis Science & Technology, 6, 5183-5195. https://doi.org/10.1039/C5CY02161H
- 36. Liu, Y., Zhang, G., Wang, J., et al. (2021) Promoting Propane Dehy-drogenation with CO2 over Ga2O3/SiO2 by Eliminating Ga-Hydrides. Chinese Journal of Catalysis, 42, 2225-2233. https://doi.org/10.1016/S1872-2067(21)63900-1
- 37. Solymosi, F., Tolmacsov, P. and Kedves, K. (2003) CO2 Reforming of Propane over Supported Rh. Journal of Catalysis, 216, 377-385. https://doi.org/10.1016/S0021-9517(02)00071-4
- 38. Pradhan, S., Upham, D.C., Metiu, H., et al. (2016) Partial Oxidation of Propane with CO2 on Ru Doped Catalysts. Catalysis Science & Technology, 6, 5483-5493. https://doi.org/10.1039/C6CY00011H
- 39. Nowicka, E., Reece, C., Althahban, S.M., et al. (2018) Elucidating the Role of CO2 in the Soft Oxidative Dehydrogenation of Propane over Ceria-Based Catalysts. ACS Catalysis, 8, 3454-3468. https://doi.org/10.1021/acscatal.7b03805
- 40. Zhang, W., Wang, H., Jiang, J., et al. (2020) Size Dependence of Pt Catalysts for Propane Dehydrogenation: From Atomically Dispersed to Nanoparticles. ACS Catalysis, 10, 12932-12942. https://doi.org/10.1021/acscatal.0c03286
- 41. Luo, W., Baaziz, W., Cao, Q., et al. (2017) Design and Fabrication of Highly Reducible PtCo Particles Supported on Graphene-Coated ZnO. ACS Applied Materials & Interfaces, 9, 34256-34268. https://doi.org/10.1021/acsami.7b10638
- 42. Bian, K., Zhang, G., Zhu, J., et al. (2022) Promoting Propane Dehydrogenation with CO2 over the PtFe Bimetallic Catalyst by Eliminating the Non-Selective Fe(0) Phase. ACS Catalysis, 12, 6559-6569. https://doi.org/10.1021/acscatal.2c00649
- 43. Wang, H., Zhang, X., Su, Z., et al. (2024) Dealuminated Beta Stabi-lized Bimetallic PtCo Nanoparticles for Oxidative Dehydrogenation of Propane with CO2. Fuel, 358, Article ID: 130248. https://doi.org/10.1016/j.fuel.2023.130248
- 44. Mata-Martinez, A., Jimenez-Lam, S.A., Talavera-López, A., et al. (2018) The Effect of Sn Content in a Pt/KIT-6 Catalyst over Its Performance in the Dehydrogenation of Propane. Inter-national Journal of Chemical Reactor Engineering, 16, Article ID: 20170237. https://doi.org/10.1515/ijcre-2017-0237
- 45. Wang, Y., Wang, J., Zhang, Y., et al. (2022) Revealing the Catalytic Role of Sn Dopant in CO2-Oxidative Dehydrogenation of Propane over Pt/Sn‐CeO2 Catalyst. ChemCatChem, 14, e202200982. https://doi.org/10.1002/cctc.202200982
- 46. Yang, G.Q., Ren, X., Kondratenko, V.A., et al. (2023) Promotional Nature of Sn on Pt/CeO2 for the Oxidative Dehydrogenation of Propane with Carbon Dioxide. Nano Research, 16, 6237-6250. https://doi.org/10.1007/s12274-022-5316-0
- 47. Zhai, P., Xie, Z., Huang, E., et al. (2023) CO2-Mediated Oxidative Dehydrogenation of Propane Enabled by Pt-Based Bimetallic Catalysts. Chem, 9, 3268-3285. https://doi.org/10.1016/j.chempr.2023.07.002
- 48. Xing, F., Ma, J., Shimizu, K., et al. (2022) High-Entropy Inter-metallics on Ceria as Efficient Catalysts for the Oxidative Dehydrogenation of Propane Using CO2. Nature Communica-tions, 13, Article No. 5065. https://doi.org/10.1038/s41467-022-32842-8
- 49. Reber, A.C. and Khanna, S.V. (2017) Superatoms: Electronic and Geometric Effects on Reactivity. Accounts of Chemical Research, 50, 255-263. https://doi.org/10.1021/acs.accounts.6b00464
- 50. Sun, Q., Wang, N., Fan, Q., et al. (2020) Subnanometer Bime-tallic Platinum-Zinc Clusters in Zeolites for Propane Dehydrogenation. Angewandte Chemie International Edition, 59, 19450-19459. https://doi.org/10.1002/anie.202003349
- 51. Poths, P., Li, G., Masubuchi, T., et al. (2023) Got Coke? Self-Limiting Poisoning Makes an Ultra Stable and Selective Sub-Nano Cluster Catalyst. ACS Catalysis, 13, 1533-1544. https://doi.org/10.1021/acscatal.2c05634
- 52. Rong, H., Ji, S., Zhang, J., et al. (2020) Synthetic Strate-gies of Supported Atomic Clusters for Heterogeneous Catalysis. Nature Communications, 11, Article No. 5884. https://doi.org/10.1038/s41467-020-19571-6
- 53. Álvarez, A., Borges, M., Corral-Pérez, J.J., et al. (2017) CO2 Activation over Catalytic Surfaces. ChemPhysChem, 18, 3135-3141. https://doi.org/10.1002/cphc.201700782
- 54. Austin, N., Butina, B. and Mpourmpakis, G. (2016) CO2 Activation on Bimetallic CuNi Nanoparticles. Progress in Natural Science: Materials International, 26, 487-492. https://doi.org/10.1016/j.pnsc.2016.08.007
- 55. Le, T.A., Kang, J.K. and Park, E.D. (2018) CO and CO2 Methana-tion over Ni/SiC and Ni/SiO2 Catalysts. Topics in Catalysis, 61, 1537-1544. https://doi.org/10.1007/s11244-018-0965-7
- 56. Pakhare, D. and Spivey, J. (2014) A Review of Dry (CO2) Re-forming of Methane over Noble Metal Catalysts. Chemical Society Reviews, 43, 7813-7837. https://doi.org/10.1039/C3CS60395D
- 57. Dong, J. (2022) Insights into the CeO2 Facet-Depended Performance of Propane Oxidation over Pt-CeO2 Catalysts. Journal of Catalysis, 407, 174-185. https://doi.org/10.1016/j.jcat.2022.01.026
- 58. Gao, X. (2012) Structural Effects of Cerium Oxides on Their Ther-mal Stability and Catalytic Performance in Propane Oxidation Dehydrogenation. Chinese Journal of Catalysis, 33, 1069-1074. https://doi.org/10.1016/S1872-2067(11)60404-X
- 59. Sun, G., Zhao, Z.J., Mu, R., et al. (2018) Breaking the Scaling Relationship via Thermally Stable Pt/Cu Single Atom Alloys for Catalytic Dehydrogenation. Nature Communi-cations, 9, Article No. 4454. https://doi.org/10.1038/s41467-018-06967-8
- 60. Xiao, L., Shan, Y.L., Sui, Z.J., et al. (2020) Beyond the Reverse Horiuti-Polanyi Mechanism in Propane Dehydrogenation over Pt Catalysts. ACS Catalysis, 10, 14887-14902. https://doi.org/10.1021/acscatal.0c03381
- 61. Jiang, F., Zeng, L., Li, S.R., et al. (2014) Propane Dehydrogenation over Pt/TiO2-Al2O3 Catalysts. ACS Catalysis, 5, 438-447.
- 62. Sun, X., Liu, M., Huang, Y., et al. (2019) Electronic In-teraction between Single Pt Atom and Vacancies on Boron Nitride Nanosheets and Its Influence on the Catalytic Perfor-mance in the Direct Dehydrogenation of Propane. Chinese Journal of Catalysis, 40, 819-825. https://doi.org/10.1016/S1872-2067(18)63196-1
- 63. Furukawa, S. and Komatsu, T. (2017) Intermetallic Com-pounds: Promising Inorganic Materials for Well-Structured and Electronically Modified Reaction Environments for Effi-cient Catalysis. ACS Catalysis, 7, 735-765. https://doi.org/10.1021/acscatal.6b02603
- 64. Xing, F., Jeon, J., Toyao, T., et al. (2019) A Cu-Pd Single-Atom Alloy Catalyst for Highly Efficient NO Reduction. Chemical Science, 10, 8292-8298. https://doi.org/10.1039/C9SC03172C
- 65. Gomez, E., Kattel, S., Yan, B., et al. (2018) Combining CO2 Reduction with Propane Oxidative Dehydrogenation over Bimetallic Catalysts. Nature Communications, 9, Article No. 1398. https://doi.org/10.1038/s41467-018-03793-w
- 66. Gomez, E., Xie, X.H. and Chen, J.G. (2019) The Effects of Bi-metallic Interactions for CO2-Assisted Oxidative Dehydrogenation and Dry Reforming of Propane. AIChE Journal, 65, e16670. https://doi.org/10.1002/aic.16670
- 67. Guo, M., Liu, X. and Amorelli, A. (2019) Activation of Small Molecules over Praseodymium-Doped Ceria. Chinese Journal of Catalysis, 40, 1800-1809. https://doi.org/10.1016/S1872-2067(19)63369-3
- 68. Nawaz, Z., Tang, X., Wang, Y., et al. (2010) Parametric Characterization and Influence of Tin on the Performance of Pt-Sn/SAPO-34 Catalyst for Selective Propane Dehydro-genation to Propylene. Industrial & Engineering Chemistry Research, 49, 1274-1280. https://doi.org/10.1021/ie901465s
- 69. Zhang, Y., Zhou, Y., Qiu, A., et al. (2006) Propane Dehydrogenation on PtSn/ZSM-5 Catalyst: Effect of Tin as a Promoter. Catalysis Communications, 7, 860-866. https://doi.org/10.1016/j.catcom.2006.03.016
- 70. Xing, F.L., Ma, J., et al. (2022) High-Entropy Intermetallics on Ceria as Efficient Catalysts for the Oxidative Dehydrogenation of Propane Using CO2. Nature Communications, 13, Ar-ticle No. 5065. https://doi.org/10.1038/s41467-022-32842-8
