Botanical Research
Vol.
08
No.
03
(
2019
), Article ID:
30528
,
12
pages
10.12677/BR.2019.83039
Study on the Microwave-Assisted Extraction of Essential Oil from Cinnamomum longipaniculatum with Deep Eutectic Solvents
Junming Shi, Tingting Li, Shizheng Song, Yangyang Zi, Chunhui Ma*
College of Material Science and Engineering, Northeast Forestry University, Harbin Heilongjiang
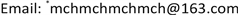
Received: May 10th, 2019; accepted: May 22nd, 2019; published: May 29th, 2019

ABSTRACT
In this study, essential oil of Cinnamomum longepaniculatum was obtained by microwave assisted distillation with deep eutectic solvent (DES). Eutectic salt made by melting 1,4-butanediol and choline chloride was added into the solvent water of traditional steam distillation. The molar ratio of hydrogen bond acceptor and hydrogen bond donor was optimized; the optimum proportion of eutectic salt was obtained (the molar ratio of choline chloride to 1,4-butanediol is 1:5); the volume ratio of eutectic salt to water was optimized (the volume ratio of eutectic solvent to water is 5:5), the best solvent was obtained by steam distillation. The process parameters of microwave assisted distillation were optimized by single factor test and response surface. The results showed that microwave power is 700 W; the operating temperature is 120˚C; microwave time is 20 min. The extraction yield of essential oil from Cinnamomum longepaniculatum is 25.0 mL/Kg. Under the same microwave-assisted extraction conditions, the amount of essential oil extracted by steam distillation is 21.3 mL/Kg. The response surface optimization experiment was carried out for the solid-liquid ratio at microwave time, microwave power and microwave temperature, in which multi linearity regress mechanic to analyze data is used. It is known that microwave time and microwave power have a strong interaction. GC-MS was used to analyze the components of essential oils, and the results were compared with that of microwave steam distillation. The DPPH and ABTS free radical scavenging experiments showed that the DPPH anion scavenging rate of 50% essential oil was 55.47% and the ABTS cation scavenging rate was 98.78%. As a result, Camphor oil has high scavenging rate of two free radicals, and the clearance ability of ABTS is much higher than that of DPPH.
Keywords:Cinnamomum longipaniculatum, Essential Oil, Deep Eutectic Solvents, Microwave-Assisted Extraction, Free Radical Scavenging Experiment, Response Surface, GC-MS
低共熔溶剂微波辅助萃取油樟精油及抗氧化 特性分析
史峻铭,李婷婷,宋诗政,訾阳阳,马春慧*
东北林业大学材料科学与工程学院,黑龙江 哈尔滨

收稿日期:2019年5月10日;录用日期:2019年5月22日;发布日期:2019年5月29日

摘 要
本研究采用低共熔溶剂微波辅助蒸馏法获得油樟精油,在传统水蒸气蒸馏的溶剂水中加入了由氯化胆碱和1,4-丁二醇熔融制成的低共熔盐,通过优化氢键受体与氢键供体的摩尔比,得到低共熔盐的最佳配比(氯化胆碱与1,4-丁二醇的摩尔比为1:5);通过优化低共熔盐与水的体积比(低共熔盐与水的体积比为5:5),得到水蒸气蒸馏的最佳溶剂。然后通过单因素试验及响应面优化微波辅助蒸馏的过程参数为:微波功率700 W,操作温度120℃,微波时间20 min。所得油樟精油萃取量为25.0 mL/Kg,在同样的微波辅助萃取条件下,水蒸气蒸馏所得精油萃取量为21.3 mL/Kg。对微波时间、微波功率、微波温度、料液比进行响应面优化实验,利用多元线性回归方程进行数据分析,可知微波时间与微波功率具有较强的交互作用。利用GC-MS分析精油的成分,并与水蒸气蒸馏、微波水蒸汽蒸馏精油得分成分做出对比。在DPPH阴离子、ABTS阳离子自由基清除实验中,50%浓度的精油对DPPH阴离子清除率为55.47%,5%浓度的精油对ABTS阳离子清除率为98.78%。可见,油樟精油对两种自由基具有较高的清除率,且对ABTS阳离子的清除能力远高于DPPH阴离子。
关键词 :油樟,精油,低共熔溶剂,微波辅助萃取,清除自由基,响应面,气质联用法(GC-MS)

Copyright © 2019 by author(s) and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
油樟(拉丁名:Cinnamomum longipaniculatum (Gamble))是樟科、樟属常绿乔木,具有生长速度快、萌蘖强、载叶多、病虫少,树形美观、姿态雄伟、木质柔韧、纹理致密等特点,其主要分布于宜宾、川南以及盆周、重庆、湖南、江西等省,又称“宜宾油樟” [1] 。叶互生,卵形或椭圆形,基部楔形至近圆形,边缘软骨质,内卷,薄革质,上面深绿色,光亮,下面灰绿色,晦暗,两面无毛,羽状脉。油樟精油是一种植物源天然活性物质,具有抗氧化活性,清除体内自由基,且对人体副作用少、毒性小、不易产生耐药性,对高效低毒的天然抗氧化剂及低副作用的天然抗炎活性成分的研发有重要意义 [2] 。
植物精油的提取方法多种多样,且不同用途的精油产品需要不同的提取方法来生产。目前主要提取精油的技术有水蒸气蒸馏法 [3] ,同时蒸馏压榨萃取法 [4] ,超临界流体萃取法 [5] ,亚临界水萃取法 [5] ,无溶剂微波萃取法 [6] 和及时控制降压萃取法 [5] 。传统的水蒸气蒸馏法具有设备简单、容易操作、成本低、对环境友好等特点。但由于植物材料长时间的处于高温之下,可能会使其含有的热敏性成分发生热分解,易水解成分发生水解及原料焦化等,对精油产品质量造成不利影响 [7] 。索氏提取与溶剂萃取存在有机溶剂残留以及回收成本过多等问题 [8] [9] 。微波辅助提取法是利用植物样品在微波场中吸收大量的电磁辐射能量,细胞内部含水量及其他极性物质的存在,对微波有选择吸收特性,而周围的非极性萃取剂则吸收少,从而在细胞内部产生热应力 [7] ,强化了提取过程;超声波辅助提取处理具有促进超混相之间的不混溶相之间的传质的机械效应 [10] 。
本实验以微波辅助为加热方式,采用水蒸气蒸馏法提取精油,在水中加入由氢键受体季铵盐(氯化胆碱)和氢键供体(多元醇)所组成的低共熔绿色溶剂(Deep Eutectic Solvents, DES)。DES 具有与传统离子液体相似的物理和化学特性(可作为传统萃取溶剂的绿色替代品,用于从多种基质中分离和预浓缩分析物。DES一般由氢键受体和氢键供体组成。因此,DES是一种由混合物组成的溶剂,这种混合物形成的共晶熔点远低于单个组分 [11] 。它们具有新的有利特征。其中,化学稳定性好,粘度范围广,室温挥发性小,制备简单 [12] 。)但它们的制备在适当的温度下混合两种成分,无需进一步纯化,具有100%的原子经济性 [13] 。与传统的有机溶剂相比,DES不仅具有环保、无毒的、可生物降解性的性质而且具有成本低,易于在实验室合成等优点 [14] 。
本实验在研究现状的基础上,采用低共熔溶剂微波辅助提取方法。以氯化胆碱和1,4-丁二醇按比例配成的低共熔盐溶于水为低共熔溶剂提取精油。通过单因素试验探究了低共熔溶剂最佳配比条件和微波萃取法的最优条件。提取后的精油清除DPPH阴离子、ABTS阳离子自由基实验探究了油樟精油的抗氧化活性。
2. 实验
2.1. 材料与仪器
油樟叶子原料2018年9月采自四川宜宾,粉碎至40~60目待用。
紫外分光光度计采用T6系列紫外分光光度计(北京普析通用仪器有限责任公司),微波合成萃取仪(XH300A,北京祥鹄科技发展有限公司),Agilent气质联用仪。
2.2. 实验方法
2.2.1. 低共熔溶剂的配制
选取氢键受体氯化胆碱和氢键供体多元醇以一定的摩尔比加热熔融,配制成低共熔盐,将其与水分别以一定体积比混合均匀配制成低共熔溶剂,根据精油的提取率,确定低共熔溶剂最佳的组成。
2.2.2. 微波辅助萃取法提取油樟精油
精密称取8.00 g (绝干)风干样品,转移至圆底烧瓶中,加入80mL低共熔溶剂,室温浸渍12 h,使原料与溶剂充分浸润,然后放入微波辅助萃取仪,接上精油提取器收集蒸馏出的精油。
2.2.3. 清除自由基能力测试
清除DPPH阴离子自由基能力测定。DPPH即1,1-二苯基-3-硝基苯肼,是一种很稳定的氮中心的自由基。DPPH检测法的原理是通过DPPH分子中一个稳定的自由基与抗氧化剂提供的一个电子配对结合,生成无色产物,使自由基溶液的典型紫色变浅 [3] 。用95%乙醇配制浓度为0.0%、10.0%、20.0%、30.0%、40.0%、50.0%的精油样品和150 mg/L的DPPH阴离子溶液,取0.1 mL不同浓度样品与3.9 mL DPPH阴离子溶液混合,在黑暗处放置30 min后,在517 nm处测定吸光值,浓度为0.0%的样品的吸光值为A对照,所有吸光值均测定三次,取平均值。DPPH阴离子溶液吸光值与浓度有很好的线性关系,吸光值可以反映不同浓度的精油对自由基的清除率 [3] 。SC% = (1 − A样品/A对照) × 100%,其中A样品为样品溶液在固定波长下的吸光值,A对照为不加样品的溶液在t = 0处的吸光值 [15] 。
清除ABTS阳离子自由基能力测定。ABTS 经活性氧氧化后生成稳定的蓝绿色阳离子自由基ABTS阳离子,如果加入其中的样品溶液有抗氧化成分,那么该物质就会与 ABTS 阳离子自由基发生反应而使溶液褪色 [16] 。精密称取ABTS阳离子0.0406 g和过硫酸钾0.0070 g,分别用去离子水定容到10 mL,等量混合两种溶液,在室温黑暗条件下反应12 h。取1.0 mL溶液,在744 nm处获得用甲醇稀释10倍的ABTS阳离子溶液的吸光值。分别取0.150 mL浓度为0.0%、1.0%、2.0%、3.0%、4.0%和5.0%的精油样品与2.850 mL的ABTS阳离子溶液混合,在室温黑暗条件下放置2 h,测定吸光值,所有吸光值均测定三次,取平均值。SC% = (1 − A样品/A对照) × 100%,其中A样品为样品溶液在固定波长下的吸光值,A对照为不加样品的溶液在t = 0处的吸光值 [15] 。
2.2.4. 油樟精油化学组成分析方法
使用Agilent气质联用仪对三种方法提取所得的油樟精油进行化学组成分析,操作条件:毛细管石英色谱柱(0.25 mm × 0.25 μm,长30 m),气化室和进样温度分别设定为230℃和280℃;升温程序:先以60℃维持5 min,接着以10℃/min的升温速度从60℃升高到120℃保持5 min,然后以10℃/min的升温速度从120℃升高到200℃并维持5 min,再以10℃/min的升温速度从200℃升高到280℃并维持15 min;载气为高纯度氦气,流速1.0 mL/min;样品稀释到乙醚中,比为1:100 (v/v),进样量1 μL;分流比为1:2。质谱条件为:电子轰击(EI)离子源;电子能量为70 eV;原子量范围为15~500 amu;油樟精油的各化学组成与NIST11质谱库信息进行比对确认。
3. 结果与分析
3.1. 低共熔溶剂的组成
选取氢键受体氯化胆碱和氢键供体多元醇(1,4-丁二醇和乙二醇)分别以1:1、1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9的摩尔比加热熔融,配制成低共熔盐,分别取40 mL低共熔盐与40 mL蒸馏水混合均匀,放入8g油樟叶原料进行微波萃取,获得萃取精油的体积随配比不同的变化数据如图1(a)所示。将其与水分别以9:1、8:2、7:3、6:4、5:5、4:6、3:7、2:8、1:9的体积比比混合均匀配制成低共熔溶剂,分别取80 mL上述溶剂,加入8g油樟叶原料进行微波萃取,获得油樟精油的体积随低共熔溶剂与水的配比不同的变化数据如图1(b)所示。根据精油的提取率,确定低共熔溶剂最佳的组成。
3.2. 单因素实验分析
3.2.1. 微波提取精油动力学
精密称取8.00 g (绝干)风干样品,转移至圆底烧瓶中,加入80 mL低共熔溶剂,室温浸渍12 h,使原料与溶剂充分浸润,然后放入微波辅助萃取仪,接上精油提取器收集蒸馏出的精油,每隔1 min读取一次获得精油的体积,如图2(a)所示。在5 min后,提取精油体积大约保持不变。
3.2.2. 微波功率对精油提取率的影响
精密称取8.00 g (绝干)风干样品,转移至圆底烧瓶中,加入80mL低共熔溶剂,室温浸渍12 h,使原料与溶剂充分浸润,然后放入微波辅助萃取仪,接上精油提取器收集蒸馏出的精油,将微波反应时间设置为5 min,加热温度为120℃,微波功率分别为500 W、600 W、700 W、800 W、900 W,记录获得精油的体积,如图2(b)。在500W、600W时,提取精油体积为12.5 mL/Kg;在700 W时,提取精油体积为25 mL/Kg;在800 W时,提取精油体积为11.25 mL/Kg;在900 W时,提取精油体积为13.75 mL/Kg。萃取完成后收集油樟精油,−20℃冷冻保存。
 (a)
(a)
 (b)
(b)
Figure 1. Effect of DES composition on the extraction yield of essential oil. (a) Effect of the mole ratio of choline chloride to 1,4-butanediol on the extraction yield of essential oil; (b) Effect of the volume ratio of deep eutectic salt to water on the extraction yield of essential oil
图1. 低共熔溶剂的组成对精油提取率的影响。(a) 氯化胆碱与1,4-丁二醇的摩尔比对精油提取率的影响;(b) 低共熔盐与水的体积比对精油提取率的影响

Figure 2. Single factor analysis of microwave extraction of essential oil. (a) Kinetic curve of microwave extraction of essential oil; (b) Effect of microwave power on the extraction yield of essential oil; (c) Effect of microwave temperature on the extraction yield of essential oil; (d) Effect of solid-liquid ratio on the extraction yield of essential oil
图2. 微波提取精油单因素分析。(a) 微波提取精油动力学曲线;(b) 微波功率对精油提取率的影响;(c) 微波温度对精油提取率的影响;(d) 料液比对精油提取率的影响
3.2.3. 微波温度对精油提取率的影响
精密称取8.00 g (绝干)风干样品,转移至圆底烧瓶中,加入80 mL低共熔溶剂,室温浸渍12 h,使原料与溶剂充分浸润,然后放入微波辅助萃取仪,接上精油提取器收集蒸馏出的精油,将微波反应时间设置为5 min,微波功率为700 W,加热温度分别为105℃、110℃、115℃、120℃、125℃,记录获得精油的体积,如图2(c)。萃取完成后收集油樟精油,−20℃冷冻保存。从105℃至120℃,提取精油体积增加,120℃与125℃提取精油体积均为25.0 mL/Kg。
3.2.4. 料液比对精油提取率的影响
精密称取8.00 g (绝干)风干样品,转移至圆底烧瓶中,分别以1:6、1:8、1:10、1:12、1:14的料液比加入低共熔溶剂,室温浸渍12 h,使原料与溶剂充分浸润,然后放入微波辅助萃取仪,接上精油提取器收集蒸馏出的精油,将微波反应时间设置为5 min,微波功率为700 W,加热温度为120℃,记录获得精油的体积,如图2(d)。萃取完成后收集油樟精油,−20℃冷冻保存。1:6至1:10,精油体积增加,在1:10时提取精油体积为25.0 mL/Kg,但随后精油体积逐渐减小。精油的提取率出现下降,原因是水油比例增加,部分物质与水结合形成水包油结构,导致挥发油溶解现象 [17] 。
3.3. 响应面优化实验
3.3.1. 响应面试验设计与结果分析
在单因素试验的基础上,根据Box-Behnken试验设计原理,以精油提取率(Y)为响应值,选取A (微波时间)、B (微波功率)、C (微波温度)、D (液料比)四个因素,进行响应面优化实验,实验结果见表1。
3.3.2. 回归模型的建立与显著性分析
运用Design-Expert对表1进行多元回归拟合,得到精油提取率(Y)对自变量微波时间(A)、微波功率(B)、微波温度(B)、液料比(D)的多元回归方程:Y = 25.05 + 2.32A + 0.77B + 1.01C + 1.74D + 1.09AB − 0.32AC + 1.32AD + 0.78BC + 0.53BD + 0.51CD − 1.93A2 − 3.05B2 − 1.48C2 − 1.26D2。对回归模型进行方差分析,结果见表2。
为了进一步研究各因素之间的相互作用,我们对微波功率、提取时间和液料比进行了测定。在表2中,F值5.89表明模型具有显著性,但这种模型F值出现的概率仅为0.08%,可以作为噪声处理。“可能性 > F”小于0.0500表明模型具有显著性,在表格中,A,B,C,D,A2,B2,C2,D2都是显著模型。大于0.1000的数值表明模型不具有显著性。如果有很多显著模型(不包括那些需要支持层次结构的),模型降阶(或提纯)是必须的。失拟项1036.19表明失拟项是显著的,F值失拟项发生的概率只有0.01%,,可被作为噪声处理。显著的拟合不足是不利的,所以希望模型能够拟合。在表3中,决定系数是0.8461,调整平方是0.7024,两者之间存在合理的一致性。精密度测量了信噪比,比值大于4是可取的。目前比值为7.924,表明存在一个错误信号。此模型可用于导航设计空间。最终萃取效率(Y)方程为Y = 25.05 + 2.32A + 0.77B + 1.01C + 1.74D + 1.09AB − 0.32AC + 1.32AD + 0.78BC + 0.53BD + 0.51CD − 1.93A2 − 3.05B2 − 1.48C2 − 1.26D2。由方程可知,我们需要研究A与B、A与C、A与D、B与C、B与D、C与D相互作用对萃取效率的影响。该软件对精油提取率条件进行了预测,精油的理论提取率为26.87 mL/Kg;精密称取三份油樟叶片粉末8.00 g进行验证试验,选择微波功率为700 W,微波提取温度为120℃,料液比1:10 g/mL,微波加热5.0 min,精油的提取率分别为25.82、25.64、26.10 mL/Kg,与理论值误差为3.78%。
从表3中得知,预测平方0.1136与调整平方0.7024是合理的,“精密度”测量的是信噪比,比值大于4时可取的,目前的比值是7.924,是合理信号。从图3中看出,六个因素的曲面都比较陡峭,说明微波提取时间、微波温度、微波功率、料液比对提取效果都有明显的显著。另外,微波提取时间、微波温度、微波功率、料液比在所选的水平范围内都有定点,说明最佳值在所选的范围内。由响应面图曲面坡度越陡峭、等高线越密集成椭圆形表示两两因素交互影响越大的原则 [18] [19] [20] ,因子A(微波时间)与因子D(微波功率)之间所形成的响应面曲面坡度在两因素交互作用响应面中最为陡峭,即微波时间与微波功率之间具有最强的交互作用。
Table 1. Response surface test design and results
表1. 响应面试验设计方案及结果

Figure 3. Response surfaces diagram of the interaction of two factors
图3. 两两因素交互作用的响应面图
Table 2. Regression coefficient test
表2. 回归系数检验
Table 3. Reliability analysis of regression equation
表3. 回归方程的可信度分析
3.4. 油樟精油抗氧化能力测试
在人体内,当电子流变成非耦合(出现未配对单电子)时就会产生自由基 [21] ,自由基对人类有着双重影响,在生命系统中扮演着双重角色 [7] 。正常情况下,机体自由基的产生与消退处于平衡状态 [22] 。在本研究中自由基清除率用SC%表示,SC% = (1 − A样品/A对照) × 100%,其中A样品为样品溶液在固定波长下的吸光值,A对照为不加样品的溶液在t = 0处的吸光值 [15] 。
精油清除DPPH阴离子自由基能力
测定新配的不加精油样品的DPPH阴离子溶液在517 nm处的吸光值,此吸光度值是最大吸光度值,为1.244。待精油样品与DPPH阴离子溶液反应30 min后,在517 nm处测得各样品的吸光度值,不同浓度的精油对DPPH阴离子的清除率如图4(a)所示。DPPH阴离子溶液浓度为 0.0015 g/100 mL,空白对照组吸光值0.420。由图可知,10%浓度的精油对DPPH阴离子的清除率为7.4%,50%浓度的精油对DPPH阴离子的清除率为55.47%,随着精油浓度的提高,对DPPH阴离子的清除率也逐渐提高。可见油樟精油对DPPH阴离子的抗氧化活性很高。对比微波水蒸气蒸馏和传统水蒸气蒸馏,微波水蒸气蒸馏中50%浓度的精油对DPPH阴离子的清除率为45.68%,传统水蒸气蒸馏中50%浓度的精油对DPPH阴离子的清除率为33.45%。可见微波低共熔溶剂蒸馏出的精油比微波水蒸气蒸馏和传统水蒸气蒸馏对DPPH阴离子的清除率要高。
精油清除ABTS阳离子自由基能力
新配置的ABTS阳离子溶液在744 nm处取得最大吸光度值为1.095,空白对照组吸光度值为1.812。不同浓度的精油对ABTS阳离子的清除率随精油浓度的变化曲线如图4(b)所示。1%浓度的精油对ABTS阳离子的清除率为56.34%,5%浓度的精油对ABTS阳离子的清除率为98.78%,可见较低浓度的精油对ABTS阳离子有较高的清除率。而且随着精油浓度的提高,对ABTS阳离子的清除率也逐渐提高。对比微波水蒸气蒸馏和传统水蒸气蒸馏,微波水蒸气蒸馏中5%浓度的精油对ABTS阳离子的清除率为95.24%,传统水蒸气蒸馏中5%浓度的精油对ABTS阳离子的清除率为85.11%。可见微波低共熔溶剂蒸馏出的精油比微波水蒸气蒸馏和传统水蒸气蒸馏对ABTS阳离子的清除率要高。
3.5. 油樟精油化学组成分析
使用Agilent气质联用仪对三种方法提取所得的油樟精油进行化学组成分析,主要的化学组成见表4所示。由表4可知,油樟挥发性成分主要由烯烃和醇类化合物组成。低共熔溶剂微波水蒸馏法、微波水蒸馏法、传统水蒸馏法获得的精油中成分种类大致相同,但含量稍有差异。低共熔溶剂微波水蒸馏法获得的精油中,含量最高的为桉叶油醇,相对含量为63.43%;其次是桧烯,相对含量为12.54%;α-松油醇的含量也较高,相对含量为10.28%。微波水蒸馏法获得的精油中,含量最高的也为桉叶油醇,相对含量为62.81%;其次是桧烯,相对含量为12.23%;α-松油醇的含量也较高,相对含量为9.45%。传统水蒸馏法获得的精油中,含量最高的也为桉叶油醇,相对含量为54.55%;其次是α-松油醇,相对含量为19.87%;桧烯的含量也较高,相对含量为10.22%。由于在低共熔溶剂微波水蒸馏法获得的精油中不饱和烯烃成分所占比例较大,所以清除自由基效果更强。而在传统水蒸馏法获得的精油中,醇类成分所占比例较大。
Table 4. Volatile compounds in C. longepaniculatum essential oil
表4. 油樟精油挥发性成分分析
注:“-”代表未检出。

Figure 4. Free radical scavenging ratio of essential oil. (a) DPPH anion free radical scavenging ratio of essential oil with different concentration; (b) ABTS cation free radical scavenging ratio of essential oil with different concentration
图4. 清除自由基能力测试结果。(a) 不同浓度的精油对DPPH阴离子自由基的清除率;(b) 不同浓度的精油对ABTS阳离子自由基的清除率
4. 结论
本研究采用低共熔溶剂微波辅助萃取法提取油樟精油,在传统水蒸气蒸馏的溶剂水中加入了由氯化胆碱和1,4-丁二醇组成的低共熔溶剂,通过筛选低共熔溶剂的条件得知氯化胆碱与1,4-丁二醇的摩尔比为1:5,低共熔溶剂与水的体积比为5:5,通过单因素试验和响应面优化法优化了微波萃取的过程参数为:微波时间20 min,微波功率700 W,操作温度120℃,微波时间20 min,最佳料液比为1:10。所得油樟精油萃取量为25.0 mL/Kg,在同样的微波辅助萃取条件下,水蒸气蒸馏所得精油萃取量为21.3 mL/Kg。对微波时间、微波温度、微波功率、料液比进行响应面测试实验,得到多元线性回归方程,分析数据可得知微波时间与微波功率具有较强的交互作用。利用GC-MS对精油的成分进行分析,并对比水蒸气蒸馏、微波水蒸汽蒸馏的精油成分,得知三种方法获得精油成分相同但含量不同。低共熔溶剂微波水蒸馏法获得的精油中,含量最高的为桉叶油醇,相对含量为63.43%;其次是桧烯,相对含量为12.54%;α-松油醇的含量也较高,相对含量为10.28%。微波水蒸馏法获得的精油中,含量最高的也为桉叶油醇,相对含量为62.81%;其次是桧烯,相对含量为12.23%;α-松油醇的含量也较高,相对含量为9.45%。传统水蒸馏法获得的精油中,含量最高的也为桉叶油醇,相对含量为54.55%;其次是α-松油醇,相对含量为19.87%;桧烯的含量也较高,相对含量为10.22%。在DPPH阴离子、ABTS阳离子自由基清除实验,50%浓度的精油对DPPH阴离子清除率为55.47%,5%浓度的精油对ABTS阳离子清除率为98.78%。可见,油樟精油对两种自由基具有较高的清除率,且对ABTS的清除能力远高于DPPH。微波低共熔溶剂蒸馏对ABTS和DPPH的清除率高于微波水蒸汽蒸馏和传统水蒸汽蒸馏。
致 谢
作者感谢东北林业大学大学生创新训练(CL201801)项目,东北林业大学双一流建设启动金(YQ2015-02)和黑龙江省博士后启动金(LBH-Q16001)的资助。
文章引用
史峻铭,李婷婷,宋诗政,訾阳阳,马春慧. 低共熔溶剂微波辅助萃取油樟精油及抗氧化特性分析
Study on the Microwave-Assisted Extraction of Essential Oil from Cinnamomum longipaniculatum with Deep Eutectic Solvents[J]. 植物学研究, 2019, 08(03): 307-318. https://doi.org/10.12677/BR.2019.83039
参考文献
- 1. 文楚前. 油樟良种繁育及栽培利用研究[J]. 种子科技, 2018, 36(11): 77-78.
- 2. 丛赢, 张琳, 祖元刚, 杨磊, 昝鹏. 油樟(Cinnamomum longepaniculatum)精油的抗炎及抗氧化活性初步研究[J]. 植物研究, 2016, 36(6): 949-954 + 960
- 3. 赵天明. 植物精油提取技术研究进展[J]. 广州化工, 2016, 44(13): 16-17 + 44.
- 4. Eikani, M.H., Golmohammad, F. and Rowshanzamir, S. (2007) Subcritical Water Extraction of Essential Oils from Coriander Seeds (Coriandrum sativum L.). Journal of Food Engineering, 80, 735-740. https://doi.org/10.1016/j.jfoodeng.2006.05.015
- 5. Lucchesi, M.E., Chemat, F. and Smadja, J. (2004) Solvent-Free Microwave Extraction of Essential Oil from Aromatic Herbs: Comparison with Conventional HydroDistillation. Journal of Chromatography A, 1043, 323-327. https://doi.org/10.1016/j.chroma.2004.05.083
- 6. 张艳东, 程翠林, 樊梓鸾, 王振宇. 植物精油的提取、成分分析以及抗氧化活性研究[J]. 食品工业科技, 2017, 38(3): 390-394.
- 7. 杨君, 张献忠, 高宏建, 尹洁, 叶兴乾. 天然植物精油提取方法研究进展[J]. 中国食物与营养, 2012, 18(9): 31-35.
- 8. Sodeifian, G., Ardestani, N.S., Ali Sajadian, S. and Ghorbandoost, S. (2016) Application of Supercritical Carbon Dioxide to Extract Essential Oil from Cleome Coluteoides Boiss: Experimental, Response Surface and Grey Wolf Optimization Methodology. The Journal of Supercritical Fluids, 114, 55-63. https://doi.org/10.1016/j.supflu.2016.04.006
- 9. Feng, X.-F., Jing, N., Li, Z.-G., Wei, D. and Lee, M.-R. (2014) Ultrasound-Microwave Hybrid Assisted Extraction Coupled to Headspace Solid Phase Microextraction for Fast Analysis of Essential Oil in Dry Traditional Chinese Medicine by GC-MS. Chromatographia, 77, 619-628. https://doi.org/10.1007/s10337-014-2642-8
- 10. Yang, B., Zhao, M., Shi, J., Yang, N. and Jiang, Y. (2007) Effect of Ultrasonic Treatment on the Recovery and DPPH Radical Scavenging Activity of Polysaccharides from Longan Fruit Pericarp. Food Chemistry, 106, 685-690. https://doi.org/10.1016/j.foodchem.2007.06.031
- 11. Tang, B. and Row, K.H. (2013) ChemInform Abstract: Recent Developments in Deep Eutectic Solvents in Chemical Sciences. ChemInform, 44, 1427-1454. https://doi.org/10.1002/chin.201350241
- 12. Shishov, A., Chroma, R., Vakh, C., Kuchar, J., Simon, A., Andruch, V. and Bulatov, A. (2019) In Situ Decomposition of Deep Eutectic Solvent as a Novel Approach in Liquid-Liquid Microextraction. Analytica Chimica Acta, 1065, 49-55. https://doi.org/10.1016/j.aca.2019.03.038
- 13. Tran, P.H. and Tran, P.V. (2019) A Highly Selective and Efficient Method for the Production of 5-Hydroxymethylfurfural from Dehydration of Fructose Using SACS/DES Catalytic System. Fuel, 246, 18-23. https://doi.org/10.1016/j.fuel.2019.02.112
- 14. 李上, 赵奕萍, 王鹏, 李祖光. 低共熔溶剂在环境分析中的应用进展[J]. 分析仪器, 2019(2): 138-142.
- 15. 王艺蓓, 孙莉寒, 武剑栋, 马春慧. 基于近红外光谱和GC-MS法对油樟叶中挥发油的抗氧化研究和化学组成分析[J]. 植物学研究, 2018, 7(3): 251-259.
- 16. 朱玉昌, 焦必宁. ABTS法体外测定果蔬类总抗氧化能力的研究进展[J]. 食品与发酵工业, 2005, 31(8): 77-80.
- 17. 罗华磊. 影响黄芪挥发油提取的因素[J]. 食品安全导刊, 2018(33): 167.
- 18. 刘琨毅, 王琪, 郑佳, 等. 乳酸链球菌素在中式腊肠防腐保鲜中的应用[J]. 中国食品添加剂, 2018(2): 144-149.
- 19. 黄壹杨, 刘琨毅, 王琪, 等. 基于响应面法优化红豆米酒发酵工艺的研究[J]. 食品与发酵工业, 2018, 44(5): 130-134.
- 20. 罗小芳, 郭乙颖, 胡柳, 等. 响应面法优化云南宣木瓜齐墩果酸和熊果酸的提取工艺研究[J]. 食品研究与开发, 2018, 39(17): 31-36.
- 21. Valko, M., Rhodes, C.J., Moncol, J., Izakovic, M. and Mazur, M. (2006) Free Radicals, Metals and Antioxidants in Oxidative Stress-Induced Cancer. Chemico-Biological Interactions, 160, 1-40. https://doi.org/10.1016/j.cbi.2005.12.009
- 22. 黄元乔, 黄元汛, 宋高晴, 章进. 活性氧自由基特性及对衰老过程的作用[J]. 湖北体育科技, 1995(4): 62-63 + 61.
NOTES
*通讯作者。
