Metallurgical Engineering
Vol.02 No.04(2015), Article ID:16548,9
pages
10.12677/MEng.2015.24025
The Removal Methods of Iron Ions in Non-Ferrous Metallurgy and Other Industrial Processes
Jiehao Xue, Kai Huang*
School of Metallurgical & Ecological Engineering, University of Science and Technology Beijing, Beijing
Received: Nov. 25th, 2015; accepted: Dec. 14th, 2015; published: Dec. 17th, 2015
Copyright © 2015 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
The current removal methods of iron ions in hydrometallurgical processes and other industrial processes have been reviewed. In this review, an extensive list of iron removal processes has been discussed. It is well known that the traditional methods such as precipitation may cause severe secondary pollution and resources waste, but some of the removal methods show good removal efficiency for iron ion. This may offer the prospect of a novel, ecofriendly, cleaner and shortened process for many traditional industrial processes.
Keywords:Iron Ions Pollution, Removal Methods, Biosorption

有色冶金等工业过程中铁离子污染 及其处理方法探讨
薛捷豪,黄凯*
北京科技大学冶金与生态工程学院,北京

收稿日期:2015年11月25日;录用日期:2015年12月14日;发布日期:2015年12月17日

摘 要
对有色冶金及其他工业过程中铁离子污染现状、危害、治理途径及可行性进行了简要的概述,并对各种处理方法的原理、特点等前景作了进一步的展望,为实现对铁离子污染水体进行有效的生态治理及高效安全利用提供了新的技术途径。
关键词 :铁离子污染,治理途径,生物吸附

1. 引言
铁在地壳中含量仅次于氧、硅、铝而居于第四位,是仅次于铝而居于第二位的金属。铁在日常生活中随处可见,常见的含铁矿物主要有磁铁矿(Fe3O4)、赤铁矿(Fe2O3)、菱铁矿(FeCO3)、黄铁矿(FeS2)、褐铁矿(2Fe2O3∙3H2O)等。从污染或危害的角度来认识和评价铁的作用,这方面的研究还比较少,但是正因为其作为一种地壳中高丰度的元素,普遍存在,因此其被视为污染或者有害元素的场合并不少见,对其这方面的性质和特点做一探究,具有较重要的实用意义。
2. 铁污染危害
2.1. 铁在有色冶金过程工业中的危害
铁是600多种矿物的主要组成元素[1] ,差不多所有以矿物为原料的冶金工业,均涉及铁的分离或者提取。
在长期的冶金实践中,人们习惯将冶金分为铁冶金以及非铁冶金(即有色金属冶金)。铁冶金是从自然界中含铁成分高的矿石中提取铁,而非铁冶金诸如在湿法炼锌、氯化湿法冶金[2] 、硫酸铝生产[3] 、镉回收工艺[4] ,铜冶金中硫酸镍回收工艺[5] 、钴冶金过程[6] 等,以上诸多程序均普遍包含除铁工序,即将铁与需要提取的有用金属分离。
火法冶金常通过造渣,使铁成为氧化物或硅酸盐进入渣中从而与需要提取的金属分离,但造渣之后常形成金属分散以及难以回收有用金属等问题。而湿法冶金的发展及应用,与铁的分离有着密切的联系[7] 。其中,锌冶炼过程中的除铁问题,在湿法冶金中最具有代表性。许多重要的除铁工艺,都是从湿法炼锌发展来的。
铁在湿法冶金中具有很大的危害。例如在湿法炼锌电解时,Fe2+会在阳极氧化为Fe3+,在阴极又还原为Fe2+,如此不断循环,会增加电能消耗,降低电流效率。一般控制铁含量为2~5 mg/L。而原料矿中一般含铁5%~15%,有的高铁闪锌矿含铁可达20%~25%,酸性浸出后,进入浸出液,必须通过除铁步骤使溶液含Fe < 20 mg/L,大量Fe进入铁渣,同时可带走As、Sb杂质,使溶液含As、Sb < 0.1 mg/L。湿法炼锌厂产出的铁渣量大,且含H2SO4,含Cu、Cd、Pb、Zn、In、As、Sb、F、Cl等有害杂质,长期堆存会造成环境污染和资源浪费,必须寻找合适的方法处理[8] 。
铁的控制不仅存在于湿法冶金工业中,在无机盐制造和轻工业生产中也日益受到重视,如适应生产高级纸张的高岭土中除铁、磷酸生产[9] 以及生产优质玻璃的石英砂中除铁,均是当前广为研究的课题。
故铁含量的控制不仅对冶金工业,对无机制造以及轻工业生产也非常重要。
2.2. 铁对酿酒工业的危害
铁对诸如清酒[10] 、梅酒[11] 、曲酒[12] 、黄酒[13] 、啤酒等酒的酿造过程以及酒的口感和风味也有很大的影响。
以啤酒为例,啤酒酿造过程中铁离子对麦汁发酵性能及成品酒分为特性有着不同程度的影响。新鲜啤酒中的铁离子主要以Fe2+的形式存在,老化啤酒以Fe3+的形式存在。铁离子可参与羟基自由基的形成反应。羟基自由基形成后,可将啤酒中的醇类。异葎草酮及不饱和脂肪酸类物质迅速氧化成啤酒老化物质,影响啤酒的风味稳定性[14] 。故酿酒工业中铁含量的控制对酒的风味非常重要。直接用天然矿泉水做酿酒的水原料,则往往含有超标的铁元素,而影响到所酿制成酒的口感和风味。
为避免相关元素的干扰,目前国内的酒企业,有相当部分采用膜分离过滤水来酿酒,会将水中的矿物质元素和某些有益的微生物也会被彻底去除,影响到酒的质量和风味。
2.3. 铁对人体的作用及危害
铁是人体的必需元素。当人体对铁摄入量过多时,会引起免疫功能下降,消化功能减弱,神经活动衰退,从而导致一系列疾病的发生,如少年儿童在生长发育时期,易导致肝脾肿大,精神涣散,记忆力减退或生长发育迟缓等症状的出现[15] ,还会导致胃癌[16] 、肺癌[17] 等的发生。
据调查,我国含铁、锰地下水占地下水总量的20%,全国有18个省市的地下水中含有过量的铁和锰。东北地区地下水中普遍含有铁、锰,其中黑龙江省的地下水更甚,已经发现的铁的最高含量超过60 mg/L,锰的最高含量也达5 mg/L [18] 。我国饮用水卫生标准(GB5749-85)和地下水质量标准 (GB14848-93)均规定生活饮用水铁元素含量不应超过0.3 mg/L [19] ,而锰的允许质量浓度为0.1 mg/L [20] 。
人体摄入的铁元素主要来源于饮水和食物,一般饮水中的铁元素比食物中的铁元素易被人体吸收,而地下水是饮水的重要水源,故地下水中铁含量的控制对人们的身体健康至关重要。
3. 现有铁污染的消除方法
现有的除铁方法主要包括沉淀法、萃取法、电化学法、离子交换法以及生物吸附法等几种方法。
3.1. 沉淀法除铁
3.1.1. 黄钾铁矾法
黄钾铁矾法除铁是使三价铁从有K+、Na+、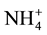 等离子存在的硫酸盐溶液中以赭黄色结晶化合物即A2Fe6(SO4)(OH)12的形式被分离出去[21] 。(式中A代表K、Na等),反应方程式如下[22] :
等离子存在的硫酸盐溶液中以赭黄色结晶化合物即A2Fe6(SO4)(OH)12的形式被分离出去[21] 。(式中A代表K、Na等),反应方程式如下[22] :

由上式可以看出,黄钾铁矾生成过程之中酸量是增加的,1 g铁生成矾时越要放出1.75 g硫酸。因此要满足铁矾生成的pH值,必须连续不断地用碱中和铁矾生成过程中的酸。
若溶液中没有足够的碱金属阳离子存在时,则高铁离子有可能和氢离子或水和氢离子(H3O)+按下式生成矾。
 的沉降性能并不比氢氧化铁好多少,过滤和洗涤都不够理想,溶液中残留铁仍很高。所以这是应当尽量避免的。
的沉降性能并不比氢氧化铁好多少,过滤和洗涤都不够理想,溶液中残留铁仍很高。所以这是应当尽量避免的。
黄钾铁矾法的主要优点是[23] [24] :
(1) 可获得适于电解的硫酸盐溶液,同时锌、镉、铜的回收率提高;
(2) 铁呈结晶状态除去,过滤和洗涤性能较好;
(3) 铅、银、金富集在二次渣中,适于作炼铅厂的配料或作进一步处理;
(4) 常压过程易和现有的电解锌车间结合;
(5) 最重要的优点是能从循环的电解液中除掉硫酸根,维持硫酸根在系统中的平衡。
黄铁矾法除铁的缺点是渣量大,共沉的重金属离子对环境污染严重。
为进一步提高铅、银、金等有价金属的回收率,减轻对铁渣的污染,80年代兴起了以减少或避免在除铁过程中加入中和剂的低污染铁矾法。低污染铁矾法炼锌工艺,实现了无中和剂成矾除铁,操作简便,稳定,易于掌握,开辟了除铁的新途径[25] 。
3.1.2. 针铁矿法
针铁矿的含水氧化铁的主要矿物之一,常称为α型–水氧化铁,它的组成为α-Fe2O3·H2O或α-FeOOH,于纤铁矿(γ-FeOOH)是同质多相变体。
针铁矿除铁法是在高温中性硫酸锌溶液中通入分散的空气,使其中的Fe2+氧化成Fe3+,同时形成于针铁矿在结晶和化学成分上相同的化合物沉淀。
针铁矿法除铁过程具有以下几个方面的优越性[26] [27] :
(1) 针铁矿法的除铁过程是在常压下进行的,工艺设备较简单。与黄钾铁矾法相比,减少了氨水的使用。
(2) 针铁矿沉淀物呈结晶态,易于沉降、过滤和洗涤,含铁量也比较高(50%),若经适当预处理,有希望作为炼铁富矿使用。
(3) 采用针铁矿法可使铟、锗、镓等稀散金属得到较为理想的富集。
(4) 针铁矿对阴离子有很强的强吸附性能。故此法不仅可以除铁,而且还可除氟、氯,利于电解。
针铁矿法流程中硫酸盐的平衡问题未得到很好的解决,目前主要依靠控制焙烧条件、加入含有生成不溶硫酸盐的原料(如铅)、排除硫酸锌溶液以及用石灰中和电解液等方法维持硫酸盐平衡[28] 。
3.1.3. 赤铁矿法
赤铁矿法是使硫酸锌水溶液中主要赤铁矿(Fe2O3)形态沉淀除去的锌热酸浸出除铁方法,它与锌焙砂热酸浸出组成完整的锌焙砂浸出系统[25] 。赤铁矿法的沉铁条件是在高温(200℃)、高压(1.8~2.0 MPa),Fe3+以赤铁矿Fe2O3的形式从低浓度Fe2(SO4)3溶液中沉淀出来[29] 。
该法于1972年在日本饭岛电锌厂获得工业应用,1979年在西德鲁尔锌公司的Datlen冶炼厂也实现了工业化生产,但是在目前国内尚无工厂应用。
赤铁矿法的优点是:赤铁矿渣渣量少,含铁高,可作为炼铁原料,不需要建设渣场,减轻环境污染,可综合回收有价金属Ga和In,渣过滤性能好。缺点则是:投资费用高,需昂贵的钛材制造高压设备,蒸汽、硫酸耗量大,为回收金属,有还原、沉铜、中和等过程,比较复杂[30] 。
3.1.4. 其它沉淀方法
溶液除铁,通常都是指酸性浸液来说的。因为在酸浸时,铁及其它化合物易进入溶液。最具代表性的酸性溶液除铁的工业实例是湿法炼锌的除铁过程。
上世纪70年代发展起来的三大除铁方法有力地推动着湿法炼锌工业的发展。除了三大沉淀法之外,还有如氢氧化铁沉淀法、RPC硫酸化焙烧–浸出过程中铁的控制、局部焙烧–亚硫酸盐沉淀法、硫酸铁盐沉淀法以及磷酸盐沉淀法等沉淀法。其中磷酸盐除铁法是新近除铁研究中一个对铁选择沉淀较好的实验方法,是一个新颖并有望在工业上应用的除铁新工艺[31] 。
这些独特的控制铁过程促进了湿法工艺过程的不断发展。
3.2. 萃取法除铁
各种沉淀方法都有沉淀物难以合理利用、固液分离过程投资高、带走有用金属以及沉淀物的堆放及不同程度上带来的环境保护问题等,故萃取除铁的方法应运而生。
萃取除铁的大致流程是,从酸性溶液中用溶剂萃取的方法,将铁转入有机溶剂相,与溶液中其它有用金属分离,然后再利用反萃法与有机相接触,将铁转入含反萃剂的水相中,同时有机溶剂得到再生,可返回循环使用。
萃取除铁,萃取剂的有效官能团往往与三价铁离子之间具有良好的结合能力,所以该法从水介质中脱除铁离子的效果很好,但是在实际的操作过程中却存在一个现实的难题,即反萃铁非常困难。所以往往需要使用强酸来有效地从萃合有机相中反萃出铁离子,这样就出现了一个新问题:强酸性的含铁溶液如何妥善地处置?这个问题是限制萃取除铁目前最大的一个瓶颈性因素。
3.2.1. 硫酸介质中萃取除铁
硫酸是湿法冶金中最常用的浸出溶剂,因此自硫酸体系中萃取除铁是一个常见的问题。由于硫酸根配位能力弱,在溶液中金属常以阳离子形态存在,因此只适合采用酸性萃取剂。
除铁机理多属于阳离子交换或螯合萃取类型。羧酸萃取剂是用得最早的萃取剂之一,我国在钴冶金中用过的7~9碳脂肪酸就是一个实例。对属于这一类的叔碳羧酸(如Veratic-10)和环烷酸都做过较多的研究,主要用于铜镍分离和钇的回收,同时也都面临除铁的要求[32] 。
值得重视的是烷基磷酸萃取剂对在硫酸介质中提取有价金属具有重要的作用。其中(乙基己基)磷酸(D2EHPA类似国内P204),对于铀、稀土、钴、镍、铍、铟等都有优良的萃取性能[33] ,特别是价格便宜,易得到,应用普遍。在这些金属生产的流程中控制和分离铁也都是不可忽视的。特别是(D2EHPA)萃铁能力强、萃取容量大,结合牢固,反萃困难,故实践中常在萃取前用其他方法(如中和沉淀或黄钾铁矾沉淀)预先除铁,或在萃取过程中控制pH,或将铁还原成不萃的低价形式,或利用萃取速度的差异,而实现所需要的分离目的。烷基磷酸萃取剂D2EHPA类似国内(P507)分离铁镍的效果极佳,国内外都有应用,而同D2EHPA工艺一样地存在铁的难反萃问题。
3.2.2. 氯化物介质中萃取除铁
在氯化物介质,铁离子可与氯离子形成配合阴离子形式,故许多碱性萃取剂都可应用来分离铁。采取的方式可以单一工序选择性萃取除铁,也可在萃取过程中进行分离。仲辛醇、酰胺(A101, N503)、磷酸三丁酯(TBP)碱性较弱,可以利用在一定的酸度和氧离子浓度下仅将铁萃取除掉。二丁基卡必醇(TBP)萃取金、酰胺萃取铊,则是在萃取过程中的分离。它们都是利用形成的氯络合物稳定性和电荷密度的差异,控制在较低酸度下多级萃取和洗涤,简便地获得高纯度的产品[34] 。
3.3. 离子交换法除铁
离子交换树脂可视作一种用途广泛的功能高分子材料。自1935年酚醛系离子交换树脂问世以来,已有近一个世纪。离子交换树脂按交换基团分,有强酸性、强碱性、弱酸性、弱碱性四大类。其中强酸性树脂占总产量50%以上,强碱性占25%,弱酸性占5%,弱碱性占15%。
利用树脂的交换、吸附及选择性可以达到脱盐、脱色、分离精制的目的,对现代化工业发展起了重要的作用。它可以用于湿法冶金中稀土分离、杂质去除及金属电解液净化;医药中抗生素的分离净化,氨基酸、酶、多肽的分离;食品工业中重金属离子的去除,以及无机物制备工艺及三废治理等。各种树脂中,再生型螯合树脂多用于重金属吸附,大多数在聚合母体中引入亚胺型螯合基,具有较高的亲水性和耐有机污染能力,选择性和机械性能都较高。
但是在实际的操作过程中,树脂的“中毒”失效现象,就往往是水介质中铁离子的存在造成的,因为三价铁离子极易水解沉淀形成氢氧化铁胶体物,从而堵塞树脂的微孔,覆盖其表面的活性官能团,使树脂的吸附活性下降甚至消失。此外,离子交换树脂除铁,与萃取法除铁一样,面临同样的一个问题,即铁离子易被选择性的优先结合而脱除,但是从吸附树脂上解吸出铁反而非常困难且产生的产出强酸性解吸液的妥善处理也是一个问题。
3.4. 电化学法除铁
城市建筑物中的供水系统由于管道锈蚀等原因,会导致自来水因铁含量过高而发黄、发浑且带有铁腥味。而油田废水中含油和悬浮物过高,容易导致系统污染、结垢问题严重,铁离子的存在,更增加了油田污水处理难度,污水回注后易造成注水管网的损坏,地层堵塞和测试投捞工具的锈蚀、卡死,导致注水量的减少和注水效果的降低,严重影响了注水开发油田的水平[35] 。
目前有一种利用电化学除铁的水处理新技术,不需添加化学药剂且无二次污染,其作用机理是利用阳极(不溶性)反应产生的新生态氧和溶解氧将Fe2+氧化成Fe3+,进而水解形成氢氧化铁胶体,再通过砂滤去除。阴极反应生成的OH−引起pH值上升,提高了氧化速度;产生的微气泡促使高铁胶体集聚成较大的颗粒,改善了过滤条件。电流密度越高除铁能力越强,但电流效率下降。采用循环处理方法可有效清除水箱黄锈水,其耗电量较低,适用于城市建筑物的供水系统[36] 。
电流效率以及实际操作的便利性等方面的因素,将是决定该方法除铁能否广泛推广应用的主要限制性方面。
3.5. 生物吸附法除铁
生物吸附法是一种较为新颖的处理含重金属废水的方法,因具有高效、廉价的潜在优势逐渐引起人们的研究兴趣。所谓生物吸附法就是利用某些生物体本身的化学结构及成分特性来吸附溶于水中的金属离子,再通过固液两相分离来去除水溶液中的金属离子的方法。这种新型方法,适宜处理大体积低浓度重金属废水,甚至降低到ppb级水平,自20世纪80年代以来受到广泛的关注与研究[37] 。
生物吸附法对于污染物的去除可以依赖或不依赖于生物体细胞的新陈代谢作用,活细胞、死细胞或细胞分泌物、提取物等都可能用于生物吸附的研究。生物体吸收金属离子的过程主要有两个阶段。第一个阶段是金属离子在细胞表面的吸附,即细胞外多聚物、细胞壁上的官能基团于金属离子结合的被动吸附;另一阶段是活体细胞的主动吸附,即细胞表面吸附的金属离子于细胞表面的某些酶相结合而转移至细胞内,包括传输和积累。由于细胞本身结构组成的复杂性,目前吸附机理还没有形成完整的理论[38] 。
生物吸附重金属的能力受到很多因素的影响,主要包括三个方面的因素:细胞状态、金属离子性质和反应条件。细胞状态包括营养供应、生理状态、细胞年龄;吸附条件包括pH、离子强度、温度、接触时间、共存离子,离子浓度等。
离子性质对生物吸附的影响是本质性的、内在的,但是研究起来则较为困难。清华大学王建龙教授课题组利用定量结构活性关系方法,探讨了重金属离子性质对生物吸附容量的影响,选用了22种参数来表征金属离子的物理化学性质,建立了金属的离子特性与生物吸附容量之间的关系[39] 。离子性质与吸附量之间的线性拟合分析结果表明,共价指数X2mr与qmax具有良好的线性关系,共价指数越高,离子吸附量越大,金属离子与吸附剂表面官能团共价结合所占比重越大,键结合越牢固。对金属离子进行分类(按价态或离子的软硬性质),可以改善拟合效果[37] 。
溶液的pH值对细胞表面的金属吸附位点和金属离子的化学状态及物种分布有着强烈的影响,对水解、有机或无机配体的络合作用、氧化还原反应、沉淀反应等也有着直接的影响。因而,对于大多数吸附过程而言,系统pH值是影响重金属生物吸附量的决定性因素。研究表明,金属阳离子的吸附容量随pH值得升高而增大,但不是简单的线性关系,且存在一个最佳的pH值,不同的金属离子和不同的生物吸附剂的最佳pH值吸附作用范围也不尽相同。通常,pH低时的吸附效果不好,普遍认为这是由于水合氢离子占据了生物吸附剂表面重金属的吸附位点,因斥力作用阻碍重金属离子接近细胞壁。Dhakal [40] 等在研究改性后的橘子皮对水溶液中重金属离子的吸附时,发现吸附后,溶液的pH 降低,说明重金属与橘子皮高分子表面上的H+发生了交换,即可能水合氢离子占据了吸附位点。当pH过高时,溶液中的重金属离子会以不溶解的氧化物、氢氧化物微粒存在,从而使得吸附过程无法进行。pH对吸附过程有着十分重要的影响,对pH值变化的探讨有助于对具体的吸附机理进行更深入的研究。
温度对金属的吸附量有着一定的影响,但影响不大,不如pH影响那么明显。重金属生物吸附通常比较快速,吸附时间的延长,吸附效率会提高,吸附容量会增大,若考虑金属的洗脱和生物吸附剂的再生,则需综合考虑反应时间。
在系统中欲被分离的金属离子称为目标离子,溶液中的其它金属离子也有可能被结合到吸附位点上,因此被称为竞争离子。通常情况下,其它重金属离子对目标离子具有竞争效应,会减少目标离子的吸附量。而轻金属或碱土金属对生物吸附剂的亲和力远小于重金属。目前,对于多种离子间的竞争吸附研究还处于初级阶段,还没有一个较好的数学模型来描述,因此,利用多参数模型来描述多种重金属离子间的竞争吸附,是目前生物吸附研究的一个重要方向[37] 。
能够吸附重金属及其它污染物的生物材料称为生物吸附剂,主要包括细菌、真菌、藻类和农林废弃物,与传统的吸附剂相比,它们具有以下主要特征[41] :
(1) 适应性广,能在不同pH值,温度及加工过程下操作;
(2) 选择性高,能从溶液中吸附重金属离子而不受碱金属离子的干扰;
(3) 金属离子浓度影响小,在低浓度(<10 mg/L)和高浓度(>100 mg/L)
下都有良好的金属吸附能力;
(4) 对有机物耐受性好,有机物污染(≤5000 mg/L)不影响金属离子的吸附;
(5) 再生能力强、步骤简单,再生后吸附能力无明显降低[42] 。
主要的生物吸附剂见表1。
生物吸附方法经过过去20多年的高速发展,在原料选择、吸附机理研究、处理各种金属离子的效果等方面的数据非常厚实,为生物吸附技术的应用推广奠定了坚实的基础。在公开报道的众多文献中,可以发现一个很有趣的现象,即绝大多数的生物吸附剂材料,对三价铁离子的吸附脱除效果方面,都几乎一律具有高度的优先选择性。比如在铁、铜、镍、镉、锌、钴等多种金属离子共存的水介质中,绝大多数的吸附剂投入之后,会在较低的pH下就先行选择性吸附脱除水中的铁离子。利用这个特点,可望使生物吸附技术在脱除各类低浓度铁离子方面做出特殊贡献。由于生物吸附技术具有原料便宜、丰富易得、改性过程简单、对三价铁离子具有较高选择性吸附的特点等综合优势,不必担心如萃取、离子交换那样的反萃难或解吸难等问题,因为便宜,完全可以作为一次性的吸附材料,将吸附负载了铁离子的生物质吸附剂通过焚烧而浓缩出铁,也可以原位还原制备成铁单质微粉,作为功能材料使用。农林废弃物是农、林也生产和加工过程中产生的副产品,具有价格低、产量大、可再生、再生周期短、可生物降解、环境友好等诸多优点,是重要的生物资源。我国每年都产生大量的农林废弃物,在广大农村,这些废弃物主要用于直接燃烧产热,还有一部分作为饲料、肥料和造浆造纸的原料,但这些利用量不足农林废弃物的50%,剩余的农林废弃物则被弃置或露天燃烧,既造成了环境的巨大污染,又造成了潜在资源的巨大浪
Table 1. Several biological adsorbents [43]
表1. 生物吸附剂种类[43]
费。随着环境保护力度的加强以及化石资源的日益减少,将农林废弃物等再生资源用于工业生产已成为一种新的发展趋势,越来越多的国家已经把农林生物质等可再生资源的转化利用列入社会经济可持续发展的重要战略。低成本的农林废弃物还可用于制备活性炭,活性炭可用于工业水净化中,由于传统用的生产活性炭原料如生煤、泥煤、褐煤等价格较高,低成本的使用农林废弃物原料制备活性炭吸附重金属离子的技术便应运而生了[44] -[48] 。农林废弃物还可用于去除废水中的铁离子,既能降低废水处理的成本,又能充分利用资源,为农林废弃物的综合利用提供了新途径。
4. 展望
铁污染问题,不同于常见的重金属污染,虽然看起来没有那么严重和令人害怕,但是由于其广泛的存在,而成为一个不可忽视的问题。传统的处理技术如沉淀、萃取、离子交换等方法都存在着不少问题,生物吸附则在此方面可能会有不可替代的良好功效。紧密结合各种铁污染引起的现实问题,开展合作研究,乃是实现铁污染问题的良好解决以及推广生物吸附除铁技术的一个良好契机。
文章引用
薛捷豪,黄 凯. 有色冶金等工业过程中铁离子污染及其处理方法探讨
The Removal Methods of Iron Ions in Non-Ferrous Metallurgy and Other Industrial Processes[J]. 冶金工程, 2015, 02(04): 177-185. http://dx.doi.org/10.12677/MEng.2015.24025
参考文献 (References)
- 1. Chen, T.T. and Cabri, L.J. (1986) Mineralogical Overview of Iron Control in Hydrometallurgical Processing. In: Dutrizac, J.E. and Monhemius, A.J., Eds., Conference of Iron Control in Hydrometallurgy, At Toronto, John Wiley & Sons, Hoboken, 19-55.
- 2. 陈家镛, 杨守志, 柯家骏, 等. 湿法冶金的研究与发展[M] . 北京: 冶金工业出版社, 1998.
- 3. 沈纬, 王英, 傅洵. 硫酸铝生产过程中的萃取法除铁[J]. 应用化学, 2002, 19(5): 464-467.
- 4. 牛勤学. 镉回收工艺中除铁方法的改进[J]. 中国钼业, 1998(S1): 42-43.
- 5. 张爱黎, 杨春芳, 符岩, 等. 铜厂副产品硫酸镍中除铁的研究[J]. 有色矿冶, 2001, 17(2): 23-26+22.
- 6. 林娟. 钴溶液除铁的工艺改进[J]. 山西冶金, 2004, 27(4): 58-59.
- 7. 陈家镛, 于淑秋, 伍志春. 湿法冶金中铁的分离与利用[M]. 北京: 冶金工业出版社, 1991: 1.
- 8. 森维, 孙红燕, 李正永. 锌湿法冶炼过程中除铁方法的研究进展[J]. 矿冶, 2013, 22(3): 71-74.
- 9. 马晓梅, 李倩, 汤德元. 湿法磷酸净化除铁的现状[J]. 贵州化工, 2010, 35(5): 22-26.
- 10. 山下浩一, 山中信介, 松尺一幸, 等. 清酒中铁离子的快速测定法[J]. 酿酒科技, 1993(5): 82.
- 11. 朱美笑. 梅酒生产过程中降铁的措施[J]. 食品工业, 1998(4): 21-22.
- 12. 陆培基, 梅海鹤, 周琴珍, 等. 曲酒二价铁离子污染查处报告[J]. 食品科学, 1984(8): 46.
- 13. 白少勇. 黄酒中蛋白质的沉淀机理与处理方法的研究[D]: [硕士学位论文]. 杭州: 浙江大学, 2005.
- 14. 王树庆. 铁离子对啤酒质量影响的研究. 酿酒, 2001, 28(4): 58-59.
- 15. 唐诗怡. 食物中的微量元素及其生理功能[J]. 江西医学, 1994(增刊): 128.
- 16. 曾昭华, 曾雪萍. 中国胃癌与土壤环境中化学元素的相关性[J]. 青海地质, 1999, 8(1): 67-72.
- 17. 曾昭华, 曾雪萍. 中国肺癌与土壤环境中元素的相关性研究[J]. 中华流行病学杂志, 1998, 19(2-A): 308-330.
- 18. 马恩, 王刚. 地下水除铁除锰技术的研究进展[J]. 环境保护与循环经济, 2008, 28(7): 36-39.
- 19. GB14848-93. 中华人民共和国地下水质量标准[S]. 北京: 国家技术监督局, 1994.
- 20. 严煦世, 范瑾初, 等. 给水工程[M]. 北京: 中国建筑工业出版社, 2003.
- 21. 陈远强, 林娟. 黄钠铁矾法除铁在钴系统中的应用[J]. 四川有色金属, 2002(1): 38-41.
- 22. 宿宪章. 钴冶炼[M]. 北京: 冶金工业出社, 1988: 2.
- 23. Chen, T.T. and Cabri, L.J. (Dutrizac, J.E. and Monhemius, A.J., Eds.) (1986) Iron Control in Hydrometallurgy. Ellis Horwood, London, 19.
- 24. Basu , G.A., et al. (Dutrizac, J.E. and Monhemius, A.J., Eds.) (1986) Iron Control in Hydrometallurgy. Ellis Horwood, London, 223.
- 25. 周桂英, 刘美荣. 湿法冶金过程净化除铁的研究进展[C]//中国矿业科技大会. 中国采选技术十年回顾与展望. 北京: 冶金工业出版社, 2012: 8.
- 26. 徐采栋, 汪大成, 林蓉. 针铁矿法除铁的物理化学[J]. 有色金属(冶炼部分), 1978(1): 37-45.
- 27. 陈家镛, 于淑秋, 伍志春. 湿法冶金中铁的分离与利用[M]. 北京: 冶金工业出版社, 1991: 162.
- 28. Osseo-Asare, K., Miller, J.D. and Meeting, A. (1982) Hydrometallurgy: Research, Development and Plant Practice. In: Proceedings of the 3rd International Symposium on Hydrometallurgy, The Metallurgical Society of AIME, Warrendale.
- 29. 吴胜男. 湿法炼锌过程中锌铁分离与铁资源利用[D]: [硕士学位论文]. 长沙: 中南大学, 2010.
- 30. 森维, 孙红燕, 李正永, 等. 锌湿法冶炼过程中除铁方法的研究进展[J]. 矿冶, 2013, 22(3): 71-74.
- 31. 窦明民, 周德林, 瞿开流. 磷酸盐除铁新工艺研究[J]. 云南冶金, 2000, 29(l): 23-24.
- 32. 李雁南. 溶剂萃取法从硫酸介质中除铁[J]. 湿法冶金, 1996(1): 40-42.
- 33. Sole, K.C., Feather, A.M. and Cole, P.M. (2005) Solvent Extraction in Southern Africa: An Update of Some Recent Hydrometallurgical Development. Hydrometallurgy, 78, 52-78. http://dx.doi.org/10.1016/j.hydromet.2004.11.012
- 34. Cole, P.M. and Sole, K.C. (2003) Zinc Solvent Extraction in the Process Industries. Mineral Processing and Extractive Metallurgy Review: An International Journal, 24, 91-137. http://dx.doi.org/10.1080/08827500306897
- 35. 邵长新, 李相远, 张传江, 等. 油田污水电氧化除铁的试验研究[J]. 石油机械, 2005, 33(8): 17-18+32-2.
- 36. 吴星五, 高廷耀. 电化学除铁用于建筑物的供水系统[J]. 中国给水排水, 2002, 18(6): 10-13.
- 37. 王建龙, 陈灿. 生物吸附法去除重金属离子的研究进展[J]. 环境科学学报, 2010, 33(4): 673-701.
- 38. 刘瑞霞, 汤鸿霄. 重金属的生物吸附机理及吸附平衡模式研究[J]. 化学进展, 2002, 14(2): 87-92.
- 39. 陈灿, 王建龙. 利用QSAR模型探讨分类条件下金属离子性质与酵母吸附容量之间的关系[J]. 环境科学学报, 2008, 28(1): 76-82.
- 40. Dhakal, R.P., Ghimire, K.N. and Inoue, K. (2005) Adsorptive Separation of Heavy Metals from an Aquatic Environment Using Orange Waste. Hydrometallurgy, 79, 182-190. http://dx.doi.org/10.1016/j.hydromet.2005.06.007
- 41. 梁莎, 冯宁川, 郭学益. 生物吸附法处理重金属废水研究进展[J]. 水处理技术, 2009, 35(3): 13-17.
- 42. Ahluwalia, S.S. and Goyal, D. (2007) Microbial and Plant Derived Biomass for Removal of Heavy Metals from Wastewater. Bioresource Technology, 98, 2243-2257. http://dx.doi.org/10.1016/j.biortech.2005.12.006
- 43. 王岚, 杜郢. 生物吸附剂及其应用[J]. 江苏工业学院学报, 2006, 18(3): 61-64.
- 44. Namasivayam, C. and Kadirvelu, K. (1997) Activated Carbons Prepared from Coir Pith by Physical and Chemical Activation Methods. Bioresource Technology, 62, 123-127. http://dx.doi.org/10.1016/S0960-8524(97)00074-6
- 45. Kadirvelu, K. and Namasivayam, C. (2003) Activated Carbons from Coconut Coir-Pith as Metal Adsorbent: Adsorption of Cd(II) from Aqueous Solution. Advances in Envi-ronmental Research, 7, 471-478. http://dx.doi.org/10.1016/S1093-0191(02)00018-7
- 46. Johns, M.M., Marshall, W.E. and Toles, C.A. (1999) The Effect of Activation Method on the Properties of Pecan Shell-Activated Carbons. Journal of Chemical Technology & Biotechnology, 74, 1037-1044.
- 47. Daifullah, A.A.M., Girgis, B.S. and Gad, H.M.H. (2003) Utilization of Agro-Residues (Rice Husk) in Small Waste Water Treatment Plans. Materials Letters, 57, 1723-1731. http://dx.doi.org/10.1016/S0167-577X(02)01058-3
- 48. Mohan, D. and Singh, K.P. (2002) Single-and Mul-ti-Component Adsorption of Cadmium and Zinc Using Activated Carbon Derived from Bagasse—An Agricultural Waste. Water Research, 36, 2304-2318. http://dx.doi.org/10.1016/S0043-1354(01)00447-X
