Material Sciences
Vol.
09
No.
02
(
2019
), Article ID:
28742
,
9
pages
10.12677/MS.2019.92016
Effect of Annealing Temperature on the Performance of TiO2(B) Nanosheet as Anode Material in Lithium Ion Battery
Zhiyong Yang, Yu Wang*, Xiaohong Xia, Kevin Peter Homewood, Yun Gao*
School of Materials Science and Engineering, Hubei University, Wuhan Hubei

Received: Jan. 4th, 2019; accepted: Jan. 24th, 2019; published: Jan. 31st, 2019

ABSTRACT
The monoclinic phase of TiO2(B) has a more open pore structure than that of anatase, rutile and brookite TiO2. The nanosheet structure of TiO2(B) shows a large deformation capacity and a short ion diffusion path for ions transport, so it serves as a new candidate for the anode material in lithium ion batteries. In this paper, ultra-thin nanosheet TiO2(B) was prepared by hydrothermal method. The crystal structure and morphology of the samples were investigated by X-ray diffraction (XRD) and transmission electron microscopy (TEM). We annealed the samples at different temperatures and then investigated the effect of annealing temperature on its performance as anode material of lithium ion battery. Annealing as an effective method for improving the capacity performance of TiO2(B) was proposed, and the annealing temperature was optimized.
Keywords:TiO2(B), Ultra-Thin Nanosheet, Hydrothermal, Annealing Temperature, Anode Material
退火温度对TiO2(B)纳米片作为锂离子电池负极材料性能影响
杨志勇,王宇*,夏晓红,Kevin Peter Homewood,高云*
湖北大学,材料科学与工程学院,湖北 武汉

收稿日期:2019年1月4日;录用日期:2019年1月24日;发布日期:2019年1月31日

摘 要
TiO2(B)较锐钛矿、金红石和板钛矿TiO2孔道更加开放,其纳米片结构拥有较大的形变能力和较短的离子扩散路径,成为锂离子电池负极材料的一种新的选择。本文通过水热法制备了一种超薄纳米片TiO2(B),使用X射线衍射(XRD)和透射电子显微镜(TEM)研究了所制备样品的晶型和形貌。样品经不同温度退火后组装扣式电池,系统比较了退火温度对TiO2(B)纳米片作为锂离子电池负极材料性能的影响。本文提出了一种改善TiO2(B)纳米片作为锂离子电池负极材料电化学性能的方法,选取了较优的退火温度。
关键词 :TiO2(B),超薄纳米片,水热法,退火温度,负极材料

Copyright © 2019 by author(s) and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
自Sony公司实现锂离子电池的商业化以来,锂离子电池的负极材料研究受到广泛关注,涵盖了炭类材料,硅基材料,锂金属,钛酸锂,过渡金属氧化物,氮化物,锡基材料、合金材料等。商用最广泛的石墨负极材料的理论比容量为372 mAh/g,目前实际容量已经接近理论容量导致锂离子电池比容量难以进一步提升,同时石墨负极的工作电位低,容易形成锂枝晶造成短路,且在石墨材料中锂离子扩散系数较低、内阻大,高倍率充放电时性能较差。锂金属电池循环时产生锂枝晶刺穿隔膜,引起安全问题。随着能源需求的日益增大,这些负极已经制约了锂离子电池的进一步发展,开发新型的安全、无毒、低成本和循环稳定的负极材料,替代传统负极是锂离子电池发展的必然选择。
TiO2氧化物材料储量丰富,电化学性能稳定,较传统石墨负极材料具有更优异的倍率特性和更高的安全性,成为一种极具前景的锂离子电池负极材料 [1] [2] 。锂离子电池电解液多为有机成分,TiO2在电解液中化学性能稳定,溶解度低,且随着锂离子的嵌入和脱出体积变化小,可有效提升电池的循环性能和循环寿命 [3] [4] [5] 。TiO2主要有锐钛矿型、金红石型、板钛矿型和TiO2(B)型四种晶型,均由TiO6八面体组成,但八面体单元的畸变程度不同,并以不同的方式共享边缘和角。
TiO2(B)主要来源于层状钛酸盐,单斜晶系的TiO2(B)具有类似钙钛矿的分层结构,它由瓦楞状组成,边缘和角共享TiO6八面体 [6] 。层状结构的TiO2(B)具有锂离子嵌入和脱出的通道,锂离子的嵌入是一个伪法拉第感应电流的过程,而非金红石型和锐钛矿型的固态扩散过程 [7] ,这种赝电容效应使TiO2(B)可以在高倍率下充放电。1980年Marchand第一次通过钛酸盐热处理发现了TiO2(B) [8] 。TiO2(B)理论容量达335 mAh/g,接近金红石型和锐钛矿型的2倍 [9] [10] [11] 。
目前制备TiO2(B)的主要方法有水热法和高温固相法。水热法制备的TiO2(B)尺寸小,可制备纳米结构的TiO2(B)。高温固相法工艺简单可大量制备,但尺寸较大且易产生杂质,对锂离子的传输不利。TiO2(B)纳米颗粒 [12] 、纳米管 [13] 、纳米线 [14] 和纳米带 [15] 作为锂离子电池负极材料具有良好的倍率特性已经得到了广泛报道,超薄纳米片形貌的TiO2(B)拥有更短的离子扩散路径,较大的形变能力和与电解液更大的接触面积,作为锂离子电池负极材料表现出更优异的性能。
本文通过一种简单的水热法以钛酸异丙酯为原料制备出了高质量的TiO2(B)纳米片,采用TEM表征样品形貌,XRD分析样品的物相,研究了其作为负极材料的锂离子电池的电化学性能。通过不同温度对所制备的TiO2(B)纳米片进行退火处理,研究了退火温度对TiO2(B)的形貌和其作为锂离子电池负极材料性能的影响,探讨了TiO2(B)适合作为锂离子电池负极材料的最佳退火温度。
2. 实验部分
本文采用简单的水热法制备TiO2(B)纳米片,使用管式炉进行退火处理,组装扣式电池来表征电极的电化学性能。
2.1. TiO2(B)纳米片的制备
将5 ml钛酸异丙酯加入3 ml盐酸中磁力搅拌10 min得到溶液1,将1 ml的聚氧乙烯–聚氧丙烯–聚氧乙烯加入10 ml的无水乙醇中磁力搅拌10 min得到溶液2。将溶液2滴加进溶液1中磁力搅拌30 min以后加入90 ml乙二醇,磁力搅拌10 min得到溶液3。将溶液3加入聚四氟乙烯反应釜中,150℃加热反应20小时。反应结束后冷却至室温取出,使用无水乙醇高速离心洗涤样品,重复4次。置于60℃的鼓风干燥箱中8 h烘干。干燥的样品研磨得到TiO2(B)粉末,得到的样品通过德国布鲁克公司的D8 Discover XRD研究晶体结构。使用美国FEI公司的Tecnai G20 TEM分析其形貌。
2.2. TiO2(B)纳米片退火处理
将TiO2(B)粉末放在管式炉中大气气氛退火处理1小时,退火温度分别为100℃、150℃、200℃、250℃、300℃和350℃,升温速率为4℃/min,自然降温。退火后的TiO2(B)粉末使用德国布鲁克公司的D8 Discover XRD研究晶体结构,采用美国FEI公司的Tecnai G20 TEM观察不同温度退火样品形貌的变化,组装扣式电池测试其储锂性能。
2.3. 电池性能的测试
将TiO2(B)和不同温度退火后的样品粉末作为活性物质,与乙炔黑、PVDF按照质量比为8:1:1的比例一起研磨,加入NMP搅拌成浆料涂覆在9 μm厚的铜箔集流体上。通过鼓风干燥箱60℃干燥3 h和真空干燥箱80℃真空干燥10 h后裁剪成极片。在O2和水含量均低于0.1 ppm的氩气气氛的手套箱中组装扣式半电池,制备极片为工作电极,高纯锂片为对电极和参比电极,PP/PE/PP三层膜为隔膜,1 mol L−1 LiPF6溶于EC/DMC (体积比1:1)的溶液为电解液的扣式电池。在新威电池测试系统上测试电池的倍率和循环性能。
3. 实验结果及讨论
3.1. TiO2(B)纳米片
图1(a)为水热法制备的粉末样品的XRD图,位于15.2˚、28.2˚和48.6˚特征峰分别与标准TiO2(B) PDF (46-1273)卡片中(100)、(110)和(020)晶面的衍射峰一致,证明水热法制备的产物为TiO2(B)。衍射峰中(100)峰强度低,相对较宽,表明样品(100)晶面间距较小,根据Scherrer公式和该峰的半高宽计算得到晶面间距约为3 nm,纳米片厚度为3个原子层左右。图1(b)是水热法制备的样品的拉曼光谱图,位于210 cm−1、256 cm−1、382 cm−1、422 cm−1、477 cm−1、553 cm−1、632 cm−1和828 cm−1处的拉曼振动峰和文献报道的TiO2(B)的振动峰完全吻合 [16] ,进一步证明了所制备的样品为纯相TiO2(B)。
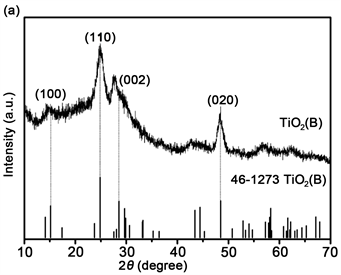
Figure 1. XRD pattern (a) and Raman pattern (b) of the TiO2(B) nanosheets
图1. TiO2(B)纳米片的XRD图谱(a)和拉曼光谱(b)
图2是样品的透射电镜照片。从图中可以看出TiO2(B)样品为超薄纳米片,纳米片尺寸与计算得到的纳米片的厚度一致。纳米片质量好,结构完整稳定。纳米片自然分散,呈花状。
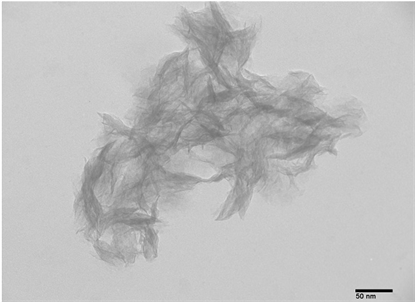
Figure 2. TEM images of the TiO2(B) nanosheets. Scale bar: 50 nm
图2. 水热法制备的TiO2(B)纳米片的TEM图。标尺为50 nm
将TiO2(B)样品组装扣式电池测试性能。图3为TiO2(B)扣式电池的电池特性图。图3(a)为TiO2(B)扣式电池在0.5 C倍率下循环充放电100圈性能图,根据充电比容量和放电比容量与循环圈数的关系,首次充电比容量为283 mAh/g,在30圈以后逐渐稳定在150 mAh/g左右。100圈以后比容量为149 mAh/g,较30圈时容量保留率有96%,说明了TiO2(B)超薄纳米片作为锂离子电池负极材料的循环稳定性。图3(b)为0.5C倍率下前5圈的容量电压分布图。红色、蓝色、绿色的线条分别为第一圈、第二圈和第五圈的充电放电容量电压分布曲线,测试的电压范围从0 V到3 V。从图中可以看出第一圈的充电比容量为283 mAh/g,第二圈的充电比容量为232 mAh/g,第五圈的充电比容量为205 mAh/g,首圈不可逆容量为51 mAh/g,应是前几圈循环时在TiO2(B)表面逐渐形成了稳定的SEI膜,在后面的循环中表现出稳定的容量。前5圈的充放电曲线稳定,电压平台一致,表现其稳定性。制备的TiO2(B)稳定性良好,但是其容量较理论容量尚有差距,我们认为在纳米片的合成制备过程中有部分乙二醇分子嵌入到纳米片层间,在有机环境的扣式电池中这部分有机小分子与电解液相互作用影响到了电池材料的导电性等,导致较大的容量损失。因此我们选择使用退火处理,尽可能的去除纳米片间的有机小分子。由于过高的温度容易引起纳米片结构的坍塌,降低材料的比表面积和孔道,我们选择的温度低于350℃。
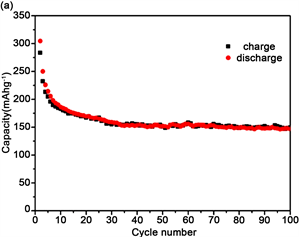
Figure 3. Battery performance of TiO2(B). (a) Cycling performance of 100 cycles at a current rate of 0.5C; (b) Charge and discharge curves of the first 5 turns during constant current charging and discharging at 0.5 C rate
图3. TiO2(B)扣式电池的电池性能:(a) 0.5C倍率下循环充放电100圈的循环性能;(b) 0.5C倍率恒流充放电时前5圈的充放电曲线
3.2. 退火温度对TiO2(B)纳米片的影响
图4为6种不同温度退火后的TiO2(B)纳米片的XRD图谱,从图中可以看出这种较低的退火温度并未改变TiO2(B)的晶体结构,所有衍射峰和PDF标准卡片中TiO2(B)的衍射峰吻合。随着退火温度的升高,各衍射峰的强度有所下降,衍射峰半高宽增大,说明样品的晶体结构发生了微量改变,晶体结构出现了些许畸变。
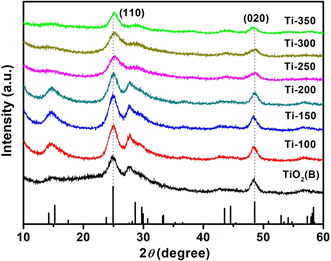
Figure 4. XRD pattern of the TiO2(B) samples annealed at different temperatures
图4. TiO2(B)纳米片不同温度退火样品的XRD图谱
图5是不同温度退火样品的TEM照片。图5(a)是未退火的TiO2(B),图5(b)、图5(c)、图5(d)、图5(e)、图5(f)分别对应退火温度为150℃、200℃、250℃、300℃、350℃。从图中可以看出,随着退火温度的提升,超薄纳米片的形貌并未发生明显的变化,纳米片的形貌依然维持。图5(b)、图5(c)、图5(d)的纳米片形貌与图5(a)基本保持一致,说明样品在250℃以下温度退火仍然能保持完整稳定、自然分散的超薄纳米片结构。当温度继续升高到300℃和350℃时,纳米片分散性变差,产生了轻微的团聚现象,纳米片边缘出现了有些毛刺,如图5(e)、图5(f)所示。

Figure 5. TEM images of the TiO2(B) samples annealed at different temperatures. (a) Unannealed; (b) T = 150℃; (c) T = 200℃; (d) T = 250℃; (e) T = 300℃; (f) T = 350℃. Scale bar: 100 nm
图5. 不同温度退火条件的TiO2(B)样品的TEM照片。(a) 未退火;(b) T = 150℃;(c) T = 200℃;(d) T = 250℃;(e) T = 300℃;(f) T = 350℃。标尺100 nm

Figure 6. Cycling performance of annealed TiO2(B) samples at different current rates: (a) Cycling performance at 0.5 C rate of unannealed TiO2(B) and annealing samples at different temperatures; (b) Cycling performanceat 1 C rate of annealed TiO2(B) samples at different temperatures
图6. 不同倍率下退火TiO2(B)样品的循环性能。(a) 0.5 C倍率下未退火TiO2(B)和不同温度退火条件样品的循环性能;(b) 1 C倍率下不同温度退火TiO2(B)样品的循环性能
图6为不同温度退火的TiO2(B)样品作为锂离子电池负极材料的循环性能曲线。图6(a)为各样品组装的电池在0.5C倍率的循环性能,从图中可以看出,相对于未退火样品,所有退火处理的样品的电池循环性能均得到有效提升。100℃、150℃、200℃退火样品的电池循环性能接近,性能提升最明显。在循环100圈后比容量均超过500 mAh/g。其中200℃退火样品的比容量最高,首次充电比容量达到1245 mAh/g循环20圈后电池性能趋于稳定,循环100圈后比容量保持在571 mAh/g,且样品在循环过程中基本保持稳定。退火处理大幅提升样品的电池循环性能的原因可能是退火去除了片层间的有机物残留,扩大了锂离子容量和传输通道。350℃退火样品的电池容量较未退火样品略有提升,其原因可能是高温下TiO2(B)纳米片的层状结构在高温退火遭到破坏,材料变得致密,材料的脱锂嵌锂能力降低。图6(b)为1 C倍率下不同温度退火TiO2(B)样品的电池循环性能。可以看出在1 C倍率的大电流恒流充放电循环200圈时,退火处理对样品电池性能的影响与0.5 C倍率循环时表现出一致的规律。退火样品都表现出较高的比容量和循环稳定性,200℃退火样品比容量最优,循环20圈后电池的容量损失很少,表现出优异的大电流充放电稳定性。
图7(a)为200℃退火TiO2(B)作为负极材料的锂离子电池在不同倍率循环测试200圈的性能对比图。随着充放电倍率升高,样品的比容量有所降低,但是在不同倍率下均保持了一个较稳定的高比容量。降低图7(b)是采用5 C高倍率循环1000圈的循环性能曲线。从图中可以看出,该样品具有较高的比容量和优异的循环稳定性,尤其是在1 C和5 C的高倍率下,1 C倍率下从40圈循环至200圈容量损失极小,比容量保持在约400 mAh/g。5 C的高倍率下大循环1000圈,比容量依然保持在287 mAh/g,较第5圈容量保留率为95%,电池容量没有明显的衰减,表现出了高倍率下极佳的循环稳定性,展示了TiO2(B)作为负极材料的锂离子电池适应快充的潜力。比容量在后面的循环中有一个轻微提升的原因可能是随着循环增加电解液完全浸润纳米片形成稳定的SEI膜,纳米片的通道变得稳定,与此同时,前面充放电过程中锂离子的嵌入与脱嵌使得活性物质不断的被活化,活性物质能够充分的参与充放电。图7(c)为0.5 C循环时第10、20、50、100圈时的充放电曲线,电压范围为0 V到3 V,可以发现0.5 C循环第100圈较第20圈容量保留率为78%。图7(d)为5 C倍率循环时第10、100、500、1000圈时的充放电曲线,可以发现第1000圈容量衰减极小,表现了优异的循环稳定性容量保留率。有报道称钛酸锂电池在循环使用中会持续产气,导致电池包鼓胀,影响力正负极接触,增加电池阻抗从而影响电池性能发挥,但是本实验中二氧化钛纳米片大电流充放电1000圈之后性能有很好的延续性,并没出现明显消退。
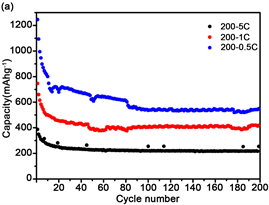

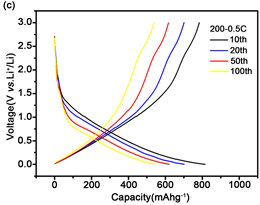

Figure 7. Cycling performance of TiO2(B) samples annealed at 200℃. (a) Cycling performance at different current rates of 0.5 C, 1 C and 5 C; (b) Capacity and Coulombic efficiency at a high rate of 5 C; (c) The 10 th, 20 th, 50 th and 100 th charge-discharge curves at a current rates of 0.5 C; (d) The 10th, 100th, 500th and 1000th charge-discharge curves at a high rates of 5 C
图7. 200℃退火TiO2(B)样品的循环性能。(a) 不同倍率的循环性能;(b) 5 C高倍率循环和库伦效率;(c) 0.5 C倍率10 th,20 th,50 th和100 th的充放电曲线;(d) 5 C高倍率下10 th,100 th,500 th和1000 th的充放电曲线
4. 结论
本文采用水热法制备了一种超薄的TiO2(B)纳米片,以所制备的TiO2(B)作为锂离子电池负极材料的扣式半电池具有良好的循环稳定性能,0.5 C倍率100圈循环比容量稳定在147 mAh/g。对TiO2(B)进行退火处理可以有效提升TiO2(B)纳米片锂离子电池的储锂性能。高于300℃退火会造成纳米片团聚和破碎。200℃退火的TiO2(B)纳米片在低倍率和高倍率下均表现出最优的电池性能,1 C循环500圈后比容量为421 mAh/g,表现了高容量的优点,5 C高倍率循环1000圈后,比容量依然保持在287 mAh/g,较第5圈容量保留率为95%,体现了高倍率下优异的循环稳定性,表现出其应用于快充的巨大潜力。退火处理有效提升TiO2(B)比容量以及循环稳定性的主要原因在于:1) 超薄纳米片具有较大的与电解液的接触表面积和超短的离子传输距离,结构稳定;2) 退火处理可有效去除水热反应残留在纳米片层间的有机物,提升锂离子的容量,疏通了锂离子的传输路径。本文所制备的超薄TiO2(B)纳米片用于锂离子电池负极材料,有望为快充锂离子电池提供一种新的选择。
基金项目
本研究由国家自然科学基金(11874144、51602096、11574076)、湖北省科技厅(2018CFA026)、武汉市科技局(2018010401011268)和高校学科创新引智计划(111项目,D18025)资助。
文章引用
杨志勇,王 宇,夏晓红,Kevin Peter Homewood,高 云. 退火温度对TiO2(B)纳米片作为锂离子电池负极材料性能影响
Effect of Annealing Temperature on the Performance of TiO2(B) Nanosheet as Anode Material in Lithium Ion Battery[J]. 材料科学, 2019, 09(02): 127-135. https://doi.org/10.12677/MS.2019.92016
参考文献
- 1. Li, J., Wan, W., Zhou, H., et al. (2011) Hydrothermal Synthesis of TiO2(B) Nanowires with Ltrahigh Surface Area and Their Fast Charging and discharging properties in Li-Ion Batteries. Chemical Communications, 47, 3439-3441. https://doi.org/10.1039/c0cc04634e
- 2. Zhang, Z., Chu, Q., Li, H., et al. (2013) One-Pot Solvothermal Synthesis of Graphene-Supported TiO2(B) Nanosheets with Enhanced Lithium Storage Properties. Journal of Colloid and Interface Science, 409, 38-42. https://doi.org/10.1016/j.jcis.2013.07.053
- 3. Wagemaker, M., Kearley, G.J., van Well, A.A., et al. (2003) Mul-tiple Li Positions inside Oxygen Octahedra in Lithiated TiO2 Anatase. Journal of the American Chemical Society, 125, 840-848. https://doi.org/10.1021/ja028165q
- 4. Wei, Z., Liu, Z., Jiang, R., et al. (2010) TiO2 Nanotube Array Film Prepared by Anodization as Anode Material for Lithium Ion Batteries. Journal of Solid State Electrochemistry, 14, 1045-1050. https://doi.org/10.1007/s10008-009-0910-6
- 5. Etacheri, V., Yourey, J.E. and Bartlett, B.M. (2014) Chemically Bonded TiO2-Bronze Nanosheet/Reduced Graphene Oxide Hybrid for High-Power Lithium Ion Batteries. ACS Nano, 8, 1491-1499. https://doi.org/10.1021/nn405534r
- 6. Feist, T.P. and Davies, P.K. (1992) The Soft Chemical Syn-thesis of TiO2(B) from Layered Titanates. Journal of Solid State Chemistry, 101, 275-295. https://doi.org/10.1016/0022-4596(92)90184-W
- 7. Zukalova, M., Kalbac, M., Kavan, L., Exnar, I. and Graetzel, M. (2005) Pseudocapacitive Lithium Storage in TiO2(B). Chemistry of Materials, 17, 1248-1255.
- 8. Marchand, R., Brohan, L. and Tournoux, M. (1981) TiO2(B) a New Form of Titanium-Dioxide and the Potassium Octatitanate K2Ti8O17. Materials Research Bulletin, 15, 1129-1133.
- 9. Liu, H., Bi, Z., Sun, X.G., Unocic, R.R., Paranthaman, M.P., Dai, S. and Brown, G.M. (2011) Mesoporous TiO2-B Microspheres with Superior Rate Performance for Lithium Ion Batteries. Advanced Materials, 23, 3450-3454. https://doi.org/10.1002/adma.201100599
- 10. Yan, X., Zhang, Y., Zhu, K., Gao, Y., Zhang, D., Chen, G. and Wei, Y. (2014) Enhanced Electrochemical Properties of TiO2 (B) Nanoribbons Using the Styrene Butadiene Rubber and Sodium Carboxyl Methyl Cellulose Water Binder. Journal of Power Sources, 246, 95-102. https://doi.org/10.1016/j.jpowsour.2013.07.072
- 11. Chen, C., Hu, X., Hu, P., Qiao, Y., Qie, L. and Huang, Y. (2013) Ionic-Liquid-Assisted Synthesis of Self-Assembled TiO2-B Nanosheets under Microwave Irradiation and Their Enhanced Lithium Storage Properties. European Journal of Inorganic Chemistry, 30, 5320-5328. https://doi.org/10.1002/ejic.201300832
- 12. Wessel, C., Zhao, L., Urban, S., Ostermann, R., Djerdj, I., Smarsly, B.M. and Sallard, S. (2011) Ionic-Liquid Synthesis Route of TiO2(B) Nanoparticles for Functionalized Materials. Chemistry-A European Journal, 17, 775-779. https://doi.org/10.1002/chem.201002791
- 13. Armstrong, G., Armstrong, A.R., Canales, J. and Bruce, P.G. (2006) TiO2 (B) Nanotubes as Negative Electrodes for Rechargeable Lithium Batteries. Electrochemical and Solid-State Letters, 9, A139-A143.
- 14. Armstrong, A.R., Armstrong, G., Canales, J., García, R. and Bruce, P.G. (2005) Lithium-Ion Intercalation into TiO2-B Nanowires. Advanced Materials, 17, 862-865. https://doi.org/10.1002/adma.200400795
- 15. Beuvier, T., Richard-Plouet, M., Mancini-Le Granvalet, M., Brousse, T., Crosnier, O. and Brohan, L. (2010) TiO2 (B) Nanoribbons as Negative Electrode Material for Lithium Ion Batteries with High Rate Performance. Inorganic Chemistry, 49, 8457-8464. https://doi.org/10.1021/ic1010192
- 16. Etacheri, V., Kuo, Y., Ven, A.V.D., et al. (2013) Mesoporous TiO2-B Microflowers Composed of (110) Facet-Exposed Nanosheets for Fast Reversible Lithium-Ion Storage. Journal of Ma-terials Chemistry A, 1, 12028-12032. https://doi.org/10.1039/c3ta12920a
NOTES
*通讯作者。