Advances in Clinical Medicine
Vol.08 No.02(2018), Article ID:24466,7
pages
10.12677/ACM.2018.82036
Accuracy of Various Intraocular Lens Calculation Formulas in Shallow Anterior Chamber Patients with Normal Axial Length
Liying Bing1,2, Guibo Liu2, Yuna Ma2, Lin Leng2
1Medical College of Qingdao University, Qingdao Shandong
2Department of Ophthalmology, The Affiliated Hospital of Qingdao University, Qingdao Shandong

Received: Mar. 23rd, 2018; accepted: Apr. 16th, 2018; published: Apr. 23rd, 2018

ABSTRACT
Objective: To compare the accuracy of five intraocular lens calculation formulas (Haigis, SRK II, Hoffer Q, Holladay1 and SRK/T) in shallow anterior chamber patients with normal axial length. Methods: 45 patients who underwent uncomplicated cataract surgery were involved in this retrospective analysis. This study was performed in the Department of Ophthalmology at the Affiliated Hospital of Qingdao University from January 2016 to October 2017. The IOL Master was used to predict the refractive outcomes for five formulas. Actual postoperative refractions were taken on 3 to 8 weeks after surgery. Refractive error and absolute refractive error were calculated. The SPSS19.0 was used for statistical analysis to compare the refractive errors, absolute refractive errors and the refractive error distribution of different IOL formulas. Results: The mean refractive error of the Haigis formula (–0.13 ± 0.76 D) differed significantly from Hoffer Q (–0.34 ± 0.74 D, P < 0.01), Holladay1 (–0.33 ± 0.73 D, P < 0.01) and SRK/T (–0.31 ± 0.72 D, P < 0.01) formulas. The mean absolute refractive error were 0.58 ± 0.50 D,0.62 ± 0.50 D, 0.62 ± 0.51 D, 0.61 ± 0.51 D and 0.58 ± 0.53 D with Haigis, SRK II, HofferQ, Holladay1, and SRK/T formulas, respectively, and there was no significant differences among them (χ2 = 4.027, P = 0.402). There was no significant difference in the distribution of refractive error between different IOL formulas (χ2 = 3.782, P = 0.872). Conclusion: The Haigis formula can predict refraction in shallow anterior chamber patients with normal axial length with less error.
Keywords:Cataract, Intraocular Lens, Refractive Errors, Anterior Chamber, Axial Length
人工晶体计算公式在正常眼轴合并浅前房白内障患者中的准确性比较
邴丽英1,2,刘桂波2,马玉娜2,冷林2
1青岛大学医学部,山东 青岛
2青岛大学附属医院眼科,山东 青岛

收稿日期:2018年3月23日;录用日期:2018年4月16日;发布日期:2018年4月23日

摘 要
目的:比较5种人工晶体(Intraocular lens, IOL)计算公式(Haigis、SRK II、HofferQ、Holladay1以及 SRK/T)在预测正常眼轴合并浅前房白内障患者术后屈光度的准确性,探讨适合此类患者的IOL计算公式。方法:回顾性系列病例研究。纳入2016年1月至2017年10月于青岛大学附属医院眼科就诊的正常眼轴长度(Axial length, AL)合并浅前房白内障患者共45例(45眼)。使用IOL Master计算不同公式的预测术后屈光度数,术后3至8周验光确定患者实际术后屈光度数,计算屈光误差、绝对屈光误差。应用 SPSS19.0进行统计学分析,比较对不同IOL计算公式的屈光误差、绝对屈光误差及屈光误差分布。结果:Haigis公式的平均屈光误差(−0.13 ± 0.76 D)最小,与Hoffer Q (−0.34 ± 0.74 D,P < 0.01)、Holladay1 (−0.33 ± 0.73 D, P < 0.01)以及SRK/T(−0.31 ± 0.72 D,P < 0.01)公式比较,差异具有统计学意义。Haigis、SRK II、HofferQ、Holladayl以及SRK/T公式的平均绝对屈光误差分别为0.58 ± 0.50 D, 0.62 ± 0.50 D, 0.62 ± 0.51 D,0.61 ± 0.51 D及0.58 ± 0.53 D,差异无统计学意义(χ2 = 4.027, P = 0.402)。不同IOL计算公式的屈光误差分布差异无统计学意义(χ2 = 3.782, P = 0.872)。结论:Haigis公式在正常眼轴合并浅前房白内障患者术后屈光度预测中的准确性高,选择Haigis公式在将有助于减少屈光误差。
关键词 :白内障,人工晶体,屈光误差,前房,眼轴长度

Copyright © 2018 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
随着白内障手术技术的进步,高端人工晶体的使用,白内障手术已经由复明手术向屈光手术转变 [1] 。如何减小白内障术后屈光误差成为了眼科医生与患者共同关注的重要问题。术前眼球生物测量的准确性,IOL计算公式的选择是造成术后屈光误差的两大主要原因 [2] [3] 。IOL Master的应用有效减小了生物测量误差 [4] ,而选择合适的IOL计算公式便成了减小白内障术后屈光误差的关键因素。已有研究表明,在正常眼轴白内障患者中,不同IOL计算公式准确性均较好 [5] [6] 。还有研究表明,短眼轴合并正常前房深度患者,Haigis公式、HofferQ公式准确性一致,而对于短眼轴合并浅前房的患者,Haigis公式更为准确 [7] 。而对正常眼轴合并浅前房患者的研究甚少,本研究比较IOL Master测量正常眼轴合并浅前房患者不同IOL计算公式的准确性,旨在为该类患者的IOL计算公式选择提供理论依据。
2. 材料和方法
2.1. 临床资料
所有研究对象均来自2016年1月至2017年10月青岛大学附属医院眼科行白内障超声乳化吸除联合人工晶体植入术患者。符合如下条件者纳入研究:眼轴长度22.0~24.5 mm,前房深度(Anterior chamber depth, ACD) £ 2.70 mm,术后矫正视力0.8~1.0的患者。排除标准:合并翼状胬肉、角膜病、青光眼、虹膜睫状体炎、眼外伤、眼底病变及内眼手术史的患者,合并术中、术后并发症(如后囊膜破裂、后发性白内障)的患者。共入选45例45眼,患者平均年龄73.69 ± 8.21岁;其中男性17名(37.8%),女性28名(62.2%);平均眼轴长度23.15 ± 0.54 mm,平均前房深度2.49 ± 0.17 mm。
2.2. 仪器和检查
术前应用IOL Master测量眼轴长度、角膜曲率、前房深度等相关参数,应用IOL Master内置的SRK/T公式计算IOL屈光度。根据手术者术中植入的IOL度数,通过IOL Master内置软件(Version 7.7.4.0326)计算出不同IOL计算公式(本研究包括第二代公式SRK II公式以及第三代公式SRK/T,HofferQ,Holladay1及第四代公式Haigis公式)的预测术后屈光误差。术后3至8周内复查时,用自动验光仪(ARK-1a,日本NIDEK公司)进行电脑验光,在此基础上进行主觉验光,以主觉验光的等效球镜度(SE)作为实际术后屈光度。
2.3. 手术方法及植入的IOL的常数
所有手术均由同一位熟练的手术医师完成。手术经3.0 mm透明角膜切口进入前房,连续环形撕囊,直径约5.5 mm,水分离,乳化晶状体核,吸除皮质,IOL均植入囊袋内,光学面居中,水密角膜切口。本研究中植入的IOL类型为AMO Tecnis 1 ZCB00。Haigis公式a0 = −1.302,al = 0.210,a2 = 0.251。Hoffer Q公式的pACD为5.80。Holladay1公式的SF为2.02。SRK/T公式的A常数为119.30。
2.4. 仪器和检查
IOL计算公式屈光误差定义为实际术后屈光度数与预测术后屈光度数的差值,其绝对值为绝对屈光误差,数据以均数 ± 标准差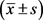 表示。应用SPSS19.0进行统计学分析。对不同IOL公式的各组数据进行Shapiro-Wilk正态性检验,对不同IOL计算公式的屈光误差值比较行随机区组设计资料的方差分析,其后的两两检验采用Bonferroni法,对不同IOL计算公式的绝对屈光误差值比较行随机区组设计资料的Friedman秩和检验;对不同公式的屈光误差分布进行卡方检验。以P < 0.05为差异有统计学意义。
表示。应用SPSS19.0进行统计学分析。对不同IOL公式的各组数据进行Shapiro-Wilk正态性检验,对不同IOL计算公式的屈光误差值比较行随机区组设计资料的方差分析,其后的两两检验采用Bonferroni法,对不同IOL计算公式的绝对屈光误差值比较行随机区组设计资料的Friedman秩和检验;对不同公式的屈光误差分布进行卡方检验。以P < 0.05为差异有统计学意义。
3. 结果
3.1. 不同IOL计算公式的平均屈光误差、中位屈光误差、屈光误差范围
Haigis、SRK II、Hoffer Q、Holladayl以及SRK/T公式的屈光误差表1。所有患者不同IOL计算公式的屈光误差见图1。各个IOL计算公式的平均屈光误差值均为负值。Haigis的平均屈光误差最小,为–0.13 ± 0.76 D。不同公式屈光误差值之间的差异有统计学意义(F = 9.951,P = 0.000),各个公式两两比较,Haigis公式与Hoffer Q (P < 0.01)、Holladayl (P < 0.01)以及SRK/T (P < 0.01)公式之间的差异有统计学意义,其他各公式间比较差异均无统计学意义。
3.2. 不同IOL计算公式的平均绝对屈光误差、中位绝对屈光误差、绝对屈光误差范围
Haigis、SRK II、Hoffer Q、Holladayl以及SRK/T公式的绝对屈光误差见表2。Haigis、SRK II、Hoffer Q、Holladayl以及SRK/T公式的平均绝对屈光误差分别为0.58 ± 0.50 D,0.62 ± 0.49 D,0.62 ± 0.51 D,0.61 ± 0.51 D及0.58 ± 0.53 D。各个公式绝对屈光误差值之间的差异无统计学意义(χ2 = 4.027,P = 0.402)。

Figure 1. Refractive error of the different IOL formulas in all patients
图1. 不同IOL计算公式的平均屈光误差、中位屈光误差、屈光误差范围
Table 1. Mean refraction error, medium refractive error and refractive error range of different IOL formulas
表1. 不同IOL计算公式的平均屈光误差、中位屈光误差、屈光误差范围
a示正常眼轴长度合并浅前房患者不同IOL计算公式间屈光误差差异有统计学意义,α = 0.05 (随机区组设计的方差分析);b示与Haigis公式相比差异有统计学意义,α’ = 0.005 (随机区组设计的方差分析合并两两多重比较Bonferroni法)
Table 2. Mean absolute refractive error, median absolute refractive error, and absolute refractive error range for different IOL formulas
表2. 不同IOL计算公式的平均绝对屈光误差、中位绝对屈光误差、绝对屈光误差范围
a示正常眼轴合并浅前房患者不同IOL计算公式绝对屈光误差差异无统计学意义,α = 0.05(随机区组设计的Friedman秩和检验)
3.3. 不同IOL计算公式的屈光误差分布
Haigis、SRK II、Hoffer Q、Holladayl以及SRK/T公式的屈光误差的分布见表3。以−0.5~0.5 D作为正视,<−0.5 D作为近视屈光误差,>0.5 D患者作为远视屈光误差组。Haigis公式术后屈光状态处于正视的比例最高,但差异无统计学意义(χ2 = 3.782,P = 0.872)。
4. 讨论
白内障术后的屈光误差主要来源于术前生物测量(包括角膜曲率、眼轴、前房深度等)误差和IOL计算公式误差两方面 [2] [3] 。随着IOL Master在临床上的广泛应用,其具有良好的可重复性和准确性,大大减少了因眼轴、角膜曲率测量误差导致的屈光误差 [8] [9] ,故IOL计算公式的合理选择受到眼科医师的重视。既往的研究表明随着前房深度的减小,屈光误差会明显增加 [7] [10] 。术后IOL有效位置(Effective lens position, ELP)是指IOL植入术后等效光学面所在位置,其无法通过术前测量获得。在正常前房
Table 3. Refractive error distribution of different IOL formulas
表3. 不同IOL计算公式的屈光误差分布
χ2 = 3.782,P = 0.872。
深度下,各个IOL计算公式预测ELP的准确性均较好。然而浅前房患者的眼球发育异常,前房深度与眼轴长度不成比例,造成了ELP预测准确性下降。Eom的研究表明,在短眼轴(AL £ 22.0 mm)患者中,在ACD ≥ 2.40 mm时,HofferQ公式和Haigis公式的准确性均较好,随着前房深度变浅,在ACD < 2.40 mm时,Haigis公式的准确性更好 [7] 。目前对于正常眼轴长度合并浅前房患者的研究甚少。因此,对于正常眼轴合并浅前房白内障患者怎样合理选择IOL计算公式,尽可能减少术后发生屈光误差,提高患者术后视觉质量,值得深入研究。
本研究中Haigis公式的平均屈光误差(−0.13 ± 0.76 D)最小,与Hoffer Q、Holladayl以及SRK/T公式比较,差异具有统计学意义。该结果与Miraftab的研究相符 [11] 。在Miraftab的研究中,在ACD £ 3.00 mm的正常眼轴长度(22.0~24.5 mm)患者中,Haigis公式与SRK II公式的屈光误差较小,分别为−0.18 ± 0.79 D,−0.09 ± 0.71 D,但两者间的差异无统计学意义。第三代公式Hoffer Q、Holladayl以及SRK/T公式通过眼轴长度、角膜曲率来预测ELP [12] [13] [14] [15] 。相较第三代公式,而第四代公式Haigis公式引用术前ACD、眼轴长度及a0、a1、a2三个常数来预测ELP [15] [16] 。故基于术前ACD的IOL计算公式Haigis公式较HofferQ、Holladay1、SRK/T公式屈光误差更小,准确性更好。尽管SRK II公式的平均屈光误差(−0.20 ± 0.78 D)较小,但从图1可以看出,SRK II的公式波动较大,稳定性差。这可能是与SRK II公式未进行个性化ELP计算,仅对不同眼轴设置了统一的调整常数有关 [17] 。本研究中,不同IOL计算公式的平均绝对屈光误差之间的差异无统计学意义。与Miraftab的研究相一致 [11] 。在Miraftab的研究中,对于前房深度 £ 3.0 mm的正常眼轴(22.0~24.5 mm)患者,Haigis、SRK II、Hoffer Q、Holladayl以及SRK/T公式的平均绝对屈光误差之间的差异无统计学意义。
在本研究中,各个IOL计算公式(Haigis、SRK II、Hoffer Q、Holladay 1以及SRK/T公式)平均屈光误差值均为负值,这表明对于正常眼轴长度合并浅前房患者,不同IOL计算公式均发生近视飘移现象。在Kim的研究显示在浅前房白内障患者中,SRK II、SRK/T公式术后均出现近视性屈光飘移 [18] 。Joo的研究表明,在浅前房白内障患者中,Haigis公式的平均屈光误差接近于0,而HofferQ、SRK/T公式出现远视性屈光飘移 [19] 。杨斐 [20] 、董丽华 [21] 的研究均采用SRK/T公式,纳入正常眼轴长度(22~24.5 mm)合并浅前房(ACD £ 2.7 mm)白内障患者,术后平均屈光误差分别+0.73 ± 0.26 D、+0.73 ± 0.27 D,均为远视飘移。目前国内外研究尚无一致性结论,这可能是因为浅前房患者具有晶体厚、前房拥挤等解剖特点。厚晶体(即大囊袋体积)可能是术后IOL不稳定的原因,IOL前后位移导致近视或远视屈光误差,IOL旋转或离心导致散光。这些结果的不一致性也可能与各研究眼轴长度、前房深度不一致、样本数不同、植入晶体类型不同及手术医师的操作等因素有关。
综上所述,对于正常眼轴合并浅前房白内障患者,Haigis公式在术后屈光度预测中的准确性高,选择Haigis公式在将有助于减少屈光误差。我们建议尽量避免使用SRK II公式进行该类患者的IOL屈光度计算。由于正常眼轴合并浅前房白内障患者在人群中比例较低,本研究纳入例数较少,因此存在一定的局限性。正常眼轴合并浅前房白内障患者IOL计算公式的合理选择还需进一步扩大样本量进行深入研究。
基金项目
2016年青岛大学附属医院青年基金优秀项目(QDFY201612)。
文章引用
邴丽英,刘桂波,马玉娜,冷 林. 人工晶体计算公式在正常眼轴合并浅前房白内障患者中的准确性比较
Accuracy of Various Intraocular Lens Calculation Formulas in Shallow Anterior Chamber Patients with Normal Axial Length[J]. 临床医学进展, 2018, 08(02): 210-216. https://doi.org/10.12677/ACM.2018.82036
参考文献
- 1. 俞阿勇. 屈光性白内障手术的若干挑战[J]. 中华眼视光学与视觉科学杂志, 2017, 19(2): 65-70.
- 2. Kim, S.M., Choi, J. and Choi, S. (2009) Refractive Predictability of Partial Coherence Interferometry and Factors That Can Affect It. Korean Journal of Ophthalmology, 23, 6-12.
https://doi.org/10.3341/kjo.2009.23.1.6 - 3. 汤欣, 于莎莎. 重视和优选白内障术前生物学测量与人工晶状体屈光度计算的联合方案[J]. 中华实验眼科杂志, 2015, 33(4): 289-293.
- 4. Eleftheriadis, H. (2003) IOL Master Biometry: Refractive Results of 100 Consecutive Cases. British Journal of Ophthalmology, 87, 960-963.
https://doi.org/10.1136/bjo.87.8.960 - 5. Aristodemou, P., Knox Cart-wright, N.E., Sparrow, J.M. and Johnston, R.L. (2011) Formula Choice: Hoffer Q, Holladay 1, or SRK/T and Refractive Outcomes in 8108 Eyes after Cataract Surgery with Biometry by Partial Coherence Interferometry. Journal of Cataract and Refractive Surgery, 37, 63-71.
https://doi.org/10.1016/j.jcrs.2010.07.032 - 6. Narváez, J., Zimmerman, G., Stulting, R.D. and Chang, D.H. (2006) Accuracy of Intraocular Lens Power Prediction Using the Hoffer Q, Holladay 1, Holladay 2, and SRK/T Formulas. Journal of Cataract and Refractive Surgery, 32, 2050-2053.
https://doi.org/10.1016/j.jcrs.2006.09.009 - 7. Eom,Y., Kang, S.Y., Song, J.S., Kim, Y.Y. and Kim, H.M. (2014) Comparison of Hoffer Q and Haigis Formulae for Intraocular Lens Power Calculation According to the Anterior Chamber Depth in Short Eyes. American Journal of Ophthalmology, 157, 818-824.
https://doi.org/10.1016/j.ajo.2013.12.017 - 8. Connors III, R., Boseman III, P. and Olson, R.J. (2002) Accuracy and Reproducibility of Biometry Using Partial Coherence Interferometry. Journal of Cataract and Refractive Surgery, 28, 235-238.
https://doi.org/10.1016/S0886-3350(01)01179-8 - 9. Olsen, T. and Thorwest, M. (2005) Calibration of Axial Length Measurements with the Zeiss IOLMaster. Journal of Cataract and Refractive Surgery, 31, 1345-1350.
https://doi.org/10.1016/j.jcrs.2004.12.066 - 10. Kang, S.Y., Hong, S., Won J.B., Gong, J.S. and Chan, Y.K. (2009) Inaccuracy of Intraocular Lens Power Prediction for Cataract Surgery in Angle-Closure Glaucoma. Yonsei Medical Journal, 50, 206-210.
https://doi.org/10.3349/ymj.2009.50.2.206 - 11. Miraftab, M., Hashemi, H., Fotouhi, A., Khabazkhoob, M., Rezvan, F. and Asgari, S. (2014) Effect of Anterior Chamber Depth on the Choice of Intraocular Lens Calculation Formula in Patients with Normal Axial Length. Middle East African Journal of Ophthalmology, 21, 307-311.
- 12. Hoffer, K.J. (1993) The Hoffer Q Formula: A Comparison of Theoretic and Regression Formulas. Journal of Cataract and Refractive Surgery, 19, 700-712.
https://doi.org/10.1016/S0886-3350(13)80338-0 - 13. Holladay, J.T., Prager, T.C., Chandler, T.Y., Musgrove, K.H., Lewis, J.W. and Ruiz, R.S. (1988) A Three-Part System for Refining Intraocular Lens Power Calculations. Journal of Cataract & Refractive Surgery, 14, 17-24.
https://doi.org/10.1016/S0886-3350(88)80059-2 - 14. Retzlaff, J.A., Sanders, D.R. and Kraff, M.C. (1990) De-velopment of the SRK/T Intraocular Lens Implant Power Calculation Formula. Journal of Cataract and Refractive Surgery, 16, 333-340.
https://doi.org/10.1016/S0886-3350(13)80705-5 - 15. Olsen, T. (2007) Calculation of Intraocular Lens Power: A Review. Acta Ophthalmologica Scandinavica, 85, 472-485.
https://doi.org/10.1111/j.1755-3768.2007.00879.x - 16. Haigis, W., Lege, B., Miller, N. and Schneider, B. (2000) Comparison of Immersion Ultrasound Biometry and Partial Coherence Interferometry for Intraocular Lens Calculation According to Haigis. Graefe’s Archive for Clinical and Experimental Ophthalmology, 238, 765-773.
https://doi.org/10.1007/s004170000188 - 17. Sanders, D.R., Retzlaff, J. and Kraff, M.C. (1998) Comparison of the SRK II Formula and Other Second Generation Formulas. Journal of Cataract and Refractive Surgery, 14, 136-141.
https://doi.org/10.1016/S0886-3350(88)80087-7 - 18. Kim, Y.C., Sung, M.S., Heo, H. and Park, SW. (2016) An-terior Segment Configuration as a Predictive Factor for Refractive Outcome after Cataract Surgery in Patients with Glaucoma.BMC Ophthalmology, 16, 179-187.
https://doi.org/10.1186/s12886-016-0359-1 - 19. Joo, J., Whang, W.J., Oh, T.H., Kang, K.D., Kim, H.S. and Moon, J.I. (2011) Accuracy of Intraocular Lens Power Calculation Formulas in Primary Angle Closure Glaucoma. Korean Journal of Ophthalmology, 25, 375-379.
https://doi.org/10.3341/kjo.2011.25.6.375 - 20. 杨斐, 侯宪如, 吴慧娟, 鲍永珍. 年龄相关性白内障合并浅前房患者白内障术后屈光状态研究[J]. 中华眼科杂志, 2014, 50(2): 84-88.
- 21. 董丽华, 孙红艳, 朱江, 赵娜娜, 等. 年龄相关性白内障并发浅前房患者手术治疗后的屈光状况分析[J]. 国际眼科杂志, 2015, 15(6): 1083-1085.
