Material Sciences
Vol.
12
No.
03
(
2022
), Article ID:
49249
,
7
pages
10.12677/MS.2022.123017
MDOPD双季铵盐抑制SRB腐蚀的研究
黄金营1*,黄翰弈1,罗洪秦2
1武汉翰弈石油科技有限公司,湖北 武汉
2湖北大学材料学院,湖北 武汉
收稿日期:2022年2月7日;录用日期:2022年3月1日;发布日期:2022年3月11日

摘要
利用动电位扫描极化曲线、原子力显微镜和电子探针等方法研究了在硫酸盐还原菌SRB的培养基介质中,双季铵盐化合物MDOPD对碳钢SRB腐蚀行为的影响。结果表明:含菌介质中MDOPD具有杀灭SRB的作用,MDOPD可在Q235钢电极表面吸附形成有机缓蚀保护膜,除自身抑制介质的腐蚀外,还可阻碍SRB的代谢产物及腐蚀产物在电极表面吸附和沉积,从而降低了SRB生长代谢产物的次生腐蚀促进作用。MDOPD双季铵盐是一种性能优良的SRB腐蚀抑制剂。
关键词
硫酸盐还原菌,双季铵盐,吸附,代谢,抑制腐蚀

Study on Inhibition of SRB Corrosion by Double Quaternary Ammonium Salt MDOPD
Jinying Huang1*, Hanyi Huang1, Hongqin Luo2
1Wuhan Hanyi Petroleum Technology Co., Ltd., Wuhan Hubei
2School of Materials Science and Engineering, Hubei University, Wuhan Hubei
Received: Feb. 7th, 2022; accepted: Mar. 1st, 2022; published: Mar. 11th, 2022

ABSTRACT
The effect of double quaternary ammonium compound MDOPD on the SRB (sulfate reducing bacteria) corrosion behavior of carbon steel in the culture medium was studied by potentiodynamic scanning polarization curve, atomic force microscope and electron probe microanalysis. The results show that MDOPD in bacteria containing medium can kill SRB. MDOPD can adsorb on the surface of Q235 steel electrode to form an organic corrosion inhibition protective film. In addition to inhibiting the corrosion of medium, it can also hinder the metabolites and corrosion products to adsorb and deposit on the electrode surface, thus reducing the secondary corrosion promotion effect of SRB growth metabolites. Double quaternary ammonium salt MDOPD is an excellent SRB corrosion inhibitor.
Keywords:Sulfate Reducing Bacteria, Double Quaternary Ammonium Salt, Adsorption, Metabolism, Corrosion Inhibition

Copyright © 2022 by author(s) and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY 4.0).
http://creativecommons.org/licenses/by/4.0/


1. 引言
当环境介质中有硫酸盐还原菌(SRB)存在时,SRB吸附于基材表面形成生物膜,其生命活动可以改变基体材料的表面状况,包括改变介质以及膜内pH、形成 、O2、Cl−等促进腐蚀过程的物种等 [1] [2]。因此SRB生物膜的存在常导致点蚀、缝隙腐蚀、选择性溶解、应力腐蚀或垢下腐蚀,硫酸盐还原菌生物膜引起的腐蚀越来越受到人们的关注 [3] [4] [5]。
双季铵盐化合物是一种具有广阔应用前景的表面活性剂,属于阳离子型表面活性剂,较之单季铵盐,双季铵盐结构中有更多带正电荷的吸附中心,更容易吸附于带负电的SRB细胞膜表面,与细胞作用相互作用,结构中含有两个疏水链,对细胞膜半渗透性的破坏也更显著,同时其表面活性剂的分子结构特性也有利于其吸附于金属表面起到保护缓蚀作用 [6],因此成为针对SRB腐蚀缓蚀剂的重要开发方向。
本文主要利用动电位扫描极化曲线、原子力显微镜(AFM)和电子探针(EPMA)等方法研究了实验室自制双季铵化合物MDOPD对Q235钢表面SRB生物膜代谢以及腐蚀诱导行为的影响作用。
2. 实验方法
2.1. 试剂
本文中所有试剂除均为商用分析纯试剂。
2.2. MDOPD的合成
以甲硝唑为基质,二氯乙醚为连接剂,合成了一种杂环双季铵盐化合物MDOPD。合成步骤如下:将0.2 mol 2,2-二氯二乙醚加入到四口烧瓶中,缓慢升温至80℃,搅拌下将0.1 mol长链烷基叔胺缓慢滴加到2,2-二氯二乙醚中,约3 h滴加完,停止加热。溶液冷却后加入50 g乙腈,再升温至乙腈回流,然后将0.1 mol甲硝唑分次加入到反应溶液中,待甲硝唑溶解,再回流反应8 h后,溶液逐渐由黄色变成红棕色,冷却。室温下减压蒸去溶剂和未反应的原料后得到粗品,再用丙酮洗涤过滤得到棕色蜡状固体产物,将该产物命名为MDOPD。
2.3. 细菌培养
菌种来自中原油田(中国河南省)。细菌在人工培养基(API RP-38)中进行生长,培养基组成如下:乳酸钠4.0 mL;酵母提取物1.0 g;维生素C 0.1 g;七水硫酸镁0.2 g;磷酸二氢钾0.01 g;氯化钠10.0 g。由1 mol/L氢氧化钠将pH值调节至7.0至7.2。培养基用紫外线辐射灭菌。SRB在37℃无氧培养基中生长。SRB的数量通过API RP-38中的四管多重稀释和最可能数(MPN)方法进行测试。
2.4. 动电位扫描极化曲线测定
动电位扫描极化曲线测试采用传统的三电极体系。工作电极为碳钢电极,辅助电极为Pt电极,饱和甘汞(SCE)电极作为参比电极。
取两组带塞的250 ml三口烧瓶,每组烧瓶中的介质分别为空白培养基、培养基 + 0.1 g∙L−1 MDOPD,将已经过表面处理和紫外灯消毒的Q235钢电极分别插入烧瓶,并使培养基完全浸没电极,然后将烧瓶各口密闭后放入培养箱,在40℃ ± 1℃的条件下接种入经过活化的SRB菌种,分别培养不同时间(1 d、3 d、5 d和7 d)后取出烧瓶,用已灭菌注射器吸取1 ml含菌培养液进行菌量的测定,然后接上已经紫外灯消毒的参比电极和辅助电极,在40℃ ± 1℃水浴条件下,稳定2 h后进行动电位扫描极化曲线的测试,电位扫描速度0.5 mV/s,相对于开路电位−500 mV扫描至600 mV。
2.5. 生物膜形貌观察
将经过表面处理和紫外灯消毒的Q235钢试片(15 mm × 15 mm × 2 mm)浸入含菌培养基和加有0.1 g∙L−1 MDOPD的含菌培养基介质中(初始菌量3.5 × 106 cells∙ml−1),40℃ ± 1℃下密闭培养5d后取出试片,移入厌氧操作箱中,在1000 ml含2%戊二醛的灭菌培养基中固化8 h后,取出样品,用不同浓度的酒精脱水(50%、70%、80%、85%、90%、95%酒精脱水各10 min,100%酒精脱水30 min),待试片干燥后利用原子力显微镜(SPI3800, Seiko Instruments Inc.)对碳钢表面生物膜形貌进行微观分析测试,实验采用接触模式,探针型号为SN-AF01。生物膜元素构成的分析采用电子探针分析仪(JXA-8800R),束流2 × 10−8 mA,加速电压20 KV。
3. 结果与讨论
3.1. MDOPD对菌液中菌量及pH的影响
为了跟踪MDOPD对菌液中菌量的影响,利用绝迹稀释法测定了不同生长周期含菌培养基介质中的SRB菌量,结果如表1所示。
Table 1. Changes of SRB number in culture medium with culture time (T = 40˚C ± 1˚C)
表1. 培养基中SRB数随培养时间的变化(T = 40℃ ± 1℃)
表1中数据显示,在空白含菌培养基介质中,菌量变化较为微弱,此时菌量的变化仅与其自身的新陈代谢有关;而在加有双季铵盐化合物MDOPD的含菌介质中,随着培养时间延长,菌量有明显的下降趋势,这由MDOPD对液相中SRB的杀菌作用所致。
同时我们利用pH电极测定了SRB菌液的pH值随碳钢试片浸泡时间的变化情况,结果如图1所示。可见,空白含菌培养基中,由于SRB的生长繁殖和新陈代谢使介质的pH值降低,使培养基介质的腐蚀性增强 [7];而MDOPD的加入使SRB菌量降低,代谢活动减弱,从而使介质的pH值的变化较为微弱,MDOPD通过在碳钢表面的吸附成膜,也降低了介质的腐蚀性和生物膜下酸浸蚀的可能性。
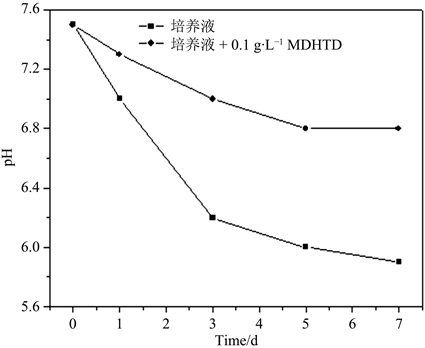
Figure 1. Change of pH value with immersion time of carbon steel
图1. SRB菌液pH值随碳钢试片浸泡时间的变化
3.2. 动电位扫描研究
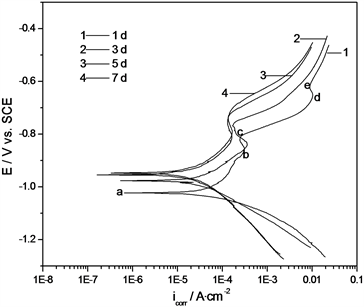
图2是碳钢在空白及含有0.1 g∙L−1 MDOPD的含菌培养基介质中的动电位扫描极化曲线随浸没时间的变化图。
 (a)
(a)
 (b)
(b)
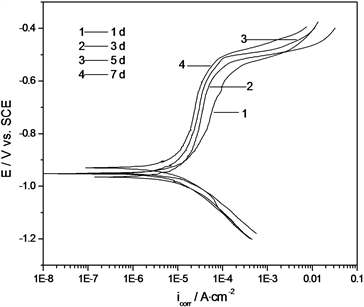
Figure 2. Potentiodynamic polarization curves of carbon steel samples in SRB inoculated medium under different soaking time. (a) Blank solution; (b) Containing 0.1 g∙L−1 MDOPD
图2. 不同浸泡时间下碳钢在接种SRB培养基中的动电位极化曲线。(a) 空白溶液;(b) 添加0.1 g∙L−1 MDOPD
如图2(a)所示,在空白含菌培养基介质中浸没1d的Q235钢电极的极化行为呈现二次钝化曲线的特征,ab段对应金属Fe的活化溶解区;b点是Q235钢的第一个“致钝点”,bc段对应Fe的“过渡钝化区”和“一次钝化区”,此区间内钢表面生成一层疏松的生物膜,该钝化区较窄,说明生物膜不够完整致密,因而随着电位正移而发生破裂;c点对应生物膜的破裂电位,即cd段为“过钝化区”,电极表面的SRB生物膜随电位正移而被击穿或脱落,对碳钢电极的保护作用减弱,从而使腐蚀电流进一步上升;d点为第二个“致钝点”,可能是因溶液中组分参加电极反应所致,e点以上的电位区间内,碳钢电极表面的保护膜会随着电位继续正移而再次出现破裂,阳极电流在e点后继续增大。
在SRB菌的培养基介质中,碳钢表面生成生物膜,阻碍了溶液介质与电极的接触,同时SRB菌的新陈代谢产物和腐蚀产物进一步导致碳钢基体表面电化学性质的不均匀性 [8],促进了碳钢腐蚀的形成和发展。受SRB附着和新陈代谢的影响,碳钢表面在不同生长周期的SRB培养基介质中所形成生物膜的组成和结构不同,对介质中溶解氧以及Cl−离子和Na+离子等具有不同的屏蔽性,从而影响基体金属的腐蚀过程。
随浸没时间延长,碳钢在含菌培养基中的阳极极化区“二次钝化”特征逐渐减弱,自腐蚀电位逐渐正移且趋于稳定,碳钢的腐蚀倾向减缓。可以判断,生长繁殖初期的SRB菌生物活性较强,其生长繁殖和新陈代谢速度较快,产生的代谢产物和腐蚀产物能够快速地在电极表面沉积,表面状态的变化较快;随着SRB菌进入稳定生长期,生长繁殖趋于稳定,碳钢电极表面保护膜趋于完整致密,对碳钢电极呈现一定程度的保护作用。
与空白培养基介质相比,含咪唑杂环的双季铵盐化合物MDOPD的加入使体系的自腐蚀电位正移,腐蚀电流密度迅速减小,腐蚀过程的阳极反应受到抑制。阳极极化曲线明显出现三段特征不同的区域:1) MDOPD存在并发挥缓蚀作用的缓蚀区;2) 腐蚀电流密度随电位正移而迅速增大的“平台”区,代表着电极表面的MDOPD发生了阳极脱附;3) 随着极化电位继续正移,出现类似无MDOPD时的无缓蚀区。
3.3. 碳钢试片表面生物膜的微观分析
将两组菌量相同的含菌培养基活化24 h后,把两组Q235钢试片分别悬挂于含有SRB的空白和加有0.1 g∙L−1 MDOPD的培养基中,40℃条件下恒温培养5d后,取出试片,按照1.3实验方法处理后利用原子力显微镜进行表面形貌的观察。
图3(a)显示了暴露于MDOPD之前碳钢表面上SRB生物膜的图像,但暴露于MDOPD 5天后,如图3(b)所示SRB生物膜变得松散,表面形貌发生了明显改变。说明添加MDOPD之后,MDOPD吸附膜使SRB表面的物理性能发生了变化,从而发生了形貌改变。
 (a) (b)
(a) (b)
Figure 3. AFM height mapping of carbon steel sample surface immersed in blank (a) and 0.1 g∙L−1 MDOPD containing culture medium for 5 days (T = 40˚C ± 1˚C)
图3. 培养基(T = 40℃ ± 1℃)中浸渍5 d碳钢试样的AFM高度图。(a) 空白培养液;(b) 培养液 + 0.1 g∙L−1 MDOPD
为了对比生物膜中的元素组成,采用JXA-8800R电子探针测量分析法对生物膜表面和生物膜下的碳钢表面进行了分析,得到的元素成分分析结果如表2所示。
Table 2. Percentage of elements on SRB biofilm surface and carbon steel surface under membrane (T = 40˚C ± 1˚C, immersion time: 5 d)
表2. 培养基中SRB膜表面及膜下碳钢表面元素百分比(T = 40℃ ± 1℃,浸渍时间:5 d)
由表2中O、S、P三种元素的百分含量对比可知,空白含菌培养基中碳钢生物膜表面呈现高的S含量,而P的含量为零;MDOPD含菌培养基介质中,则呈现高的P含量和较低的S含量。这说明SRB代谢产物极大改变了碳钢表面环境的化学组成。在空白含菌介质中,SRB菌群在生物膜表面大量地生长繁殖,其代谢产生的S与Fe结合为硫化物;而在加有MDOPD的含菌培养基中,由于MDOPD吸附和杀灭的双重作用使得SRB的代谢活动受到有效的抑制。SRB在碳钢表面形成代谢产物的机会降低,生物膜的大量沉积得到缓解,由生物膜内SRB直接或间接引起的局部腐蚀也因此而受到抑制。
3.4. MDOPD作用机制分析
结合以上各项研究数据的解析结果可推断:含咪唑杂环的双季铵化合物MDOPD通过对介质中的浮游SRB菌的有效杀灭,使液相中的菌量极大地减少,同时抑制了残余菌量的新陈代谢活动。同时,碳钢表面附近的菌量也难以得到补充,SRB对金属表面状态的影响和电化学腐蚀过程的参与都会受到有效的抑制。即首先MDOPD本身可以通过在电极表面吸附成膜对电极的腐蚀反应进行抑制作用,MDOPD的吸附还使得介质中SRB的代谢产物及腐蚀产物也难以在电极表面直接吸附和沉积,最后MDOPD还通过杀菌作用低了SRB生长代谢的次生过程(包括酸浸蚀等)对腐蚀的促进作用。三方面机制共同作用抑制了培养液中碳钢的SRB腐蚀。
4. 结论
1) 合成的双季铵盐MDOPD对培养基中碳钢的SRB腐蚀体现出明显的抑制作用。
2) MDOPD的缓蚀机制体现在自身吸附成膜缓蚀、抑制生物膜及腐蚀产物沉积于金属表面、直接灭杀细菌三方面。三种机制共同作用获得了良好的SRB腐蚀抑制效果。
文章引用
黄金营,黄翰弈,罗洪秦. MDOPD双季铵盐抑制SRB腐蚀的研究
Study on Inhibition of SRB Corrosion by Double Quaternary Ammonium Salt MDOPD[J]. 材料科学, 2022, 12(03): 169-175. https://doi.org/10.12677/MS.2022.123017
参考文献
- 1. Beer, D., Stoodley, P., Roe, F., et al. (1994) Effects of Biofilm Structures on Oxygen Distribution and Mass Transport. Biotechnology and Bioengineering, 3, 1131-1138. https://doi.org/10.1002/bit.260431118
- 2. 刘靖, 郑家燊, 许立铭, 等. 电场和杀菌剂对杀灭生物膜下硫酸盐还原菌的协同作用[J]. 腐蚀科学与防护技术, 2002(1): 23-26.
- 3. Miller, L.P. (1950) Formation of Metal Sulfides through the Activities of Sulfate-Reducing Bacteria. Boyce Thompson Institute for Plant Research, 85.
- 4. Bacon, P.B., Brewer, P.G., Spencer, D.W., et al. (1980) Lead-210, Polonium-210, Manganese and Iron in the Cariaco Trench. Deep-Sea Research, 27A, 119-135. https://doi.org/10.1016/0198-0149(80)90091-6
- 5. Webb, J.S., McGinness, S. and Lappin-Scott, H.M. (1998) Metal Removal by Sulfate-Reducing Bacteria from Natural and Constructed Wetlands. Journal of Applied Microbiology, 84, 240-248. https://doi.org/10.1046/j.1365-2672.1998.00337.x
- 6. 孟琳, 周丽萍, 葛双启, 等. 双季铵盐杀菌剂的合成及其杀菌性能研究[J]. 化学工程师, 2005(4): 59-60.
- 7. Postgate, J.R. (1979) The Sulfate-Reducing Bacteria. Cambridge University Press, Cambridge.
- 8. Postgate, J.R. (1981) The Sulfate Reducing Baceria. 2nd Edition, Cambridge University Press, Cambridge.
NOTES
*通讯作者。
