Pharmacy Information
Vol.07 No.04(2018), Article ID:25819,6
pages
10.12677/PI.2018.74015
The Rat Plasma Protein Binding of YM0402 Enantiomers
Xiawen Liu*, Yunying Zhang, Mu Yuan*
School of Pharmaceutical Sciences, Guangzhou Medical University, Guangzhou Guangdong

Received: Jun. 25th, 2018; accepted: Jul. 4th, 2018; published: Jul. 11th, 2018

ABSTRACT
OBJECTIVE: To study the stereo selective protein binding of YM0402 enantiomers in rat plasma, and to clarify the interactions between YM0402 enantiomers. METHODS: Equilibrium dialysis method combined with liquid chromatograpy-tandem mass spectrometry was employed to determine the protein binding rate with rats plasma protein. RESULTS: The rat plasma protein binding of YM0402 enantiomers was 90% - 99%. A-YM0402 showed slightly higher binding rate than that of B-YM0402. The bounding rate of both enantiomers in racemate form was higher than that of single enantiomers. CONCLUSION: The binding rate of YM0402 enantiomers with rat plasma protein was higher than 90%. There might be different binding site on rat plasma protein with YM0402 enantiomers.
Keywords:YM0402, Enantiomers, Plasma Protein Binding Rate
YM0402对映体与大鼠血浆蛋白结合率研究
刘夏雯*,张芸影,袁牧*
广州医科大学药学院,广东 广州

收稿日期:2018年6月25日;录用日期:2018年7月4日;发布日期:2018年7月11日

摘 要
目的:明确YM0402对映体与大鼠血浆蛋白结合是否存在立体选择性差异,揭示两对映体与血浆蛋白结合时的相互作用。方法:本研究通过平衡透析法对YM0402对映体与大鼠血浆进行共孵育,并利用手性高效液质联用法进行定量检测。结果:YM0402对映体与大鼠血浆蛋白在考察浓度范围内(0.2~20 μM)结合率均高于90%;在低浓度范围(0.2、1 μM),A-YM0402的结合率略高于B-YM0402;高浓度下(大于5 μM) YM0402对映体与大鼠血浆蛋白结合趋于饱和。外消旋体中两个异构体的结合率均比单独结合时高。结论:YM0402对映体与大鼠血浆蛋白具有高结合率。两对映体与大鼠血浆蛋白结合可能具有不同位点。
关键词 :YM0402,对映体,血浆蛋白结合率

Copyright © 2018 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 前言
YM0402是选择性的α1D/1A-肾上腺素受体拮抗剂,与其它α1D/1A-肾上腺素受体拮抗剂相比(例如,坦索罗辛),YM0402具有更好的活性 [1]。然而YM0402对映体在大鼠体内的生物利用度都很低(B-YM0402,14.5%;A-YM0402,6.8%) [2]。另外,在大鼠肝、肾和前列腺中,B-YM0402的器官暴露量分别是A-YM0402的1.33,2.90和3.16倍 [3]。
药物被吸收后,进入血液循环,其中一部分与血浆蛋白结合,另一部分以游离态通过毛细血管壁到达各个靶点,发挥药效。当手性药物与血浆蛋白作用时,通常作用的时间和强弱也影响着对映体的药动学和药效作用。然而YM0402对映体与血浆蛋白结合率尚未报道。
因此,本研究对YM0402对映体与血浆蛋白结合进行研究。利用手性液质联用法对透析膜两测的YM0402对映体进行分析。明确YM0402对映体与大鼠血浆蛋白结合率是否具有立体选择性差异。为理解YM0402对映体的在大鼠体内的手性药代动力学特征提供依据。
2. 实验部分
2.1. 材料与试剂
Rac(±)-YM0402,A-YM0402和B-YM0402以及内标Z10 (专利号201210145152.1)均由本实验室合成。大鼠血浆来自SPF级大鼠禁食12 h血浆。大鼠的饲养及取血过程均经广州医科大学伦理委员会审核通过。PBS (0.1 M, pH 7.4)购自美国GIBCO公司。色谱级甲醇和乙腈购于美国Fisher。其它试剂为化学纯。RED快速平衡透析装置购于美国Thermo。液质联用系统为Agilent1260-6460三重四级杆液质联用系统。
2.2. 方法与结果
2.2.1. 样品预处理
内标储备液10 μL 20 μg/mL NZ-10置于2 mL离心管中,N2吹干后,加入样品100 μL,后加入300 μL 甲醇,涡旋混合5分钟,于4℃下13,000 × g离心5分钟,取上清,N2吹干,残渣用200 μL流动相复溶,2 μL进样。
2.2.2. RRLC-MS/MS方法及方法验证
液相和质谱条件
色谱柱:大赛璐Chiralpak IA-3 (150 mm × 2.1 mm, 3 μm);流动相:甲醇;流速:0.25 mL/min;柱温度:25℃;质谱采集设置为:正离子模式;对目标化合物的检测采用多反应监测,离子通道分别设为m/z 393~249,0.6 V (YM0402)和m/z 427~235,0.4V (I.S.)。基质中A-YM0402和B-YM0402以及内标Z10的保留时间分别为3.5 min,5.9 min和4.9 min (如图1)。
方法验证
方法验证按照中国食品药品监督管理局相关规定实施。验证包括选择性,基质效应,回收率,线性,准确度,精密度和稳定性。
分别取6个不同供体的大鼠空白血浆,以及空白PBS溶液,按照“样品预处理”项下方法操作,得到各空白基质。血浆样品和含蛋白样品中低、中和高浓度质控样品(QC)终浓度为4,80,和160 μM;PBS中低、中和高浓度质控样品终浓度为0.06,0.96和3 μM。在YM0402和内标的出峰时间未见干扰信号。基质效应通过计算生物基质中YM0402对映体峰面积和流动相中YM0402对映体标准品峰面积比值获得,每种基质做三个平行样品。所测基质中,基质效应影响均小于15%。回收率通过比较预处理空白基质加入YM0402对映体峰面积与空白基质加入YM0402对映体再进行预处理后的峰面积获得,回收率为74.3%~92.6% (结果见表1)。线性通过对YM0402对映体与内标峰面积比值和YM0402对映体浓度进行绘图,得出标准曲线的回归系数。批内及批件准确度通过批内和批间不同浓度QC获得浓度与标示浓度的百分比值衡量。要求准确度在85%~115%,最低定量限范围80%~120%。批内和批间精密度通过计算批内和批间QC样品的变异系数获得。变异系数要求不超过15%,定量下限变异系数不超过20% (结果见表2)。不同基质中YM0402对映体的稳定性考察条件为室温,−20℃,三次冻融,以及预处理后室温放置24小时内。以上条件下,样品均稳定。
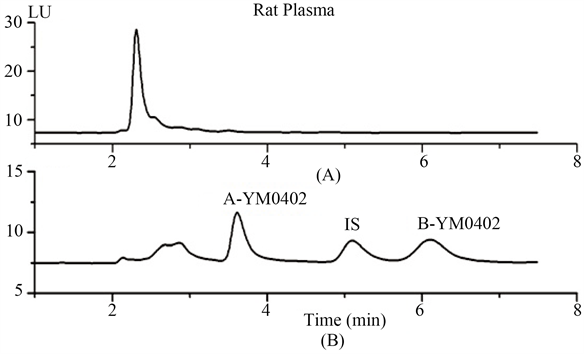
Figure 1. Chromatograms of YM0402 enantiomers and IS in rat plasma. (A) Blank rat plasma matrix; (B) Blank rat plasma spiked with YM0402 enantiomers and IS
图1. YM0402对映体在大鼠血浆中的色谱图。(A) 空白大鼠血浆色谱图;(B) YM0402对映体及内标在大鼠血浆中色谱图
Table 1. Recovery (%) of YM0402 enantiomers from rat plasma and PBS (mean (SD), n = 6)
表1. YM0402对映体在大鼠血浆和PBS中的回收率(平均值(标准差),n = 6)
Table 2. Calibration curves, accuracy and precisions of YM0402 enantiomers in rat plasma and PBS (mean (SD), n = 6)
表2. 大鼠血浆和PBS中YM0402对映体浓度测量方法学验证参数(平均值(标准差),n = 6)
2.2.3. 药物与蛋白结合数学模型及数据处理
药物与蛋白的结合可以描述成: 。根据质量作用定律,药物蛋白结合动力学可描述成:
(1)
其中Ka为结合常数,[CB]指结合药物浓度,[CU]指游离药物浓度,[P]指蛋白浓度。总药物浓度和游离药物浓度在利用数学模型拟合后,一般利用图解法可以得到nKa的粗略值。对于方程式(1)我们可以改写其为:
(2)
利用该Scatchard方程,以CB为X轴,CB/CU为Y轴,由非线性最小二乘法估计得出Y轴上的截距,即nKa,从而得到药物的结合常数。药物与蛋白结合率按 计算;对映体之间血浆蛋白结合差异的显著性考察按照双样本t检验进行统计。
2.2.4. 孵育时间筛选
对含有YM0402对映体5 μM (有机溶剂含量小于1%)的大鼠血浆于37℃分别孵育2,4,6小时。LC-MS/MS按照1.2.3项下方法进行检测。发现4 h和6 h,血浆中YM0402对映体含量无差异。因此,平衡透析孵育时间设定为4 h。
2.2.5. YM0402对映体与大鼠血浆蛋白结合反应
取空白大鼠血浆,分别加入YM0402对映体和外消旋体使其终浓度为0.2、1、5、10、15 mM。取200 μL含药血浆加入样品室,取350 μL PBS加入缓冲液室,于37℃孵育4 h。样品室和缓冲液室分别吸取100 μL和250 μL,按照“样品预处理”项下方法操作,由LC-MS检测血浆样品药物总浓度(CB),缓冲液样品Z中游离药物浓度(CU)。
YM0402对映体与大鼠血浆蛋白在考察浓度范围内(0.2~20 μM)结合率均高于90%。在低浓度范围呈现浓度依赖性,随着药物浓度的增大,结合率升高,当对映体浓度达到5 μM后,结合率趋于饱和。在低浓度范围(0.2、1 μM),A-YM0402的结合率略高于B-YM0402。在消旋体的形式下,YM0402对映体与大鼠血浆蛋白结合均明显高于对映体单体的血浆结合率(见图2)。
3. 讨论
YM0402对映体与大鼠血浆存在广泛结合,结合率高达90%~99%。在与实际大鼠口服给药以后的血药浓度更加接近的低浓度水平(<5 μM),YM0402对映体与大鼠血浆的蛋白结合率存在立体选择性,他们的结合率从大到小依次为:消旋体中B-YM0402 > 消旋体中A-YM0402 > B-YM0402 > A-YM0402。
根据“游离药物假说”药物-血浆蛋白复合物不能通过被动转运或细胞旁渗透而透过细胞膜。只有游离药物能透过膜到达组织,且只有游离药物分子可被肝代谢和肾清除。因此,血浆蛋白结合能够限制血液中的化合物,限制药物分子透过到把组织而产生药理效应,并限制他们进入其他身体组织和清除器官(如肝、肾)。研究结果发现以消旋体为研究对象时,在低浓度水平下血浆蛋白结合率显著高于单一对映体。那么依据以上假说可做如下推测:大鼠分别口服消旋体和单一对映体后,前者给药方式下,YM0402对映体会被更多的限制在血浆中,因而导致进入靶组织和清除器官的药物数少,最终导致药物的排泄量更低。这与我们前期研究结果,消旋体给药后原药的排泄量低于单体给药后的排泄量相符。因此,YM0402对映体与大鼠血浆蛋白结合的差异影响了药物在体内的消除。
当存在另一对映体时,YM0402两对映异构体会与大鼠的血浆蛋白共同作用,导致两个对映体的血浆蛋白结合率共同升高。这种现象可能与结合蛋白的构象改变有关。据文献报道,S-(+)-布洛芬的存在可以使S-乙酸氯羟去甲安定与人血清白蛋白的结合显著增加 [4]。布洛芬和乙酸氯羟去甲安定分别在HSA上的苯二氮卓和华法林位点结合,当布洛芬与HSA上苯二氮卓位点结合的同时会引起华法林位点构象的改变,从而使得另一个药物与华法林位点结合更加紧密。同样的,S-苯二氮卓类药物的存在也可以使得S-华法林与HSA的结合率增加 [5]。因此YM0402与大鼠血浆蛋白结合在消旋体中和单一对映体中的差异,推测可能是两对映体与蛋白不同位点结合从而使蛋白发生了具有协同作用的变构现象,从而导致外消旋体中两个异构体的结合率均比单独结合时高。
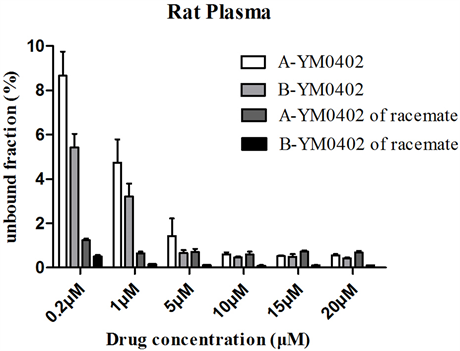
Figure 2. The unbound fraction of YM0402 enantiomers with rat plasma. Data are expressed as mean and SD, n = 3
图2. 大鼠血浆中游离YM0402对映体比例。数据表示为平均值和标准误差,n = 3
基金项目
国家自然科学基金(81503131)。
文章引用
刘夏雯,张芸影,袁 牧. YM0402对映体与大鼠血浆蛋白结合率研究
The Rat Plasma Protein Binding of YM0402 Enantiomers[J]. 药物资讯, 2018, 07(04): 79-84. https://doi.org/10.12677/PI.2018.74015
参考文献
- 1. Masumori, N. (2011) Naftopidil for the Treatment of Urinary Symptoms in Patients with Benign Prostatic Hyperplasia. Therapeutics and Clinical Risk Management, 7, 227-238. https://doi.org/10.2147/TCRM.S13883
- 2. Liu, X., et al. (2012) Determination of Naftopidil Enantiomers in Rat Plasma Using Chiral Solid Phases and Pre-Column Derivatization High-Performance Liquid Chroma-tography. Journal of Chromatography B, 907, 140-145. https://doi.org/10.1016/j.jchromb.2012.09.021
- 3. Liu, X., et al. (2015) Enantiospecific Determination of Naftopidil by RRLC-MS/MS Reveals Stereoselective Pharmacokinetics and Tissue Distributions in Rats. Journal of Pharmaceutical and Biomedical Analysis, 112, 147-154. https://doi.org/10.1016/j.jpba.2015.04.034
- 4. Fitos, I., et al. (1999) Stereoselective Allosteric Binding Interaction on Human Serum Albumin between Ibuprofen and Lorazepam Acetate. Chirality, 11, 115-120. 3.0.CO;2-R>https://doi.org/10.1002/(SICI)1520-636X(1999)11:2<115::AID-CHIR6>3.0.CO;2-R
- 5. Fitos, I. and Simonyi, M. (1992) Ste-reoselective Effect of Phenprocoumon Enantiomers on the Binding of Benzodiazepines to Human Serum Albumin. Chirality, 4, 21-23. https://doi.org/10.1002/chir.530040106
NOTES
*通讯作者。
