Bioprocess
Vol.07 No.04(2017), Article ID:23265,6
pages
10.12677/BP.2017.74008
Analysis of Mono(sesqui)terpenes by GC-MS/MS in Rice Leaves
Huanran Yin, Yuchi He, Yang Li*
School of Life Science, Hubei University, Wuhan Hubei
*通讯作者。

Received: Nov. 30th, 2017; accepted: Dec. 19th, 2017; published: Dec. 29th, 2017

ABSTRACT
Six monoterpenes and two sesquiterpenes were identified by GC-MS from rice leaves using hexane as solvent. To quantitatively analyze these eight compounds, we established a target method (MRM) for these six monoterpenes and two sesquiterpenes in rice leaves. Results showed that sesquiterpene trans-farnesol was the major compounds of these volatile terpenes and the fresh weight of trans-farnesol reached to 10359.1 ± 117.7 ng∙g−1 FW.
Keywords:Rice, Monoterpenes, Sesquiterpenes, GC-MS/MS, MRM
GC-MS/MS法分析水稻叶子单萜倍半萜类化合物的组成
殷焕然,何玉池,李洋*
湖北大学生命科学学院,湖北 武汉

收稿日期:2017年11月30日;录用日期:2017年12月19日;发布日期:2017年12月29日

摘 要
以正己烷为提取溶剂,采用气相色谱–质谱联用法(GC-MS)鉴定出水稻三叶期叶片6种单萜类化合物和2种倍半萜类化合物。针对鉴定出来的8种化合物建立靶向定量代谢组方法,采用多反应监测(MRM)的质谱方法对水稻三叶期叶片中的6种单萜类物质及2种倍半萜类物质进行定量分析。结果表明,倍半萜trans-金合欢醇的含量在这8种化合物中含量最高(10359.1 ± 117.7ng∙g−1 FW),同时也是水稻叶子中单萜倍半萜类化合物的主要组成成分。
关键词 :水稻,单萜,倍半萜,气相色谱–质谱联用,多反应监测

Copyright © 2017 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
次生代谢产物是指生物体内一大类并非生长发育所必需的小分子有机化合物。次生代谢是生物长期进化中对生态环境适应的结果,因此次生代谢产物的产生和分布通常有种属、器官、组织、和生长发育的特异性 [1] 。植物次生代谢产物是次生代谢产物中很大的一类,这些丰富种类的化合物在医药、农业和工厂生产中扮演了很重要的角色 [2] 。萜类化合物是已知植物次生代谢产物中种类最多的物质,目前已经在植物中发现了超过15,000种的各种萜类物质。很多萜类物质具有重要的医药价值,例如从黄花蒿中提取出来的倍半萜类化合物青蒿素是目前有效的抗疟药,红豆杉中提取出来的二萜类物质紫杉醇是常用的抗癌药物 [3] [4] 。因此对植物次生代谢产物萜类物质的研究一直以来都是研究的热点。
水稻是我国主要的粮食作物之一,对于其产量以及抗逆相关的研究一直是东南亚乃至世界学者们的研究热点 [5] 。已有的研究表明,挥发性萜类物质如单萜倍半萜在主要的农作物例如水稻、玉米中具有间接防御的作用,这些易挥发的香气物质可以吸引害虫天敌从而起到保护自身的目的 [6] [7] [8] [9] 。而对于这些易挥发的单萜倍半萜类物质在植物体内的功能研究却寥寥无几。我们以水稻叶子为材料建立了并优化了一种测定体内单萜倍半萜的方法,成功检测到了水稻三叶期叶片中的8种单萜倍半萜类化合物,并对这8种化合物进行了定量分析,为接下来单萜倍半萜在植物体内功能的研究奠定了基础。
2. 仪器与材料
2.1. 仪器
Shimadzu TQ8040三重四级杆气相色谱–质谱联用仪,METTLER电子分析天平,Retsch MM400磨样机。
2.2. 试剂
8种萜类化合物标准品均购自美国Sigma公司;正己烷为色谱纯(Sigma);其它试剂均为分析纯。
3. 方法
3.1. 色谱条件
色谱柱:Rtx-5MS capillary column (5% diphenyl/95% dimethyl siloxane, 30 m × 0.25 mm inside diameter, 0.25 mm film thickness, GL science);流动相:高纯氦气;He流速:0.8 mL/min;进样方式:不分流进样;进样量:1 μL;进样口温度:250℃;柱温箱温度:50℃;柱温箱升温程序:50℃保持1 min,然后以5℃/min升温至300℃,保持5 min。
3.2. 质谱条件
溶剂延时时间:3 min;EI源:70 eV;离子源温度:200℃;连接杆温度:250℃;检测器电压:0.9 kV (TIC),1.6 kV (MRM);全扫描方法:Q3 Scan m/z 45-300;MRM方法:RT 5-14 min Ch1 m/z 93.00 > 73.10,CE 10 eV。RT 14-30 min Ch1 m/z 69.00 > 53.10,CE 10 eV。
3.3. 样品制备
采用溶剂提取法,以纯正己烷为溶剂制备样品 [10] 。取新鲜水稻三叶期叶片0.1~0.2 g,置于2 mL EP管中,迅速放入液氮速冻。用磨样机磨碎后,按0.1 g/700 μL的比例加入正己烷,每隔10 min剧烈震荡10 s,共3次,置于4℃冰箱过夜。第二天4℃冷冻离心13,000 g 10 min,取上清微孔滤膜过滤至进样瓶待测。
4. 结果与分析
4.1. 水稻叶子代谢样全扫描分析
我们首先对样品进行了全扫描分析,质谱碎片(m/z)扫描范围为45-300。TIC峰图如图1所示,对该图进行提取质谱分析,分别提取69与93这两个单萜倍半萜特征碎片,对提取出来的峰进行库(NEST)比对,找到了8种萜类物质(图2)。其中6种单萜类物质分别为α-蒎烯(RT 7.1 min)、β-月桂烯(RT 8.6 min)、柠檬烯(RT 9.8 min)、罗勒烯(RT 10.3 min)、芳樟醇(RT 11.8 min)、香叶醇(RT 16.1 min),2种倍半萜类物质分别为trans-橙花叔醇(RT 24.3 min)和trans-金合欢醇(RT 27.9 min)。为进一步验证物质鉴定结果,我们购买并测定了以上8种物质的标准品(图3),通过对比保留时间及二级碎片,发现上述8种物质的鉴定结果完全正确。
4.2. MRM方法的建立及优化
基于四级杆质谱的扫描特点,全扫描虽然能收集到更多的碎片信息,利于物质的鉴定,但是由于背景碎片的影响,对于物质的定量尤其是低含量物质的定量略显不足。MRM是基于三重四级杆质谱的一种扫描方法,这种扫描方法通过对一级碎片的筛选、进一步中性裂解、裂解后二级碎片的再次筛选来进行物质的扫描,所以这种方法具有灵敏度高、准确度高、重现性好的优点,非常有利于物质的定量。针对我们所检测到的8种萜类化合物,选取特异性高、丰度高的69和93这两个母离子进行碎片离子扫描,并对其碰撞能量进行优化(图4),找出最适宜的离子对及其所对应的CE能量。
4.3. 水稻叶子代谢样MRM定量分析
GC方法不变,设定MS的MRM方法为93.00 > 77.10 (CE 10 eV) RT 5~14 min,69.00 > 53.10 (CE 10 eV) RT 14~30 min。重新对水稻叶子代谢样进行测定,并对混合标准品进行测定,对水稻叶子中8种萜类化合物进行定量分析(表1)。其中,倍半萜trans-金合欢醇的含量在这8种化合物中含量最高(10359.1 ± 117.7 ng∙g−1 FW),为水稻叶子中单萜倍半萜类物质的主要成分(74.93%) (图5);单萜香叶醇为含量最高的单萜类物质(797.4 ± 6.9 ng∙g−1 FW)。
5. 结论
本研究通过建立一种MRM的方法,成功对水稻叶片中的8种易挥发单萜倍半萜类物质进行定量检测,其中的主要成分金合欢醇是一种重要的生物活性物质或活性物质中间体,也是重要的高级香料之一 [11] 。已有的研究表明,玉米在被害虫咬食后其金合欢醇的挥发量有明显的上升 [12] ,表明金合欢醇很有
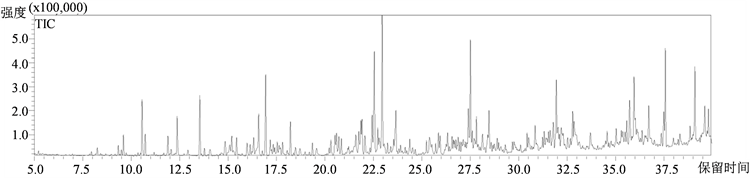
Figure 1. TIC of rice leaves
图1. 水稻叶片总离子图

Figure 2. 8 mono(sesqui)terpenes in rice leaves. 1 linalool, 2 geraniol, 3 α-pinene, 4 β-myrcene, 5 limonene, 6 ocimene, 7 trans-nerolidol, 8 trans-farnesol
图2. 水稻叶子中的8种单萜倍半萜类物质。1. 芳樟醇 2. 香叶醇 3. α-蒎烯 4. β-月桂烯 5. 柠檬烯 6. 罗勒烯 7. trans-橙花叔醇 8. trans-金合欢醇

Figure 3. TIC of 8 mono(sesqui)terpenes mix-standard material
图3. 8种单萜倍半萜类物质混合标样的总离子图
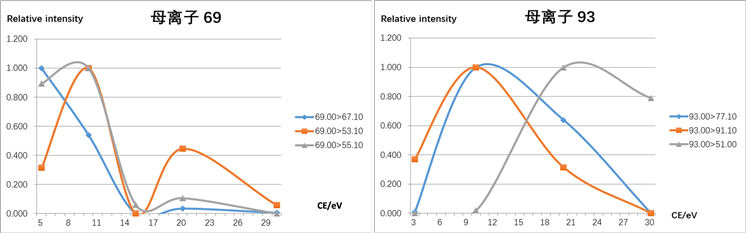
Figure 4. Result of MRM Optimization (Graph)
图4. MRM碎片能量优化图。CE碰撞能量Relative intensity相对强度
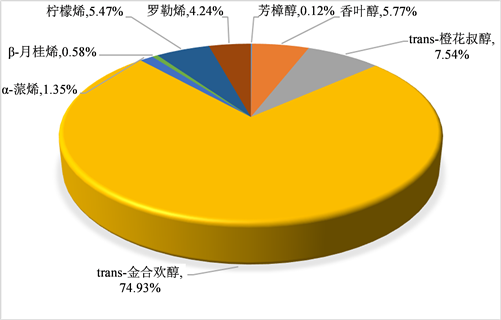
Figure 5. Components of mono(sesqui)terpenes in rice leaves
图5. 水稻叶子中单萜倍半萜的组成成分
Table 1. List of monoterpene and sesquiterpene compounds in rice leaves
表1. 水稻叶子中单萜和倍半萜类物质含量表
Values are means ± SE of three replicates. Three leaf blades were used per 1 replicate. 一共有3个生物重复. 每个生物重复中含3片叶子。
可能参与了植物受害虫侵食过后的一系列抗逆反应。同时金合欢醇在自然界中具有广泛的资源分布,主要存在于植物的花、叶子和种子的精油中,尤其是在中草药植物中具有较高的含量,是中草药植物重要的活性成分之一,可用于精神抑制药和防癌抗癌药物等 [13] 。本文通过对水稻叶片中单萜倍半萜的检测及定量,建立了稳定性重现性好的挥发性萜类物质检测方法。同时在研究过程中发现金合欢醇为水稻叶片中的主要单萜倍半萜类物质,暗示了它在水稻的一系列抗逆反应中可能起到了很关键的作用,后续将围绕金合欢醇在水稻抗逆中的作用展开研究。
基金项目
国家自然科学基金(31400273);湖北省科技厅创新团队项目2017CFA023;2016年武汉市黄鹤英才创新人才项目。
文章引用
殷焕然,何玉池,李洋. GC-MS/MS法分析水稻叶子单萜倍半萜类化合物的组成
Analysis of Mono(sesqui)terpenes by GC-MS/MS in Rice Leaves[J]. 生物过程, 2017, 07(04): 54-59. http://dx.doi.org/10.12677/BP.2017.74008
参考文献 (References)
- 1. 董妍玲, 潘学武. 植物次生代谢产物简介[J]. 生物学通报, 2002(11): 17-19.
- 2. 王莉, 史玲玲, 张艳霞, 刘玉军. 植物次生代谢物途径及其研究进展[J]. 武汉植物学研究, 2007(5): 500-508.
- 3. 张铁军, 王于方, 刘丹, 李力更, 郭瑞霞, 史清文, 董燕平. 天然药物化学史话:青蒿素——中药研究的丰碑[J]. 中草药, 2016, 47(19): 3351-3361.
- 4. 史清文. 天然药物化学史话:紫杉醇[J]. 中草药, 2011, 42(10): 1878-1884.
- 5. 程勇翔, 王秀珍, 郭建平, 赵艳霞, 黄敬峰. 中国水稻生产的时空动态分析[J]. 中国农业科学, 2012, 45(17): 3473-3485.
- 6. 周妮, 朱莉, 郎志宏, 黄大昉. 萜类化合物在植物间接防御中的作用[J]. 中国生物工程杂志, 2010, 30(7): 101-107.
- 7. 刘芳. 挥发物在调节稻飞虱及其天敌种内种间关系中的作用[D]: [博士学位论文]. 杭州: 浙江大学, 2001.
- 8. 玉米虫害间接防御基因表达调控机制取得新进展[J]. 种业导刊, 2015(10): 32.
- 9. 李圣彦. 玉米ERF转录因子通过调控tps10基因来影响植物间接防御[C]//中国植物保护学会. 2014年中国植物保护学会学术年会论文集. 北京: 中国植物保护学会, 2014: 1.
- 10. Ma, D.M., et al. (2015) A Genome-Wide Scenario of Terpene Pathways in Self-pollinated Artemisia annua. Molecular Plant, 8, 1580-1598. https://doi.org/10.1016/j.molp.2015.07.004
- 11. 赵振东, 苏文强, 陈风雨, 毕良武. 金合欢醇的资源及其生物活性应用研究进展[J]. 林产化学与工业, 2005(S1): 175-178.
- 12. Schnee, C., et al. (2002) The Maize Gene terpene synthase 1 Encodes a Sesquiterpene Synthase Catalyz-ing the Formation of (E)-Beta-Farnesene (E)-Nerolidol, and (E,E)-Farnesol after Herbivore Damage. Plant Physiology, 130, 2049-2060. https://doi.org/10.1104/pp.008326
- 13. 陈风雨, 王忠, 毕良武, 赵振东. 金合欢醇合成方法的研究进展[J]. 林产化工通讯, 2005(5): 34-38.
