Botanical Research
Vol.05 No.03(2016), Article ID:17719,10
pages
10.12677/BR.2016.53012
Nanostructures of Salix mongolica Cellulose and Structure Determination
Zhenhua Xue*, Qidong Shang
Inner Mongolia Agricultural University, Hohhot Inner Mongolia

Received: May. 6th, 2016; accepted: May. 22nd, 2016; published: May. 30th, 2016
Copyright © 2016 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
The preparation process of nanocellulose was introduced in this paper using Salix branches by a method of sulfuric acid hydrolysis. And then the structure and characteristics of nanocellulose were detected with a series of modern analytic methods using advanced apparatus. The experimental results show that Salix mongolica cellulose was no longer fiber clusters but dispersed into many monofilaments after sulfuric acid hydrolysis. Its molecular chains were interrupted, the decomposition temperature was lower than before treatment, chemical composition remained basically and the crystallinity increased.
Keywords:Salix mongolica, Nanocellulose, Sulfuric Acid Hydrolysis, Crystal Structure

沙柳纤维素纳米化及其结构测定
薛振华*,尚琪冬
内蒙古农业大学,内蒙古 呼和浩特

收稿日期:2016年5月6日;录用日期:2016年5月22日;发布日期:2016年5月30日

摘 要
本文以沙柳枝条为原料,应用硫酸水解法制备了沙柳纳米纤维素,借助现代仪器分析手段分析了沙柳纳米纤维素的结构和性能。研究结果表明,经硫酸水解处理后,沙柳纤维素不再成纤维簇而是分散成许多纤维单丝,其分子链被打断,分解温度较处理前降低,化学成分基本保持不变,纳米纤维素晶体的结晶度较原纤维有一定程度的提高。
关键词 :沙柳,纳米纤维素,硫酸水解,晶体结构

1. 引言
沙柳(学名:Salix psammophila)别名筐柳、降马(藏名)为沙漠植物。其幼枝黄色,并呈叶线形或线状披针形,枝条丛生不怕沙压,根系发达,萌芽力强,是广泛生长在西北地区和内蒙西部地区的一种沙生植物,具有良好的防风固沙特性,是三北防护林的主要速生灌木。沙柳属阔叶散孔材,主要由导管、木纤维、木射线薄壁细胞及少量轴向薄壁细胞组成。其中导管占27.1%、木纤维占68.4%、木射浅薄壁细胞占3.4%、其它占1.1%。沙柳材的纤维素含量较高,用亚氯酸钠法测定其综纤维素含量为78.96%、其半纤维素为23.37%、木质素为18.20% [1] 。
纳米技术是20世纪80年代末、90年代初逐步发展起来的一门崭新的科学技术。纳米技术的发展和纳米材料的出现标志着人类认识自然达到了一个新的层次,而且对未来的产业升级和经济增长都将产生重要影响。因此,纳米科学技术近年来已成为许多发达国家和新兴工业国家优先支持和发展的领域 [2] 。2000年1月21日,美国总统克林顿在加州理工学院正式宣布一项新的国家计划——国家纳米技术计划 (NNI, National Nanotechnology Initiative),旨在整合联邦各机构的力量,加强其在开展纳米尺度的科学、工程和技术开发工作方面的协调,该计划被克林顿作为联邦政府科技研究与开发的第一优先计划 [3] [4] 。中国政府在2001年7月发布了《国家纳米科技发展纲要》,此纲要对我国纳米研究的发展起到了重要的推动作用。目前,世界上已有50多个国家制定了国家级的纳米技术计划,一些国家虽然没有专项的纳米技术计划,但其他计划中也往往包含了纳米技术相关的研发。
现代材料研究表明,当物质尺寸进入纳米数量级时,由于较小的晶粒尺寸,使其晶界上的原子数的比例增大,产生高浓度晶界,从而赋予其许多不同于粗晶材料的特异的性质,如体积效应、表面与界面效应、量子尺寸效应、宏观量子隧道效应、特殊的光吸收特性、电化学性质等,因而使纳米材料可广泛应用于高力学性能环境、光热吸收、非线性光学、磁记录、特殊导体、分子筛、超微复合材料、催化剂、热交换材料等领域 [5] 。
林产工业中纳米技术的研发对经济地、可持续地生产新材料和发展以生物质为基础的经济甚为重要 [6] 。木材本身就是一种天然的复合材料,其成分包括纤维素、半纤维素及木质素。同时,木材也是由纳米纤维、微纤维、管胞、导管分子及薄壁组织细胞组成的复合材料 [7] 。尽管现在有许多合成聚合物可用来制备纳米复合材料,但是它们的可处理性、生物相容性、生物降解性与天然聚合物相比还有很大的局限性。纤维素是世界上最丰富的可生物降解、可再生的天然高分子材料,植物每年通过光合作用,能生产出亿万吨的纤维素。天然纤维素主要从树木、草、农作物、芦苇等植物中提取,植物的主要结构物质是纤维素,其约占木材的40%~50%,亚麻中占80%,而在棉花中高达90%以上。一些细菌和动物细胞壁以及绿色藻类中也含有纤维素链 [8] 。在纳米尺度范围内操控纤维素分子自组装和多功能化,可制备出具有优异性能的纳米纤维素晶体 [9] ,如较大的比表面积、高强度、高结晶度、超精细结构等。这些特殊性能可以明显改善现有木质复合材料的电学、光学、磁力学、绝缘性甚至超导性,并可减少对材料和能源的消耗,实现林产工业的可持续性 [10] 。目前纳米纤维素晶体的研究开发以及利用仍处于初级阶段,对其物理化学结构、作用机制及形成机理的研究,可为研发高效、易控制、无污染的纳米纤维素晶体制备方法,以及纳米纤维素晶体的有效利用提供理论基础与科学依据。
2. 纳米纤维素的制备
天然纤维素在结构上可以分为晶体区(Crystalline regions)和无定形区(Amorphous regions),这些晶体和无定形的纤维素依靠其分子内和分子外的氢键以及弱作用力的范德华力维持着大分子结构。利用酸水解可以在一定的条件下选择性地降解掉无定形区,将天然纤维素通过控制前处理、解链及机械作用等过程,使其β-1,4-D-葡萄糖苷键断裂,控制好水解条件,可以得到纳米级纤维素晶体。
纤维素大分子中的β-1,4-D-葡萄糖苷键是一种缩醛键,对酸特别敏感,在适当的氢离子浓度、温度和时间作用下,发生酸水解反应,糖苷键断裂,降解掉纤维素无定形区,留下纤维素晶体,原理如图1所示。Nickerson和Habrle [11] 在1947年就用HCl和H2SO4混合酸水解纤维素原料分离得到纳米纤维素晶体。Ranby [12] 在1952年用硫酸水解微原纤制得纳米纤维素晶须。Bondeson等 [13] 在2006年优化了硫酸水解挪威云杉制备纳米微晶纤维素的条件。
2.1. 实验材料、试剂及主要设备
原材料:沙柳(产自内蒙古自治区鄂尔多斯市),用植物粉碎机将其制成木粉。试剂:硝酸、95%乙醇(分析纯)、98%浓硫酸、30%过氧化氢、氢氧化钠固体粉末。
主要设备:TENSOR 27型红外光谱分析仪(德国布鲁克光谱仪器公司)、BK300生物显微镜(重庆奥特光学仪器有限责任公司)、NETZCH STA409PC热分析仪(德国耐驰公司)、XRD-6000衍射仪(日本岛津公司)。
2.2. 沙柳纤维素的制备
将实验所用沙柳原料切割成平均长度25 mm左右的小段,然后放在鼓风恒温干燥箱中,在95℃的条件下干燥24小时,利用粉碎机将条状沙柳制成木粉,过40目筛,装入样品袋中保存待用。
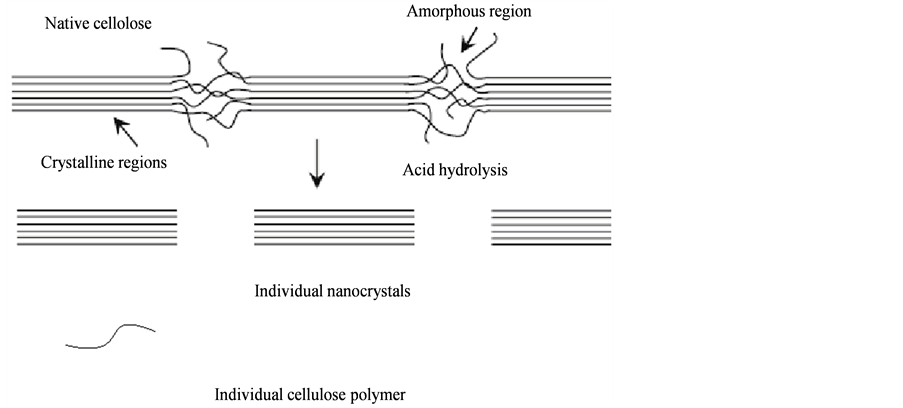
Figure 1. Nanocellulose crystal separated by acid hydrolysis method
图1. 酸水解纤维素分离纳米纤维素晶体
① 硝酸–乙醇混合液的制备:量取800 ml乙醇(95%)于干的1000 ml烧杯中。徐徐分次加入200 mL硝酸(密度1.42 g/cm3),每次加入少量(约10 ml)并用玻璃棒搅匀后始可续加。待全部硝酸加入乙醇后,再用玻璃棒充分和匀,贮于棕色试剂瓶中备用。
② 称取1.0 g 40目的木粉于250 mL洁净干燥的锥形瓶中,加入25 mL硝酸–乙醇混合液、装上回流冷凝器,放在沸水浴上加热1 h。
③ 移去冷凝管,将锥形瓶自水浴上取下、静置片刻。待残渣沉积瓶底后,用倾泻法滤经已恒重的1G2玻璃滤器,尽量不使试样流出。用真空泵将滤器中的滤液吸干,再用玻璃棒将流人滤器的残渣移入锥形瓶中。量取25 mL硝酸–乙醇混合液,分数次将滤器及锥形瓶口附着的残渣移人瓶中。装上回流冷凝器,在沸水浴中加热1 h。如此重复数次,直至纤维变白为止。
④ 最后将锥形瓶内容物全部移入滤器,用10 mL硝酸-乙醇混合液洗涤残渣,再用热水洗涤至洗涤液用甲基橙试之不呈酸性反应为止。最后用乙醇洗涤两次。吸干洗液。将滤器移入烘箱,于(105 ± 2)℃烘干至恒重置于干燥器备用。纤维素烘干后收集装入样品袋中待用。
2.3. 沙柳纤维制备纳米纤维素
准确量取1.0 g沙柳纤维素置于1000 ml的烧杯中,加入20 ml 35%、40%、45%、50% H2SO4,在50℃水浴锅中搅拌处理40 min,离心洗涤至中性,取出产物。用30% H2O2在45℃温水浴中漂白纯化10 h,用NaOH固体将溶液PH调至11,反应结束后离心洗涤至中性,然后进行过滤、离心分离、真空冷冻干燥、50℃真空干燥箱干燥后得到絮状纳米纤维素固体,最后研磨成粉末。
3. 纳米纤维素的结构检测
硫酸水解法制得的纳米纤维素的形态如图2所示。
其中图2(a)是由1.5 g硝酸乙醇法制得纤维素与50%硫酸水溶液配置的悬浮液(溶液浓度约为7.6‰),图2(b)是所制得的纳米纤维素用研钵研磨后的宏观形貌图。
3.1. 光学显微镜观察
光学显微镜测试方法:1) 观察硝酸–乙醇法制得的沙柳纤维时,直接将沙柳纤维素至于载玻片上(铺成薄薄一层),盖上盖玻片,用金属夹固定标本,调节显微镜焦距及光强,找到清晰的视野即可。2) 观察水解法所得纳米纤维素时,滴一滴纳米纤维素悬浮液于载玻片上,盖上盖玻片,用金属夹夹紧,调节显微镜焦距、光强及放大倍数,找到清晰视野即可。
一定放大倍数的显微镜可以初步观察比较木质纤维的形貌、长度以及纤维的分散程度。基于这一原理,分别采用物镜放大倍数为40×和100×的显微镜观察经硫酸水解前后纤维素的长度及分散程度的变化,得图3。对比图3(a)与图3(b)可以看出,水解前沙柳纤维未分散。图3(a)中所观察到的长条状纤维簇实际是由多条单根纤维彼此通过分子内和分子间的氢键以及弱作用力范德华力维持着的大分子结构。经质量分数为50%的硫酸水解后,得到的纳米纤维素显微观察见图3(b),沙柳纤维素的长度明显变短,这是由于强酸的水解作用使得纤维素中糖苷键断裂、无定形区降解,纤维素长链分子也因此被打断。纤维素不再是簇状,而是分散成了许多丝状物质(图3(b))。
3.2. SEM观察
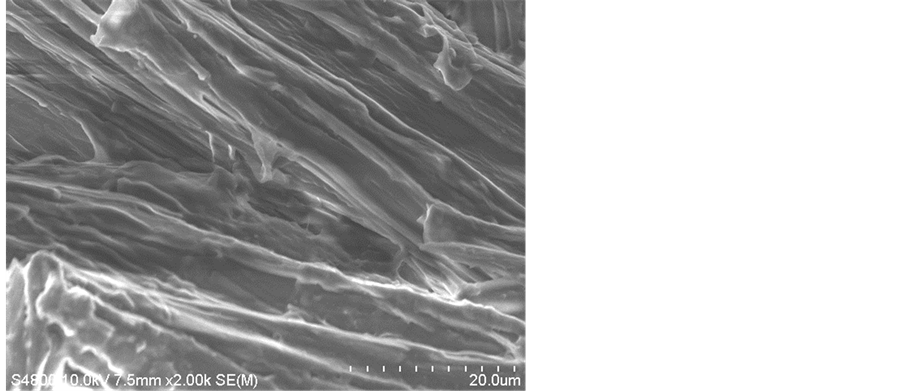
将硫酸浓度分别为35%、40%、45%、50%条件下制备的纳米纤维素粉末取适量样品粘在专用的铝板上,用扫描的就对样品进行测定,测定结果如图4所示。

 (a)(b)
(a)(b)
Figure 2. Macrostructure of nanocellulose
图2. 纳米纤维素的宏观形貌

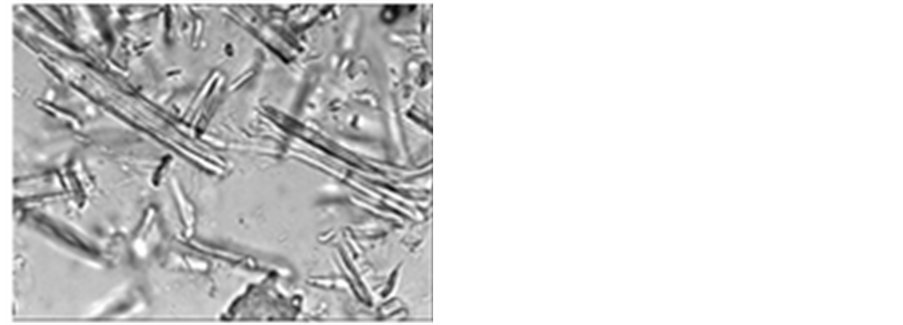 (a) 水解前沙柳纤维显微镜观察(40×) (b) 水解后沙柳纤维素显微镜观察(100×)
(a) 水解前沙柳纤维显微镜观察(40×) (b) 水解后沙柳纤维素显微镜观察(100×)
Figure 3. Observation of microscope of Salix mongolica cellulose before and after hydrolyzed by H2SO4
图3. 硫酸水解前后沙柳纤维素的显微镜观察
 (a) 35% H2SO4
(a) 35% H2SO4
 (b) 40% H2SO4
(b) 40% H2SO4
 (c) 45% H2SO4
(c) 45% H2SO4 (d) 50% H2SO4
(d) 50% H2SO4
Figure 4. SEM patterns of Salix NCC in different concentration of H2SO4
图4. 不同硫酸浓度制得的沙柳纳米纤维素SEM图片
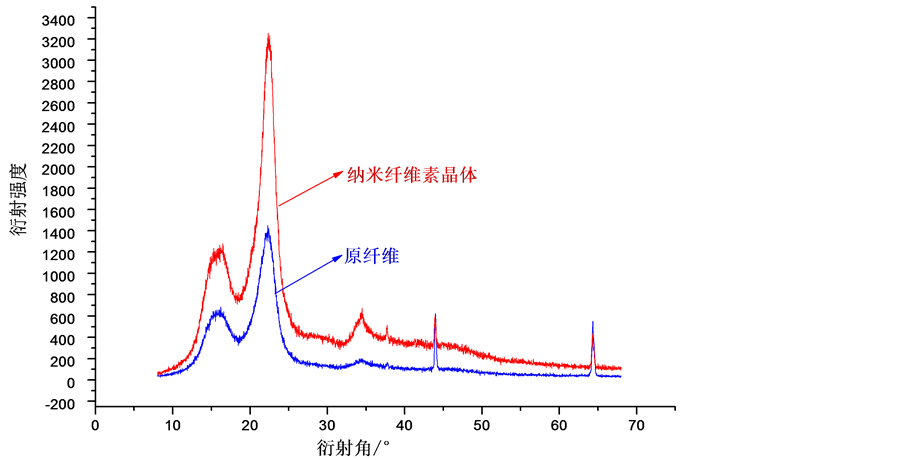
Figure 5. XRD patterns of salix cellulose and NCC
图5. 原纤维和纳米纤维素晶体的XRD曲线图谱
3.3. XRD测试分析
样品制成粉末压片安放在样品架上,在稳定条件下分析。测试条件为Cu靶、40 Kv、30.0 mA下2θ连续扫描,扫描范围8˚~68˚,扫描速度2˚/min,步长0.02˚。得到原纤维和纳米纤维素的XRD谱图见图5。
3.4. FTIR分析
将沙柳纤维和纳米纤维素晶体分别制成溴化钾压片,用红外光谱对样品进行表征,结果如图6所示。
3.5. TG分析
原纤维与纳米纤维素晶体在N2气氛中进行热重测试,系统的升温速率为10℃/min,N2气氛流量为30 ml/min,所得结果见图7。
4. 结果讨论
样品催化水解后再经离心洗涤至中性,可直接得到具有一定浓度的稳定的纳米纤维素悬浮液(如图2(a)),这是因为硫酸酯化纤维素表面羟基从而使纳米纤维素表面带有大量负电荷 [14] 。因此,由于静电排斥力的作用而形成一个稳定的纳米纤维素悬浮液体系。
由图3中(a)图、(b)图,可以清楚观察到沙柳纤维彼此间已经分离开,纤维周围的胶质已经消失,纤维变得比较光滑。说明经强酸水解,不仅能够溶解纤维间的果胶、单宁、无机物等物质,还对纤维化学成分产生作用。
由图4的SEM照片可以看到,经硫酸水解后,在超微构造上,纤维素尽管没有实现单分子链分离,但其线性组合结构明显,具有明显的结晶片层结构(图4(b)),其层片已经到达纳米级。
由图5观察到纳米纤维素晶体与原沙柳纤维衍射峰位置基本保持一致。图中三个最强峰分别位于14.6˚、16.6˚和22.5˚,分别对应于纤维素晶体的{101}、{10 }、{002}面,因此认为硫酸水解法制备的纳
}、{002}面,因此认为硫酸水解法制备的纳
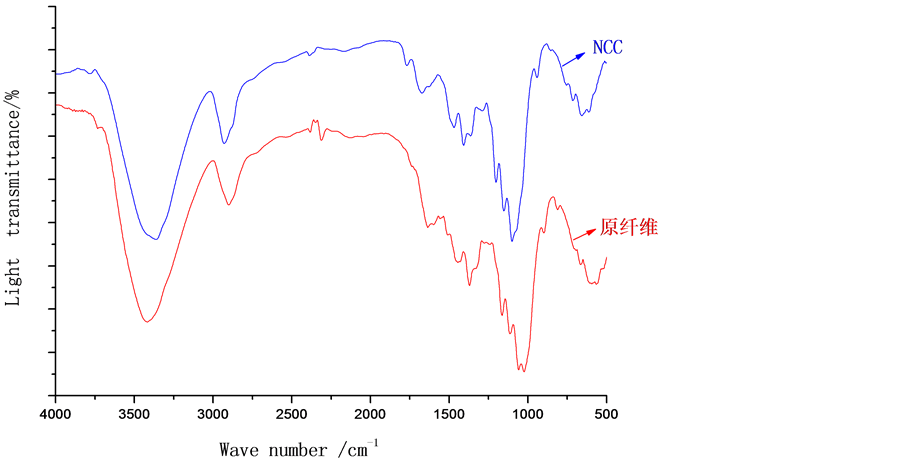
Figure 6. Infrared absorption spectrum of salix cellulose and Nanocellulose crystal
图6. 沙柳纤维素和纳米纤维素晶体(NCC)的傅立叶红外吸收光谱谱图

Figure 7. Thermal decomposition curves of salix cellulose and NCC
图7. 原纤维和NCC的TG热解曲线
米纤维素晶体仍属于纤维素I型 [14] ,其特征峰比原纤维尖锐,结晶度较高。由图5可以算出,原纤维的结晶度为71.4%,而硫酸水解得到的纳米纤维素晶体的结晶度提高为77.3%。这是由于在酸水解过程中,氢离子可以进入到纤维素非晶区,加速糖苷键的水解分裂,最终残留下纤维素晶体 [15] 。纤维素的无定形区的可及性和反应活性比结晶区的大,在进行水解反应时,无定形区的纤维素全部参加反应而降解,而结晶区的纤维素只有晶体表面参与反应,因此与原纤维素相比,纳米纤维素晶体的结晶度就有较大程度的提高。纳米化后,衍射峰强度明显增强,说明纤维素分子链的结晶区内部及表面的羟基间形成了氢键,结合更紧密。
根据图6特征基团的振动频率可以看出,在3350~3450 cm−1的频率范围内存在一个较强的吸收峰是-OH的伸缩振动 [16] - [18] ,其波数为3410 cm−1;2800~2900 cm−1的频率范围内出现一个次强的吸收峰为-C-H的伸缩振动区,其波数为2830 cm−1;另一个较强的吸收峰为1060 cm−1,对应于纤维素醇的-C-O伸缩振动;根据东北林业大学李坚教授的《木材波谱学》分析得出 [19] ,在1100波数范围附近有许多较弱的肩峰,对应于纤维素分子内醚-C-O的伸缩振动;在1430 cm−1范围附近有饱和-C-H的弯曲振动峰,1700 cm−1范围附近出现吸收峰为C=O的伸缩振动引起的,897 cm−1为β-糖苷键振动(碳水化合物特征峰)。综上所述,硫酸水解法制备的纳米纤维素与原沙柳纤维相比,谱图上的特征峰并没有明显的变化,说明NCC仍具有原沙柳纤维素一样的化学成分。另一方面也说明,NCC表现出的特殊性能是由于其纳米尺寸效应引起而非化学成分改变。
从图7 NCC的起始降解温度、最大降解速率温度和终止降解温度分别为211.31℃、297.11℃、352.01℃,远低于原纤维的各个降解温度283.47℃、345.87℃、368.77℃。其原因主要有以下两点:首先沙柳纤维通过硫酸水解得到NCC后,粒径减小,比表面积增加,因此表面上的末端碳和外露的反应活性基团数量显著增加,导致其热稳定性降低;其次,在水解过程中,必然会导致大量的纤维素链段被破坏和断裂,这样使得NCC的表面存在着许多低分子量的的链段和许多纤维素分子链的断裂点,加之排列不紧凑和不规整,形成许多缺陷点,在较低的温度下NCC表面的这些低分子链段和缺陷点由于分子间作用力小、键合强度低,首先吸热并逐步分解 [20] 。在质量变化率方面,由于纤维素中的非晶部分被去除,晶体部分的热稳定性好,因此热解后,NCC残余部分多于原纤维残余。
5. 结论
1) 硝酸–乙醇法可以获得适合进一步处理的纤维素;硫酸水解沙柳纤维可以制备出粒径在100 nm以内的纳米纤维素晶体。
2) 硫酸打断纤维素长链分子,因而所得纳米纤维素长度较原纤维变短;纤维素不再是簇状,而是分散成了许多丝状纤维。
3) 纳米纤维素晶体主要呈短棒状,还有一些呈不规则形状。并且由于硫酸水解法所得NCC表面羟基多、比表面积大、分子间氢键作用力大,在干燥过程中易团聚。
4) 硫酸水解处理后得到的纳米纤维素晶体仍为纤维素I型,其结晶结构属于单斜晶系,结晶度由原纤维的71.4%提高为77.3%。
5) 硫酸处理所得纳米纤维素晶体的粒径减小、反应活性基团增多、分子链断裂、缺陷增多从而使得NCC降解温度远低于原纤维的降解温度。
6) 硫酸水解法制备出的纳米纤维素晶体的化学成分与原纤维基本相同,说明NCC表现出的特殊性能是由于其纳米尺寸效应引起而非化学成分改变。
基金项目
国家自然基金资助项目(31260157)。
文章引用
薛振华,尚琪冬. 沙柳纤维素纳米化及其结构测定
Nanostructures of Salix mongolica Cellulose and Structure Determination[J]. 植物学研究, 2016, 05(03): 83-92. http://dx.doi.org/10.12677/BR.2016.53012
参考文献 (References)
- 1. 冯利群, 高晓霞, 王喜明. 沙柳木材显微构造及其化学成份分析[J]. 内蒙古林学院学报(自然科学版), 1996, 18(1): 38-42.
- 2. Wegner, T.H. and Jones, P.E. (2006) Advancing Cellulose-Based Nanotechnology. Cellulose, 13, 115-118. http://dx.doi.org/10.1007/s10570-006-9056-1
- 3. Gardner, D.J., Oporto, G.S., Mills, R. and Samird, M.A.S.A. (2008) Adhesion and Surface Issues in Cellulose and Nanocellulose. Journal of Adhesion Science and Technology, 22, 545-567. http://dx.doi.org/10.1163/156856108X295509
- 4. Sargent, J.F. (2008) The National Nanotechnology Initiative: Overview, Reauthorization, and Appropriations Issues. US:CRS Report R L 34401.
- 5. 代平祥. 浅谈纳米材料的应用[J]. 大众科技, 2006, 94(8): 26,37.
- 6. Iversen, T., Larsson, T., Lindström, M., et al. (2005) Nanoforest: A Nanotechnology Roadmap for the Forest Products Industry. STFI-Packforsk, No.48, Stockholm.
- 7. 唐丽荣. 纳米纤维素晶体的制备、表征及应用研究[D]: [硕士学位论文]. 福州: 福建农林大学, 2010.
- 8. Chakraborty, A., Sain, M. and Kortschot, M. (2005) Cellulose Microfibrils: A Novel Method of Preparation Using High Shear Refining and Cryocrushing. Holzforschung, 59, 102-107. http://dx.doi.org/10.1515/HF.2005.016
- 9. 叶代勇. 纳米纤维素的制备[J]. 化学进展, 2007(10): 1568-1575.
- 10. Gogotsi, Y. (2006) Nanotubes and Nanofibers. CRC Press, Boca Raton. http://dx.doi.org/10.1201/9781420009385
- 11. Nickerson, R.F. and Habrle, J.A. (1947) Cellulose Intercrystalline Structure. Industrial & Engineering Chemistry Research, 39, 1507-1512. http://dx.doi.org/10.1021/ie50455a024
- 12. Ranby, B.G. (1952) The Cellulose Micelles. Tappi, 35, 53-58.
- 13. Bondeson, D., Mathew, A. and Oksman, K. Optimization of the Isolation of Nanocrystals from Micro-crystalline Cellulose by Acid Hydrolysis. Cellulose, 13, 171-180. http://dx.doi.org/10.1007/s10570-006-9061-4
- 14. 杨洁, 叶代勇. 纳米纤维素晶须表面接枝及其液晶性能研究进展[J]. 化工进展, 2012(9): 1990-1997.
- 15. Bodin, A., Backdahl, H., Risberg, B., et al. (2007) Nano Cellulose as a Scaffold for Tissue Engineered Blood Vessels. Tissue Engineering, 13, 885-885.
- 16. 蒋玲玲, 陈小泉. 纳米纤维素晶体的研究现状[J]. 纤维素科学与技术, 2008(2): 73-78.
- 17. 李金玲, 周刘佳, 叶代勇. 硫酸铜助催化制备纳米纤维素晶须[J]. 精细化工, 2009, 26 (9): 844-849.
- 18. 高洁, 汤烈贵. 纤维素科学[M]. 北京: 科学出版社, 1996: 50-58.
- 19. 李坚. 木材波谱学[M]. 哈尔滨: 东北林业大学出版社, 2003: 104-116.
- 20. 黄涛, 蒋建敏, 王金丽, 等. 菠萝叶纤维结构及热力学性能研究[J]. 上海纺织科技, 2009, 37(10): 9-12.
*通讯作者。