Material Sciences
Vol.06 No.03(2016), Article ID:17588,7
pages
10.12677/MS.2016.63019
The Performance of Zn Doped TiO2 Films in Photo-Electrochemical Water Splitting
Wei Yang, Xiaohong Xia, Yun Gao*
Faculty of Materials Science and Engineering, Hubei University, Wuhan Hubei

Received: Apr. 25th, 2016; accepted: May 16th, 2016; published: May 20th, 2016
Copyright © 2016 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
In this work, we prepared Zn-doped TiO2 thin films by magnetron co-sputtering, using Ti metal and ZnO ceramic as targets, and high-purity Ar and O2 as working gases, respectively, followed by rapid thermal annealing at 600˚C. It was found that Zn dopants induce a little red shift of TiO2 films band gaps. The carrier densities decreased in the beginning, and then improved with the Zn element concentration increasing. Zn dopant also caused negative shifts of both the flat band potential and the onset potential of redox reaction of films in the light. The results showed that saturated photocurrent density of Zn-doped TiO2 films at 3.5% Zn concentration is 2.1 times as that of un-doped ones, indicating the best water splitting performance.
Keywords:Zn-Doped TiO2 Thin Films, Water Splitting, Rapid Thermal Annealing, Magnetron Sputtering

Zn掺杂的TiO2薄膜的光分解水性能的研究
阳溦,夏晓红,高云*
湖北大学材料科学与工程学院,湖北 武汉

收稿日期:2016年4月25日;录用日期:2016年5月16日;发布日期:2016年5月20日

摘 要
本文采用磁控溅射的方法,以金属Ti和ZnO陶瓷为靶材,Ar和O2混合气为工作气体,进行双靶共溅,对沉积的薄膜进行600℃快速退火处理以得到Zn-TiO2薄膜。结果表明,Zn掺杂TiO2引起带隙少量红移。随Zn掺杂元素的含量的增加,Zn-TiO2薄膜的载流子浓度先减小后增加。Zn掺杂引起薄膜的平带电压和光照下薄膜氧化还原反应起始电位值均向负方向移动。Zn掺杂浓度为3.5%时,薄膜光饱和电流密度是不掺杂样品的2.1倍,光分解水性能最佳。
关键词 :Zn-TiO2薄膜,光分解水,快速退火,磁控溅射

1. 引言
光电化学光分解水是一种将太阳能转化为可储存的清洁能源——氢能的方法 [1] - [3] 。TiO2由于其具备合适的带隙条件、优越的化学稳定性、良好的抗光腐蚀性以及低廉的价格等优点,被广泛用作光电化学分解水领域的光阳极材料 [4] [5] 。历史上最早利用半导体电极实现光电化学分解水产生氢气和氧气的日本学者Fujishima和Honda,采用的即为TiO2单晶电极 [6] 。然而,由于TiO2的带隙太宽(Anatase: 3.2 eV, Rutile: 3.0 eV),使得其对太阳光的吸收仅局限在紫外光区,对太阳光能的利用率小于5% [7] 。为提升TiO2在紫外和可见光区的吸收,主要有两条途径:1) 引入光吸收材料如敏化剂、量子点、染料等;2) 通过掺杂以调节能带结构,使带隙变窄 [4] [5] 。
关于TiO2的掺杂研究分金属掺杂和非金属掺杂,其中非金属掺杂(如C、N、S等)通常只是通过提升TiO2的价带边或者与价带中的O2p轨道混合(如N2p)来使得TiO2带隙变窄,而不会在TiO2的带隙中引入新的能级。而金属掺杂又分贵金属掺杂(如Pt)和过渡元素掺杂,其中过渡元素(如Fe,Cr,Co,V等)的掺杂由于能有效增强TiO2的光活性而得到广泛研究。目前过渡元素Zn掺杂的TiO2主要研究集中在太阳能电池光阳极材料和光催化降解有机物(如甲基橙)等方面的应用,在光分解水方面的研究较少。邵 [8] 等人通过理论计算表明,Zn掺入TiO2后会成为浅受主杂质,为p型掺杂。Rachel A. Caruso [9] 等人采用液相模板法制备了多孔的Zn-TiO2纳米材料,且表明一定范围内的Zn的引入可使光电流密度和载流子浓度增大,这会使光分解水产氢的能力增强 [4] [9] 。
本研究采用工业上常用的磁控溅射的方法制备薄膜,对刚沉积的薄膜进行600℃快速退火处理以得到Zn-TiO2薄膜。重点探究不同Zn掺杂含量的材料的微结构变化和光吸收性质,以及对光解水性能的影响,以得到具备优异的光电化学分解水性能的Zn-TiO2薄膜。
2. 实验
采用中科院沈阳科学仪器制造厂的高真空磁控溅射系统,以金属Ti靶(直流电源激发)和ZnO陶瓷(射频电源激发,13.56 MHz)为靶材进行双靶共溅制备Zn掺杂氧化钛薄膜。衬底采用石英玻璃和FTO,经丙酮、无水乙醇、去离子水依次超声清洗20 min后放入沉积腔内。沉积过程中Ar和O2流量分别为20 sccm和3 sccm,本底真空度为4 × 10−4 Pa,沉积气压为0.5 Pa,沉积时间2 h。通过分别调节两个靶的直流和射频激发功率以及ZnO靶材上包裹金属Ti片的面积比使Zn/Ti原子比例控制在0%~8%之间。沉积过程中样品保持自转以得到均匀薄膜。将沉积的薄膜采用BEIJING EASTATAR LABS公司的RTP-500 RAPID THERMAL PROCESSOR型快速退火炉进行600℃快速退火处理,最终得到Zn-TiO2薄膜。
对样品进行微结构分析,采用英国雷尼绍公司的Renishaw invia型共聚焦显微拉曼光谱仪研究薄膜物相,其中激发光源为空气制冷氩离子激光器(Spectra-Physics Model 163-C4260),激发波长532 nm,扫描范围100~800 cm−1。采用日本电子(JEOL)的JSM 7100F型场发射扫描电镜测定薄膜中Zn的元素含量以及表面微观形貌。采用CHI600E电化学工作站,三电极测试系统,并辅以上海蓝晟电子有限公司的XQ350W可调型氙灯作为光源,测试样品的光电化学性能。采用日本岛津UV3600紫外可见分光光度计测试薄膜的光吸收性能。
3. 结果与讨论
3.1. Zn元素掺杂含量的测定
对石英衬底上制备的薄膜样品在扫描电镜中进行EDS分析,如表1所示,结果表明样品主要含有Zn、Ti、O、Si等元素,其中Si元素来源于玻璃衬底,O元素来源于玻璃衬底以及沉积的氧化物薄膜。对测得的Zn-TiO2样品的Zn和Ti的质量比进行换算,得掺杂样品的Zn/Ti原子比例分别为1.76%,3.5%,5.54%,8%。
3.2. Raman光谱分析
用532 nm激光波长对FTO玻璃上制备的薄膜进行Raman测试,如图1所示。结果表明,掺Zn含量为0%~8%范围内的Zn-TiO2薄膜,其Raman图谱都在145 cm−1、398 cm−1、512 cm−1、637 cm−1位置处出现峰位,分别对应于anatase相的Eg、B1g、A1g、Eg拉曼模 [10] ,因此薄膜均为TiO2的anatase相。0%,1.76%,3.5%,5.54%,8%组薄膜位于145 cm−1最强拉曼峰的半高宽依次为15.19 cm−1,13.04 cm−1,12.24 cm−1,14.03 cm−1,19.91 cm−1,故随着掺杂浓度增加,拉曼光谱半高宽值先减少后增加,3.5%掺杂样品对应于最小半高宽值。半高宽增加意味着晶体中晶格无序态的增加。当掺杂浓度高于3.5%时,晶体结晶质量下降,相应缺陷态浓度增加。
3.3. 光吸收谱分析
图2为FTO玻璃衬底上制备的Zn-TiO2薄膜的光吸收图谱。由图可知,掺Zn元素后,TiO2样品的光学带隙随着Zn元素浓度从0%,1.76%,3.5%,5.54%,8%的逐渐上升,带隙值依次为3.56 eV、3.51 eV、3.53 eV、3.54 eV、3.51 eV。可以看出,Zn掺杂仅引起光吸收带边少量红移,因此可以保持TiO2材料的良好的可见光透光性。这与邵的理论计算结果指出了Zn掺杂仅引起带隙微量变化相一致 [8] 。
3.4. 光电化学分析
采用CHI600E电化学工作站,以Pt丝为对电极,饱和甘汞电极(SCE)为参比电极,FTO玻璃上制备的TiO2薄膜为工作电极,1M KOH水溶液为电解质,组成三电极测试体系。用上海蓝晟电子有限公司的XQ350W可调型氙灯作为光源,光强通过调节输出电流值为7.7 A来控制。用Linear Sweep Voltammetry模式测量薄膜的电流密度随电压的变化,扫描速度为0.1 V/s,用Amperometric i-t Curve 模式测量薄膜的电流密度在光照条件和黑暗条件下的变化,用Impedance-Potential模式测量薄膜在黑暗条件下的Mott- Schottky曲线,结果如图3所示。
图3(a)表明,黑暗条件下,在−1 V~+0.8 V vs SCE范围内的低电压(<+0.5 V)时,不同Zn含量(Zn/Ti = 0%~8 at.%)的TiO2薄膜的电流密度都很低,几乎可忽略;直到电压升至+0.5 V,电流密度才开始显著增大,这是由于较高的电压下Zn-TiO2薄膜与电解质界面处的电荷运输效果更好 [11] 。在光照条件下,不同Zn掺杂浓度样品光电流随电压变化的趋势一致,都表现为先增加后趋向饱和,然后显著增大。不掺杂的

Figure 1. Raman spectrum of Zn-TiO2 films at different Zn concentrations (Zn/Ti = 0% - 8 at.%)
图1. 不同Zn含量(Zn/Ti = 0%~8 at.%)的TiO2薄膜的Raman图谱

Figure 2. Optical absorption spectrum of Zn-TiO2 films at different Zn concentrations
图2. 不同Zn含量的TiO2薄膜样品的光吸收图谱

 (a) (b)
(a) (b)
 (c)(d)
(c)(d)
Figure 3. (a) Current density-potential plots on the light and dark; (b) photocurrent densities at +0.179 V vs SCE (1.23 V vs RHE); (c) current density-time plots on the light and dark; (d) Mott-Schottky plots on the dark of Zn-TiO2 films at different Zn concentrations
图3. 不同Zn含量的TiO2 (Zn/Ti = 0%~8 at.%)薄膜的(a) 光照和黑暗条件下的电流密度J对电压V曲线;(b) 不同Zn含量的TiO2薄膜在+0.179 V vs SCE (即1.23 V vs RHE)电势下的光电流密度;(c) 光照和黑暗条件下的电流密度J-时间t曲线;(d) 黑暗条件下的Mott-Schottky曲线
Table 1. EDS contents of Zn-TiO2 films at different Zn concentrations
表1. 不同Zn掺杂量的TiO2薄膜的EDS含量值
TiO2薄膜的光饱和电流对应的电压值为−0.38 V vs SCE,Zn掺杂样品达到光饱和电流对应的电压值均为−0.51 V vs SCE,相对不掺杂样品向负值方向移动−0.13 V。这一结果表明Zn掺杂TiO2样品的界面载流子的分离和输运比纯TiO2的效果更好 [4] 。表2给出了图3(a)的各样品氧化还原反应起始电位值(onset potential)。结果表明,Zn元素的掺入使得起始电位值向负值方向移动。
1M KOH水溶液中,在相对可逆氢标准电极(RHE)电压为1.23 V位置对应于溶液中的氢产生热动力学势能。由于E (RHE) = E (SCE) + 1.051 V [12] ,故1.23 V vs RHE即0.179 V vs SCE下,随Zn含量按0%,1.76%,3.5%,5.54%,8%的增加,光饱和电流密度依次为0.255 mA/cm2,0.162 mA/cm2,0.536 mA/cm2,0.355 mA/cm2,0.221 mA/cm2,如图3(b)所示。由于光电流密度正比于光分解水产生氢气和氧气的能力 [13] ,故3.5% Zn组样品的光分解水性能最佳,是没掺杂样品的2.1倍。
化学和结构稳定性是探索材料是否能够应用于电化学分解水产氢的一个重要的因素。图3(c)给出了在外加偏压为−0.22 V vs SCE条件下几个不同Zn掺杂样品的光电流随时间的依赖关系曲线。测试结果表明,掺Zn量3.5%组样品的光电流密度最大;而且经过模拟太阳光开和关的多次循环若干个循环后,光电流密度保持一致可重复,无衰减迹象,说明薄膜的化学和结构稳定性好 [14] 。此外,矩形光电流瞬态谱形状说明样品具有极低的电子反向复合几率,光阳极产氢过程重复性好。
图3(d)的Mott-Schottky曲线斜率为正值,表明薄膜为n型 [4] 。薄膜中施主载流子浓度Nd和平带电压VFB可以通过Mott-Schottky公式(1)得到。
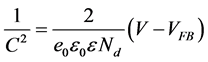 (1)
(1)
其中,TiO2的相对介电常数ε取值170 [4] [5] ,e0为元电荷电量,ε0为真空介电常数,V为外加电压,C为测量电容值。计算结果如表3所示。
可以看到,样品的载流子浓度都在1019量级。随Zn含量增加,载流子浓度先减少后增加,在3.5%处达到最低为1.171 × 1019 cm−3。Zn在氧化钛中有两种可能的作用。1) 根据邵的理论计算,Zn掺杂在TiO2中引起p型掺杂。由于TiO2中本征氧空位Vo2−的存在导致TiO2表现为n型,Zn掺杂首先补偿了TiO2中的施主掺杂,引起载流子浓度的下降。2) Zn离子的存在可以将Ti4+还原成Ti3+和氧空位,引起氧空位的增加。因此,随着Zn掺杂浓度进一步增加,由于Zn的还原竞争超过了掺杂效应,导致载流子浓度再次上升。通过Mott-Schottky曲线的分析可以发现Zn元素的引入引起平带电压都向负值方向移动。通常认为平带电压向负值移动意味着薄膜的费米能级靠近导带方向移动 [9] [11] 。根据实验结果,掺杂引起载流子浓度降低,这应该引起费米能级远离导带。因此这个平带电压向负值方向移动应该是氧化层界面存在固定Zn2+、Ti3+正电荷引起的。Zn掺杂引起平带电压的移动与图3(a)中光照下氧化还原反应起始电位值向负值方向移动相一致。
Table 2. Onset potentials of J-V plots of Zn-TiO2 films at different Zn concentrations
表2. 不同Zn含量的TiO2薄膜J-V曲线计算所得起始电位
Table 3. Carrier densities and flat band potentials calculated from Mott-Schottky plots
表3. 由Mott-Schottky曲线计算得到的载流子浓度和平带电压值
4. 结论
本研究采用双靶磁控共溅并经快速退火处理的方法制备Zn掺杂的TiO2薄膜,重点探究了不同Zn掺杂含量对光分解水性能的影响,研究结果表明,600℃快速退火得到的Zn-TiO2薄膜均为anatase型。Zn掺杂TiO2引起吸收带边的少量红移。电化学测试表明,Zn掺杂TiO2薄膜均为n型导电。随着Zn掺杂浓度的增加,薄膜中载流子浓度先减少后增加。在Zn/Ti = 0~8 at.%范围内,光饱和电流密度随Zn含量增加呈现先增加后减小的趋势,且在掺杂浓度为3.5%处达到最大值0.536 mA/cm2,是不掺杂样品的2.1倍,相应光电化学分解水性能最好。另外,Zn掺杂引起平带电压和光照下氧化还原反应起始电位值均向负值方向移动,可能原因是氧化薄膜中固定正电荷积累引起。
致谢
国家自然科学基金(批准号:11374091,11274100),国家教育部基金(批准号:211108,20134208110005)。
文章引用
阳 溦,夏晓红,高 云. Zn掺杂的TiO2薄膜的光分解水性能的研究
The Performance of Zn Doped TiO2 Films in Photo-Electrochemical Water Splitting[J]. 材料科学, 2016, 06(03): 149-155. http://dx.doi.org/10.12677/MS.2016.63019
参考文献 (References)
- 1. Hill, J.C., Landers, A.T. and Switzer, J.A. (2015) An Electrodeposited Inhomogeneous Metal-Insulator-Semiconductor Junction for Efficient Photoelectrochemical Water Oxidation. Nature Materials, 14, 1150-1155. http://dx.doi.org/10.1038/nmat4408
- 2. Kang, D., Kim, T.W., Kubota, S.R., Cardiel, A.C., Cha, H.G. and Choi, K.S. (2015) Electrochemical Synthesis of Photoelectrodes and Catalysts for Use in Solar Water Splitting. Chemical Reviews, 115, 12839-12887. http://dx.doi.org/10.1021/acs.chemrev.5b00498
- 3. Katsuya, I., Akihide, I., Hau, N.Y., Rosel, A. and Akihiko, K. (2015) Z-Schematic Water Splitting into H2 and O2 Using Metal Sulfide as a Hydrogen-Evolving Photocatalyst and Reduced Graphene Oxide as a Solid-State Electron Mediator. Journal of the American Chemical Society, 137, 604-607. http://dx.doi.org/10.1021/ja511615s
- 4. Wang, G.M., Wang, H.Y., Ling, Y.C., Tang, Y.C., Yang, X.Y., Fitz-morris, R.C., Wang, C.C., Zhang, J.Z., and Li, Y. (2011) Hydrogen-Treated TiO2 Nanowire Arrays for Photoelectro-chemical Water Splitting. Nano Letters, 11, 3026- 3033. http://dx.doi.org/10.1021/nl201766h
- 5. Shin, S.W., Lee, J.Y., Ahn, K.S., Kang, S.H. and Kim, J.H. (2015) Visible Light Absorbing TiO2 Nanotube Arrays by Sulfur Treatment for Photoelectrochemical Water Splitting. The Journal of Physical Chemistry C, 119, 13375-13383. http://dx.doi.org/10.1021/acs.jpcc.5b01104
- 6. Fujishima, A. and Honda, K. (1972) Electrochemical Photolysis of Water at a Semiconductor Electrode. Nature, 238, 37-38. http://dx.doi.org/10.1038/238037a0
- 7. Hisatomi, T., Kubota, J. and Domen, K. (2014) Recent Advances in Semiconductors for Photocatalytic and Photoelectrochemical Water Splitting. Chemical Society Reviews, 43, 7520-7535. http://dx.doi.org/10.1039/C3CS60378D
- 8. Han, X.P. and Shao, G.S. (2013) Theoretical Prediction of p-Type Transparent Conductivity in Zn-Doped TiO2. Physical Chemistry Chemical Physics, 15, 9581-9589. http://dx.doi.org/10.1039/c3cp44031a
- 9. Huang, F.Z., Li, Q., Thorogood, G.J., Cheng, Y.B. and Caruso, R.A. (2012) Zn-doped TiO2 Electrodes in Dye-Sensi- tized Solar Cells for Enhanced Photocurrent. Journal of Materials Chemistry, 22, 17128-17132. http://dx.doi.org/10.1039/c2jm32409a
- 10. Liu, G., Yang, H.G., Wang, X.W., Cheng, L., Lu, H.F., Wang, L.Z., (Max) Lu, G.Q. and Cheng, H.M. (2009) Enhanced Photoactivity of Oxygen-Deficient Anatase TiO2 Sheets with Dominant {001}Facets. The Journal of Physical Chemistry C, 113, 21784-21788. http://dx.doi.org/10.1021/jp907749r
- 11. Wang, D., Zhang, X.T., Sun, P.P., Lu, S., Wang, L.L., Wang, C.H. and Liu, Y.C. (2014) Photoelectrochemical Water Splitting with Rutile TiO2 Nanowires Array: Synergistic Effect of Hy-drogen Treatment and Surface Modification with Anatase Nanoparticles. Electrochimica Acta, 130, 290-295. http://dx.doi.org/10.1016/j.electacta.2014.03.024
- 12. Liang, Y.Y., Li, Y.G., Wang, H.L., Zhou, J.G., Wang, J., Regier, T. and Dai, H.J. (2011) Co3O4 Nanocrystals on Graphene as a Synergistic Catalyst for Oxygen Reduction Re-action. Nature Materials, 10, 780-786. http://dx.doi.org/10.1038/nmat3087
- 13. Khan, S.U.M., Mofareh, A.S. and Ingler, W.B. (2002) Efficient Photo-chemical Water Splitting by a Chemically Modified n-TiO2. Science, 297, 2243. http://dx.doi.org/10.1126/science.1075035
- 14. Liu, J., Yu, X.L., Liu, Q.Y., Liu, R.J., Shang, X.K., Zhang, S.S., Li, W.H., Zheng, W.Q., Zhang, G.J., Cao, H.B. and Gue, Z.J. (2014) Surface-Phase Junctions of Branched TiO2 Nanorod Arrays for Efficient Photoelectrochemical Water Splitting. Applied Catalysis B: Environmental, 158-159, 296-300. http://dx.doi.org/10.1016/j.apcatb.2014.04.032
*通讯作者。
