Hans Journal of Biomedicine
Vol.
11
No.
01
(
2021
), Article ID:
40121
,
8
pages
10.12677/HJBM.2021.111004
POCT技术研究现状及临床应用
冯亚普,李丹杰,李燕虹,赵安琪,张丙霞,程杰*,崔景强*
河南驼人医疗器械研究院有限公司,河南省医用高分子材料技术与应用重点实验室,河南 长垣

收稿日期:2020年12月23日;录用日期:2021年1月6日;发布日期:2021年1月28日

摘要
POCT (Point of Care Testing)是一种在采样现场进行的、利用便携式分析仪器及配套试剂快速得到结果的检测方式,本文主要阐述了POCT (Point of Care Testing)的微流控芯片技术、传感器技术、干化学技术、免疫层析技术、生物芯片技术等主要检测技术,并介绍了其在临床上的广泛应用。
关键词
POCT,便携式检测技术,临床应用
Technologies Research Status and Clinical Applications of Point of Care Testing
Yapu Feng1, Danjie Li2, Yanhong Li, Anqi Zhao, Bingxia Zhang, Jie Cheng*, Jingqiang Cui*
Henan TuoRen Medical Device Research Institute Co. LTD., Key Laboratory of Medical Polymer Materials Technology and Applications in Henan, Changyuan Henan

Received: Dec. 23rd, 2020; accepted: Jan. 6th, 2021; published: Jan. 28th, 2021

ABSTRACT
POCT (Point of Care Testing) is defined as medical diagnostic testing that can be performed at the patient’s bedside. This paper mainly discussed various POCT (Point of Care Testing) devices developed by different technologies including microfluidics, sensor technology, dry reagent technology, immunochromatography, biochip technology. As healthcare becomes more consumer-focused, POCT (Point of Care Testing) is rapidly expanding worldwide and has been widely used in clinical.
Keywords:POCT, Portable Detection Technology, Clinical Application

Copyright © 2021 by author(s) and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY 4.0).
http://creativecommons.org/licenses/by/4.0/


1. 引言
POCT (Point of Care Testing)也称为即时检验或者床边检测,指在患者床前进行的利用便携式分析仪器以及配套试剂快速得到检测结果的一种检测方式 [1],是一种在不同临床环境下提供检测结果的快速手段,可排除标本运输等因素对结果的影响,即时检验是一种新型的检验方法且被临床广泛应用,使患者在有效的时间里进行治疗,优势有程序简洁、操作方便、时间短、精确度和灵敏度高等,同时互补传统诊断 [2]。
POCT仪的分类方法有两种,一种根据POCT的重量和大小,可分为便携型、手提式及其一次性使用型、桌面型;另一种根据用途分为血气分析仪、电解质分析仪、药物应用监测仪、快速血糖检测仪、抗凝测定仪、放射免疫分析仪、甲状腺激素检测仪、心肌损伤标志物检测仪等等。本文主要阐述了POCT的主要检测技术以及临床应用。目前POCT的检测技术主要有微流控芯片技术、传感器技术、干化学技术、免疫层析技术、生物芯片技术等 [3]。在近几年的临床检测中,POCT发展迅速且涉及到的领域非常广泛,比如小儿科、心内科、感染科、急诊科、内分泌科等各个临床科室,对病人及一些特殊人群的需要提供了很大的方便。
2. POCT主要技术
1) 微流控芯片技术
在一块几平方厘米的芯片上构建生物或化学实验室称为微流控芯片。微流控芯片是将微电极、微阀、微通道、微储液器、微泵和连接器等功能性元件,通过微细加工技术集成在芯片材料上的微全分析系统。目前很多检测技术都已经应用到微流控芯片的研究当中,检测方法主要有质谱、电化学检测、光学检测等。在POCT领域,微流控芯片技术已应用于生化检测、核酸检测、蛋白质检测、细胞计数等方面。传统的核酸检测包括样品前处理、PCR扩增及扩增产物的检测等多个复杂、耗时的步骤,对操作人员有特殊要求,同时需要使用到昂贵的试剂和设备,在特定疾病的检测中核酸检测有较高的灵敏度和特异性 [4] - [9]。
对于PCR扩增过程,温度控制系统和扩增产物的光学检测系统最终输出检测结果的用户接口都有较高的整合性要求。POCT核酸检测需要考虑体积、功耗、成本等等。目前,已经发表的多种技术和方法都有各自的优势和缺陷,针对不同的检测目标和应用场合,注重的有检测速度、多重检测、高通量等等。核酸芯片可以将这些处理过程简洁化、微型化,并统一集中在一个微小芯片内,核酸芯片的流体控制系统比较复杂。Oblath利用嵌入氧化铝薄膜为PCR扩增过程提供稳定的温度条件,成功实现唾液中的某些致病菌检测 [10]。Liu在样品前处理阶段利用生物素标记和特定修饰的磁珠捕获目标DNA,极大提高PCR扩增效率 [11] [12] [13]。随着新材料技术的发展和信息化水平的提高,微流控芯片POCT仪器在功能深度和应用广度上将会有更大的提高。在芯片制作方面,Easley等人使用蠕动泵和PDMS阀门制作了集核酸提取、PCR扩增及毛细管电泳全过程的检测芯片 [14],如图1(a)所示。Lee利用真空抽吸式泵和硅凝胶膜制作的检测芯片实现了对线粒体DNA变异和HIV-1病毒检测,该系统检测HIV感染T细胞的谱带强度达到了台式PCR仪的水平 [15] [16],如图1(b)所示。Chen等人将样品前处理、PCR及免疫层析试纸条技术检测相结合,用于检测唾液中的HIV RNA含量 [17],如图2所示。
 (a) (b)
(a) (b)
Figure 1. POCT nucleic acid lab chips. (a) Images of the integrated glass lab chip [14]; (b) Schematic illustration of the HIV-1 microfluidic chip [15] [16]
图1. POCT核酸芯片。(a) 集成玻璃实验室芯片的图像 [14];(b)HIV-1微流控芯片示意图 [15] [16]
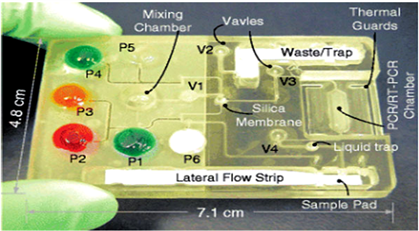
Figure 2. A lateral-flow strip based nucleic acid cassette in its storage state [17]
图2. 基于侧流层析试纸法的核酸芯片 [17]
2) 传感器技术
生物传感器技术是利用生物活性物质比如抗体、酶、生物膜、蛋白质、DNA、抗原等,是与物理化学换能器结合的一门技术,是一种物质分子水平的微量分析方法,也是一种先进的检测方法和监控方法。
生物感应器和换能器是生物传感器的两个组成部分,生物感应器有对被测物质进行选择的功能,被测物质与生物感应器发生生物学反应(物理、化学变化),产生物理、化学现象或新的化学物质,通过换能器将其变化结果转变为可以定量、传输、处理的电信号。换能器有电势测量式、电流测量式、阻抗测定式、光强测量式等主要形式。血糖仪是生物传感器技术在临床医学POCT领域的典型应用。
3) 干化学技术
干化学技术的检测方法是在特殊结构的试剂载体上将多种反应试剂固化,其被测样品(如血液、尿液等)中的液体作反应介质,被测成分直接与固化的干试剂进行反应,从而对样品进行分析测定,属于固相化学技术。干化学试剂载体有二层,三层和多层膜结构。检测特征信号的变化主要采用的是差示电位法和反射光度法 。
a) 差示电位法
基于ISE原理的差示电位法,干化学试剂载体上通过盐桥连接两个完全相同的离子选择电极。一是样品电极,二是参比电极。样品的离子浓度与两个电极间的电位差成比例关系,被测样品离子浓度由测量两个电极间的电位差计算得出。
b) 反射光度法
固相化学涉及的反射光度法主要为漫反射,它有两个主要特点:① 固相反应膜界面间存在多重内反射;② 因显色反应发生在固相,对入射光和反射光都有散射作用,因而不服从朗伯比尔(Lamber-Beer)定律。反射光强度变化受反应区域颜色变化的影响,反射光强度变化与分析物浓度成比例关系,由此计算出被测样品的分析物浓度。
4) 免疫层析技术
免疫层析技术是在20世纪60年代在发达国家兴起并被用于检测血清蛋白的一种结合了免疫技术和色谱层析技术的快速检测分析方法,利用胶体金、胶体碳、磁性纳米材料、稀土纳米材料、量子点等着色标记物,在层析时,标记物与待测物的络合物被相应的配体捕获而浓集显色于硝酸纤维素膜上的检测线,以纤维膜上显色条带的有无、颜色深浅和反射光线来定性或定量,在即时检测(POCT)中应用极为广泛 [18],如图3所示。免疫层析试纸条由样品垫、结合垫、硝酸纤维素(NC)膜、检测线(T线)、质控线(C线)、吸水垫、聚氯乙烯(PVC)底板等部分组成,根据待检测物的大小和抗原抗体结合的方式,分为双抗体夹心法和竞争法。

Figure 3. Principle of immunochromatography [18]
图3. 免疫层析技术原理 [18]
免疫层析技术是一种结合了色谱层析技术、免疫技术的检测分析方法。免疫层析技术是一种膜检测技术,检测基于抗原抗体特异性免疫反应。层析过程中结合了标记物的待测液通过流动与固相膜上受体发生特异性反应。根据测定标记物的光、电、磁等特性变化来定性或者定量检测被测物质的浓度。目前免疫层析技术研究主要方向有胶体金免疫层析技术、量子点免疫层析技术、上转换发光免疫层析技术、荧光免疫层析技术、磁珠免疫层析技术等。美国Alere的Triage系统是比较成功的免疫层析POCT商业产品,该系统可直接通过全血高效检测急性心肌梗塞相关标志物 [19],如图4所示。

Figure 4. Alere Triage POCT system, cartridge [19]
图4. Alere的Triage POCT系统和检测盒 [19]
5) 生物芯片技术
生物芯片,是一种高度集成平行化处理生物信息指甲盖大小的薄片,生物芯片技术是通过缩微技术,根据分子间特异性地相互作用的原理,将生命科学领域中不连续的分析过程集成于硅芯片或玻璃芯片表面的微型生物化学分析系统。在载体表面固化可与靶分子互相作用,与反应的生物分子形成固相表面,在载体材料上,它通过微加工和微电子技术构建微型生物化学系统。待检靶生物分子与生物芯片发生化学反应,利用相应的检测手段进行信号的收集,检测结果以荧光、化学发光或酶显色等形式表现。目前生物芯片技术在临床上广泛用于疾病筛查、药物分析等领域。在未来五年,生物芯片主要分为两种,一种是研究型的,一种是应用型的,研究型的主要是指在基因芯片的功能等方面会有进一步进展,应用型的蛋白芯片会有更好的发展。生物芯片的主要优点有分析全过程自动化、防污染、生产成本低、分析速度成千上万倍的提高、极高的样品并行处理能力等。美国Affymetrix公司首先使用生物芯片,图5是该公司在2003年为罗氏生产的检测CYP450基因的生物芯片,用于个性化用药 [18]。它是以单晶硅为衬底,通过多层掩膜版的制造过程,在几十万个20 µm2的检测区上合成出不同的基因片段。因为使用了单晶硅硅片,采用了半导体行业常用的掩膜版光刻技术,最后产品外观和半导体芯片非常类似,故被称为生物“芯片”。类似技术已经在基因检测领域大规模使用,但是在免疫检测领域还没有产品出现。

Figure 5. Gene biochip [18]
图5. 基因生物芯片 [18]
3. POCT的临床应用
1) POCT血气分析仪和血液分析仪
血气分析仪是利用电极对血样中的酸碱度、二氧化碳分压和氧分压进行测定的仪器,POCT血气分析仪具有检测快、携带方便、操作简单等特点,在各医院急诊科及其他科室的应用都非常广泛,尤其是急诊科的重症患者血气及电解质均会紊乱,导致患者严重酸碱失衡,由此可加重对人体各脏器功能损害,所以一份准确的血气分析结果使急诊科医生能够快速知道患者的酸碱失衡情况,并作对应的及时处理措施。由于急诊医学的不断发展,急诊患者的血气分析检测项目是必不可少的,尤其血气分析结果的准确性至关重要,直接影响急诊科医生对患者病情的判断以及抢救 [20] [21] [22] [23]。Shi等人设计了一种可以对四种白细胞进行计数的非鞘流式细胞计数仪,该仪器避免了过多的稀释步骤和鞘流结构,如图6所示。检测效果与Beckman Coulter的Coulter LH750血液分析仪的相关系数达到了0.90~0.98 [24]。

Figure 6. POCT hematology analyzers [24]
图6. POCT血液分析仪 [24]
2) 血糖检测仪
在救助和改进糖尿病患者的生活质量方面,血糖仪的研发和应用做出了重要的贡献。随着全球经济的快速发展以及人类生活水平的显著提高,糖尿病的患者在逐年增多。控制糖尿病患者的病情需要经常监测血糖含量,家用血糖仪已经在市场上普及,它可以满足临床和患者自我监测的需求,是糖尿病日常监测的主要检测手段。目前,市场上的血糖仪是为了检测血液中葡萄糖的含量而设计,所以检测对象仅是葡萄糖,且葡萄糖的动态检测范围符合人体血糖含量,即10~600 mg/d L (或0.6~33 mmol/L) [25]。血糖监测给血糖治疗和控制提供有效参考,良好的血糖控制,可以减少或延缓糖尿病并发症的产生。为了适应时代的发展和未来POCT的需求,需要发展更灵活、更敏感、可检测物质更丰富的便携式传感器。血糖仪通过测量葡萄糖氧化酶或葡萄糖脱氢酶催化的氧化还原反应来检测葡萄糖。由于酶具有特异的选择性,不可能对所有的目标物进行催化反应。因此,为了扩大血糖仪的应用范围,将之用于其他物质的检测,就要设计一个最终生成产物是葡萄糖的目标识别系统,使得测试结果能够用血糖仪读出以实现定量检测。近年来,研究人员使用血糖仪与功能化DNA或抗体相连接,实现了对一系列涉及到疾病诊断和环境监测的非葡萄糖目标物的检测。
3) 心肌损伤标志物检测仪
目前POCT仪器可以检测常规凝血功能指标。在心脏手术时凝血功能的术中监测,肺部血栓和深层静脉血栓的检测等方面POCT能提供快速地、准确地检测数据,为及时调整患者用药提供方便。在溶栓治疗前,需要确定病人是否有止血缺陷,是否对所使用的溶栓药物有抵抗作用。溶栓治疗过程中,需要及时地了解到使用的药物是否起到作用以及溶栓目的是否达到。应用POCT技术快速判断发生性纤溶,对于血栓病的诊断及溶栓治疗的疗效监测具有重要意义。
例如通过对急性心肌梗死(AMI)相关的标志物检测(肌钙蛋白、肌红蛋白、肌酸激酶同工酶等),能够快速评估心肌梗死患者的发病风险,使AMI患者得到及时预防和救治。
4) 放射免疫分析仪
放射免疫技术是一种将放射性同位素测量的高度灵敏性、精确性和抗原抗体反应的特异性相结合的体外测定超微量物质的新技术,也称为免疫放射分析。放射免疫技术由Yalow和Berson于1959年创立,有竞争性RIA (radioimmunoassay)和非竞争性RIA两类。
放射免疫分析的特点有特异性强、敏感度高、精密度高,而且可测定小分子和大分子物质,在医学检验中的应用非常广泛。可测定胰岛素、甲状腺激素等各种激素以及肿瘤标志物、微量蛋白质、药物(如庆大霉素、苯巴比妥)等,各种检测项目均有供应的试剂盒,因此放射免疫分析仪应用非常广泛,近年来,发光免疫分析、酶免疫分析等发展非常迅速,放射免疫分析有可能会被取代,但是在生物医学的基础研究中,对于研究新的活性物质和某些疾病发生的关系,仍然需要高特异性的检测方法,因此放射免疫分析仪仍是首选。
4. 总结
POCT技术自从应用到临床以来,POCT在提供方便快捷的同时,需要进一步完善其检测结果的规范化管理,POCT使用及其检测成本相对高,所以POCT技术还存在一定的局限性。为了使POCT能够更充分地发挥其优越的诊断功能,POCT的相关技术及仪器的使用标准应受到重视。POCT仪器的临床应用尚缺乏成熟的行业规范和管理体系,检测结果较高的不确定性限制了其推广和用于临床决策 [26] [27]。
文章引用
冯亚普,李丹杰,李燕虹,赵安琪,张丙霞,程 杰,崔景强. POCT技术研究现状及临床应用
Technologies Research Status and Clinical Applications of Point of Care Testing[J]. 生物医学, 2021, 11(01): 23-30. https://doi.org/10.12677/HJBM.2021.111004
参考文献
- 1. 李琦. POCT的应用现状与不足[J]. 临床检验杂志, 2013(3): 22-24.
- 2. 张玲. 即时检验(POCT)的应用[J]. 医疗装备, 2015, 28(1): 49-50.
- 3. 赵卫国. 即时检验[M]. 上海: 上海科学技术出版社, 2007: 38.
- 4. 贺志安. 检验仪器分析[M]. 北京: 人民卫生出版社, 2010: 202-205.
- 5. 辛晓敏, 关秀茹. 现代临床检验技术与应用[M]. 北京: 科学出版, 2005: 232-234.
- 6. 丛辉, 王惠民, 王跃国. 微流控芯片技术及应用展望[J]. 现代检验医学杂志, 2005(1): 88-89.
- 7. 李阳, 王云龙. 免疫层析技术的研究进展[J]. 中国卫生检验杂志, 2015, 25(22): 3978-3980.
- 8. 于新芬, 潘劲草, 孟冬梅. 生物传感器在医学检测中的应用[J]. 检验医学与临床, 2004, 1(3): 120-122.
- 9. 马新秀, 胡文忠, 冯可, 等. 生物芯片在微生物检测中的应用[J]. 商品与发酵工业, 2018(2): 273-277.
- 10. Oblath, E.A., et al. (2013) A Microfluidic Chip Integrating DNA Extraction and Real-Time PCR for the Detection of Bacteria in Saliva. Lab on a Chip, 7, 1325-1332. https://doi.org/10.1039/c3lc40961a
- 11. Liu, P., et al. (2011) Integrated DNA Purification, PCR, Sample Cleanup, and Capillary Electrophoresis Microchip for Forensic Human Identification. Lab on a Chip, 11, 1041-1048. https://doi.org/10.1039/c0lc00533a
- 12. Beyor, N., Yi, L., Seo, T.S., et al. (2009) Integrated Capture, Concentration, Polymerase Chain Reaction, and Capillary Electrophoretic Analysis of Pathogens on a Chip. Analytical Chemistry (Washington), 81, 3523-3528. https://doi.org/10.1021/ac900060r
- 13. Toriello, N.M., et al. (2008) Integrated Microfluidic Bioprocessor for Single-Cell Gene Expression Analysis. Proceedings of the National Academy of Sciences of the United States of America, 105, 20173-20178. https://doi.org/10.1073/pnas.0806355106
- 14. Easley, C.J., et al. (2006) A Fully Integrated Microfluidic Genetic Analysis System with Sample-in-Answer-Out Capability. Proceedings of the National Academy of Sciences of the United States of America, 103, 19272-19277. https://doi.org/10.1073/pnas.0604663103
- 15. Chang, C.M. (2013) Integrated Three-Dimensional System-on-Chip for Direct Quantitative Detection of Mitochondrial DNA Mutation in Affected Cells. Biosensors & Bioelectronics, 48, 6-11. https://doi.org/10.1016/j.bios.2013.02.015
- 16. Wang, J.H., et al. (2013) An Integrated Chip Capable of Performing Sample Pretreatment and Nucleic Acid Amplification for HIV-1 Detection. Biosensors & Bioelectronics, 41, 484-491. https://doi.org/10.1016/j.bios.2012.09.011
- 17. Chen, D., et al. (2010) An Integrated, Self-Contained Microfluidic Cassette for Isolation, Amplification, and Detection of Nucleic Acids. Biomedical Microdevices, 12, 705-719. https://doi.org/10.1007/s10544-010-9423-4
- 18. 单万水. 从层析荧光到微流控生物芯片——现场快速检验(POCT)技术基础概述[J]. 中国医疗器械信息, 2017, 23(7): 45-52.
- 19. Apple, F.S. (1999) Simultaneous Rapid Measurement of Whole Blood Myoglobin, Creatine Kinase MB, and Cardiac Troponin I by the Triage Cardiac Panel for Detection of Myocardial Infarction. Clinical Chemistry, 45, 199-205. https://doi.org/10.1093/clinchem/45.2.199
- 20. 谢华斌, 张忠英. POCT血糖仪的质量管理[J]. 实验与检验医学, 2008, 26(2): 173-174.
- 21. 樊绮诗, 钱士匀, 等. 临床检验仪器与技术[M]. 北京: 人民卫生出版社, 2015.
- 22. 陈宇琼, 朱清峰, 李国祥, 等. 放射免疫分析与化学发光免疫检测应用对比及发展趋势[J]. 同位素, 2014, 27(3): 188-192.
- 23. 董家书, 蒋丽君. POCT的发展及应用现状[J]. 医学研究杂志, 2009, 38(10): 122-123.
- 24. Shi, W.D., et al. (2013) Four-Part Leukocyte Differential Count Based on Sheathless Microflow Cytometer and Fluorescent Dye Assay. Lab on a Chip, 7, 1257-1265. https://doi.org/10.1039/c3lc41059e
- 25. Montagnana, M., Caputo, M., Giavarina, D., et al. (2009) Overview on Self-Monitoring of Blood Glucose. Clinica Chimica Acta, 402, 7-13. https://doi.org/10.1016/j.cca.2009.01.002
- 26. 张坚. 医院急救医学装备配置中POCT的应用与管理[J]. 生物医学工程学进展, 2013, 34(3): 191-193.
- 27. Aguilera-Herrador, E. (2010) Analytical Connotations of Point-of-Care Testing. The Analyst, 9, 2220-2232. https://doi.org/10.1039/c0an00307g
NOTES
*通讯作者。