Advances in Analytical Chemistry
Vol.
09
No.
03
(
2019
), Article ID:
31811
,
8
pages
10.12677/AAC.2019.93021
Method Validation of Determination of Nitrofuran Metabolites in Animal Derived Food by Ultra High Performance Liquid Chromatography-Mass Spectrometry
Changli Mu, Bei Wang, Zhijuan Chi, Jiao Wang, Yizheng Zhou, Chunchun Wang
The Supervision, Inspection Testing Center of Agricultural Quality Security, Taicang Jiangsu

Received: Jul. 26th, 2019; accepted: Aug. 15th, 2019; published: Aug. 22nd, 2019

ABSTRACT
To improve detection capability, the laboratory verified the applicability of Ministry of Agriculture Notice No. 781-4-2006 Determination of nitrofuran metabolites in animal derived food by high performance liquid chromatography-tandem mass spectrometry. This method is mainly verified from the test coverage, standard curve, linearity, sensitivity, precision and recovery rate. Through the test, it is found that the standard curve, linearity, sensitivity, precision and recovery rate of the applicable range meet the requirements of the standard. The standard can be used to conduct external testing operations.
Keywords:Ultra High Performance Liquid Chromatography-Mass Spectrometry, Animal Derived Food, Nitrofuran Metabolites, Method Validation
超高效液相色谱–质谱法测定动物源食品中硝基呋喃类代谢物残留量的方法验证
母昌立,王蓓,迟志娟,王姣,周益政,王淳纯
江苏省太仓市农产品质量监督检验测试中心,江苏 太仓

收稿日期:2019年7月26日;录用日期:2019年8月15日;发布日期:2019年8月22日

摘 要
为提高检测能力,本实验室验证了农业部781号公告-4-2006《动物源食品中硝基呋喃代谢物残留量的测定,高效液相色谱法–串联质谱法》的适用性。本方法验证主要从适用范围、标准曲线、线性、灵敏度、精密度及回收率进行,通过试验发现,本实验室的适用范围标准曲线、线性、灵敏度、精密度及回收率均满足该标准的要求,可以利用该标准对外开展检测业务。
关键词 :超高效液相色谱–质谱法,动物源食品,硝基呋喃类代谢物,方法验证

Copyright © 2019 by author(s) and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
标准方法是一种经过全面研究的方法,清楚而严密地说明所需条件和操作程序,用于对物质一种或多种特性值进行测量。CNAS-CL01:2018《检测和校准实验室能力认可准则》 [1] 7.2.1.4条款规定:“当客户未指定所用的方法时,实验室应选择适当的方法并通知客户。推荐使用以国际标准、区域标准或国家标准发布的方法,或由知名技术组织或有关科技文献或期刊中公布的方法,或设备制造商规定的方法。实验室制定或修改的方法也可使用。”在7.2.1.5条款中规定:“实验室在引入方法前,应验证能够正确地运用该方法,以确保实现所需的方法性能。”2018版《检验检测机构资质认定评审准则》 [2] 4.5.14条款规定:“检验检测方法包括标准方法、非标准方法(含自制方法)。应优先使用标准方法,并确保使用标准的有效版本。在使用标准前,应进行证实。”因此,实验室在使用标准方法前,需要对实验室使用标准方法的技术能力是否达标进行验证。
本文以农业部781号公告-4-2006《动物源食品中硝基呋喃代谢物残留量的测定高效液相色谱法–串联质谱法》 [3] 为例做方法验证。此次验证包括:适用范围、标准曲线、线性、灵敏度、精密度及回收率。
2. 材料与仪器设备
2.1. 材料
农业部781号公告-4-2006适用于动物源食品中呋喃唑酮、呋喃它酮、呋喃妥因和呋喃西林单个或混合物的相应代谢产物AOZ (3-Amino-2-Oxazolidinone)、AMOZ (3-Amino-5-morpholinomethyl-2-oxazolidinone)、AHD (1-Aminohydantoin)和SEM (Semicarbazide) (结构式见图1)残留量的检测。本方法以猪肉、猪肝、鲫鱼和禽蛋为试验材料,验证该标准是否适用于本实验室。
2.2. 试剂与耗材
AOZ、AMOZ、AHD、SEM浓度均为100 mg/L,农业部环境保护科研监测研究所; AOZ-D4 (>99.0%)、AMOZ-D5 (>99.0%)、AHD-13C3 (>99.0%)、SEM-13C15N2 (>99.0%),德国Witega公司;二甲基亚砜(>99.0%)、2-硝基苯甲醛(>99.0%),日本东京化成工业株式会社;乙酸铵(色谱纯),美国fisher公司;GHP微孔滤器(0.22 μm),美国waters公司。

Figure 1. The Chemical structures of AOZ (a), AMOZ (b), AHD (c) and SEM (d)
图1. AOZ (a)、AMOZ (b)、AHD (c)和SEM (d)的化学结构式
2.3. 仪器设备
5500型高效液相色谱–串联质谱仪:美国AB公司;XS205电子天平:瑞士METTLER TOLEDO公司;3-18K高速离心机:德国Sigma公司;涡旋振荡器:德国IKA公司;恒温水浴锅(DK-600),上海冉绘实业有限公司。
3. 试验方法
3.1. 前处理方法
取10,000 r/min匀浆1 min的试料2 ± 0.05 g置离心管中,加100 ng/mL的AOZ-D4,AMOZ-D5,AHD-13C3,SEM·HCl-[1,2-15N2;13C]标准工作液50 µL,再加4 mL 1 mol/L盐酸溶液0.5 mL,50 mmol/L 2-硝基苯甲醛的二甲亚砜溶液150 µL,涡旋混匀。37℃避光水域16 h。
衍生物加0.1 mol/L磷酸氢二钾溶液5 mL,用5 mol/L氢氧化钠溶液调节PH7.2-7.4,加乙酸乙酯5 mL,涡旋,中速振荡5 min,2000 r/min离心15 min,吸取上清液,加乙酸乙酯5 mL,重复提取一次,合并上清液于50℃氮吹。初始流动相1.0 mL溶解残余物,经滤膜,供高效液相色谱–串联质谱法测定。
3.2. 检测方法
色谱柱:C18,50 mm × 2.1 mm,3 µm;流动相:0.1%甲酸水溶液(A) + 0.1%甲酸乙腈溶液(B),梯度洗脱,梯度见表1;.3柱温:40℃;进样量:5 µL;离子源:电喷雾ESI,正离子;扫描方式:多反应监测MRM;气帘气:30.0;离子源温度:650℃;Gas 1:60.0;Gas 2:55.0;监测离子对及对应质谱参数,见表2。
Table 1. The mobile phase gradient of liquid chromatography for the separation of nitrofuran metabolites
表1. 分离硝基呋喃类代谢物的液相色谱流动相洗脱梯度
Table 2. The acquisition parameters of UPLC-MS/MS for analysis of nitrofuran metabolites and their isotopic labels
表2. 硝基呋喃类代谢物及其同位素标记物的主要质谱参数
3.3. 标准曲线的制作
精密量取2.5、5.0、10、20、50、100、200 ng/mL AOZ,AMOZ,AHD,SEM混合标准工作液100 µl置不同离心管中。按3.1处理,制得0.2、0.5、1.0、2.0、4.0、10.0和20.0 ng/mL各个浓度,利用2.2进行测定,每个浓度测定2次。
3.4. 灵敏度的验证
本标准中,AOZ、AMOZ、AHD、SEM在动物源食品中的检测限为0.25 ng/g,定量限为0.50 ng/g。在每种样品中加入适量的AOZ、AMOZ、AHD、SEM混合标准溶液,使AOZ、AMOZ、AHD、SEM在样品中的浓度分别为0.25 ng/g和0.50 ng/g,每种样品每个浓度重复10次,按照3.1进行前处理,利用3.2进行检测。若浓度为0.25 ng/g时,信噪比大于等于3,则实验室的检测限满足标准检测线;若浓度为0.50 ng/g时,信噪比大于等于10,则实验室的定量限满足标准定量线 [4] 。
3.5. 精密度的验证
中华人民共和国农业部第235号公告规定,呋喃唑酮、呋喃它酮、呋喃妥因和呋喃西林均为禁止使用药物,在动物性食品中不得检出。因此,在检测限、2倍检测限和10倍检测限3个浓度水平进行检测 [5] ,每种样品每个浓度水品重复10次,计算相对标准偏差。
3.6. 回收率的验证
在每种样品中加入适量的AOZ、AMOZ、AHD、SEM混合标准溶液,使AOZ、AMOZ、AHD、SEM在样品中的浓度分别为0.5 ng/g、1.0 ng/g和2.5 ng/g,每种样品每个浓度重复10次,按照3.1进行前处理,3.2进行检测。
4. 验证结果
4.1. 标准曲线
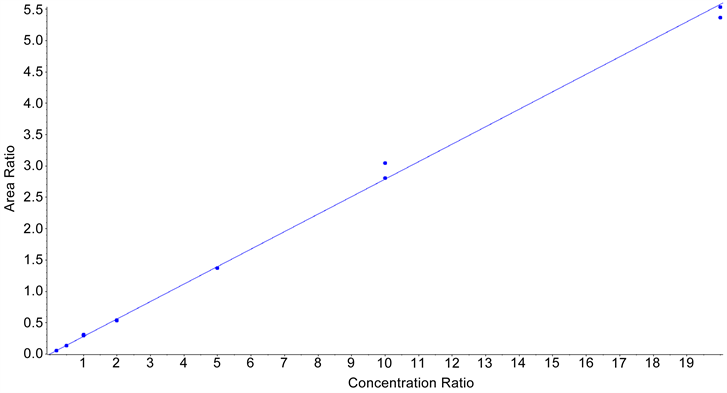
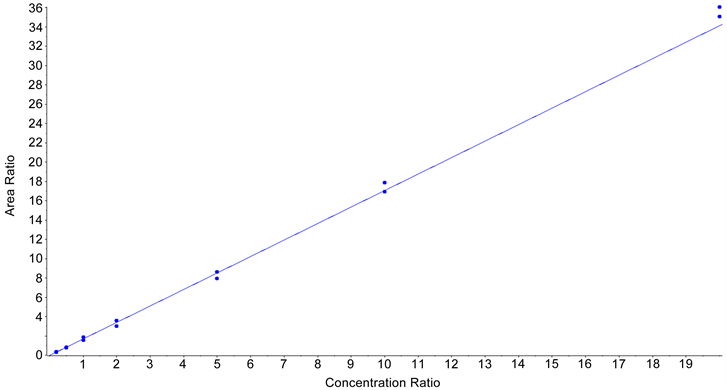
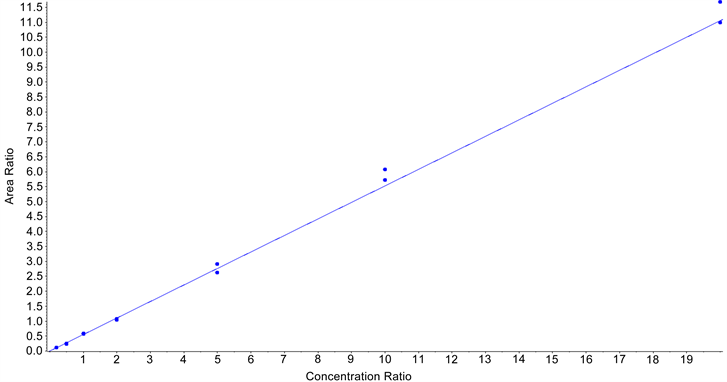
将3.3中得到的各浓度标准溶液,按照方法3.2进行检测,每浓度检测2次。以标准溶液中目标物的浓度为横坐标,对应浓度目标物峰面积与相应同位素内标峰面积比值为纵坐标,得到AOZ、AMOZ、AHD、SEM的标准曲线(见图2)和线性方程及相关系数(见表3)。
由表3看出,AOZ、AMOZ、AHD、SEM线性方程的相关系数均大于0.99,相关性良好,可用于准确定量 [6] 。
 (a)
(a)
 (b)
(b)
 (c)
(c)
 (d)
(d)
Figure 2. The standard curves of AOZ (a), AHD (b), AMO Z (c) and SEM (d)
图2. AOZ (a)、AHD (b)、AMOZ (c)、SEM (d)的标准曲线
Table 3. The Linear equations and correlation coefficients of AOZ, AMOZ, AHD and SEM
表3. AOZ、AMOZ、AHD、SEM的线性方程及相关系数
4.2. 灵敏度
在每种样品中加入适量的AOZ、AMOZ、AHD、SEM混合标准溶液,使AOZ、AMOZ、AHD、SEM在样品中的浓度分别为0.25 ng/g和0.50 ng/g,每种样品每个浓度重复10次,按照3.1进行前处理,利用3.2进行检测。经检测发现,当各样品中AOZ、AMOZ、AHD、SEM浓度为0.25 ng/g时,信噪比均大于3;当各样品中AOZ、AMOZ、AHD、SEM的浓度为0.50 ng/g时,信噪比均大于10。由此可见,本实验室的方法检测限和定量限均满足农业部781号公告-4-2006的要求。
4.3. 精密度
每种样品在检测限、2倍检测限和10倍检测限3个浓度水平进行检测,每种样品每个浓度重复10次,按照3.1进行前处理,利用3.2进行检测,得到表4所示结果。
Table 4. The precisions of AOZ, AMOZ, AHD, SEM in Pork, Porkliver, Carp and Eggs
表4. AOZ、AMOZ、AHD、SEM在猪肉、猪肝、鲫鱼、禽蛋的精密度
由表4可以看出,4种化合物在猪肉、猪肝、鲫鱼和禽蛋中添加回收的相对标准偏差均小于30%,满足农业部781号公告-4-2006的要求。
4.4. 回收率
添加AOZ、AMOZ、AHD、SEM,使其在各种样品中的浓度分别为0.5 ng/g、1.0 ng/g和2.5 ng/g,每种样品每个浓度重复10次,按照2.1进行前处理,利用2.2进行检测,得到表5所示结果。
Table 5. The recovery rates of AOZ, AMOZ, AHD and SEM in Pork, Porkliver, Carp and Eggs
表5. AOZ、AMOZ、AHD、SEM在猪肉、猪肝、鲫鱼、禽蛋的回收率
由表5可以看出,4种化合物在猪肉、猪肝、鲫鱼和禽蛋中添加回收率均在60%~120%,满足农业部781号公告-4-2006的要求。
5. 结论
经过验证,本实验室在适用范围、标准曲线、线性、灵敏度、精密度及回收率均满足农业部781号公告-4-2006动物源食品中硝基呋喃代谢物残留量的测定高效液相色谱法–串联质谱法的要求,本实验室可以利用此标准对外开展检测业务。
文章引用
母昌立,王 蓓,迟志娟,王 姣,周益政,王淳纯. 超高效液相色谱–质谱法测定动物源食品中硝基呋喃类代谢物残留量的方法验证
Method Validation of Determination of Nitrofuran Metabolites in Animal Derived Food by Ultra High Performance Liquid Chromatography-Mass Spectrometry[J]. 分析化学进展, 2019, 09(03): 160-167. https://doi.org/10.12677/AAC.2019.93021
参考文献
- 1. 中国合格评定国家认可委员会. ISO/IEC17025:2017. 检测和校准实验室能力认可准则[S]. 中国合格评定国家认可委员会, 2017.
- 2. 国家认证认可监督管理委员会. 检验检测机构资质认定评审准则[S]. 国家认证认可监督管理委员会, 2016.
- 3. 中华人民共和国农业部. 农业部781号公告-4-2006动物源食品中硝基呋喃代谢物残留量的测定高效液相色谱法–串联质谱法[S]. 中华人民共和国农业部, 2006.
- 4. 鲁静, 付凌燕, 王旭. 质量分析方法验证中检出限和定量限测定方法探讨[J]. 中国药品标准, 2012, 13(1): 33-35.
- 5. 康婕. 实验室检测与校准的方法验证和方法确认[J]. 农产品加工, 2018(5): 60-62.
- 6. 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. GB/T27417-2017合格评定化学分析方法确认和验证指南[S]. 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会, 2017.
