Sustainable Energy
Vol.04 No.03(2014), Article ID:13634,9
pages
10.12677/SE.2014.43006
Preparation of 2,5-Diformylfuran through Selective Electro-Catalytic Oxidation with Modified Metallic Electrodes
Shengqiang Zhang, Weifeng Li, Lu Lin*
College of Energy & School of Energy Research, Xiamen University, Xiamen
Email: joseph201x@icloud.com, *lulin@xmu.edu.cn
Received: Apr. 30th, 2014; revised: May 6th, 2014; accepted: May 12th, 2014
Copyright © 2014 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
In recent years, the production of furan derivatives from biomass has become an exciting research field, because it contributes to building one of the major routes for achieving sustainable energy supply and the production of alternative chemicals. As one of the most important furan derivatives, 2,5-diformylfuran (DFF) is a multifunctional organic intermediate with the prospective app- lication potentiality in the future. Although it has been proven very useful, DFF is still not easy to be obtained in industry. Up to now, there are several catalytic methods available for the preparation of DFF, but mainly concentrated on chemical catalysis, which are prone to bring about serious environmental pollution. Preparation method for producing DFF through electric-catalytic oxidation, taking the advantages of the electrochemical reaction, is a kind of clean oxidation technology. Main reaction routes and mechanisms of the electric-catalytic oxidation technology applied to the preparation of DFF were introduced; its technical advantages as well as existing problems were also elaborated; and combined with its research status, the technology of preparation of DFF through selective electric-catalytic oxidation was prospected. In a word, the introduced method could provide a potentially feasible transformation path for the industrial production of DFF through this kind of clean oxidation technology, instead of common chemical catalysis.
Keywords:2,5-Diformylfuran, 5-Hydroxymethylfurfural, Electro-catalytic Oxidation, Chemically Modified Electrode, 2,5-Hydroxymethylfuran, Carbohydrates, Biomass

修饰电极上选择性电催化氧化制备 2,5-二甲酰基呋喃
张盛强,李维烽,林鹿*
厦门大学能源学院,能源研究院,厦门
Email: joseph201x@icloud.com, *lulin@xmu.edu.cn
收稿日期:2014年4月30日;修回日期:2014年5月6日;录用日期:2014年5月12日

摘 要
近年来,由生物质生产呋喃衍生产品已成为一个热点研究领域,因其是有助于构建实现可持续能源供应和生产替代化学品的主要途径之一。作为一种重要的呋喃衍生品,2,5-二甲酰基呋喃是一种具有潜在广泛应用前景的多功能有机中间体。虽然2,5-二甲酰基呋喃已被证明非常有用,但其在工业上仍不易获得。迄今为止,已有很多催化方法可用于2,5-二甲酰基呋喃的制备,但多为化学催化法,环境污染大。电催化氧化法制备2,5-二甲酰基呋喃利用电化学反应的优势,是一种清洁氧化技术。本文介绍了电催化氧化技术应用于制备2,5-二甲酰基呋喃的主要反应途径及机制;对其技术优势和存在的问题也作了较为详细的阐述;并结合其研究现状对选择性电催化氧化制备2,5-二甲酰基呋喃技术进行了展望。总之,所述方法能够为未来工业上通过该清洁氧化技术而不是常见的化学催化法进行2,5-二甲酰基呋喃的生产提供一条潜在的可行的转化途径。
关键词 :2,5-二甲酰基呋喃,5-羟甲基糠醛,电催化氧化,化学修饰电极,2,5-二羟甲基糠醛,碳水化合物,生物质

1. 引言
随着化石资源的日渐枯竭,人类环境的不断恶化,寻求可替代化石能源的燃料和基础化学品已迫在眉睫。生物质是唯一可以替代化石能源生产化学品的可再生资源。以资源丰富、可再生的生物质生产化学品和燃料及其衍生产品能为缓解全世界对逐渐枯竭的化石能源的强大依赖提供一条可行的路线 [1] - [3] 。由生物质碳水化合物转化得到的5-羟甲基糠醛(5-hydroxymethylfurfural, HMF)由于能通过不同催化反应进一步形成多种基础化学品和能源分子,被称为是连接石油化工和生物质化工的桥梁 [3] - [11] 。作为HMF重要衍生产品之一的2,5-二甲酰基呋喃(2,5-diformylfuran, DFF),是一种未来具有广泛应用前景的高附加值生物质基化学品。DFF常温下以固体粉末形态存在,具有晶体外观,其分子式为(O=CH)2-(C4H2O)。DFF具有多种用途 [12] - [16] ,如通过将DFF分子与一定量的二元胺缩合可生成含呋喃基团的聚合型席夫碱,合成高端药物,大环配体以及农药抗真菌剂等;由于其具有对称性与不饱和性的结构,它可以作为单体用于各种聚合材料如2,5-二甲酰基呋喃-尿素树脂等新型聚合物材料的合成。但目前工业上DFF产品价高量少,其制备途径不成熟,仍处于不断探索和完善中。
由于HMF分子中含有呋喃环、羟甲基和甲酰基,HMF的氧化反应往往伴随着很多副反应,如过氧化反应、脱羰基反应、交联聚合反应等。由HMF生成DFF的反应主要是对HMF分子中的羟甲基进行选择性氧化,而不进攻更具活性的不饱和甲酰基,否则将形成其他氧化产物 [17] [18] ,如5-羟甲基-2-糠酸(5-hydroxymethyl-2-furancarboxylic acid, HMFCA)、5-甲酰基-2-糠酸(5-formyl-2-furancarboxylic acid, FFCA)、2,5-呋喃二甲酸(2,5-furandicarboxylic acid, FDCA)等(如图1所示 [18] )。因此,如何实现HMF向DFF的有效转化是一个极大的难点问题。高收率和高选择性获得DFF的研究仍具有挑战性。为此,各种采用均相、非均相催化剂以及辅以更为绿色的分子氧作为氧化剂的催化方法得到了广泛的研究 [19] - [26] 。此外,对于DFF的制备,还有其他方法可以选用,如电催化氧化法以及酶催化氧化法 [27] 等。电催化氧化技术原是用于水处理领域的一项技术,一般是对有机废水进行处理;也有将其应用于化学品生产领域的研究,但不多。本文综述了电催化氧化技术应用于制备2,5-二甲酰基呋喃技术的研究历史、现状并对其未来发展进行了展望。
2. 电催化氧化技术 [28] - [37]
2.1. 电催化氧化的含义、机理及特性
电催化是指在电场下,存在于电极表面或是溶液相中的修饰物能促进或是抑制在电极上发生的电子转移反应,而电极表面或是溶液相中的修饰物本身并不发生明显变化的一类化学作用。据有关研究及推测表明,其机理主要是通过电极或是电极表面修饰物的作用产生超氧自由基、羟基自由基等活性基团来进行氧化。其特性主要体现在对所处理的有机物表现出较高的反应速率,并且具有很高的选择性。此外,电催化作用还具有良好的环境相容性。
2.2. 电催化氧化技术的应用
电催化氧化的应用主要包括:电化学燃烧,即电催化氧化程度较深时发生的深度氧化,其最终产物是H2O和CO2;电催化转化,已有报道多是用于将有机大分子物质转化为易降解的有机小分子或是将有毒有机物转化为无毒有机物。另外,有时可以将环状化合物开环生成易降解的脂肪类化合物。
2.2.1. 有机废水处理领域中的应用 [29] - [32]
电催化氧化技术原是一种广泛应用于有机废水处理领域中的一项技术,其原理主要是利用电极阳极所具有的高电位以及催化活性来直接降解废水中的有机物,或是利用其产生的羟基自由基等强氧化基团进行有机废水降解。可见电极在这项技术中起着十分重要的作用,废水处理效率一定程度上取决于电极选择是否合理。可选用的电极材料包括金属电极、活性炭纤维电极、金属氧化物电极等。实际选用过程中不仅应当考虑到电极材料需具有良好的导电性和稳定性,还应考虑其是否具有良好的电催化活性和选
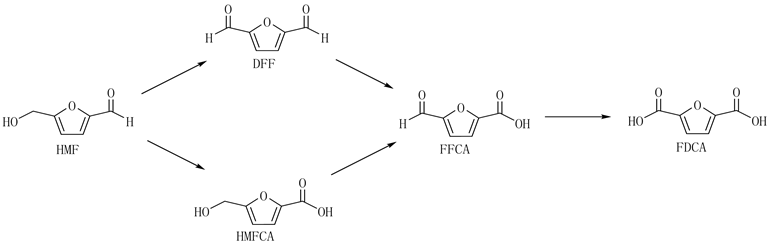
Figure 1. Possible oxidation products derived from HMF [18]
图1. 可由HMF衍生得到的氧化产品 [18]
择性,此外还应兼顾电极材料的成本问题。上述三种电极材料各具特点,其中的金属氧化物电极因其能满足电催化活性高、稳定性好、成本较低等优点而在电催化氧化处理有机废水领域中获得了较为广泛的应用。传统上电催化氧化技术能够借助具有电催化活性电极材料在温和条件下产生的羟基自由基使难于自然分解的有机物转化为可生物降解物,这在废水无害化处理上具有技术优势和良好的应用前景。
2.2.2. 化学品生产领域中的应用 [38] - [43]
电催化氧化技术也可应用于化学品生产领域,如可将其用于制备高附加值生物质基化学品2,5-二甲酰基呋喃(DFF)的工艺中。已有研究结果表明采用金属电极或经修饰后的金属电极为电催化氧化电极,碱性反应介质中,获得较高收率的DFF,且所得产物几乎以该醛类物质存在,也即产物DFF选择性接近100%。采用该技术生产DFF能避免繁琐而耗能的分离和纯化步骤,可成为未来工业化生产DFF较为理想的技术选择之一。以下就该技术用于制备DFF工艺的报道进行较为详细的阐述和总结。
3. 电催化氧化制备DFF [38] - [41]
电催化氧化制备DFF可选取由生物质衍生的2,5-二羟甲基呋喃(2,5-dihydroxymethylfuran, DHMF)或HMF为基质(亦有其他起始原料可供选择,比如呋喃-2,5-二甲腈(furan-2,5-dicarbonitrile)或呋喃(furan)等)。利用上述提及的两种有机分子对电化学反应的活性来生成目标产物DFF。迄今为止,对该技术的研究及拓展应用方面还鲜见报道,相关研究报道及分析如下。
3.1. HMF为起始原料
Romuald Skowroński等 [38] 研究了电催化氧化HMF生成DFF的反应过程及其转化机理。伯醇物质(primary alcohols)一般在电催化氧化作用下易于转化为羧酸类物质,但生成醛类物质却比较难。铂电极中,苄基型醛能够在吡啶或H2O/叔丁醇混合体系中生成。而在NiO/NiOOH电极中,各种醇类物质在二元相体系中的电催化氧化反应生成的却是相应的醛和羧酸类物质的混合物。基于此,Romuald Skowroński等 [38] 选用铂电极,在H2O/CH2Cl2二元相体系中进行选择性电催化氧化HMF生成DFF的反应,其反应式如图式1所示。
其反应条件是:室温下,在电解槽中由无机盐H2O和CH2Cl2组成二元相体系,设定一定的电流密度,加入反应基质后进行恒电流电解。产物DFF收率的变化主要取决于反应时间以及所用电解质的不同,其结果如表1所示。
由表1可知,改变电解条件使得摩尔电容从2F·mol−1增大到5 F·mol−1时,原先低于50%收率均得以增长,但总的来说电流效率并不高。在给定的实验条件下,当以Na2HPO4为电解质时,DFF最高收率达到68%。此外,相关检测表明该反应的产物选择性很好,产物仅为DFF而未检测到FDCA。能检测到的物质还有存在于水相层中未反应完全的HMF,其浓度会随着摩尔电容的增大而降低。通过1H NMR检测,能够将反应混合液的有机相层中存在的DFF和少量未反应完全的HMF检测出来,该反应对DFF的选择性达到100%。DFF能在Pt电极下,完全为非水溶剂体系中反应并停留在生成醛的反应阶段,但若存在水介质,DFF将形成偕二醇,该物质会在给定的反应条件下继续氧化生成羧酸类物质。其反应过程如图式2所示。

Scheme 1. The formation of DFF choosing HMF as substrate by electric-catalytic oxidation method [38]
图式1. HMF为基质电催化氧化法生成DFF [38]
Table 1. The formation of DFF with HMF as substrate by electric-catalytic oxidation method in biphasic system [38]
表1. HMF为基质在二元相体系中电催化氧化生成DFF [38]
aYield of isolated product, bDetermined by 1H NMR spectroscopy.

Scheme 2. [38] Probable transformations involved in the electric-catalytic oxidation process of organic alcohols
图式2. [38] 有机醇类物质电催化氧化过程中可能涉及的转化
由此可见羧酸类物质易在水相层中生成,将反应溶剂体系更换为碱性水溶液,不含有机相时,HMF经电催化氧化的产品仅有为FDCA。可见二元相体系会对DFF的生成有利,因为DFF在水中溶解性相对较差却极易溶解于有机溶剂CH2Cl2。该有机相层几乎成为一种“捕捉器”,能够将反应生成的DFF及时捕获,能避免其进一步氧化为FDCA,从而能够提高DFF的收率和选择性。Grzegorz Grabowski等 [39] 在以NiO/NiOOH为电极材料时,碱性介质体系下HMF电催化氧化反应生成了收率为71%的FDCA。该研究也说明了两相反应溶剂体系对电催化氧化HMF生成DFF的反应的有效性。
3.1.1. 电催化氧化转化HMF生成DFF的机理
有机小分子的氧化过程具有复杂性,迄今为止仅有少数文献涉及这方面的研究,而目前对于选择性电催化氧化HMF生成DFF的研究报道甚少,对其氧化机理的研究也尚不够深入。研究HMF到DFF的选择性电催化氧化过程,对认识有机小分子选择性电催化氧化反应机理也具有特殊的意义。
HMF为基质电催化氧化法生成DFF机理主要涉及HMF分子在电极表面上的吸附和氧化过程研究。此外,HMF分子的吸附氧化及其DFF产物的解离是一个对电极表面结构极其敏感的过程。氧化过程和氧化产物与电极表面有着极其密切的关系。例如,纯金属电极或是金属氧化物电极经外来吸附原子修饰后能产生奇特效应,电极表面上的吸附原子如Sb、Pb吸附原子能够在较低电位下吸附氧,可显著提高复合电极的电催化氧化活性。与未经修饰电极相比,修饰电极氧化峰电位将会发生负移,峰电流也将增加。但有些原子吸附会对该氧化过程起抑制的作用,如S修饰电极表面,其S吸附原子会消耗表面吸附的氧,从而抑制HMF分子的氧化。
由此可见,不论HMF分子是在纯金属电极或原子掺杂抑或化学修饰电极下发生电化学吸附和氧化,其选择性电催化氧化的效果很大程度上取决于电极表面的状态。综合以上讨论可知,在HMF为基质电催化氧化法生成DFF过程中,要高收率获得DFF产品,主要是从反应介质体系和电极材料的选择上考虑,如采用二元相介质体系和修饰电极材料可使该反应朝着期望的方向进行。
3.2. DHMF为起始原料
3.2.1. 纯金属电极或单金属氧化物下电催化氧化DHMF
A. Al Baradii等 [40] 研究了选择性电催化氧化DHMF生成HMF的反应过程及其转化机制。实验是以诸如Pt、Au、Ni或NiOOH为电极材料,在碱性介质中进行。建立适宜的HPLC分析条件以检测生成的各个产物。反应结果表明:在Pt、Au、Ni或NiOOH电极下,DHMF在碱性介质中经电催化氧化反应主要生成的是HMF。HMF是一种不太稳定的化合物,但其还原产物DHMF却比较稳定,其贮存性能十分良好。因此,当需要HMF这一物质时,我们可以通过以Pt、Au、Ni或NiOOH为电极材料在碱性介质条件下进行DHMF的选择性电催化氧化反应来实现,但需进一步改善反应条件,从而能以较高收率获得该产品。
3.2.2. 修饰纯金属电极下电催化氧化DHMF
A. Al Baradii等 [40] 还对修饰纯金属电极下电催化氧化DHMF生成DFF的反应及其转化机制进行了研究。其研究表明:在Pb吸附原子原位修饰的Pt电极下,碱性介质条件下电催化氧化DHMF的反应能够获得61%收率的DFF。这表明原电催化氧化反应所用的纯金属电极经原位金属吸附原子的修饰改性后,在同一工艺过程中会生成不同的氧化产物。尽管色谱分析表明,HMF未完全转化,但产物中DFF的选择性非常高。这进一步表明:若能建立用于Pt/Pb上电催化氧化反应的适宜条件,就能以更高收率获得DFF,或许能够接近100%。K. B. Kokoh和E. M. Belgsir [41] 也进行过类似研究。他们也是在Pb吸附原子原位修饰的Pt电极下,碱性介质条件下对DHMF进行电催化氧化,获得80%收率的DFF。传统上可以采用锰氧化物、铬氧化物或是化学计量的无机或有机氧化剂催化氧化DHMF为DFF。与以上化学催化氧化法不同,K. B. Kokoh和E. M. Belgsir [41] 着眼于通过电催化氧化醇类物质生成羰基化合物的研究。
电催化氧化法的一个关键问题是需要不断开发非均相催化及相应界面电化学的理念及方法。在水相介质体系下,由于电化学活性位点(如金属氧化物表面)处于高电势下,电催化氧化醇类物质主要生成羧酸类物质。如前所述,在纯金属电极或是金属氧化物电极下,若想醇类物质氧化为醛类物质后不发生进一步的氧化,可以选用二元相介质体系。或是让选择性电催化氧化氧化醇类物质转化为相应醛类物质的反应在较低电位下进行。相关研究发现:采用欠电位吸附(Under Potential Deposition, UPD)原子和不可逆吸附(Irreversible Deposition, IRD)原子修饰纯金属电极,可改变纯金属电极表面的组成和结构,从而改变纯金属电极的催化活性。比如,由于有一些毒化过程会使贵金属电极在低电势下失活,该失活电极能够通过外来吸附原子的UPD效应而被重新活化。K. B. Kokoh和E. M. Belgsir [41] 研究发现Pb原子的UPD效应也十分明显,能够在Pt电极下的电催化氧化各种醇类物质生成醛类物质的反应中产生明显效果,特别是电极处于低电位的情况。他们也报道了欠电位铅吸附原子修饰铂电极(Pt/Pb)下,控制DHMF电催化氧化时的电位,获得了DFF产品。这表明:Pt/Pb电催化氧化方法具有可行性和有效性。在该电极下需控制电位条件从而能选择性转化醇类物质中醇基官能团为相应的醛基。未来通过调整该电催化氧化过程的工艺条件并设计适宜的电化学反应器有望使该非均相电催化氧化技术获得新的应用。
4. 结论与展望
2,5-二甲酰基呋喃(DFF)是一种重要的多功能有机中间体。用于制备DFF的化学催化氧化法,对环境污染大。电化学催化氧化法利用电化学反应的优势,是一种清洁氧化技术。电催化氧化技术中电子转移只在电极和反应组分之间进行,无需外加氧化还原剂,可避免由于添加额外试剂导致的二次污染。一般通过改变外加电流和电压来随时调节反应条件,可控性较强。反应条件温和,一般都是在常温常压下进行反应。反应设备及其操作一般比较简单,如果设计合理,费用并不昂贵。此外,将该法应用于将DHMF转化为DFF的反应时,若设计反应条件得当,可以高选择性和高收率获得目标产物DFF,而且以DHMF为原料时具有成本优势且具有比HMF更为理想稳定性。
目前,对该技术的研究需解决的难点问题主要包括以下方面:电催化氧化机理还不是很明确,对电极的选择、工艺的设计以及工艺参数的确立问题比较难。另外,该法的电流效率并不是很高,如何提高经济效率是一个亟待解决的问题。因而今后有关这方面的研究需着力解决以下问题:在工艺设计方面,应当设计时空效率高、能耗低的电催化氧化反应体系,提高电流效率、降低电耗,从而利于其的实用化。在有机分子电催化合成反应中,电极材料的选择是至关重要的影响因素之一。不同的电极材料可生成不同产物。因此,在反应过程中选择合适的电极材料也具有十分重要的意义。在电极材料方面,需要合成高电催化活性的电极材料。实际操作过程中需分析影响电催化氧化的关键因素,改善工艺条件从而高效制得目标产品。
致谢
厦门市科技局重大科技平台项目(3502Z20131016)、973计划项目(2010CB732201)、国家自然科学基金项目(21106121)和福建省科技厅产学研重大项目(2013N5011)。
文章引用
张盛强,李维烽,林鹿. 修饰电极上选择性电催化氧化制备2,5-二甲酰基呋喃
Preparation of 2,5-Diformylfuran
through Selective Electro-Catalytic
Oxidation with Modified
Metallic Electrodes[J]. 可持续能源, 2014, 04(03): 31-39. http://dx.doi.org/10.12677/SE.2014.43006
参考文献 (References)
- 1. Corma, A., Iborra, S. and Velty, A. (2007) Chemical routes for the transformation of biomass into chemicals. Chemical Reviews, 107, 2411-2502.
- 2. Alonso, D.M., Bond, J.Q. and Dumesic, J.A. (2010) Catalytic conversion of biomass to biofuels. Green Chemistry, 12, 1493.
- 3. Gallezot, P. (2012) Conversion of biomass to selected chemical products. Chemical Society Reviews, 41, 1538-1558.
- 4. Roman-Leshkov, Y., Chheda, J.N., Dumesic, J.A. (2006) Phase modifiers promote efficient production of hydroxymethylfurfural from fructose. Science, 312, 1933-1937.
- 5. Zhao, H., Holladay, J.E., Brown, H., et al. (2007) Metal chlorides in ionic liquid solvents convert sugars to 5-hydroxymethylfurfural. Science, 316, 1597-1600.
- 6. Stahlberg, T., Fu, W.J., Woodley, J.M., et al. (2011) Synthesis of 5-(hydroxymethyl) furfural in ionic liquids: paving the way to renewable chemicals. ChemSusChem, 4, 451-458.
- 7. Rosatella, A.A., Simeonov, S.P., Frade, R.F.M., et al. (2011) Hydroxymethylfurfural (HMF) as a building block platform: Biological properties, synthesis and synthetic applications. Green Chemistry, 13, 754-793.
- 8. Tong, X.L., Ma, Y. and Li, Y.D. (2010) Biomass into chemicals: Conversion of sugars to furan derivatives by catalytic processes. Applied Catalysis A: General, 385, 1-13.
- 9. Koopman, F., Wierckx, N., de Winde, J.H., et al. (2010) Efficient whole-cell biotransformation of 5-(hydroxymethyl) furfural into FDCA, 2,5-furandicarboxylic acid. Bioresource Technology, 101, 6291-6296.
- 10. Zhao, Q., Wang, L., Zhao, S., et al. (2011) High selective production of 5-hydroymethylfurfural from fructose by a solid heteropolyacid catalyst. Fuel, 90, 2289-2293.
- 11. Yang, Y., Hu, C.W. and Abu-Omar, M.M. (2012) Conversion of carbohydrates and lignocellulosic biomass into 5-hydroxymethylfurfural using AlCl3•6H2O catalyst in a biphasic solvent system. Green Chemistry, 14, 509-513.
- 12. Hui, Z. and Gandini, A. (1992) Polymeric schiff bases bearing furan moieties. European Polymer Journal, 28, 14611469.
- 13. Hopkins, K.T., Wilson, W.D., Bender, B.C., et al. (1998) Extended aromatic furan amidino derivatives as anti-pneumocystis carinii agents. Journal of Medicinal Chemistry, 41, 3872-3878.
- 14. Richter, D.T. and Lash, T.D. (1999) Oxidation with dilute aqueous ferric chloride solutions greatly improves yields in the “4+1” synthesis of sapphyrins. Tetrahedron Letters, 40, 6735-6738.
- 15. del Poeta, M., Schell, W.A., Dykstra, C.C., et al. (1998) In vitro antifungal activities of a series of dication-substituted Carbazoles, furans, and benzimidazoles. Antimicrobial Agents and Chemotherapy, 42, 2503-2510.
- 16. Amarasekara, A.S., Green, D. and Williams, L.D. (2009) Renewable Resources Based Polymers: Synthesis and Characterization of 2,5-diformylfuran-urea Resin. European Polymer Journal, 45, 595-598.
- 17. Gupta, N.K., Nishimura, S., Takagaki, A. and Ebitani, K. (2011) Hydrotalcite-supported gold-nanoparticle-catalyzed highly efficient base-free aqueous oxidation of 5-hydroxymethylfurfural into 2,5-furandicarboxylic acid under Atmospheric oxygen pressure. Green Chemistry, 13, 824.
- 18. Lilga, M.A., Hallen, R.T. and Gray, M. (2010) Production of oxidized derivatives of 5-hydroxymethylfurfural (HMF). Topics in Catalysis, 53, 1264-1269.
- 19. Navarro, O., Canós, A. and Chornet, S. (2009) Chemicals from biomass: Aerobic oxidation of 5-hydroxymethyl-2-furaldehyde into diformylfurane catalyzed by immobilized vanadyl-pyridine complexes on polymeric and organofunctionalized Mesoporous supports. Topics in Catalysis, 52, 304-314.
- 20. Carlini, C., Patrono, P., Galletti, A.M.R., Sbrana, G. and Zima, V. (2005) Selective oxidation of 5-hydroxymethyl-2furaldehyde to furan-2,5-dicarboxaldehyde by catalytic systems based on vanadyl phosphate. Applied Catalysis A: General, 289, 197-204.
- 21. Moreau, C., Durand, R., Pourcheron, C. and Tichit, D. (1997) Selective oxidation of 5-hydroxymethylfurfural to 2,5furan-dicarboxaldehyde in the presence of titania supported Vanadia Catalysts. Studies in Surface Science and Catalysis, 108, 399-406.
- 22. Ma, J.P., Du, Z.T., Xu, J., Chu, Q. and Pang, Y. (2011) Efficient aerobic oxidation of 5-hydroxymethylfurfural to 2,5-diformylfuran, and synthesis of a fluorescent material. ChemSusChem, 4, 51-54.
- 23. Takagaki, A., Takahashi, M., Nishimura, S. and Ebitani, K. (2011) One-pot synthesis of 2,5-diformylfuran from carbohydrate derivatives by sulfonated resin and hydrotalcite-supported ruthenium catalysts. ACS Catalysis, 1, 15621565.
- 24. Yang, Z.Z., Deng, J., Pan, T., Guo, Q.X. and Fu, Y. (2012) A One-pot approach for conversion of fructose to 2,5-diformylfuran by combination of Fe3O4-SBA-SO3H and K-OMS-2. Green Chemistry, 14, 2986-2989.
- 25. Xiang, X., He, L., Yang, Y., Guo, B., Tong, D. and Hu, C. (2011) A one-pot two-step approach for the catalytic conversion of glucose into 2,5-diformylfuran. Catalysis Letters, 141, 735-741.
- 26. Saha, B., Dutta, S. and Abu-Omar, M.M. (2012) Aerobic oxidation of 5-hydroxylmethylfurfural with homogeneous and nanoparticulate catalysts. Catalysis Science & Technology, 2, 79.
- 27. van Deurzen, M.P.J., van Rantwijk, F. and Sheldon, R.A. (1997) Chloroperoxidase-catalyzed oxidation of 5-hydroxymethylfurfural. Journal of Carbohydrate Chemistry, 16, 299-309.
- 28. 冯晓娟, 石彦龙, 王永生, 敏世雄, 胡中爱 (2011) 铂-氧化铈/聚苯胺/聚砜复合膜电极的制备及对甲醇的电催化氧化. 应用化学, 3, 302-307.
- 29. 郝玉翠, 葛伟青, 刘艳娟 (2012) 电极材料在电催化氧化处理有机废水中的应用. 化学工程师, 1, 35-37.
- 30. 杨佳佳, 魏树权, 邓超, 高颖, 邬冰 (2011) 甲酸在Pd-Ru/C催化剂上的电催化氧化. 黑龙江大学自然科学学报, 1, 81-84.
- 31. 刘春涛, 孙雍荣, 谷宇, 王阔, 杜春雨 (2011) Pt/CeO2/CNTs催化剂对甲醇电催化氧化的研究. 中国稀土学报, 5, 533-537.
- 32. 戴启洲, 蔡少卿, 王家德, 陈建孟 (2010) 电催化氧化/生物法联用处理高浓度化工废水. 中国给水排水, 12, 9699.
- 33. 林珩, 陈声培, 林进妹, 林爱兰, 黄如莺, 陈国良 (2003) 1,4-丁二醇在Pt及其修饰电极上吸附氧化过程研究. 分子科学学报: 中英文版, 3, 159-165.
- 34. 杨宏洲, 邓友全 (2002) Au/PAni/GC 电极的制备及对甲醛的电催化氧化研究. 化学学报, 4, 569-573.
- 35. 陈国良, 林珩, 卢江红, 林进妹, 林秀梅, 陈燕鑫 (2004) 4 种有机小分子伯醇在Pt电极上吸附和氧化的比较研究. 漳州师范学院学报 (自然科学版), 4, 71-74.
- 36. 褚道葆, 吴晟, 张雪娇, 肖英, 周莹 (2010) 4-甲基吡啶在 Ti/nanoTiO2-Pt 电极上的电催化氧化. 安徽师范大学学报: 自然科学版, 2, 139-143.
- 37. 王益凡 (2004) Pt电极上Sb吸附原子对 1,3-丁二醇电催化氧化性能的影响. 上海大学学报: 自然科学版, 4, 406409.
- 38. Skowroński, R., Cottier, L., Descotes, G. and Lewkowski, J. (1996) Selective anodic oxidation of 5-hydroxymethylfurfural. Synthesis, 1996, 1291-1292.
- 39. Grabowski, G., Lewkowski, J. and Skowroński, R. (1991) The electrochemical oxidation of 5-hydroxymethylfurfural with the nickel oxide/hydroxide electrode. Electrochimica Acta, 36, 1995.
- 40. Al Baradii, A., Kokoh, K.B., Huser, H., Lamy, C. and Léger, J.M. (1999) Selective electrocatalytic oxidation of 2,5dihydroxymethylfuran in aqueous medium: A chromatographic analysis of the reaction products. Electrochimica Acta, 44, 2779-2787.
- 41. Kokoh, K.B. and Belgsir, E.M. (2002) Electrosynthesis of furan-2,5-dicarbaldehyde by programmed potential electrolysis. Tetrahedron Letters, 43, 229-231.
- 42. Vuyyuru, K.R. and Strasser, P. (2012) Oxidation of biomass derived 5-hydroxymethylfurfural using heterogeneous and electrochemical catalysis. Catalysis Today, 195, 144-154.
- 43. Hibbitts, D.D. and Neurock, M. (2013) Influence of oxygen and pH on the selective oxidation of ethanol on Pd catalysts. Journal of Catalysis, 299, 261-271.
*通讯作者。
