Advances in Geosciences
Vol.07 No.03(2017), Article ID:20969,13
pages
10.12677/AG.2017.73037
Mechanism and Factors Influencing Copper Isotopic Fractionation: A Review
Jing Ji*, Haixiang Zhao#
School of Earth Sciences and Engineering, Hohai University, Nanjing Jiangsu
Received: May 27th, 2017; accepted: Jun. 12th, 2017; published: Jun. 15th, 2017

ABSTRACT
In recent years, copper isotopes have been widely used in geology, archaeology, biology and so on. The research on the fractionation mechanism and influencing factors of fractionation is the basis of the application. This paper summarizes the fractionation mechanism and influencing factors of copper isotopic composition during ore forming and rock forming process, biochemical and soil- forming progress in supergene environment, including temperature, pH value, redox progress etc. Moreover, the prospect of copper isotopes application in ore deposit geochemistry, geochemical engineering and other fields is also expounded.
Keywords:Cu Isotopes, Fractionation Mechanism, Influencing Factors
铜同位素分馏机理及影响因素研究综述
嵇静*,赵海香#
河海大学地球科学与工程学院,江苏 南京
收稿日期:2017年5月27日;录用日期:2017年6月12日;发布日期:2017年6月15日

摘 要
近年来,铜同位素在地质、考古、生物等方面有了广泛的应用,对其分馏机理及分馏影响因素的研究是应用的基础。本文总结了铜在成岩成矿过程和表生环境下生物过程和风化成土过程中的分馏机理及分馏过程中的影响因素,包括温度、pH值、氧化还原作用等。并阐述了铜同位素在矿床地球化学、地球化学工程学等领域的应用前景。
关键词 :铜同位素,分馏机理,影响因素

Copyright © 2017 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
Cu是重要的成岩成矿元素,主要以Cu0、Cu+、Cu2+价态形式,存在于各类矿物、岩石、流体和生物体中,不同价态和相态Cu的稳定性不同,这也让Cu在流体活动、成岩成矿和生命活动过程中等呈现不同的特征 [1] [2] [3] 。自然界中Cu有两个稳定同位素:63Cu和65Cu,丰度分别为:69.17%和30.83%。铜同位素组成的表示方法一般用待测样品的铜同位素比值与标准物质的铜同位素比值δ表示 [4] 。δ65Cu = [(65Cu/63Cu)样品/(65Cu/63Cu)标准物质 − 1] × 103。对于分馏较小的样品也可采用万分偏差ε65Cu = [(65Cu/63Cu)样品/ (65Cu/63Cu)标准物质 − 1] × 104。Cu标准溶液一般选用美国国家标准局的NIST SRM 976 Cu,其中65Cu/63Cu = 0.4456 ± 0.0004 [5] 。目前该标样不断减少,新的实验室标准物质ERM-AE633、ERM-AE647也在推广使用 [2] [6] 。Cu分布于地球各个圈层中,目前δ65Cu的总体分布范围为−16.49‰~24.4‰ [7] [8] ,但是大多数最初岩浆硫化物中的变化范围却很窄 [9] [10] 。如此大的铜同位素分布范围为不同领域应用铜同位素分析问题提供了可能。比如在斑岩—矽卡岩型铜矿床的成岩成矿过程中,受沉淀作用影响,残余流体相对于硫化物沉淀会愈加富集65Cu,所以此类沉淀的矿床常会呈现随时间在水平空间位置上的分带性。这一规律也在具体矿床研究中有所体现,展现了铜同位素组成具有良好的示踪流体迁移路径的功能。
对铜同位素分馏的研究主要是从离子交换树脂实验中发现的。Marechal等(1999)首先发现洗脱溶液的过程中,阴离子交换树脂上优先保留63Cu;Marechal等(2002)又具体用离子交换树脂(AG-MP1)分离溶液中的铜,结果仍然表明63Cu优先吸附在树脂上,并得出了树脂与溶液之间的平衡分馏系数α ≈ 1.0004 [4] [11] 。该过程产生分馏的原因主要是因为相对于Cu的重同位素,Cu的轻同位素容易与有机树脂相形成有机配合物从而吸附在树脂上 [12] 。铜同位素在树脂和溶液的分馏过程中主要是通过氯络合物形式进行活动,所以实验中常选用HCl作为洗脱液。具体实验中使用的HCl浓度以及洗脱出溶液中铜的时间等,都是学者们通过实验不断总结得出的。如Marechal等(2002)分别用HCl和HNO3洗脱AG-MP1树脂时发现HCl洗脱产生的铜同位素分馏较大,而HNO3基本不产生分馏,并得出吸附在树脂上和溶液中的63Cu/65Cu的质量分馏系数α随着HCl浓度的减小而增加 [11] 。Zhu等(2002)用阴离子交换树脂(AG-MP1)进行离子交换实验和6 mol/L的HCl溶液进行洗脱实验中同样发现树脂柱相对富集63Cu;铜同位素的富集主要是以铜的氯络合物形式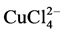 进行交换 [13] 。
进行交换 [13] 。
Cu的生物有效性、迁移性以及毒性都与Cu在溶液中的元素形态密切相关。铜既在植物的蛋白质合成、细胞膜活动、光合作用以及新陈代谢中起重要作用,也可以用来改善缺乏微量营养元素的土壤。但是随着Cu浓度的积累,会对植物的染色质等产生强烈影响,从而影响植物的光合作用、生长及老化过程 [14] 。如Navarrete等(2011a)在研究中就发现当铜达到一定浓度时,植物的发芽率明显下降,这可能就是受到了重金属毒性影响 [15] 。Weinstein等(2011)在不添加外部Cu的实验条件下发现扁豆的幼苗和发芽的种子之间发生了同位素分馏,这说明Cu在生物体中运移时会产生同位素分馏 [16] 。也有许多学者就动植物不同部位及其生长介质的铜同位素组成进行了研究,并取得了重要发现,本文后续内容将会介绍。但目前对植物的研究主要是同一植物的根、茎、叶、种子等对比研究,而比较不同植物收集的种子的同位素组成或者将种子和同一高度茎的同位素组成进行比较的实验还比较少。生物过程中,通常65Cu趋向富集于水溶液、土壤等生长介质中,63Cu会优先进入并富集于生物组织中。铜同位素的动力分馏可能是控制这一过程的重要因素,但Cu(II)还原成Cu(I)的反应同样也起了重要作用 [13] [15] [17] 。氧化还原作用是影响铜同位素分馏的重要影响因素之一,通常还原过程易发生负分馏,氧化过程易发生正分馏。如在共生矿物对中,通常氧化态越高越富集65Cu;处于氧化环境下的浅生矿床常以65Cu(II)形式运移为主。所以也有许多学者研究表明,在硫化物矿物风化过程中,Cu(I)氧化成Cu(II)是一些天然地表水富集65Cu的重要影响因素 [18] 。同样,自然水体中生物细胞和土壤中植物的生物过程产生的铜同位素分馏也达到一定数量级,所以其对水体和土壤等铜同位素组成的背景值有着不可忽视的影响。
与其它稳定同位素体系相同,铜同位素分馏主要包括由同位素交换引起的热力学分馏,以及在物理、化学与生物过程中因扩散速度和反应速度不同而引起的动力学分馏。质量差异是造成铜同位素发生分馏的根本原因,因为质量差异会造成同位素之间物理化学性质(如键强、自由能、热力学势、熵等)的差异,导致在可逆或平衡的化学反应中,以及溶解与结晶,吸附与解吸,凝聚与蒸发,扩散等物理作用过程中,都会发生同位素分馏。同时同位素所在体系的pH值、氧逸度、温度和离子浓度等因素也会影响同位素分馏的方向。本文我们就目前铜同位素分馏机制和过程在理论、实验以及应用中取得的进展进行综述。
2. 成岩成矿过程中铜同位素分馏
如今,在示踪铜矿床的成矿物质来源时,越来越多的学者开始通过直接分析Cu、S同位素代替传统的Pb、S同位素。实践证明,不同成矿阶段下Cu同位素的示踪效果更易分析和可靠 [19] 。随着研究的深入,铜同位素在不同条件下的分馏规律也不断呈现,这对于示踪铜矿床成矿物质、反演成矿流体的迁移方向、分析成矿机理有一定帮助。目前,铜同位素研究的矿床类型主要有斑岩型、矽卡岩型、热液型、岩浆矿床、块状硫化物矿床、沉积矿床等 [10] [20] [21] [22] [23] 。发表的数据主要有与岩浆岩有关的高温热液矿床中的黄铜矿、表生条件下的自然铜和铜的碳酸盐(孔雀石、蓝铜矿)、大洋黑烟囱硫化物矿床中的黄铜矿、低温热液脉状铜矿床 [24] 。据统计,矿床中不同含Cu矿物的Cu同位素组成δ65Cu的变化范围为−3.70‰~7.32‰,平均值约为0.13‰ ± 2.27‰ [7] [21] 。黄铜矿等硫化物的铜同位素是研究成岩成矿过程中的重要对象,研究表明黄铜矿是最早从成矿流体中结晶出的Cu矿物相,它可以用来反推初始流体的铜同位素特征 [25] 。成岩成矿是一个复杂的过程,所以影响其铜同位素分馏的因素也众多。
如上所述,影响铜同位素分馏的内在因素无非是同位素质量差异导致的矿物晶格能或者键强之间的差异,从而使共生矿物之间发生铜同位素分馏,如Larson等(2003)研究发现,浅生矿床环境中,赤铜矿的Cu同位素比值明显高于相关的自然铜。不同样品中黄铜矿的δ65Cu值都高于共生的斑铜矿 [26] 。杨立飞等(2016)在研究金满铜矿时同样发现,同一成矿阶段中,黄铜矿比共生矿物斑铜矿更加富集65Cu [19] 。刘文元等(2015)研究发现紫金山原生矿石中铜矿物的铜同位素组成具有类似的特征:斑铜矿 < 黄铜矿,斑铜矿 < 蓝辉铜矿 < 铜蓝 [27] 。而随着氧化还原环境、温度、pH值、溶液浓度等外在条件的改变,铜可以赋存在气相、液相、固相中,也可以是Cu0、Cu+、Cu2+中的任意价态,不同相态和价态的Cu富集的轻重同位素不同。以下将对近年来研究比较多的几大因素进行归纳阐述。
2.1. 氧化还原作用
由于铜是变价元素,氧化和还原环境的转变过程会影响铜同位素的分馏,且氧化还原作用是影响铜同位素分馏最重要的作用,这已经被很多研究所证实。通常氧化还原作用下,还原过程易发生负分馏,氧化过程易发生正分馏。如处于氧化环境下的浅生矿床常以65Cu(II)形式运移为主。Asael等(2007)研究Timna层状沉积岩型铜矿床就发现由于受氧化还原影响,含铜硫化物样品的δ65Cu值(−3.40‰~−1.2‰)明显低于共存的Cu(II)的碳酸盐、氢氧化物(−1.2‰~0.5‰) [28] 。Haest等(2009)研究Dikulushi的Cu-Pb-Zn-Fe和Cu-Ag矿床也发现来自深部矿床的Cu(I)硫化物比浅生矿床中Cu(II)的碳酸盐和硅酸盐铜同位素组成低2.7‰~3.5‰;氧化环境下含Cu矿床的再活化也会引起65Cu的再富集 [29] 。这些差异在一定程度上可以用来判别原生深成矿床、原生浅生矿床、深成再活化矿床。赵海香等(2015)在对福建紫金山矿田样品的铜同位素研究中同样发现共生矿物铜蓝样品相对于蓝辉铜矿样品富65Cu,这主要是因为铜蓝的氧化态高于蓝辉铜矿 [30] 。这与Larson等(2003)研究发现高价态化合物中易富集65Cu,低价态化合物易富集63Cu一致 [26] 。
Asael等(2009)年通过Eh-pH流体形态图关联Timna和Kupferschiefer两个沉积岩型铜矿床的铜同位素组成,发现Timna矿床中含铜硫化物样品的δ65Cu值为−2.04‰ ± 0.44‰,对应当T = 40℃,pH < 6的形成条件下,氧化还原电位Eh值为0.5~0.6 V,该值表明含铜硫化物样品在相对氧化条件下沉淀,溶液中Cu以Cu(II)的氯络合物形式存在为主,溶液中Cu(II)还原为Cu(I)的过程中发生明显的负分馏;Kupferschiefer中含铜硫化物的δ65Cu值为−0.39‰ ± 0.36‰,对应当T = 100℃,pH = 6.3的形成条件下,Eh值为0.4~0.5 V,该值表明溶液中Cu以Cu(I)形式络合物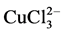 为主,大部分样品在相对还原条件下沉淀,未发生氧化还原作用,分馏小,接近岩浆铜的同位素值 [31] 。该分析与Kupferschiefer矿床中矿物以Cu的硫化物为主,而Timna矿床中Cu(II)矿物多于硫化物的现象一致。这一研究结合铜同位素组成从热力学角度分析沉积型铜矿床中不同硫化铜形成过程中的氧化还原条件,丰富了铜同位素的研究思路。
为主,大部分样品在相对还原条件下沉淀,未发生氧化还原作用,分馏小,接近岩浆铜的同位素值 [31] 。该分析与Kupferschiefer矿床中矿物以Cu的硫化物为主,而Timna矿床中Cu(II)矿物多于硫化物的现象一致。这一研究结合铜同位素组成从热力学角度分析沉积型铜矿床中不同硫化铜形成过程中的氧化还原条件,丰富了铜同位素的研究思路。
2.2. 温度
温度是铜同位素分馏的一大重要因素。理论上来说,分馏系数与温度呈负相关关系,即温度越高,分馏越小。低温条件下铜同位素分馏往往较大。Ehrlich等(2004)在不同温度下进行CuSO4和Na2S生成CuS沉淀的实验同样表明分馏值随温度的增加而减小,并得出了两者之间的关系式: 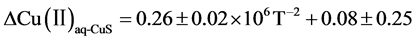 [32] 。Zhu等(2000)研究发现火成岩中黄铜矿的Cu同位素组成变化较小;而形成时受到相对低温水溶液影响的自然铜、碳酸盐、黑烟囱中黄铜矿样品Cu同位素组成变化则较大 [20] 。蒋少涌等(2001)发现云南金满低温热液脉状铜矿床中含铜硫化物的δ65Cu值为−3.70‰~0.30‰,与高温岩浆热液矿床(δ65Cu为−0.62‰~0.40‰)和大洋底块状硫化物矿床(δ65Cu为−0.48‰~1.15‰)相比,明显偏负且分馏较大 [21] 。
[32] 。Zhu等(2000)研究发现火成岩中黄铜矿的Cu同位素组成变化较小;而形成时受到相对低温水溶液影响的自然铜、碳酸盐、黑烟囱中黄铜矿样品Cu同位素组成变化则较大 [20] 。蒋少涌等(2001)发现云南金满低温热液脉状铜矿床中含铜硫化物的δ65Cu值为−3.70‰~0.30‰,与高温岩浆热液矿床(δ65Cu为−0.62‰~0.40‰)和大洋底块状硫化物矿床(δ65Cu为−0.48‰~1.15‰)相比,明显偏负且分馏较大 [21] 。
虽然高温过程中铜同位素组成变化范围明显小于低温状态,但也会发生一定程度的分馏。如黄建等(2015)人发现蚀变洋壳中高温热液蚀变的玄武岩和辉长岩样品的δ65Cu (−0.50‰~0.90‰)变化范围明显大于低温(<250˚C)热液蚀变的玄武岩样品的δ65Cu (0.08‰ ± 0.10‰) [33] 。斑岩高温成矿过程中,硫化物和蒸汽、溶液之间同样会出现Cu同位素分馏,如气液分离过程、沸腾和硫化物沉淀过程。王跃等测量铜陵冬瓜山斑岩–矽卡岩型矿床中硫化物的δ65Cu变化范围为−0.54‰~0.95‰ [22] 。Li等(2010)在研究Northpark高温斑岩型Cu-Au矿床中测得其硫化矿物样品的δ65Cu (−1.67‰~0.85‰)相比于测试的其它同位素具有明显的分馏和变化特征,如高品位中心的δ65Cu集中在0.2‰左右,而低品位外围蚀变带到矿化带最边缘的δ65Cu从0.8‰降低到了−0.4‰ [10] 。这说明成矿过程中随着时间的流逝,温度等物化条件变化,铜同位素具有一定的空间分布特性。那么,分析不同阶段铜同位素的空间分布特征也有助于反演成矿过程。
2.3. 介质流体的性质
成矿流体可以使气相,也可以是液相。不同相态优先富集Cu的不同同位素。有学者提出受气液分离作用影响,早期深部热液在高温高压下以低密度富气相流体出溶为主,63Cu优先进入气相中,所以早期形成的矿脉相对于晚期富集轻同位素63Cu [34] 。李振清等(2009)研究西藏驱龙斑岩铜矿时的数据也说明了该现象,即高压作用下,早期富气相流体形成的矿脉的δ65Cu集中在−0.44‰~−0.31‰,相对富集63Cu;之后形成的矿脉的δ65Cu集中在−0.25‰~−0.18‰,相对早期亏损63Cu;而晚期δ65Cu集中在−0.27‰~−0.05‰,平均值为−0.02‰,铜同位素组成明显升高,一方面是因为流体中63Cu不断减少,另一方面可能也与富65Cu的大气降水的混入有关 [34] [35] 。王鹏等(2015)分析云南红牛矽卡岩铜矿时发现:与成矿母岩二长斑岩相比,斑岩的全岩铜同位素相对矽卡岩带明显富集铜的重同位素65Cu [23] 。这可能是成矿早期铜主要以气态形式在岩体中搬运有关,而轻同位素63Cu优先进入气相,随气态迁移至矽卡岩带。
2.4. 沉淀作用
受沉淀作用影响,硫化物从流体沉淀的过程中,其沉淀相对于残余流体更加富集63Cu。Ehrlich等(2004)在室温和缺氧条件下,进行了CuSO4和Na2S生成CuS沉淀的实验,结果表明残余溶液(aq)中的铜同位素组成相对于沉淀更富集65Cu (Δ65Cu(Cu(II)aq-CuS) = 3.06‰ ± 0.14‰) [32] 。即当以沉淀作用为主时,随着流体的不断外迁和硫化物的沉淀,残余流体中的65Cu也愈加富集,沉淀出的矿物也越来越富集65Cu。实际调查研究结果与实验理论相符合,如王跃等(2014)研究铜陵冬瓜山斑岩–矽卡岩型矿床中发现从岩体到矿体,其空间分布上出现明显的分带性;随着远离岩体,后期沉淀的黄铜矿中相对富集65Cu [22] 。王鹏等(2015)分析云南红牛矽卡岩铜矿中黄铜矿和石英二长斑岩样品时同样发现同一矿体的水平位置上,从早期形成的矽卡岩矿体到晚期的硫化物矿石再到围岩中的黄铜矿颗粒,铜同位素组成逐渐变重 [23] 。许多矿床都呈现出类似变化,说明黄铜矿等矿物的铜同位素的组成具有反演铜矿床成矿流体的迁移方向的潜力。
2.5. 交代重结晶作用
成矿早期的硫化物容易受到后期成矿流体的叠加改造和氧化蚀变作用,使得铜同位素组成发生一定改变。如Zhu等(2000)在研究海底硫化物中发现与活跃的高温热液喷口相比,古老不活跃的沉积口相对富集63Cu,且铜同位素值变化范围相对较窄。在同一活跃烟囱中,底部相对于顶部富集轻铜同位素63Cu [20] 。吴仲玮等(2013)同样发现中印度洋脊相邻热液活动区硫化物和热液样品中停止喷发的古老烟囱中以黄铜矿为主的Cu硫化物相对于活跃期的高温热液喷口相对富集63Cu;经历交代重结晶的热液区硫化物的铜同位素组成呈现负δ65Cu特征 [36] 。Liu等(2015)调查研究发现,经过交代的橄榄岩的δ65Cu平均值与未经交代的橄榄岩(0.03‰ ± 0.24‰)相比偏重;且经过交代的橄榄岩的δ65Cu变化范围(−0.64‰~1.82‰)较大 [37] 。在低温结晶过程中,65Cu更容易进入到结晶相中从而使得Cu同位素发生分馏。李津等(2008)发现向过饱和的CuSO4溶液中加入小于0.5 mm的CuSO4∙5H2O晶核,平衡后结晶出的晶体(约6 mm)相对于残余溶液更加富集重Cu同位素,Δ65Cu晶体-溶液 = 0.17‰ ± 0.02‰ [38] 。
3. 表生环境中铜同位素的分馏
表生环境中元素的迁移循环与人类生活息息相关。铜元素在自然系统循环过程中,尤其是氧化还原过程、风化淋滤过程、吸附/解吸附过程、生物过程等会产生明显的铜同位素分馏。本文主要从岩石、土壤、生物及水系统界面分析阐述影响铜同位素分馏的主要因素。
3.1. 生物–土壤/溶液等生长介质界面的Cu同位素分馏
铜元素是生物体内必不可少的微量元素之一,但随着土地大规模的开发使用,铜污染很容易影响周边河流水质、土壤和植物生长,动植物中的重金属元素在食物链中不断累积。研究铜同位素分馏可以为植物提供适量的微量营养元素、控制污染、保障土壤可持续发展等提供更多依据。目前对生物过程中影响铜同位素的分馏因素的研究主要有:生物组织的选择性、氧化还原作用、络合作用、pH值的影响等。
3.1.1. 生物组织选择性吸收
细菌细胞和蛋白质通常来说优先摄取轻的铜同位素 [13] [16] [17] [39] 。Zhu等(2002)用天青蛋白分别从体内和体外摄取已知来源的铜的实验表明其原始溶液中明显亏损63Cu,发现63Cu会优先被细胞摄取而发生优先运移 [13] 。从而发现生物体具有选择性吸收功能。
高等植物通常优先从土壤中吸收铜的轻同位素 [15] [16] [40] 。生物体中Cu同位素质量分馏是沿着生物路径逐步进行的,即铜等元素在生物体中的运移具有一定的方向性,因此植物的不同部位也会发生铜同位素分馏。武贝等(2009)在研究具有较高铜含量的植物——海州香藿中发现,从新生叶片到成熟叶片到老叶,65Cu/63Cu同位素比值增加率明显降低 [41] 。李世珍等(2009)同样发现海州香藿的根茎叶部位存在明显的铜同位素分馏,其茎部位相对于根和叶富集63Cu [39] 。Navarrete (2010a)等研究金属累积的沙漠植物毛竹的结果同样表明63Cu优先进入植物的叶子,这可能是由于细胞内蛋白的主动运移 [15] 。Weinstein等(2011)同样发现其研究的单叶子植物和双叶子植物样品相对于土壤等生长介质富集63Cu,而且单叶子植物的铜同位素呈现种子 < 叶子 < 茎 < 土壤一定随高度变化的特征 [16] 。目前这类能富集重金属的植物如能富集铜的海州香藿、鸭拓草等已经被运用到矿区污染修复和植被修复中,同时微生物等修复方法也在不断开发研究中。
Bigalke等(2010)研究发现富集有机质的土壤层的δ65Cu轻于无机质层 [42] 。Bigalke等(2011)在研究不同土壤层的铜同位素特征仍表明:有机质层平均δ65Cu值(−0.12‰),明显轻于有机层下的矿质表层土壤样品(0.13‰) [43] ,这也从侧面说明在土壤–植物–土壤转移中出现了铜同位素分馏,植物中应该相对富集轻铜同位素,当然也有可能是大气沉积物中63Cu。Weinstein等(2011)研究同样证明了这一点,而且实验结果表明植物引起的铜同位素分馏与土壤中观察到的分馏在同一量级上,所以由植物引起的铜同位素分馏也应作为影响土壤铜同位素的原因之一 [16] 。
3.1.2. 氧化还原作用
氧化还原作用主要包括生物体内的氧化还原和生物体所处的氧化还原环境。在细菌、植物、动物等生物体中,通常是通过酶来结合、运移和储存Cu进而改变细胞内的Cu浓度,该过程中酶也会将Cu(II)还原成Cu(I) [15] 。而在细菌、酵母、植物和人类生物体中有大量结构性和功能性的金属蛋白贮存,所以Cu(II)还原成Cu(I)可能是控制生物系统中铜同位素的一种普遍因素。例如,Zhu等(2002)在含CuSO4的培养液中培养好的酵母菌中分别提取铜的金属硫蛋白和铜锌超氧化物歧化酶,结果发现二者都富集63Cu,但金属硫因蛋白更富集63Cu;Cu在培养液中以Cu2+的形式存在,而在金属硫蛋白中呈Cu+,在超氧化物歧化酶中呈Cu+和Cu2+,这可能就是生物体中的氧化还原等作用会影响Cu同位素分馏 [13] 。目前,利用生物酶与Cu等重金属络合,从而修复重金属污染的土壤,也逐渐成为环境工程学的研究热点之一 [44] 。外部的氧化还原环境也会影响铜同位素分馏。如Jouvin等(2012)观测营养液中培植的番茄、小麦、稻等高等植物的Cu等同位素分馏结果表明,植物根部相对于土壤富集轻Cu,这可能是因为在根部细胞质膜表面发生了Cu(II)的还原反应 [40] 。
3.1.3. 络合作用
99.6%以上的Cu在植物木质部汁液中以络合物等复杂形式存在 [45] 。溶液和络合物中的Cu同位素分馏主要是因为振动频率和零点能的差异,如重同位素的振动频率较低,形成的分子键较强 [46] [47] 。Jouvin等(2012)用特定营养液培植高等植物实验中发现,当营养液中的配位体与金属阳离子具有高齿合度和高亲和度,且与Cu和Zn形成很强的共价键时,Cu和Zn与这些配位体形成的络合物会相对富集65Cu [40] 。Navarrete等(2010b)在研究中发现革兰氏阴性细菌—大肠杆菌细胞吸附Cu过程中,pH值在4.1~5.1时,受热致死的大肠杆菌细胞表面的Cu和有机酸功能团的络合作用表现出优先富集65Cu的特征 [17] 。但活细胞体内则优先富集63Cu,这说明该细胞吸附变化产生的铜同位素分馏的数量级远小于生物活动过程中产生的变化。所以具体研究中还需要考虑细胞内生物过程对自然水中δ65Cu变化的影响。
3.1.4. 背景介质的影响
介质溶液的盐度、pH值等也会影响铜同位素的分馏。随着溶液pH值的变化,铜的赋存形态不同,生物组织对铜元素的吸收和铜元素的活性和迁移能力都会其影响。Navarrete等(2011b)在研究细菌表面吸附和细胞内结合Cu的过程中,pH值为2~6.5,溶液中被吸附的Cu的比例随着pH值的增加而增加,这主要是因为随着pH值得增加,更多的细菌表面功能团位点变得去质子化,可以用来与Cu(II)反应 [17] 。通常酸性条件下Cu(II)与细菌表面形成的单齿配位键的键能较弱,所以微生物表面吸附铜同位素时易富集63Cu [48] 。而Cu大约在pH > 6.5时开始沉淀 [17] ,所以随着pH值的升高,溶液逐渐呈碱性,易形成Cu(OH)2沉淀,使得生物细胞壁对Cu离子的吸附量降低,从而影响铜同位素分馏。如Pokrovsky等(2008)在研究中发现中性溶液中,生长的好氧根际细菌(致黄假单胞菌)几乎没有分馏;而酸性溶液中(1.8 ≤ pH ≤ 3.3),会产生明显的分馏且活菌上的短期可逆吸附的铜同位素明显富集63Cu [49] 。武贝等(2009)对不同pH值(3~7)下海州香藿细胞壁对铜的吸附作用研究表明,细胞壁对Cu2+的吸附量随pH值由低到高而呈现出先增加后减少(pH > 6.0时逐渐减少)的趋势 [41] 。
生物过程中铜同位素分馏的程度同样受土壤性质的影响 [50] 。Navarrete等(2011a)进行毛竹对Cu的摄取实验表明,有效Cu含量也会影响铜同位素分馏的方向与量级 [15] 。李世珍等(2009)发现在不同土壤条件下培养的海州香藿,根茎叶的δ65Cu值不同 [39] 。说明重金属超富集植物体内的铜同位素分馏特征在一定程度上也能反应出当地的土壤条件。淡水、海水等不同背景下的溶液含铜浓度和铜同位素组成不同,生活在里面的生物体的铜同位素分馏自然也会受其影响。Pokrovsky等(2008)分析来自海生和淡水培养液中硅藻消化细胞吸附铜的数据表明:海生的浮游生物相对富集65Cu (Δ65Cu = 0.23‰± 0.05‰),而淡水中的分馏则不大(Δ65Cu = 0.0‰ - 0.1‰) [49] 。
3.2. 岩石–土壤–水系统中的Cu同位素分馏
3.2.1. 氧化还原过程
岩石风化成土过程中地表元素会发生重新分配,同时也会发生元素的同位素分馏。如Bigalke等(2011)发现在氧化条件下风化的矿质土壤剖面中,有机层下的矿质表层土壤样品的δ65Cu平均值明显高于底层± [43] 。这与Bigalke等(2010a)研究的在水成土中,该层δ65Cu值明显低于底土层的特征恰好相反 [42] 。这可能是由于水成土中底土层浸在水中时处于还原环境,引起土的pH值的改变、有机物质的释放、Fe的氧化物氢氧化物的减少和Cu的氧化还原态的变化,从而明显影响了δ65Cu的分布 [43] 。由此可见,不同形成环境下的矿质土壤中δ65Cu垂向土壤分布的不同,这说明Cu同位素在一定基础上具有示踪不同氧化还原环境下形成的土壤起源及元素运移的潜力。
通常,氧化作用易使含铜矿物相对富集65Cu;还原作用则使含铜矿物相对亏损65Cu。即65Cu倾向富集于高价态的铜矿物中。如Zhu等(2002)用I−将Cu2+还原成CuI的实验表明CuI沉淀相对于原始溶液富集63Cu;运用瑞利分馏分析发现:相对于原始溶液CuI沉淀和残余Cu2+溶液都逐渐富集重同位素,残余溶液中相对富集更多的65Cu [13] 。李津等(2008)在室温下进行了纯Zn粒置换CuCl2溶液中Cu的还原实验,其结果同样表明:生成的金属Cu相对于残余溶液更加富集63Cu,而且不同的反应程度,分馏程度也不同 [48] 。Ehrlich等(2004)在研究了缺氧条件下Cu(II)aq溶液还原为矿物铜蓝(CuS, with Cu(I))过程中平均铜同位素分馏值为3.06‰ ± 0.14‰,从Cu(II)到Cu(I)的还原作用是控制这一过程中铜同位素分馏的主要因素 [32] 。当含铜硫化物在表生淋滤过程中受到多期次氧化作用会使铜同位素发生明显分馏。比如吕逸文等(2015)研究多金属富集的黑色页岩发现:风化的页岩和硅质岩样品的δ65Cu变化范围−6.42‰~19.41‰远大于新鲜样品值(0.41‰ ± 0.10‰),而δ66Zn变化则不大 [51] 。这主要是因为风化淋滤过程中,页岩中含Cu硫化物受到多期次氧化还原作用,而锌同位素不受氧化还原影响。
3.2.2. 风化淋滤过程
一般来说,受表生风化淋滤影响,65Cu会优先进入淋滤液中。淋滤液中铜同位素组成特征对指示矿源与污染源、寻找次生富集矿区、监测修复区域环境质量等有着重要意义。目前,已有学者展开关于硫化物矿物或矿石、玄武岩、高岭土、页岩等岩石风化淋滤方面的研究 [3] [20] [27] [49] [51] [52] [53] [54] 。大批次硫化物淋滤实验结果表明:非生物影响情况下淋滤液相对于硫化物富集65Cu。这可能是由于淋滤过程中,在硫化物矿物表面会发生Cu(I)/Cu(II)的氧化还原反应,在酸性条件下,这些反应使得淋滤液富集铜的重同位素 [55] 。刘文元等(2015)调查分析福建紫金山铜金矿床样品的δ65Cu (−11.84‰~1.52‰),其中未经淋滤的原生矿石样品的δ65Cu集中在零值附近;δ65Cu的低值主要是经历表生氧化淋滤作用的铜矿物样品,如铜蓝和孔雀石 [27] 。随着不断的氧化淋滤作用,矿山上一些原生矿石(斑铜矿等)会逐渐转变成次生的铜蓝,淋滤作用下残留铜矿物和这类表生的铜蓝会相对亏损重铜同位素。Pérez Rodríguez等(2013)研究瑞典北部Laver和Kristineberg矿山发现,两地尾矿中硫化物受氧化淋滤作用使得尾矿氧化带相对其原同位素组成富集63Cu,其中Laver矿区次生富集带的δ65Cu与未经氧化的尾矿的原始值(1.31±0.03‰)相比低至−4.35‰ ± 0.02‰,这主要就是因为次生的铜蓝在次生富集带沉淀 [52] 。Mathur等(2009)将受淋滤作用的斑岩铜矿床划分为三个主要的同位素储库,顶部为淋滤帽,中间为富集地带,底部为深成相矿物。其中原生矿化带的铜同位素组成变化集中在0‰附近,而矿床的淋滤帽富集63Cu,次级富集带的矿物富集65Cu。这可能是因为原生矿化带在隆升到地表附近后,遭受到了风化淋滤作用,淋滤帽中的65Cu优先进入淋滤液中,随其运移到淋滤带下部发生次生富集作用 [9] 。这与Mathur等(2005)在低温非生物淋滤实验的数据一致,辉铜矿和黄铜矿的淋滤液的铜同位素组成相对于剩余矿物相对富集重同位素 [53] 。那么铜同位素组成可以用来区分矿床的原生带、次生富集带和表生淋滤带,进而判别铜矿物是热液成因或次生成因。
在河流水系发育的地区,通常随着强烈的风化淋滤作用的不断进行,相对富集铜的重同位素的淋滤液会进入河流,并在一定程度上引起河流铜同位素组成的变化。那么多金属富集的岩石与河流中铜同位素组成的变化也可以作为当地的风化淋滤指标之一。Kimball等(2009)调查发现美国科罗拉多河矿区流域的原生矿物硫砷铜矿(−0.01‰ ± 0.10‰)和黄铜矿(0.16‰ ± 0.10‰)的δ65Cu值低于受酸性矿水影响的河流水(1.38‰ ≤ δ65Cu ≤ 1.69‰) [18] 。吕逸文等(2015)在研究多金属富集的黑色页岩中发现强风化地区相对于弱风化地区更亏损65Cu [54] 。但实际问题也需要具体问题具体分析,因为岩石中不同含Cu矿物的矿物相的淋滤速度不同,所以不同含Cu矿物的淋滤曲线也会有一定差异。比如李丹丹等(2015)淋滤实验表明在较高酸浓度淋滤下,玄武岩铜同位素组成在前期与单矿物黄铜矿的变化趋势相似,而在后期淋滤又会出现逐渐变重的变化,这可能是玄武岩样品中有部分难溶的矿物相在最后发生了溶解 [3] 。这说明部分pH值较低的污染地区的河流也有可能出现富集铜的轻同位素现象。
对矿床不断深入的研究既可以了解过去的地质历史作用,也会产生一定的经济价值。然而,随着大规模矿山的开采,大量酸性矿水也随之进入周围河流和土壤。重金属作为难降解、易残留的污染物很容易累积进入食物链,影响自然环境和生物健康如何保护矿区周边的土壤和水资源以及修复已经污染地区的环境也成了研究的一大难题。大陆岩石的风化淋滤是河流海洋中Cu等元素的重要来源。在有机配体络合下,可溶的Cu与不溶的Cu储库之间会发生同位素分馏 [56] 。不同界面储存Cu等重金属的能力不同,如在矿区尾矿受风化淋滤过程中,Cu等重金属元素会随之进入周围河流,河水和河底淤泥都可以作为重金属储库。若只考虑到河水的重金属污染治理,那么污染将不会被根除,河底淤泥会成为二次污染源。治理环境污染,首先需要确定污染源,目前对铜矿山的研究中发现铜同位素有着良好的示踪污染源的能力。因为表生环境下矿区水系流经的区域不同,铜的主导存在形式不同(离子态、微粒态、络合物等),在不同界面受到的吸附与反吸附作用以及生物作用等影响因素也会不同,δ65Cu值也会呈现不同的特征。比如Mathur等(2005)在富Cu矿物的氧化溶解实验中发现淋滤过程中氧化亚铁硫杆菌有助于重Cu同位素氧化物纳米颗粒的形成 [53] 。李丹丹等(2015)在淋滤实验中发现相同矿物受不同酸浓度流体的淋滤会出现不同特征:酸浓度较低时,玄武岩和黄铜矿等矿物中的Cu被淋滤出的速度也较缓慢,淋滤过程中矿物表面容易形成氧化膜,使开始淋滤时矿物表面富集65Cu;而当酸浓度较高时,玄武岩和单矿物黄铜矿样品表面难以形成氧化膜,矿物中的Cu活性增强,易被淋滤出,相对富集65Cu的Cu2+优先进入淋滤液中 [3] 。陈丹丹等(2016)发现的江西德兴铜矿水样的δ65Cu变化范围(−5.8‰~24.4‰)非常大;同时发现矿区硫化物的δ65Cu的变化范围为−4‰~11.9‰,其中黄铁矿的δ65Cu变化范围(−4‰~11.9‰)比黄铜矿(−0.15‰~1.65‰)明显;矿区外围水样过滤后的δ65Cu值较低而尾矿库水样过滤后的δ65Cu则非常高(图1)
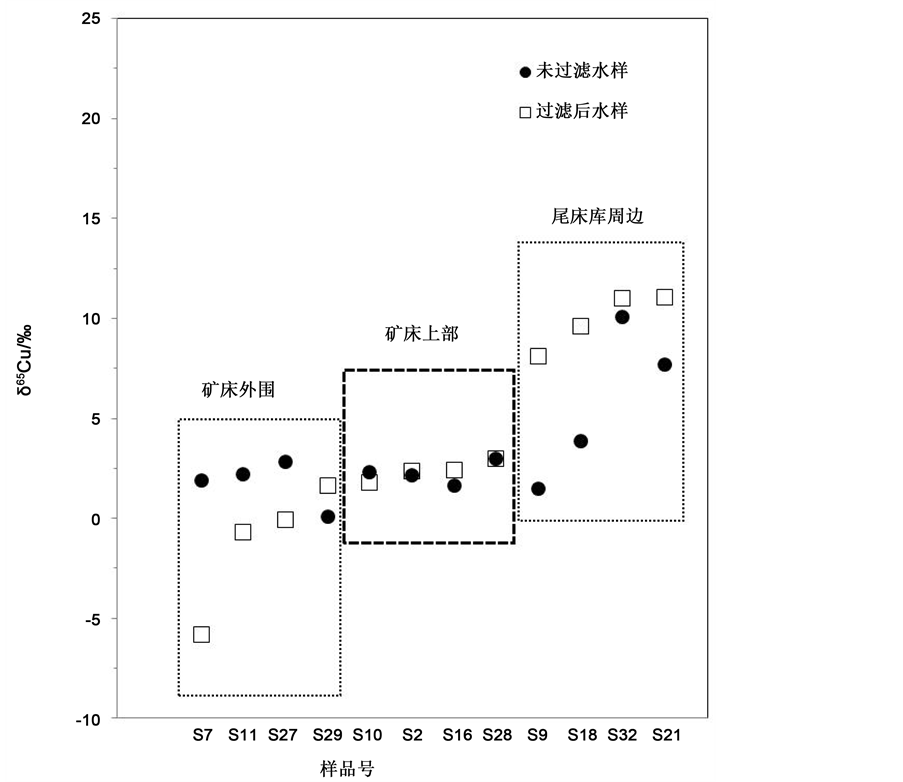
Figure 1. Cu isotopic composition before and after filtering for water samples (cited from Chen, et al., 2016)
图1. 德兴水系样品过滤前后δ65Cu值变化图(引自陈丹丹等,2016)
[8] 。这说明铜同位素在示踪污染源方面具有重要意义。而铜矿山周边环境的监测和治理就需要具体结合铜同位素在尾矿、河流、土壤等界面的运移转化,这方面有待进一步研究。但是在示踪铜冶炼厂这一人为污染源时却没有明显的效果。Bigalke等(2010c)发现由于与铜冶炼相关的Cu的变化在观测土壤范围之中,所以无法用铜同位素比例来辨别人为的Cu来源 [57] 。但铜同位素在评估重金属土壤污染中污染物的运移也具有一定价值。Bigalke等(2010c)在离Slovak铜冶炼厂和冶炼厂废弃物不同距离(1.1、3.8、5.3 km)的三处土壤样品的铜同位素分馏变化范围δ65Cu随着土壤深度的增加而减小,但在地下0.47 m深的土壤剖面样品出现了0.39‰的正偏移,而且这一深度样品的δ65Cu变化范围与基岩基本相同 [57] 。这可能说明在大于0.4 m处的土壤基本不受或很少受人类活动排放的Cu的影响,即在该地区开始冶炼铜到取样这60年之间,受人类影响产生的Cu在土壤中运移的深度约为0.4 m。当然这一结论是在研究单独的土壤样品基础上得出的。
3.2.3. 吸附/解吸附过程
在表生自然环境中,铜容易吸附在一些矿物表面,例如高岭土、铁的氧化物以及氢氧化物等。不同矿物对铜同位素的吸附能力不同,引起的铜同位素分馏也不同。通常,溶液中Cu(II)的存在形式主要为 和
和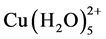 。水溶液中Cu离子的存在形式和络合形式往往会影响高岭土等黏土矿物吸附过程中的铜同位素组成。如李丹丹由XRD数据和瑞利分馏模拟得知高岭土吸附过程产生显著Cu同位素分馏的机理就是由于溶液中的Cu络合形式不同,高岭土优先吸附溶液中的
。水溶液中Cu离子的存在形式和络合形式往往会影响高岭土等黏土矿物吸附过程中的铜同位素组成。如李丹丹由XRD数据和瑞利分馏模拟得知高岭土吸附过程产生显著Cu同位素分馏的机理就是由于溶液中的Cu络合形式不同,高岭土优先吸附溶液中的 络合物(富63Cu),所以高岭土类的黏土矿物相对富集63Cu [3] 。高岭土等粘土矿物具有独特的性质,在研究时需要与其它土壤类型进行区分。
络合物(富63Cu),所以高岭土类的黏土矿物相对富集63Cu [3] 。高岭土等粘土矿物具有独特的性质,在研究时需要与其它土壤类型进行区分。
硫化物溶解淋滤过程中,容易形成铁的氧化物氢氧化物等,这些矿物会通过吸附作用或者共沉淀作用而富集微量元素,例如铜。相对于溶液中的水合离子,金属表面的金属—氧键较短、配位数较低、键能较强,Cu(II)和金属氧化物表面形成双齿配位键与四面体的内环结构的键能也较强,所以金属氧化物表面易富集65Cu,从而使得这些矿物相比溶液相更富集重的铜同位素 [48] 。如Pokrovsky等(2008)实验发现当4.2 ≤ pH ≤ 6.1时,铁和铝的氢氧化物表面呈现出富集65Cu的特征 [52] 。Balistrieri等(2008)进行合成的六方针铁矿吸附各种含铜溶液(天然水、合成的矿山废水、NaNO3溶液)的实验数据同样表明矿物表面优先吸附65Cu,并得出了铜的分馏系数αsoln-solid = 0.99927 ± 0.00008,相应的分馏值Δsoln-solid为−0.73‰ ± 0.08‰ [54] 。
铜也容易吸附在有机质上,例如腐殖质是动植物残骸在微生物作用下形成的有机物质,由于有机化合物与65Cu形成的键能更强 [57] ,所以腐殖质的存在也会影响Cu同位素分馏。如Bigalke等(2010b)研究表明相对于水溶液,不溶性腐殖质酸与Cu的络合物富集65Cu [47] 。Pérez Rodríguez等(2013)在尾矿研究中同样发现最上层的有机层包含的腐殖质可以在溶液中与Cu形成络合物,并优先吸附65Cu [48] 。
Liu等(2014)研究发现亚热带湿润气候下的美国南卡罗来纳州凯斯地区辉绿岩脉风化土样在剖面下部还原区域的δ65Cu值基本不变,而上部氧化区域的铜同位素分馏较大且富集65Cu;潮湿的热带季风气候下的中国海南岛玄武岩剖面上的风化土样在3 m以上则呈现Cu同位素分馏较小且相对富集63Cu的相反特征 [58] 。这主要是因为不同气候条件下的降水量不同,强氧化和强降水冲刷作用下铜的重同位素易发生淋滤解吸附现象并逐步向下迁移再沉淀,使得土壤剖面上部相对亏损65Cu;相对干燥的气候则有利于铜吸附到铁的(氢氧)氧化物表面上,在土壤溶液中再沉淀,使得土壤剖面上部铜含量高且富集65Cu [58] 。可见在风化成土过程中,吸附/解吸作用对铜同位素分馏变化有重要影响;土壤剖面上铜同位素分馏和组成特征在一定程度上也可以指示当地气候特征。
4. 结语与展望
如今,许多学者在斑岩型、矽卡岩矿床研究中已经应用铜同位素分析,斑岩矿体和矽卡岩矿体都呈现出一定的时间和空间变化。由于铜同位素分馏受众多因素影响,所以在具体运用时还需先划分成矿阶段,进行阶段性对比会更直观有效。表生环境下,影响铜同位素分馏的因素众多,不同界面上铜同位素分馏的研究对于自然环境中铜元素地球化学循环和环境污染治理具有重要意义。
基金项目
本文受国家自然科学基金项目(41203011)和中央高校基本科研业务费专项基金(2016B07814)资助。
文章引用
嵇静,赵海香. 铜同位素分馏机理及影响因素研究综述
Mechanism and Factors Influencing Copper Isotopic Fractionation: A Review[J]. 地球科学前沿, 2017, 07(03): 336-348. http://dx.doi.org/10.12677/AG.2017.73037
参考文献 (References)
- 1. 蒋少涌. 过渡族金属元素同位素分析方法及其地质应用[J]. 地学前缘, 2003(2): 269-278.
- 2. 王泽洲, 刘盛遨, 李丹丹, 吕逸文, 吴松, 赵云. 铜同位素地球化学及研究新进展[J]. 地学前缘, 2015(22): 72-83.
- 3. 李丹丹. 低温过程中Cu-Zn同位素分馏的实验地球化学研究[D]: [博士学位论文]. 北京: 中国地质大学, 2015.
- 4. Maréchal, C.N., Télouk, P. and Albarède, F. (1999) Precise Analysis of Copper and Zinc Isotopic Compositions by Plasma-Source Mass Spectrometry. Chemical Geology, 156, 251-273. https://doi.org/10.1016/S0009-2541(98)00191-0
- 5. Shields, W.R., Goldich, S.S. and Garner, E.L. (1965) Natural Variations in the Abundance Ratio and the Atomic Weight of Copper. Geophysical Research, 70, 291-293. https://doi.org/10.1029/JZ070i002p00479
- 6. Moeller, K., Schoenberg, R., Pedersen, R.B., Weiss, D. and Dong, S.F. (2012) Calibration of the New Certified Reference Materials ERM-AE633 and ERM-AE647 for Copper and IRMM-3702 for Zinc Isotope Amount Ratio Determinations. Geostandards and Geoanalytical Research, 36, 177-199. https://doi.org/10.1111/j.1751-908X.2011.00153.x
- 7. 王跃, 朱祥坤, 毛景文. 铜同位素在矿床学中的应用: 认识与进展[J]. 吉林大学学报(地球科学版), 2010(40): 739-751.
- 8. 陈丹丹, 宋世明, Mathur, R., 郭坤一, 康文凯, 李双喜, 赵晓丹, 张飞. 江西德兴铜矿区水系的Cu同位素地球化学特征及其地质意义[J]. 地质通报, 2016(35): 188-195.
- 9. Mathur, R., Titley, S., Barra, F., Brantley, S., Wilson, M., Phillips, A., Munizaga, F., Maksaev, V., Vervoort, J. and Hart, G. (2009) Exploration Potential of Cu Isotope Fractionation in Porphyry Copper Deposits. Journal of Geochemical Exploration, 102, 1-6. https://doi.org/10.1016/j.gexplo.2008.09.004
- 10. Li, W.Q., Jackson, S.E., Pearson, N.J. and Graham, S. (2010) Copper Isotopic Zonation in the Northparkes Porphyry Cu-Au Deposit, SE Australia. Geochimica et Cosmochimica Acta, 74, 4078-4096. https://doi.org/10.1016/j.gca.2010.04.003
- 11. Maréchal, C. and Albarède, F. (2002) Ion-Exchange Fractionation of Copper and Zinc Isotopes. Geochimica et Cosmochimica Acta, 66, 1499-1509.
- 12. 梁莉莉, 刘丛强, 王中良. 铜锌同位素方法在环境地球化学研究中的应用[J]. 地球与环境, 2006(1): 81-89.
- 13. Zhu, X.K., Guo, Y., Williams, R.J.P., O’Nions, R.K., Matthews, A., Belshaw, N.S., Canters, G.W., de Waal, E.C., Weser, U., Burgess, B.K. and Salvato, B. (2002) Mass Fractionation Processes of Transition Metal Isotopes. Earth and Planetary Science Letters, 200, 47-62.
- 14. Maksymiec, W. (1997) Effect of Copper on Cellular Processes in Higher Plants. Photosynthetica, 34, 321-342. https://doi.org/10.1023/A:1006818815528
- 15. Navarrete, J.U., Viveros, M., Ellzey, J.T. and Borrock, D.M. (2011a) Copper Isotope Fractionation by Desert Shrubs. Applied Geochemistry, 26, S319-S321.
- 16. Weinstein, C., Moynier, F., Wang, K., Paniello, R. and Foriel, J. (2011) Isotopic Fractionation of Cu in Plants. Chemical Geology, 286, 266-271.
- 17. Navarrete, J.U., Borrock, D.M., Viveros, M. and Ellzey, J.T. (2011b) Copper Isotope Fractionation during Surface Adsorption and Intracellular Incorporation by Bacteria. Geochimica et Cosmochimica Acta, 75, 784-799.
- 18. Kimball, B.E., Mathur, R., Dohnalkova, A.C., Wall, A.J., Runkel, R.L. and Brantley, S.L. (2009) Copper Isotopic Fractionation in Acid Mine Drainage. Geochimica et Cosmochimica Acta, 721, A473-A473.
- 19. 杨立飞, 石康兴, 王长明, 吴彬, 杜斌, 陈晶源, 夏锦胜, 陈晶. 西南三江兰坪盆地金满铜矿床成因研究: 来自铜和硫同位素的联合约束[J]. 岩石学报, 2016(32): 2392-2406.
- 20. Zhu, X.K., O'Nions, R.K., Guo, Y., Belshaw, N.S. and Rickard, D. (2000) Determination of Natural Cu-Isotope Variation by Plasma-Source Mass Spectrometry: Implications for Use as Geochemical Tracers. Chemical Geology, 163, 139-149.
- 21. 蒋少涌, Woodhead, J., 于际民, 潘家永, 廖启林, 吴南平. 云南金满热液脉状铜矿床Cu同位素组成的初步测定[J]. 科学通报, 2001(46): 1468-1471.
- 22. 王跃, 朱祥坤. 铜陵矿集区冬瓜山矿床斑岩-矽卡岩型矿床成矿作用过程中的Cu同位素地球化学行为初步研究[J]. 地质学报, 2014(88): 2413-2422.
- 23. 王鹏, 董国臣. 云南中甸红山–红牛矽卡岩铜矿黄铜矿和相关斑岩铜同位素特征[J]. 吉林大学学报(地球科学版), 2015, 45(S1): 7.
- 24. 何德锋, 钟宏, 朱维光. 铜同位素的分馏机制及其在矿床学研究中的应用[J]. 岩石矿物学志, 2007(4): 345-350.
- 25. 陈晓锋, 朱祥坤. 铜绿山夕卡岩型铜铁矿床Fe、Cu同位素研究[J]. 矿物学报, 2011(S1): 1001-1003.
- 26. Larson, P.B., Maher, K., Ramos, F.C., Chang, Z.S., Gaspar, M. and Meinert, L.D. (2003) Copper Isotope Ratios in Magmatic and Hydrothermal Ore-Forming Environments. Chemical Geology, 201, 337-350.
- 27. 刘文元. 福建紫金山斑岩—浅成热液成矿系统的精细矿物学研究[D]: [博士学位论文]. 北京: 中国地质科学院, 2015.
- 28. Asael, D., Matthews, A., Bar-Matthews, M. and Halicz, L. (2007) Copper Isotope Fractionation in Sedimentary Copper Mineralization (Timna Valley, Israel). Chemical Geology, 243, 238-254.
- 29. Haest, M., Muchez, P., Petit, J.C. and Vanhaecke, F. (2009) Cu Isotope Ratio Variations in the Dikulushi Cu-Ag Deposite, DRC: Of Primary Origin or Induced by Supergene Reworking. Economic Geology, 104, 1055-1064. https://doi.org/10.2113/econgeo.104.7.1055
- 30. 赵海香, 蒋少涌, 朱志勇, 李斌, 赵智, 嵇静. 福建紫金山矿田铜同位素特征初步研究[C]//2015中国地球科学联合学术年会. 中国地球科学联合学术年会论文集. 北京, 2015: 11-14, 2.
- 31. Asael, D., Matthews, A., Oszczepalski, S., Bar-Matthews, M. and Halicz, L. (2009) Fluid Speciation Controls of Low Temperature Copper Isotope Fractionation Applied to the Kupferschiefer and Timna Ore Deposits. Chemical Geology, 262, 147-158.
- 32. Ehrlich, S., Butler, I., Halicz, L., Rickard, D., Oldroyd, A. and Matthews, A. (2004) Experimental Study of the Copper Isotope Fractionation between Aqueous Cu (II) and Covellite, CuS. Chemical Geology, 209, 259-269.
- 33. 黄建, 刘盛遨, 高永军, 黄方, 肖益林, 刘禹辰. 洋壳蚀变过程中Cu和Zn同位素分馏: 对海洋Cu和Zn循环的制约[J]. 吉林大学学报(地球科学版), 2015, 45: 11.
- 34. 杨志明, 侯增谦. 西藏驱龙超大型斑岩铜矿的成因: 流体包裹体及H-O同位素证据[J]. 地质学报, 2009, 83: 1838-1859.
- 35. 李振清, 杨志明, 朱祥坤, 侯增谦, 李世珍, 李志红, 王跃. 西藏驱龙斑岩铜矿铜同位素研究[J]. 地质学报, 2009, 83: 1985-1996.
- 36. 吴仲玮, 孙晓明, 王琰, 梁业恒, 徐莉. 中印度洋脊热液活动区多金属硫化物Fe-Cu-Zn同位素组成特征的初步研究[J]. 矿物学报, 2013(S2): 672-673.
- 37. Liu, S.A., Huang, J., Liu, J.G., Worner, G., Yang, W., Tang, Y.J., Chen, Y., Tang, L.M., Zheng, J.P. and Li, S.G. (2015) Copper Isotopic Composition of the Silicate Earth. Earth and Planetary Science Letters, 427, 95-103.
- 38. 李津, 朱祥坤, 唐索寒. 低温环境下铜同位素分馏的若干重要过程[J]. 岩石矿物学杂志, 2008, 27: 298-304.
- 39. 李世珍, 朱祥坤, 唐索寒, 吴龙华, 骆永明. 铜同位素在植物中分馏的初步研究—以海州香薷为例[J]. 矿物学报, 2009(S): 605-606.
- 40. Jouvin, D., Weiss, D.J., Mason, T.F.M., Bravin, M.N., Louvat, P., Zhao, F., Ferec, F., Hinsinger, P. and Benedetti, M.F. (2012) Stable Isotopes of Cu and Zn in Higher Plants: Evidence for Cu Reduction at the Root Surface and Two Conceptual Models for Isotopic Fractionation Processes. Environmental Science & Technology, 46, 2652-2660. https://doi.org/10.1021/es202587m
- 41. 武贝. 海州香薷Cu耐性与积累机制研究[D]: [博士论文]. 杭州: 浙江大学, 2009.
- 42. Bigalke, M., Weyer, S. and Wilcke, W. (2010a) Stable Copper Isotopes: A Novel Tool to Trace Copper Behavior in Hydromorphic Soils. Soil Science Society of America Journal, 74, 60-73. https://doi.org/10.2136/sssaj2008.0377
- 43. Bigalke, M., Weyer, S. and Wilcke, W. (2011) Stable Cu Isotope Fractionation in Soils during Oxic Weathering and Podzolization. Geochimica et Cosmochimica Acta, 75, 3119-3134.
- 44. 林维晟, 吴海泉, 胡家朋, 黄雪婷, 徐颖惠. 生物酶生态修复重金属污染土壤[J]. 环境工程学报, 2015(9): 6147- 6153.
- 45. Liao, M.T., Hedley, M.J., Woolley, D.J., Brooks, R.R. and Nichols, M.A. (2000) Copper Uptake and Translocation in Chicory (Cichorium intybus L. cv. Grasslands Puna) and Tomato (Lycopersicon esculentum Mill. cv. Rondy) Plants Grown in NFT System. I. Copper Uptake and Distribution in Plants. Plant and Soil, 131, 135-142. https://doi.org/10.1023/A:1004731415931
- 46. O’Neil, J.R., Valley, J.W. and Taylor, H.P. (1986) Theoretical and Experimental Aspects of Isotopic Fractionation. Mineralogical Society of America, 16, 1-40.
- 47. Bigalke, M., Weyer, S. and Wilcke, W. (2010b) Copper Isotope Fractionation during Complexation with Insolubilized Humic Acid. Environmental Science & Technology, 44, 5496-5502. https://doi.org/10.1021/es1017653
- 48. 李津. 低温条件下过渡族元素同位素分馏及其在古海洋研究中的应用[D]: [博士学位论文]. 北京: 中国地质科学院, 2008.
- 49. Pokrovsky, O.S., Viers, J., Emnova, E.E., Kompantseva, E.I. and Freydier, R. (2008) Copper Isotope Fractionation during Its Interaction with Soil and Aquatic Microorganisms and Metal Oxy(hydr)oxides: Possible Structural Control. Geochimica et Cosmochimica Acta, 72, 1742-1757.
- 50. Zhu, X.K., Li, S.Z., Luo, Y.M. and Wu, L.H. (2010) Copper Isotope Fractionation by Higher Plants. Geochimica et Cosmochimica Acta, 74, A1234.
- 51. 吕逸文, 刘盛遨, 朱建明. 多金属富集的黑色页岩风化过程中铜、锌同位素分馏研究[J]. 吉林大学学报(地球科学版), 2015, 45(S1): 17.
- 52. Pérez, R.N., Engstrom, E., Rodushkin, I., Nason, P., Alakangas, L. and Ohlander, B. (2013) Copper and Iron Isotope Fractionation in Mine Tailings at the Laver and Kristineberg Mines, Northern Sweden. Applied Geochemistry, 32, 204-215.
- 53. Mathur, R., Ruiz, J., Titley, S., Liermann, L., Buss, H. and Brantley, S. (2005) Cu isotopic Fractionation in the Supergene Environment with and without Bacteria. Geochimica et Cosmochimica Acta, 69, 5233-5246.
- 54. Balistrieri, L.S., Borrok, D.M., Wanty, R.B. and Ridley, W.I. (2008) Fractionation of Cu and Zn Isotopes during Adsorption onto Amorphous Fe(III)oxyhydroxide: Experimental Mixing of Acid Rock Drainage and Ambient River Water. Geochimica et Cosmochimica Acta, 72, 311-328.
- 55. Fernandez, A. and Borrok, D.M. (2009) Fractionation of Cu, Fe, and Zn Isotopes during the Oxidative Weathering of Sulfide-Rich Rocks. Chemical Geology, 264, 1-12.
- 56. Vance, D., Archer, C., Bermin, J., Perkins, J., Statham, P.J., Lohan, M.C., Ellwood, M.J. and Mills, R.A. (2008) The Copper Isotope Geochemistry of Rivers and the Oceans. Earth and Planetary Science Letters, 274, 204-213.
- 57. Bigalke, M., Kobza J., Weyer, S. and Wilcke, W. (2010c) Stable Cu and Zn Isotope Ratios as Tracers of Sources and Transport of Cu and Zn in Contaminated Soil. Geochimica et Cosmochimica Acta, 74, 6801-6813.
- 58. Liu, S.A., Teng, F.Z., Li, S.G., Wei, G.J., Ma, J.L. and Li, D.D. (2014) Copper and Iron Isotope Fractionation during Weathering and Pedogenesis: Insights from Saprolite Profiles. Geochimica et Cosmochimica Acta, 146, 59-75.
NOTES
*第一作者。
#通讯作者。