Journal of Organic Chemistry Research
Vol.03 No.01(2015), Article ID:14837,12
pages
10.12677/JOCR.2015.31005
Quantum Chemical Calculations on Chemical Reactivity Index of μ-Opioid Receptor Antagonist
Qiao Wang1,2, Jinsheng Guo3, Kaiyuan Shao1, Wenxiang Hu1,2*
1Beijing
2School of Chemical Engineering & Pharmacy, Wuhan Institute of Technology, Wuhan Hubei
3Langfang Normal College, Langfang Hebei
Email: *huwx66@163.com
Received: Jan. 28th, 2015; accepted: Feb. 6th, 2015; published: Feb. 13th, 2015
Copyright © 2015 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
μ-opioid receptor antagonist is more and more widely used in clinical practice, and quantum chemistry calculations on compounds design to improve efficiency and reduce synthesis workload also play an important role. This paper designed 12 target compounds based on the structure of antagonist 1-(2-cyclohexylethyl)-4-(N-2-furoyl-N-(5-methylpy-ridin-2-yl) amino) piperidine which has good antagonist activities, and calculated the lowest energy conformations and nucleophilic reactions index (the chemical potential change rate and Fukui function value) by the quantum chemical ab initio method. In this paper, it predicted that when the substituents at the fourth position are the same, the sequence of compound activity is 1-cyclohexylseries compound, 1-phene- thylseries compound, 1-thiopheneseries compound and 1-vinylseries compound, in which 1-cyc- lohexylseries compound is the strongest. In the later work, we will compare the results with the actual results of animal experiments to establish an optimum theory algorithm, and build a reasonable QSAR model equation to provide theoretical guidance for the future compounds synthesis.
Keywords:μ-Opioid Receptor Antagonist, Reactions Index, Fukui Function Value, Compound Activity

μ型阿片受体拮抗剂化学反应性指数的 量子化学计算
王乔1,2,郭金生3,邵开元1,胡文祥1,2*
1北京神剑天军医学科学院,北京
2武汉工程大学化工与制药学院,湖北 武汉
3廊坊师范学院,河北 廊坊
Email: *huwx66@163.com
收稿日期:2015年1月28日;录用日期:2015年2月6日;发布日期:2015年2月13日

摘 要
μ型阿片受体拮抗剂在临床上具有越来越广泛的应用,量子化学计算的评估方法在提高化合物设计效率、减少合成工作量上也发挥着更加重要的作用。拮抗剂1-(2-环己基乙基)-4-(氮-2-呋喃甲酰基-氮-(5-甲基吡啶-2)氨基)哌啶具有较好的拮抗活性,本论文以其为结构基础,设计出12个目标化合物,通过基于量子化学从头计算法的理论计算获得最低能量构象和亲核性反应指数(化学势变化率和福井函数值),同时预测在4-位取代基一定时,1-位环己基系列化合物活性最强,苯乙基、噻吩基、乙烯基系列化合物活性依次减弱。后续工作中将与实际动物实验结果相比较,确立较优的理论算法,并构建出合理的构效关系模型方程,为以后的化合物设计合成提供理论指导。
关键词 :μ型阿片受体拮抗剂,反应性指数,福井函数值,化合物活性

1. 引言
化学反应中,化合物的亲核能力对反应能否发生及是否容易进行有很大影响。采用量子化学计算的方法,合理评估化合物的亲核性能,对于化学反应设计、反应机理推断及药物与受体作用机制探索具有重要意义。
随着计算机的硬件和软件技术的飞速发展,量子化学计算也得到飞速发展,计算方法推陈出新,计算速度大大提升,获得了许多可喜的成果。然而,对于药物的构效关系研究(QSAR)进展仍不十分理想,普遍使用的描述参数仍大多是非反应性的描述参数,包括传统Hansch方程中的立体参数、电性参数和疏水参数,以及不断发展的各种分子结构性质描述参数(分子原子构成参数、分子拓扑链接参数、CoMFA的分子场描述参数以及电子拓扑描述指数)等,其均是利用训练集和机器学习的方式,尽管能够形成一个高的相关系数的QSAR方程,但将其方程放到外部测试集上计算时,与实际结果相差很大,预测的成功率极低。这可能是由于存在所谓的“活性悬崖”问题,及使用这些参数没有涉及到药物分子与受体或酶作用中的电子转移变化过程,即忽略了化学反应性指数(量子化学参数),从而不能有效和精确地描述药物与受体作用过程,导致构建的QSAR模型的预测性能较差。
在此基础上,本论文将根据概念密度泛函理论[Conceptual Dendity Functional Theory (CDFT)],对12种哌啶类μ型阿片受体拮抗剂进行化学反应性指数的量子化学计算,获得其亲核性能的相关反应性指数,以期通过这些反应性指数来定性和定量地预测化合物的活性强弱,并为进一步的QSAR研究奠定基础。
2. 反应性指数的计算
μ型阿片受体拮抗剂大多在结构上与阿片受体激动剂类似,其本身对阿片受体无激动效应,但与阿片受体具有较强的亲和能力,能够与激动剂竞争性结合受体活性位点,从而移除或替代与受体结合的激动剂,达到拮抗目的,同时能够消除使用阿片类药物所引起的呼吸抑制、胃肠功能紊乱等副作用,在临床上有很大的应用价值。本文以拮抗活性的哌啶类化合物1-(2-环己基乙基)-4-(氮-2-呋喃甲酰基-氮-(5-甲基吡啶-2)氨基)哌啶[1] 结构类似物为研究对象,通过量子化学计算获得相关的反应性指数,结构见表1。
本文所有计算都是采用Gaussian03和GaussView3.09软件包,在3.0 GHZ四核和8 GB内存的微机上完成。
反应性指数的计算方法是根据我们课题组提出的化学势变化率和福井函数值来评估失去一个电子体系的反应性指数[2] ,其计算公式如下:

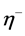 表现为失电子前后化学势的变化,即
表现为失电子前后化学势的变化,即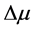 。表现为分子失电子前后最高占有轨道的能量变化与最低空轨道能量变化和的平均值,体现了分子的亲核反应能力,其值越大,说明化学反应的能力也越强。
。表现为分子失电子前后最高占有轨道的能量变化与最低空轨道能量变化和的平均值,体现了分子的亲核反应能力,其值越大,说明化学反应的能力也越强。
分子的局域反应性,对亲电试剂的敏感度,表示为:
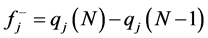
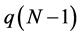 表示失去1个电子后(成为阳离子)的电荷布居。
表示失去1个电子后(成为阳离子)的电荷布居。
 为当分子失去1个电子时,第j原子的电荷变化率。其值越大,说明失去电子的能力越强,即反映亲核能力。
为当分子失去1个电子时,第j原子的电荷变化率。其值越大,说明失去电子的能力越强,即反映亲核能力。
本文选择DFT/B3LYP (6
对于中性分子Charge = 0,Spin = Single;限制条件Restricted;
对于失电子分子失去一个电子(charge = 1),spin = Doublet,非限制性条件Unrestricted (分别计算α和β轨道能量)。
3. 结果与讨论
化学势变化率的计算:
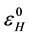 为中性分子HOMO能量;
为中性分子HOMO能量; 为中性分子LUMO能量。
为中性分子LUMO能量。
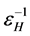 为失去一个电子分子HOMO能量;
为失去一个电子分子HOMO能量; 为失去一个电子分子LUMO能量
为失去一个电子分子LUMO能量
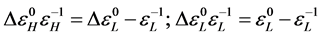
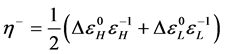
经过计算获得相关数据,化合物分子失电子前后化学势变化率参数见表2,化合物各原子福井函数值见附表1。
将附表1中各个化合物的化学势变化率和哌啶环上氮原子的福井函数值归纳结果,见表3。
从表3可以看出:1) 纵向看,4-位取代基相同,1-位环己基系列的福井函数明显高于其他系列。基本上依次为苯乙基、噻吩基、乙烯基;2) 分子的化学势变化率有差别,只有KP06较小,但其福井函数值较大。
1994年,胡文祥等[3] 在研究抗胆碱能药物抗N样作用规律时发现氮上电荷密度越大,抗N样作用越强。由此类推,当4-位取代基一定时,1-位环己基系列化合物的哌啶环上氮原子亲核能力最强,则生物活性也最好,苯乙基、噻吩基、乙烯基系列化合物以此递减。准确的生物活性数据还有待进一步动物实验验证。
Table 1. List of compounds
表1. 化合物列表
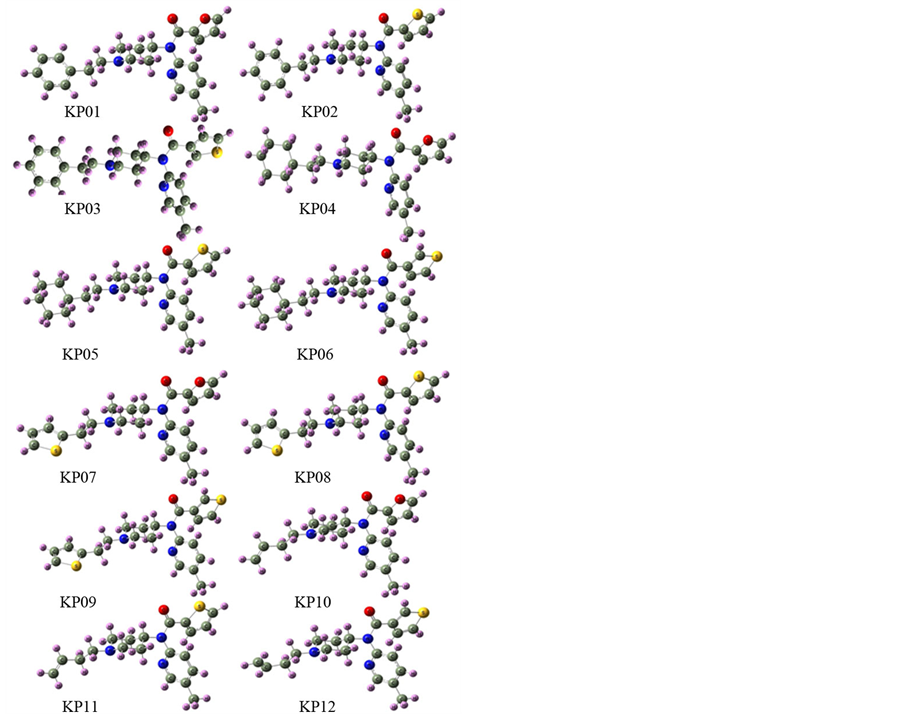
Figure 1. The structure of KP01-KP012 after ground state optimization by DFT/B3LYP (6-311G++ (2d, 2P)
图1. 经DFT/B3LYP (6-311G++ (2d, 2P)基态优化的KP01~KP012结构
Table 2. Chemical potential gradient parameters before and after losing electron
表2. 化合物分子失电子前后化学势变化率参数
Table 3. The comprehensive assessment table of chemical potential gradient and Fukui function value
表3. 化学势变化率和福井函数值综合评估表
4. 结论与展望
本论文中对μ型阿片受体拮抗剂的化学反应性指数进行了理论计算,并对拮抗活性强弱进行了预测,以期获得的理论预测值与实际的生物活性相近或相同,后续工作中将与实际动物实验结果比较,再以此确立较优的理论算法,并构建出合理的构效关系模型方程,为以后的化合物设计合成提供了理论指导。
芬太尼类镇痛药在我国广泛使用于临床,μ型阿片受体拮抗剂活性强、转移性高,是潜在的有效拮抗芬太尼激动剂的药物。几十年来人们对阿片镇痛和耐受成瘾的分子药理机制做了大量的研究,但仍有许多问题尚未阐明 ,因此,继续拓展分子药理作用机制的研究,开发作用更加高效持久、毒副作用低的新型μ阿片受体拮抗剂是阿片药学研究的发展趋势,具有重大的理论意义和实际应用价值。
文章引用
王 乔,郭金生,邵开元,胡文祥. μ型阿片受体拮抗剂化学反应性指数的量子化学计算
Quantum Chemical Calculations on Chemical Reactivity Index of μ-Opioid Receptor Antagonist[J]. 有机化学研究, 2015, 03(01): 32-43. http://dx.doi.org/10.12677/JOCR.2015.31005
参考文献 (References)
- 1. Fukutomi, R., Inoue, H., Kawamura, K., et al. (2008) 4-(2-Furoyl)aminopiperidines, intermediates in synthesizing the same, process for producing the same and medicinal use of the same. US Patent No. 7375115.
- 2. 邵开元, 王乔, 邢欣, 等 (2014) 应用量子化学反应性指数评估化合物的亲核能力. 化学通报, 3, 227-235.
- 3. 胡文祥, 恽榴红 (1994) 抗胆碱能药物抗N样作用的分子药理学研究. 科学通报, 1, 79-81.
附录
化合物各原子标号(由机器自动产生):
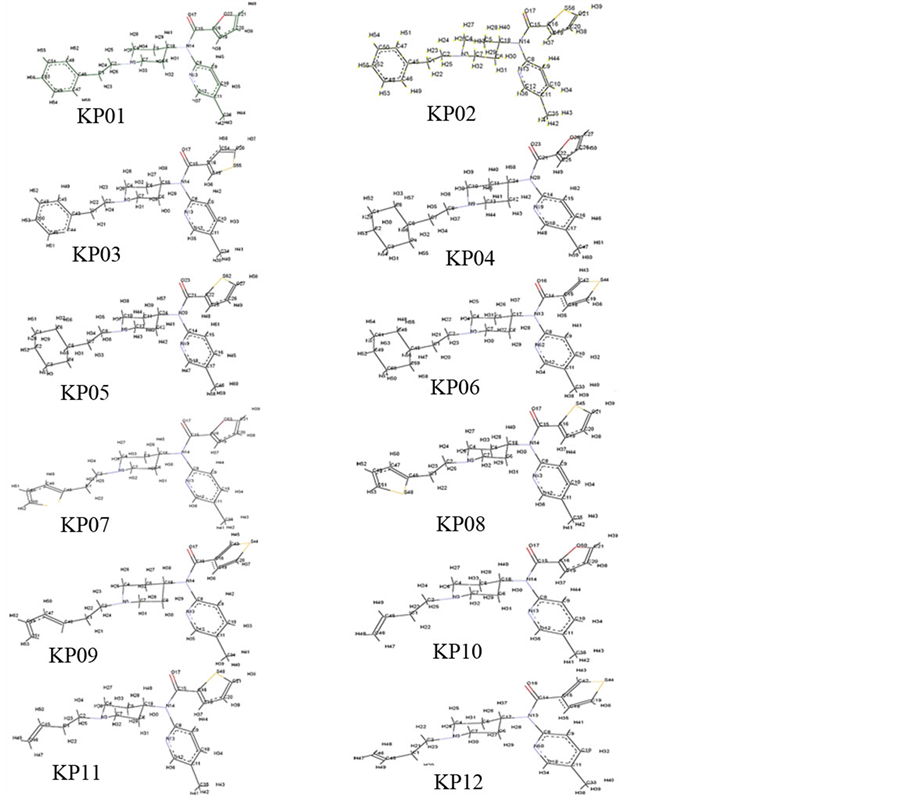
Schedule 1.Fukui function value of each atom
附表1. 化合物各原子福井函数值
注:表中黑体字为哌啶环上氮原子及其福井函数值。原子编码序号见上图。
