Material Sciences
Vol.
09
No.
05
(
2019
), Article ID:
30298
,
10
pages
10.12677/MS.2019.95061
Recent Advances in Pt-Based Ordered Intermetallic Catalysts for Oxygen Reduction Reaction
Hua Sun1, Di Qi2, Hui Liu2, Leijun Shao2, Xiaoxia Wang3*
1The Administrative Center of Shanghai R & D Public Service Platforms, Shanghai S & T Talents Development Center, Shanghai
2Shanghai Power & Energy Storage Battery System Engineering Tech. Co. Ltd., Shanghai
3School of Mechanical and Power Engineering, East China University of Science and Technology, Shanghai

Received: Apr. 28th, 2019; accepted: May 13th, 2019; published: May 20th, 2019

ABSTRACT
Proton exchange membrane fuel cells (PEMFCs), as a new type of environmentally friendly technology, will have widespread applications in the field of automobiles, distributed power stations and so on. However, high cost and low stability are the main issues, which block the further commercialization of PEMFCs. The high cost originates from the usage of Pt noble metal as oxygen reduction reaction (ORR) catalysts, which is the crucial factor on the performance of fuel cell. Herein, we review a novel kind of ORR catalysts, intermetallic compounds. The specific structural properties and the effect of transition metals composition on the catalytic activity and stability are introduced. Finally, the perspective on the development of Pt-based intermetallic catalysts and their application in PEMFCs are provided.
Keywords:Proton Exchange Membrane Fuel Cells (PEMFCs), Oxygen Reduction Reaction (ORR), Electroatalysts, Intermetallic
Pt基有序金属间化合物氧还原催化剂研究进展
孙华1,戚頔2,刘辉2,邵雷军2,王晓霞3*
1上海市研发公共服务平台管理中心(上海市科技人才发展中心),上海
2上海动力储能电池系统工程技术有限公司,上海
3华东理工大学机械与动力工程学院,上海

收稿日期:2019年4月28日;录用日期:2019年5月13日;发布日期:2019年5月20日

摘 要
质子交换膜燃料电池作为新型绿色能源技术,在未来电动汽车及分散式电站等领域将有非常广阔的应用前景。但目前制约燃料电池商业化的主要瓶颈是其高成本和低寿命,而贵金属氧还原催化剂的使用是成本的主要来源,也是决定燃料电池性能的关键因素。本文综述了一种新型的氧还原催化剂——铂基金属间化合物,介绍其结构特性以及过渡金属组成对氧还原催化反应活性和稳定性的影响,最后对铂基催化剂的发展给出了展望。
关键词 :质子交换膜燃料电池,氧还原反应,电催化剂,金属间化合物

Copyright © 2019 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
在全球能源危机以及环境问题不断恶化的严峻形势下,发展清洁与可再生能源已成为近年来世界各国关心的重要议题。在各类可持续发展的新能源中,氢能因具有出色的比能量密度优势及广泛的技术适应性,被认为是未来最具有发展前景的新能源之一。质子交换膜燃料电池(Proton Exchange Membrane Fuel Cells, PEMFCs)技术,将氢和氧中的化学能直接转化为电能,是氢能利用最直接有效的方式 [1]。近五十年,PEMFCs技术已得到迅速发展,目前最为广泛的应用就是作为电动汽车动力源,2014年日本丰田公司量产并商业化的燃料电汽车(Fuel Cell Vehicle, FCV) Mirai标志着燃料电池商业化时代的到来 [2]。
在燃料电池实际应用中,阴极氧还原反应(Oxygen Reduction Reaction, ORR)是一个动力学慢反应,其反应速率直接决定了电池的性能,需要使用贵金属Pt作为催化剂 [3]。然而Pt为稀有金属,全球储量有限,价格昂贵,致使目前PEMFCs面临成本高的问题。另一方面,目前广泛使用的Pt/C催化剂在长时间工作条件下存在纳米颗粒团聚、溶解、再沉积以及脱落的问题,使催化剂性能显著下降,电池稳定性能不好。为了降低催化剂中Pt的用量,近年来国内外的研究热点为Pt与过渡金属M (M=Fe, Co, Ni, Cu, Pd等)形成的合金催化剂,目前已有许多合金催化剂的相关报导和综述性文章 [3] [4] [5],对其现状和发展方向给予了评论。但是,在燃料电池阴极富氧和高电压的酸性条件下,合金催化剂中的过渡金属存在易溶出,并污染质子交换膜的问题,使电池性能迅速衰减。近年来,一种新型的ORR催化剂——具有有序结构的金属间化合物,因其表现出更高的催化活性和稳定性,吸引了国内外研究工作者的广泛关注。本文将根据近些年对于这类催化剂的研究,从催化剂的组成、结构、性能三个角度出发,综述几类典型的金属间化合物ORR催化剂的研究进展,并对其面临的挑战和发展方向给出一些展望。
2. 金属间化合物的有序结构与催化活性
对于纯铂催化剂的研究及ORR反应机理密度泛函理论(Density Functional Theory, DFT)计算表明,有效氧还原催化剂表面的电子状态应既有利于氧气分子的吸附并促使O=O双键断裂,又有利于反应中间产物从催化剂表面脱离,使反应顺利进行。Nørskov等人 [6] 的计算显示,纯金属铂表面对于氧分子的结合能过于强,应对铂催化剂进行合理调控,使其表面对氧气的吸附能比Pt{111}晶面弱约0.2 eV,以提高其催化活性。基于这样的理论,PtM合金催化剂被提出并广泛研究,其对于ORR催化活性的提高主要表现在两个方面:几何效应和电子效应。一方面,由于过渡金属原子直径比铂原子小,合金化作用使原有的铂-铂原子间距收缩(几何效应);另一方面,由于过渡金属更容易失电子,使合金颗粒表面电子结构发生改变(电子效应)。两者的协同作用有利于氧气分子在颗粒表面的双址吸附,以及反应产物的脱附,从而进一步提高催化活性 [7]。但是,在这类合金中,过渡金属原子以固溶体形式无序的掺杂在铂晶格中,原子排列仍保持原有铂的面心立方结构(face-centered cubic, fcc),合金催化剂所产生的几何效应和电子效应都不均匀,因而催化活性的提高也有限。同时,无序的过渡金属原子排列使其在酸性条件下很容易从合金颗粒中溶出,存在长时间循环过程中过渡金属溶解的问题,使催化性能迅速下降。
金属间化合物是由两种或多种金属组元按比例结合形成具有不同于其它组成元素的长程有序晶体结构,并且具有金属基本特性的化合物。与合金结构不同,在金属间化合物的晶格结构中,Pt和M原子都有序的占据晶格中相应格点,并以金属键或离子键相互作用,使整个晶体呈现出长程有序的晶系结构,这种长程有序的结构使其具有特殊的催化特性 [8]。根据不同原子比例,一般金属间化合物分为Pt3M,PtM,PtM3相,如图1所示。在Pt3M中(图1(a)),Pt原子占据正方体晶格六个面的中心位置,而M原子占据正方体的八个顶点(PtM3相反);而在PtM中,Pt与M按原子层交替排列(图1(b)~(c)),这种原子排列具有面心四方结构(face centered tetragonal, fct) [9] [10]。这种长程有序的结构不仅使过渡金属的调控作用得到充分发挥,而且与铂原子形成的化学键能更加稳定过渡金属原子,使其不易在酸性条件下溶解,进而更进一步的提高了催化活性和稳定性。近几年对PtM金属间化合物的研究结果均表明具有有序结构的金属间化合物催化剂比无序结构的合金催化剂表现出更好的催化活性和稳定性。早在2004年,Abruña [11] 研究小组就报道了有序金属间化合物电催化剂在燃料电池中的应用,他们制备了一系列的Pt基金属间化合物发现这些催化剂表现出比铂合金和纯金属铂更高的催化活性。
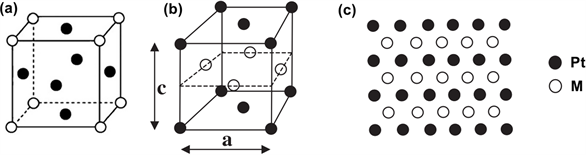
Figure 1. Unit cell atomic structure of intermetallic compounds. (a) Scheme of a Pt3M unit cell; (b) Scheme of a PtM unit cell; (c) Alternate stacking of atoms along the c-axis for PtM ordered materials [9] [10]
图1. 金属间化合物的晶格结构。(a) Pt3M;(b) PtM;(c) PtM晶格沿c轴方向的堆垛结构 [9] [10]
3. Pt基金属间化合物
3.1. PtFe金属间化合物
金属间化合物因具有特殊的有序结构因而表现出优异的物理和化学性能,其早期应用主要是作为超高密度磁性存储材料而吸引了广泛的关注。Shouheng Sun等人于2000年报道了单分散PtFe纳米颗粒的制备方法,在油酸和油胺混合溶液中,他们采用化学还原乙酰丙酮铂(Pt(acac)2)和热分羰基铁(Fe(CO)5)的方法,得到了无序结构的PtFe纳米颗粒。经过500℃的热处理,无序结构转变为有序结构的fct-PtFe纳米粒子 [12]。他们继续研究了fcc-PtFe和fct-PtFe纳米颗粒在0.5 M H2SO4中的阴极氧还原催化活性,发现有序结构的PtFe纳米颗粒表现出比无序颗粒更高的催化活性,并且在酸性溶液中,有序结构中Fe含量降低只有3.3%,而无序结构中Fe含量的损失达到36.5%,充分说明了有序结构对于铁原子的稳定作用 [13]。为了提高催化效率和贵金属的利用率,催化剂材料一般要求具有最大的表面积与体积比,即较小的颗粒尺寸以增加其比表面积,提高贵金属的利用率 [14]。但高温热处理过程往往会引起纳米颗粒的团聚长大,使催化剂的初始活性下降。在接下来的研究中,他们在热处理的过程中,采用MgO包覆PtFe-Fe3O4颗粒,得到完全有序结构的fct-PtFe纳米颗粒。这一催化剂在ORR极化曲线测试中表现出0.958 V的半波电位,其在0.9 V的比表面积比活性和质量比活性分别达到3.16 mA/cm2和0.69 A/mgPt,明显优于部分有序结构和纯铂催化剂 [15]。
另一方面,在制备过程中采用碳层保护也是阻止纳米颗粒长大的一种方法。Xinxin Du等人采用化学气相沉积法,以Fe(CO)5为催化剂、C2H2为碳源先制备得到Fe/C混合物,再采用液相化学还原法,在所得Fe/C混合物表面沉积铂纳米颗粒。在还原过程中,部分铁团簇被氧化,与铂离子发生置换反应,因而形成PtFe颗粒被非晶碳层包覆的结构,在接下来的热处理过程中直接转化为有序的PtFe纳米颗粒,其平均直径约为3.6纳米。所得的催化剂在0.1 M HClO4溶液中的半波电位达到0.89 V,经过3000个电位循环后,半波电位下降了59 mV,但Pt/C催化剂的半波电位下降了140 mV,充分说明了有序化合物的催化稳定性得到提高 [16]。Dong Young Chung等人报道了采用聚多巴胺包覆fcc-PtFe纳米颗粒,然后在约700℃条件下热处理,得到有序的fct-PtFe催化剂。在这一过程中,聚多巴胺原位碳化,直接形成氮掺杂的碳层,包覆在纳米颗粒表面,有效的阻止其团聚长大。在0.9 V,其比表面积比活性和质量比活性分别为2.3 mA/cm2和1.6 A/mgPt,而且,在电位循环的寿命测试中,该催化剂表现出很好的稳定性,几乎没有性能的衰减 [17]。Chanwon Jung等人采用液相还原的方法先制备了Pt-Fe合金纳米颗粒,将其负载在碳载体上后,用1,2十六烷二醇和乙酰丙酮铁为碳源在其表面形成包覆层,经过一系列热处理后得到均匀分散的有序金属间化合物Pt3Fe/C纳米颗粒。该催化剂的质量比活性达到0.454 A/mgPt,由于碳层的保护作用,在长时间的循环过程中没有发生颗粒的团聚和铁的溶出。DFT理论计算表明,铁原子在有序金属间结构中具有比合金中更高的溶解电位,因而比合金Pt-Fe/C更好的稳定性 [18]。
随着制备工艺的不断改进,目前采用多元醇还原的方法,已不需要在合金颗粒表面包覆,即能获得相对较小并均匀分散的金属间纳米颗粒。蔡业政等人 [19] 报道了改进多元醇方法制备碳载铂铁合金催化剂前驱体,然后在惰性气体环境中煅烧,将无序结构合金转化为有序结构的铂铁金属间化合物催化剂。所得催化剂颗粒的尺寸分布为4 nm~6 nm,且均匀负载在载体上,电化学测试结果显示,其催化活性均高于商业Pt/C催化剂。虽然PtFe金属间化合物纳米颗粒表现出了更高的催化活性和稳定性,但是实际燃料电池运行过程中,特别是在电池起停及高电位运行条件下,还是会有少量铁溶解出来。溶出的铁以离子状态存在,与极少量的氧还原反应副产物H2O2即可反应生成具有强氧化性的自由基(即芬顿试剂)。这些自由基会攻击质子交换膜和固体聚合物,使其发生氧化分解,导致质子交换膜破裂,电池失效。因而,目前国际上已经很少使用含有铁基的合金或金属间化合物作为氧还原催化剂。
3.2. PtCo金属间纳米结构
一般而言,由于只有催化剂颗粒表面原子才能接触到电解液和反应物,电催化反应主要发生在纳米颗粒表面,颗粒内部的贵金属不能参加催化反应,造成贵金属利用率低下。为了进一步提高催化活性和铂的利用率,研究人员开发了具有核壳结构的纳米催化剂,通常以低价格金属作为核,多层铂原子为壳层。核的组成和壳层的形貌及二者的相互作用将对催化活性产生至关重要的影响,理论计算研究预测Pt基双金属核壳结构催化剂将具有较好的催化活性和稳定性 [20]。钴元素是另一种极易与铂形成金属间化合物,并且对铂催化活性提高有很大帮助的过渡金属元素。通过精确调控核的结构和组成,可以获得以PtCo有序金属间化合物为核的纳米颗粒 [21]。Deli Wang等人 [22] 报道了有序结构的Pt3Co@Pt/C催化剂,他们将氯铂酸(H2PtCl6·6H2O)和氯化钴(CoCl2·6H2O)溶解在水中,再将碳黑载体分散在上述溶液里,加热蒸发掉溶剂并干燥后,将研磨过的粉末在H2/N2混合气体中分两个阶段加热,最终得到有序的核-壳结构催化剂。实验结果表明,热处理温度达到700℃时,无序结构才能完全转变为有序结构,并且颗粒表面由2~3层Pt原子的排列。在0.1 M HClO4电解液中,该催化剂的比表面积比活性和质量比活性分别是Pt/C催化剂3倍和9倍。Yezheng Cai等人 [23] 用多元醇还原方法先得到PtCo合金纳米颗粒,对比不同热处理温度,发现700℃时制备的Pt3Co/C-700和PtCo/C-700表现出最好的催化活性,充分说明温度是影响有序化的重要因素。
获得核–壳结构催化剂的另外一种方法是去合金化,即通过化学或电化学浸出的方式选择性去除合金纳米颗粒表面的过渡金属,再经过热处理使表面Pt原子重排,形成致密的壳层结构 [24]。Junrui Li等人 [25] 采用液相共还原法先制备出CoPt纳米颗粒,沉积到碳载体上后进行第一次热处理,得到具有有序结构的L10-CoPt/C纳米颗粒。再将该颗粒在0.1 M HClO4溶液中60℃浸泡24小时,分离干燥后在95% Ar和5% H2混合气体下400℃热处理2小时,最终得到L10-CoPt@Pt/C核—壳结构催化剂。这一催化剂的比表面积比活性和质量比活性分别达到8.26 mA/cm2和2.26 A/mgPt,分别是商业Pt/C的38倍和19倍。为了模拟该催化剂在实际电池中的稳定性,加速老化实验在60℃的条件下进行,经过30,000个循环后,L10-CoPt@Pt/C的极化曲线几乎没有发生变化,表现了非常好的稳定性。在实际燃料电池测试中,0.9 V时催化剂的质量比活性为0.56 A/mgPt,30000个循环后只有19%的降低。通过DFT理论计算对比不同催化剂表面铂层自由能的结果表明,当铂原子层厚度相同时,以CoPt为核的催化剂表面对氧还原反应中间产物的吸附能被削弱,证明可以通过应力作用和配位作用对催化剂表面进行有效调控,使其更有利于氧还原反应的发生。计算结果同时证实了Co原子对表面应力的改变作用强于Fe原子,这也是L10-CoPt@Pt/C催化剂性能优于PtFe催化剂的主要原因。这种以PtCo金属间化合物为核,多层铂原子为壳的核壳催化剂具有最大的潜力,成为替代Pt/C的阴极氧还原催化剂。
除了传统的球形纳米颗粒,具有特殊形貌的金属间化合物也被广泛研究。一维纳米线具有各向异性、高柔韧性以及高比表面积的特点,为提高催化活性和稳定性提供了适合的条件。基于对纯铂催化剂的研究已经证实在铂高指数晶面,具有更适宜反应物氧气的吸附能以及中间产物的脱附能,因而具有更高的氧还原催化活性。与纳米颗粒相比,纳米线表面在微观尺度下通常呈现出锯齿状的结构,表面粗糙,并且有更多的突起或凹陷,这些表面多数为高指数晶面。高指数晶面上具有更多的棱、角、面上的活性铂原子,因低配位作用表现出更高的催化活性 [26]。Lingzheng Bu等人 [27] 通过简单的油胺溶液中还原Pt(acac)2和乙酰丙酮钴(Co(acac)2),在160℃条件下即可以得到PtCo金属间结构的纳米线。这种纳米线呈现锯齿状的形貌,表面由高指数晶面[310]和[110]组成,因而很大程度上提高了催化活性。该催化剂在0.9 V时的比表面积比活性和质量比活性分别达到7.12 mA/cm2和3.71 A/mgPt,而且经过20,000个电位循环后质量比活性的保持率仍有90%。
目前,对于金属间化合物催化剂的制备,多采用分步法,即先制备得到金属间化合物纳米颗粒,再利用化学/物理吸附作用沉积在碳载体上,这就造成了金属颗粒与碳载体之间的结合作用不强,容易在长时间循环过和中发生迁移、脱落现象。而且目前使用的载体主要为碳黑,其比表面积不高,孔结构也不够丰富,不能给金属纳米颗粒提供足够的沉积点,且不利于催化剂层的传质过程。因而,通过设计新型的制备工艺,使用具有丰富孔结构的碳载体,增强金属纳米颗粒与载体之间的相互作用,是进一步提高催化活性和稳定性的可行路径 [28]。近年来,有机金属化合物骨架结构(Metal Organic Frameworks, MOF),特别是沸石咪唑酯类骨架材料(Zeolitic Imidazolate Frameworks,ZIFs),由于具有丰富的氮、碳含量和孔道结构,并且高温热解碳化后孔道结构得以保留,成为能源领域内所需碳材料的理想前驱体,引起国内外学者的广泛关注 [29]。由MOF衍生的碳材料也成功的作为PtCo金属间化合物纳米颗粒的载体,我们课题组采用钴掺ZIF-8作为前驱体,在一定条件下碳化后获得含有原子或团簇状钴分散的碳载体,再在其表面沉积铂纳米颗粒,经过一定热处理后得到具有有序结构的Pt3Co-NC系列催化剂 [30]。研究发现,前驱体中钴的掺杂量直接影响了金属间化合物形成时Pt与Co的原子比;后续热处理温度则是决定金属间化合物有序结构能否形成的关键。Lina Chong等人 [31] 也用类似的方法得到了PtCo金属间化合物催化剂,这类催化剂不但在电解液中表现出非常高的催化活性,在实际燃料电池测试中,其质量比活性达到1.08 A/mgPt,并且经过30000次电位循环后,性能保持率为64%。
为了更好的对比不同催化剂的性能,表1列出了目前部分性能优异的铂基金属间化合物氧还原催化剂的活性,并与纯Pt/C及PtM合金催化剂对比。可以明显的看出,金属间化合物催化剂不仅贵金属用量低,而且在催化活性及稳定性上都大大高于传统催化剂,是最具发展前景的氧还原催化剂之一。
Table 1. The catalytic activity for different intermetallic catalysts in acid electrolyte
表1. 不同金属间化合物催化剂在电解液中的催化活性
3.3. 其它Pt基金属间化合物与三元化合物
除了被广泛研究的铁、钴元素,其它过渡金属元素也易与铂形成金属间化合物,包括铜、铅、铝、铋、钛等,铜与钴相比,具有价格低廉的优势。Deli Wang等人 [32] 先用浸渍还原和热处理的方法制备出有序结构的Cu3Pt/C金属间化合物纳米颗粒,然后对比了电化学和化学去合金化方法对颗粒结构的影响。研究发现化学浸出去合金化的方法最终得到的是类似海绵状的PtCu纳米颗粒,而电化学去合金化则形成了以Cu3Pt为核,多层铂原子为壳的核–壳结构,两种方法对于催化活性的提高都起到一定的促进作用。对于电化学去合金化的深入研究表明,不同的扫描速度和电位区间对最终催化剂形貌产生很大影响。优化后的工艺所得到的Cu3Pt/C纳米颗粒中,Pt和Cu元素均匀分布,颗粒表面铂原子层厚度约为0.6 nm~1.0 nm,这一结构使催化性能得到很大提高 [33]。NejcHodnik等人 [34] 系统的研究了具有不同有序化程度的PtCu3纳米颗粒的ORR催化特性,他们采用溶胶-凝胶法制备PtCu合金,在不同的热处理温度下得到有序化程度不同的金属间化合物纳米颗粒。实验结果表明,有序相的比表面积比活性和质量比活性都远高于无序相,其性能提高的主要原因在于有序化的结构更能稳定Cu原子,使其几何效应和电子效应作用更加明显。
铅也被作为掺杂元素应用于金属间化合物中,Ling Zheng Bu等人 [35] 报道了PtPb/Pt核–壳结构的六边形纳米片用作ORR反应催化剂。透射电子显微镜分析显示纳米片边缘的晶格结构与内部结构不同,并在中间存在过渡区域,结合电子能量损失谱面扫描发现,纳米片内部为有序结构的PtPb,表面为4~6层的铂原子层结构。这一催化剂在半电池中表现了很好的催化活性,比表面积比活性和质量比活性分别达到7.8 mA/cm2和4.3 A/mgPt,并且经过50,000次循环后,其质量比活性只有7.7%的衰减。DFT理论分析进一步表明,在垂直和平行于纳米片的两个方向上,Pt壳层与PtPb核之间的相互作用并不相同,由于晶面取向的不同,在不同的Pt晶面上产生了大小不同的压缩应力和拉伸应力,在上下底面以压缩应力为主,而在边缘侧面以拉伸应力为主。正是由于纳米片层这种特殊的结构以及相互作用的应力效应,使PtPb/Pt纳米片催化剂表现出优异的性能。接下来,他们又研究了PtPb/PtNi金属间化合物核–壳催化剂,发现在原有制备PtPb纳米片的体系中加入镍盐,所得催化剂形貌发生变化,具有正八面体的结构,并且不同组分的比例对最终催化活性产生很大影响。优化的实验结果显示PtPb1.12Ni0.14/C正八面体催化剂的质量比活性达到1.92 A/mgPt,其性能的提高主要来源于PtNi壳层与PtPb金属间化合物核之间的相互作用 [36]。
在金属间化合物中添加第三种元素通常会起到更强的协同作用,由于不同元素的原子半径及电子特性有很大差别,所以对Pt原子的电子调控作用更加显著。Sen Zhang等人 [37] 的研究发现,在PtFe合金中引入少量Au元素,可以有助于无序相向有序相的转变,采用液相还原法得到的fcc-PtFeAu纳米颗粒在600°C的时候就转变成为有序结构,所得fct-PtFeAu中金以原子或团簇状态分散在纳米颗粒表面。金的引入显著的提高了ORR催化活性,其主要原因为化学有序结构与金原子的协同效应 [38]。铜在PtFe有序结构中的作用也被深入的研究,通过对比fct-PtFeCu和fct-PtFe催化剂的性能发现,Cu的加入不但提高了催化剂的初始活性,并且长时间循环的稳定性也得到显著提高。由电化学原理可知,合金结构催化剂中过渡金属在酸性条件下的溶解取决于过渡金属本身的氧化还原电位,以及合金中各元素的原子排列 [39]。Fe, Cu, Pt的标准氧化还原电位分别是−0.44,0.34和1.19 V,说明Fe比Cu更容易被氧化,而Cu的引入可以减弱Fe的溶解,这有助于保持原有的有序结构,因而催化剂稳定性得到提高 [40]。另外,PtFeNi [41],PtFeCo [42] [43] 三元金属间化合物也作为ORR催化剂表现出了比无序结构更高的催化活性和稳定性,这与第三种元素带来的电子效应和几何效应,及两者的协同作用有很大关系。
4. 结论与展望
Pt基金属间化合物不仅降低了贵金属的用量,而且基于其特殊的物理化学特性,通过几何及电子效应提高了ORR催化剂的活性和稳定性,是最具发展潜力的催化材料,为PEMFCs进一步商业化提供了有效策略。本文首先对比了无序合金与有序金属间化合物的结构特点,然后综述了不同种类的PtM金属间化合物催化剂,包括其形貌、组成及结构对催化活性及稳定性的影响。目前PtM金属间化合物催化剂的研究取得了很大的进展,但仍然存在很多问题,进一步研发新型催化剂及其面临的挑战可以总结为以下几个方面。
1) 深入研究ORR催化反应机理,在此基础上继续降低金属间化合物中Pt的含量,即调整Pt/M原子比为1/3。目前已研究的催化剂中Pt/M原子比多为3/1或1/1,通过继续研发新型的制备方法,获得Pt含量更低的催化剂。另外,目前过渡金属的研究主要集中在Fe,Co,Cu三种金属,对于其它过渡金属的研究还相对较少。特别是对于某些不易与Pt形成金属间化合物的过渡金属,可以通过添加第三种元素的方法促使其有序化。因而,深入探索新的制备工艺,对催化剂纳米颗粒组成、结构进行精确的设计调控,是进一步提高催化活性和稳定性的有效途径。
2) 研究催化剂在实际燃料电池中的催化性能。目前,大部分氧还原催化剂的研究仍局限在液相半电池体系中,而其在膜电极中的催化特性完全不同。在膜电极中,催化剂层与固体质子交换膜以热压方式结合,与液相相比,增加了电子和质子的传导阻力,使氧还原过程变慢,这也是催化剂在膜电极测试中通常不能达到旋转圆盘电极测试结果的主要原因。因而,优化膜电极制备工艺,研究催化剂在膜电极中的催化特性,对进一步提高活性有着具大的推动作用。
3) 深入研究催化剂在PEMFCs运行条件下性能衰减机制。目前,对于催化剂在液相半电池中经过电位循环或恒定电位寿命测试后的性能衰减,已经过多方面的研究,发现过渡金属的溶解及催化剂颗粒团聚长大是性能下降的主要原因。而对于催化剂在膜电极操作条件下的性能衰减研究较少,需要通过原位的测试技术,探索催化剂在寿命测试过程中的物理、化学特性变化,建立催化剂性能下降与纳米颗粒形貌之间的关系,为进一步提高催化剂稳定性提供理论基础。
基金项目
国家自然科学基金青年基金(21805089),上海市自然科学基金(16ZR1408600),中央高校基本科研业务费(222201814024)。
文章引用
孙 华,戚 頔,刘 辉,邵雷军,王晓霞. Pt基有序金属间化合物氧还原催化剂研究进展
Recent Advances in Pt-Based Ordered Intermetallic Catalysts for Oxygen Reduction Reaction[J]. 材料科学, 2019, 09(05): 479-488. https://doi.org/10.12677/MS.2019.95061
参考文献
- 1. 章俊良, 蒋峰景. 燃料电池——原理关键材料和技术[M]. 上海: 上海交通大学出版社, 2014: 1-5.
- 2. TOYOTA, Fuel Cell Vehicles. http://www.toyota.co.jp/jpn/tech/environment/fcv/index.html
- 3. Nie, Y., Li, L. and Wei, Z. (2015) Recent Advancements in Pt and Pt-Free Catalysts for Oxygen Reduction Reaction. Chemical Society Reviews, 44, 2168-2201. https://doi.org/10.1039/C4CS00484A
- 4. Shao, M., Chang, Q., Dodelet, J.-P. and Chenitz, R. (2016) Recent Advances in Electrocatalysts for Oxygen Reduction Reaction. Chemical Reviews, 116, 3594-3657. https://doi.org/10.1021/acs.chemrev.5b00462
- 5. Strasser, P. and Kühl, S. (2016) Dealloyed Pt-Based Core-Shell Oxygen Reduction Electrocatalysts. Nano Energy, 29, 166-177. https://doi.org/10.1016/j.nanoen.2016.04.047
- 6. Nørskov, J.K., Rossmeisl, J., Logadottir, A., Lindqvist, L., Kitchin, J.R., Bligaard, T. and Jónsson, H. (2004) Origin of the Overpotential for Oxygen Reduction at a Fuel-Cell Cathode. The Journal of Physical Chemistry B, 108, 17886-17892. https://doi.org/10.1021/jp047349j
- 7. Strasser, P., Koh, S., Anniyev, T., Greeley, J., More, K., Yu, C., Liu, Z., Kaya, S., Nordlund, D., Ogasawara, H., Toney, M.F. and Nilsson, A. (2010) Lattice-Strain Control of the Activity in Dealloyed Core-Shell Fuel Cell Catalysts. Nature Chemistry, 2, 454-460. https://doi.org/10.1038/nchem.623
- 8. Furukawa, S. and Komatsu, T. (2016) Intermetallic Compounds: Promising Inorganic Materials for Well-Structured and Electronically Modified Reaction Environments for Efficient Catalysis. ACS Catalysis, 7, 735-765. https://doi.org/10.1021/acscatal.6b02603
- 9. Luo, M., Sun, Y., Wang, L. and Guo, S. (2017) Tuning Multimetallic Ordered Intermetallic Nanocrystals for Efficient Energy Electrocatalysis. Advanced Energy Materials, 7, Article ID: 1602073. https://doi.org/10.1002/aenm.201602073
- 10. Frommen,C. and Rösner, H. (2004) Observation of Long-Period Superstructures in Chemically Synthesised CoPt Nanoparticles. Materials Letters, 58, 123-127. https://doi.org/10.1016/S0167-577X(03)00428-2
- 11. Casado-Rivera, E., Volpe, D.J., Alden, L., Lind, C., Downie, C., Vázquez-Alvarez, T., Angelo, A.C., Disalvo, F.J. and Abruña, H.D. (2004) Electrocatalytic Activity of Ordered Intermetallic Phases for Fuel Cell Applications. Journal of the American Chemical Society, 126, 4043-4049. https://doi.org/10.1021/ja038497a
- 12. Sun, S., Murray, C.B., Weller, D., Folks, L. and Moser, A. (2000) Mono-disperse FePt Nanoparticles and Ferromagnetic FePt Nanocrystal Superlattices. Science, 287, 1989-1992. https://doi.org/10.1126/science.287.5460.1989
- 13. Kim, J., Lee, Y. and Sun, S. (2010) Structurally Ordered FePt Nanoparticles and Their Enhanced Catalysis for Oxygen Reduction Reaction. Journal of the American Chemical Society, 132, 4996-4997. https://doi.org/10.1021/ja1009629
- 14. Li, X., An, L., Wang, X., Li, F., Zou, R. and Xia, D. (2012) Supported Sub-5nm Pt-Fe Intermetallic Compounds for Electrocatalytic Application. Journal of Materials Chemistry, 22, 6047-6052. https://doi.org/10.1039/c2jm16504j
- 15. Li, Q., Wu, L., Wu, G., Su, D., Lv, H., Zhang, S., Zhu, W., Casimir, A., Zhu, H., Mendoza-Garcia, A. and Sun, S. (2015) New Approach to Fully Ordered fct-FePt Nanoparticles for Much Enhanced Electrocatalysis in Acid. Nano Letters, 15, 2468-2473. https://doi.org/10.1021/acs.nanolett.5b00320
- 16. Du, X.-X., He, Y., Wang, X.-X. and Wang, J.-N. (2016) Fi-ne-Grained and Fully Ordered Intermetallic PtFe Catalyst with Largely Enhanced Catalytic Activity and Durability. Energy & Environmental Science, 9, 2623-2632. https://doi.org/10.1039/C6EE01204C
- 17. Chung, D.-Y., Jun, S.-W., Yoon, G., Kwon, S.-G., Shin, D.Y., Seo, P., Yoo, J.-M., Shin, H., Chung, Y.-H., Kim, H., Mun, B.-S., Lee, K.-S., Lee, N.-S., Yoo, S.-J., Lim, D.-H., Kang, K., Sung, Y.-E. and Hyeon, T. (2015) Highly Durable and Active PtFe Nanocatalyst for Electrochemical Oxygen Reduction Reaction. Journal of the American Chemical Society, 137, 15478-15485. https://doi.org/10.1021/jacs.5b09653
- 18. Jung, C., Lee, C., Bang, K., Lim, J., Lee, H., Ryu, H.-J., Cho, E. and Lee, H.-M. (2017) Synthesis of Chemically Ordered Pt3Fe/C Intermetallic Electrocatalysts for Oxygen Reduction Reaction with Enhanced Activity and Durability via a Removable Carbon Coating. ACS Applied Materials & Interfaces, 9, 31806-31815. https://doi.org/10.1021/acsami.7b07648
- 19. 蔡业政, 骆明川, 王芳辉, 孙照楠, 朱红. 合成具有高氧还原反应催化活性的结构有序铂铁合金催化剂[J]. 电化学, 2016, 22(2): 185-191.
- 20. Lebedeva, M.V., Pierron-Bohnes, V., Goyhenex, C., Papaefthimiou, V., Zafeiratos, S., Nazmutdinov, R.R., Da Costa, V., Acosta, M., Zosiak, L., Kozubski, R., Muller, D. and Savinova, E.R. (2013) Effect of the Chemical Order on the Electrocatalytic Activity of Model PtCo Electrodes in the Oxygen Reduction Reaction. Electrochimica Acta, 108, 605-616. https://doi.org/10.1016/j.electacta.2013.07.038
- 21. Xiong, Y., Xiao, L., Yang, Y., DiSalvo, F.J., Abruña, H.D. (2018) High-Loading Intermetallic Pt3Co/C Core-Shell Nanoparticles as Enhanced Activity Electrocatalysts toward the Oxygen Reduction Reaction (ORR). Chemistry of Materials, 30, 1532-1539. https://doi.org/10.1021/acs.chemmater.7b04201
- 22. Wang, D., Xin, H.-L., Hovden, R., Wang, H., Yu, Y., Muller, D.A., DiSalvo, F.J. and Abruña, H.D. (2013) Structurally Ordered Intermetallic Platinum-Cobalt Core-Shell Na-noparticles with Enhanced Activity and Stability as Oxygen Reduction Electrocatalysts. Nature Materials, 12, 81-87. https://doi.org/10.1038/nmat3458
- 23. Cai, Y., Gao, P., Wang, F. and Zhu, H. (2017) Carbon Supported Chemi-cally Ordered Nanoparicles with Stable Pt Shell and Their Superior Catalysis toward the Oxygen Reduction Reaction. Electrochimica Acta, 245, 924-933. https://doi.org/10.1016/j.electacta.2017.04.173
- 24. Jia, Q., Caldwell, K., Ramaker, D.E., Ziegelbauer, J.M., Liu, Z., Yu, Z., Trahan, M. and Mukerjee, S. (2014) In Situ Spectroscopic Evidence for Ordered Core–Ultrathin Shell Pt1Co1 Nanoparticles with Enhanced Activity and Stability as Oxygen Reduction Electrocatalysts. Journal of Physical Chemistry C, 118, 20496-20503. https://doi.org/10.1021/jp507204k
- 25. Li, J., Sharma, S., Liu, X., Pan, Y.-T., Spendelow, J.S., Chi, M., Jia, Y., Zhang, P., Cullen, D.A., Xi, Z., Lin, H., Yin, Z., Shen, B., Muzzio, M., Yu, C., Kim, Y.S., Peterson, A.A., More, K.L., Zhu, H. and Sun, S. (2019) Hard-Magnet L10-CoPt Nanoparticles Advance Fuel Cell Catalysis. Joule, 3, 124-135. https://doi.org/10.1016/j.joule.2018.09.016
- 26. Hoshi, N., Nakamura, M. and Hitotsuyanagi, A. (2013) Active Sites for the Oxygen Reduction Reaction on the High Index Planes of Pt. Electrochimica Acta, 112, 899-904. https://doi.org/10.1016/j.electacta.2013.05.045
- 27. Bu, L., Guo, S., Zhang, X., Shen, X., Su, D., Lu, G., Zhu, X., Yao, J., Guo, J. and Huang, X. (2016) Surface Engineering of Hierarchical Platinum-Cobalt Nanowires for Efficient Electrocatalysis. Nature Communications, 7, Article No. 11850. https://doi.org/10.1038/ncomms11850
- 28. Yarlagadda, V., Carpenter, M.K., Moylan, T.E., Kukreja, R.S., Koestner, R., Gu, W., Thompson, L. and Kongkanand, A. (2018) Boosting Fuel Cell Performance with Accessible Carbon Mesopores. ACS Energy Letters, 3, 618-621. https://doi.org/10.1021/acsenergylett.8b00186
- 29. Guan, B.-Y., Yu, X.-Y., Wu, H.-B. and Lou, X.-W. (2017) Complex Nanostructures from Materials Based on Metal-Organic Frameworks for Electrochemical Energy Storage and Conversion. Advanced Materials, 29, Article ID: 1703614. https://doi.org/10.1002/adma.201703614
- 30. Wang, X.-X., Hwang, S., Pan, Y.-T., Chen, K., He, Y., Karakalos, S., Zhang, H., Spendelow, J.S., Su, D. and Wu, G. (2018) Ordered Pt3Co Intermetallic Nanoparticles Derived from Metal-Organic Frameworks for Oxygen Reduction. Nano Letters, 18, 4163-4171. https://doi.org/10.1021/acs.nanolett.8b00978
- 31. Chong, L., Wen, J., Kubal, J., Sen, F.G., Zou, J., Greeley, J., Chan, M., Barkholtz, H., Ding, W. and Liu, D.-J. (2018) Ultralow-Loading Platinum-Cobalt Fuel Cell Catalysts Derived from Imidazolate Frameworks. Science, 362, 1276-1281. https://doi.org/10.1126/science.aau0630
- 32. Wang, D., Yu, Y., Xin, H.L., Hovden, R., Ercius, P., Mundy, J.A., Chen, H., Richard, J.H., Muller, D.A. and Disalvo, F.J. (2012) Tuning Oxygen Reduction Reaction Activity via Con-trollable Dealloying: A Model Study of Ordered Cu3Pt/C Intermetallic Nanocatalysts. Nano Letters, 12, 5230-5238. https://doi.org/10.1021/nl302404g
- 33. Wang, D., Yu, Y., Zhu, J., Liu, S., Muller, D.A. and Abruña, H.D. (2015) Morphology and Activity Tuning of Cu3Pt/C Ordered Intermetallic Nanoparticles by Selective Electrochemical Deal-loying. Nano Letters, 15, 1343-1348. https://doi.org/10.1021/nl504597j
- 34. Hodnik, N., Jeyabharathi, C., Meier, J.C., Kostka, A., Phani, K.L., Recnik, A., Bele, M., Hocevar, S., Gaberscek, M. and Mayrhofer, K.J.J. (2014) Effect of Ordering of PtCu3 Nanoparticle Structure on the Activity and Stability for the Oxygen Reduction Reaction. Physical Chemistry Chemical Physics, 16, 13610-13615. https://doi.org/10.1039/C4CP00585F
- 35. Bu, L., Zhang, N., Guo, S., Zhang, X., Li, J., Yao, J., Wu, T., Lu, G., Ma, J.-Y., Su, D. and Huang, X. (2016) Biaxially Strained PtPb/Pt Core/Shell Nanoplate Boosts Oxygen Reduction Catalysis. Science, 354, 1410-1414. https://doi.org/10.1126/science.aah6133
- 36. Bu, L., Shao, Q., B, E., Guo, J., Yao, J., Huang, X. (2017) PtPb/PtNi Intermetallic Core/Atomic Layer Shell Octahedra for Efficient Oxygen Reduction Electrocatalysis. Journal of the American Chemical Society, 139, 9576-9582. https://doi.org/10.1021/jacs.7b03510
- 37. Zhang, S., Guo, S., Zhu, H., Su, D. and Sun, S. (2012) Struc-ture-Induced Enhancement in Electrooxidation of Trimetallic FePtAu Nanoparticles. Journal of American Chemistry Society, 134, 5060-5063. https://doi.org/10.1021/ja300708j
- 38. Zhu, H., Cai, Y., Wang, F., Gao, P. and Cao, J. (2018) Scalable Preparation of the Chemically Ordered Pt-Fe-Au Nanocatalysts with High Catalytic Reactivity and Stability for Oxygen Reduction Reactions, ACS Applied Materials & Interfaces, 10, 22156-22166. https://doi.org/10.1021/acsami.8b05114
- 39. Sasaki, K., Naohara, H., Choi, Y., Cai, Y., Chen, W.-F., Liu, P. and Adzic, R.R. (2012) Highly Stable Pt Monolayer on PdAu Nanoparticle Electrocatalysts for the Oxygen Reduction Re-action. Nature Communications, 3, Article No. 1115. https://doi.org/10.1038/ncomms2124
- 40. Arumugam, B., Tamaki, T. and Yamaguchi, T. (2015) Beneficial Role of Copper in the Enhancement of Durability of Ordered Intermetallic PtFeCu Catalyst for Electrocatalytic Oxygen Reduction. ACS Applied Materials & Interfaces, 7, 16311-16321. https://doi.org/10.1021/acsami.5b03137
- 41. Kuroki, H., Tamaki, T., Matsumoto, M., Arao, M., Kubobuchi, K., Imai, H. and Yamaguchi, T. (2016) Platinum-Iron-Nickel Trimetallic Catalyst with Superlattice Structure for Enhanced Oxygen Reduction Activity and Durability. Industrial & Engineering Chemistry Research, 55, 11458-11466. https://doi.org/10.1021/acs.iecr.6b02298
- 42. Tamaki, T., Minagawa, A., Arumugam, B., Kakade, B.A. and Yamaguchi, T. (2014) Highly Active and Durable Chemically Ordered Pt-Fe-Co Intermetallics as Cathode Catalysts of Membrane-Electrode Assemblies in Polymer Electrolyte Fuel Cells. Journal of Power Sources, 271, 346-353. https://doi.org/10.1016/j.jpowsour.2014.08.005
- 43. Arumugam, B., Kakade, B., Tamaki, T., Arao, M., Imai, H. and Yamaguchi, T. (2014) Enhanced Activity and Durability for the Electroreduction of Oxygen at a Chemically Ordered Intermetallic PtFeCo Catalyst. RSC Advances, 4, 27510-27517. https://doi.org/10.1039/C4RA04744C
NOTES
*通讯作者。
