Nuclear Science and Technology
Vol.05 No.03(2017), Article ID:21369,11
pages
10.12677/NST.2017.53019
Recent Advances on Palladium Alloy Membranes for Hydrogen Purification
Zhan Zhao, Shilin Hu, Yiming Ye
China Institute of Atomic Energy, Beijing

Received: Jul. 3rd, 2017; accepted: Jul. 11th, 2017; published: Jul. 14th, 2017

ABSTRACT
With the development of science and technology, there is an ever-growing demand for hydrogen in the fields of chemistry and chemical industry, food industry, medical industry, and also nuclear industry. The requirements for the purity of hydrogen have been changed to higher and higher. Palladium alloy membrane has higher hydrogen permeability, good thermal stability and chemical stability, and mechanical strength, as well as a single selectivity to the chemical hydrogen, so it now has become the main method of extraction, separation and purification of hydrogen. This paper mainly introduces the permeation mechanism and preparation methods of palladium alloy membrane, and the researching status of the binary and ternary of palladium alloy membranes, also briefly introduces several palladium alloy membranes currently the most widely concerned, including Pd-Ag alloy and Pd-Y alloy, Pd-Cu alloy, Pd-Ag-Au alloy etc.
Keywords:Palladium Alloy Membrane, Hydrogen Purification, Binary Alloy, Ternary Alloy
钯合金氢渗透膜的研究进展
赵展,胡石林,叶一鸣
中国原子能科学研究院,北京
收稿日期:2017年7月3日;录用日期:2017年7月11日;发布日期:2017年7月14日

摘 要
随着科技的发展,氢气在化学化工、食品医疗以及核工业领域中的需求量越来越大,对纯度的要求也越来越高。钯合金膜由于具有较高的氢气渗透性,良好的热稳定性、化学稳定性及机械强度,以及对氢具有单一选择性等优点,成为了目前氢提取、分离和纯化的主要方法。本文主要介绍了钯合金膜的氢渗透机理、制备方法,以及二元及三元钯合金膜的研究现状,对目前受到最广泛关注的几种钯合金膜进行了简要的介绍,包括Pd-Ag合金、Pd-Y合金、Pd-Cu合金、Pd-Ag-Au合金等。
关键词 :钯合金膜,氢纯化,二元合金,三元合金

Copyright © 2017 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
随着科技的发展,氢在工业生产中的地位愈发重要,人们对氢的需求量也越来越大,对纯度的要求越来越高,在精细有机合成、冶金和电子工业、食品工业和医疗工业以及一些科学实验中,都需要用到高纯甚至超高纯氢气。在核工业领域中,同样涉及到氢(同位素)纯化工艺的应用。在聚变反应堆运行时,由于高温等离子气体对反应堆材料的烧烛,等离子排除气中存在大量He、N2、O2、Q2、CQ4、NQ3 (Q表示H、D、T),这些气体的积累会导致等离子室温度降低,影响聚变反应的持续进行。因此,必须及时除去杂质气体,同时回收其中含有氘氚成分的气体进行循环利用 [1] 。在Candu型反应堆中,重水作为反应堆的慢化剂和冷却剂,运行时由于中子照射将不断产生氚,从重水堆的含氚重水中提氚,成本低、效率高,是一种稳定的氚来源。以我国秦山核电站三期为例,其氚的生成量估计每年可达200 g。同时,通过对重水中的氚进行提取,不但可以降低动力堆放射性辐射水平,而且可以对重水进行升级,对提高资源利用率、保护环境安全及人员安全都具有重要意义 [2] 。由于氚具有放射性,相较于氕、氘而言,氚纯化对工艺的要求更苛刻。钯合金膜由于具有较高的氢(同位素)气渗透性,良好的热稳定性、化学稳定性及机械强度,以及对氢(同位素)具有单一选择性等优点,成为了目前氢(同位素)提取、分离和纯化的主要方法。
2. 渗透机理
科研人员对于钯及其合金膜的渗氢机理进行了广泛的研究,普遍的观点认为它的渗氢过程遵循溶解-扩散(solution-diffusion)机理,氢气从膜的高压侧向低压侧渗透,如图1所示。
具体过程包括以下七个步骤 [3] :
(a) 高压侧氢气分子扩散至金属膜表面,(b) 氢气分子在金属表面被吸附并解离为氢原子,(c) 氢原子在金属内部晶格中溶解,(d) 氢原子在金属内部向低压侧表面扩散,(e) 氢原子在金属表面结合成氢分子,(f) 氢气分子从膜表面脱附,(g) 氢气分子在表面扩散并离开(图2)。
氢气在钯膜中的渗透扩散达到稳态时,若在氢的渗透过程中氢在钯内的扩散过程是氢气渗透过程的速率控制步骤(即膜厚 > 10 μm,表面洁净未发生毒化作用),氢气扩散速率F(mol·s−1)由Fick定律及Sievert定律推导表示为:


Figure 1. Hydrogen permeation through a Pd membrane
图1. 钯膜氢渗透示意图

Figure 2. Solution-diffusion mechanism
图2. 溶解-扩散机理
式中,Π为扩散系数,mol·m−1·s−1·Pa−n;A为膜面积,m2;t为膜厚度,m;Ph、Pl分别为钯膜高、低压两侧的氢分压;n为压力指数,由Sievert定律n = 0.5。若膜厚度较小(<1 μm)或表面污染增加时,表面过程在氢气渗透过程中逐渐发挥作用,成为速率控制步骤,压力指数n = 1;表面过程和体相过程共同控制氢气渗透时,压力指数n = 0.5~1。此外,受浓差极化、外扩散阻力、膜操作压力、温度条件、载体阻力及膜致密性等因素的影响,氢气渗透速率都可能偏离Sievert定律。因此,氢气在钯膜中的渗透扩散过程十分复杂 [4] [5] 。
3. 制备方法
按结构的不同,钯合金膜主要分为自支撑膜和支撑体复合膜。支撑体复合膜由于具有提供机械强度的多孔基体作为支撑体,其所需要的金属层厚度比自支撑合金膜薄得多,因此氢渗透性更高,成本更低,因此本文主要介绍支撑体复合膜的制备。
用于制备钯(合金)氢渗透膜的多孔支撑体材料主要有两种,多孔金属支撑体和多孔陶瓷支撑体。多孔陶瓷支撑体具有更好的表面性质,可以承载更薄的选择透过层,但同时,陶瓷载体的机械强度较低,相较于金属而言更脆。目前,商用的陶瓷支撑体多为多孔陶瓷管或中空纤维。管状陶瓷支撑体主要由两部分组成:经过挤压处理的多孔陶瓷基体以及通过溶胶-凝胶法等技术覆盖于基体之上的光滑、多孔的陶瓷层。相较于陶瓷而言,金属支撑体机械强度更高,且热膨胀系数与钯(合金)相近,支撑体与钯(合金)层的热稳定性更好,但就目前已经商业化的金属支撑体(主要为管状)而言,其表面性质较差,并且金属支撑体与钯(合金)层之间存在金属间扩散,使渗透性降低。目前多孔陶瓷支撑体(主要为多孔氧化铝)的应用更为广泛。
复合钯(合金)膜的制备主要在于将钯及其他金属负载于支撑体上。目前主要的制备方法有物理气相沉积法(PVD),化学气相沉积法(CVD或MOCVD),化学镀(Electroless plating),电镀(Electroplating)以及扩散焊接(Diffusion welding)等技术 [4] 。每种技术都有各自的优势和缺点,因此,在制备钯合金膜时针对所使用载体的性质选用合适的沉积方法是十分必要的,这样制备出来的复合膜性能会更好。
3.1. 物理气相沉积(PVD)
物理气相沉积(PVD)主要包括磁控溅射、热蒸发、脉冲激光蒸发等方法,是指用物理的方法,在真空条件下将材料表面汽化成原子、分子或部分电离成离子,并通过气相(蒸汽或等离子体)过程,在材料或工件表面沉积一层具有某些特殊性能的薄膜。PVD技术是制造金属合金和化合物薄膜的一种通用的技术,可以得到较薄的膜层(<1 μm)。对多组分的合金,由于各组分金属的分压不一样,汽化速率不相同,直接沉积合金膜则较难实现,可依次沉积各组分而后经高温热处理使多层不同材料的膜的组成均匀化,各组分的比例由气化速率来调节。PVD法拥有更快的沉积速率,并能更加方便简单地控制薄膜的厚度及组成,但设备费用较高,所得到的钯(合金)膜厚度不均匀。
3.2. 化学气相沉积法(CVD)
化学气相沉积装置由反应物供应系统、气相反应器和气流传送系统组成,其过程是分子水平上的气-固相反应,即将含有构成薄膜元素的气态反应剂或液态反应剂的蒸气及反应所需其它气体引入反应室,在衬底表面发生化学反应生成薄膜的过程。此法优点是沉积速率快,镀层化学成分可以随气相组成的改变而变化,制备的钯膜厚度容易控制,一般为2~6 μm。但此法要求金属源有良好的挥发性和热稳定性,并且升华温度低于分解温度,金属源中所含有机物对膜易造成污染,金属源价格昂贵,制备过程钯收率低,易浪费。
3.3. 化学镀(ELP)
化学镀化学反应沉积镀膜法的一种。该技术是亚稳态金属盐络合物在目标表面上进行可控的自催化分解或还原反应的过程。化学镀技术中,常用钯的络合物,如Pd(NH3)4(NO3)2、Pd(NH3)4Br2或Pd(NH3)4Cl2等作为镀液,典型的还原剂为肼或连二磷酸盐。
化学镀反应需要催化剂进行引发。一般的支撑体由于目标表面活性不足,需要预种钯晶核以催化化学镀反应,反应产生的钯镀层表面进一步催化溶液中的金属离子,使其不断还原而沉积在载体表面上,因此也被称为自催化化学镀。化学镀设备简单,不需电源。可以在任何复杂形状和大表面积的支撑体上进行均匀沉积。底膜可以为非导体表面(电镀只适用于导体基体)。所得膜层薄且均匀、紧密、机械强度高。因而,在所有钯复合膜的制备技术中,化学镀技术最受欢迎。
表1对比了上述三种镀膜方法的优缺点。
4. 钯合金膜
Pd及Pd合金在氢纯化方面的研究已经有了相当长的时间。纯Pd膜在应用时最大的问题是氢脆现象。如图3 [6] 所示,Pd-H体系存在间隙固溶体(α相)和P钯氢化物(β相)两种形式,两相都具有相同的fcc (面心立方)晶体结构,但二者晶格常数不同。纯钯的晶格常数为3.89 Å (1 Å = 0.1 nm)。在室温下,H/Pd原子比例达到约0.02(记为αmax)之前,体系以α相形式存在,当H/Pd原子比例达到约0.6(记为βmin)后,体系以β相形式存在,两相的晶格常数分别为3.895 Å和4.025 Å [7] 。二者中间的两相共存区域称为混溶隙,由于α、β相晶格常数的差异,通过混溶隙循环Pd膜可能导致超过10%的晶格体积膨胀(或缩小),从而导致钯膜中产生严重的应力, 导致位移增加、材料变形、硬化, 使钯经历数次氢化/脱氢循环后过早破裂,这种现象被称为氢脆。
为避免氢脆现象的发生,需要一直在高于临界温度(Tc,纯钯时约为298℃)的条件下进行操作,此时β相只能在氢气压力极高的情况下才能形成。而若在金属钯中引入其他金属元素(如Ag、Cu、Fe、Ni、Pt、Y等)组成合金,则能够显著降低α-β相转变的临界温度(Tc),从而更容易避免氢脆现象的发生。另外,引入其他合金还能显著提高钯膜对进料气体中杂质(主要为H2S、CO等)毒化作用的抗性,从而进一步提高膜的寿命。图4为一些金属的氢渗透性随温度变化曲线 [8] 。
由于这些金属可能组合的数目太多,研究人员使用建模计算的方法验证制备氢纯化膜的最合适的组合。其中密度泛函(DFT)理论是人们很感兴趣的一种方法,用来预测各种二元或三元合金在纯氢或混合气体条件下的表现。
Table 1. Comparison: advantages and disadvantages of each method
表1. 镀膜各方法优缺点比较

Figure 3. P-C-T phase diagram of the palladium-hydrogen system
图3. Pd-H体系P-C-T相图
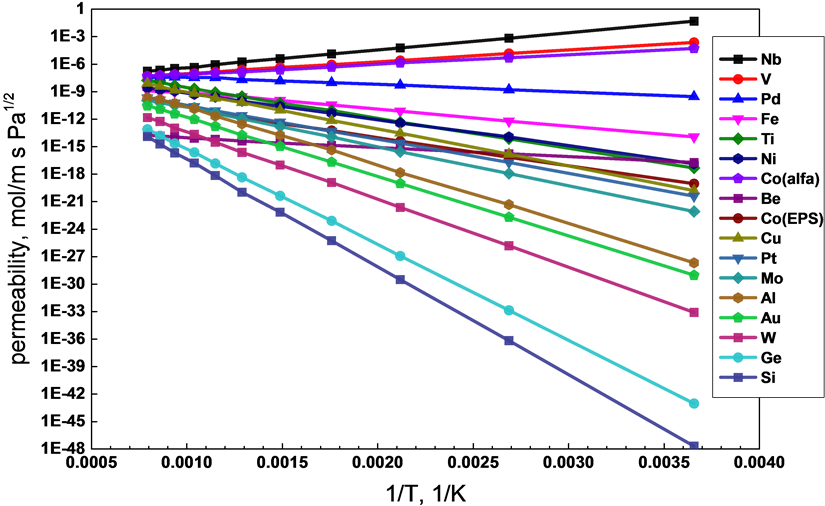
Figure 4. Hydrogen permeability through several metals as a function of temperature
图4. 几种金属的氢渗透性随温度变化曲线
4.1. 计算预测
Sholl团队 [9] 发表了一系列的论文,阐述了DFT在预测不同合金中氢的溶解度及扩散系数上的潜力,这为未来氢纯化合金膜的制备指明了方向。在对Pd-Cu基三元合金的研究中,作者运用DFT寻找对Pd-Cu合金有效的三元添加物,在保留二元合金良好的抗毒化性能的同时提升整体的氢渗透性。通过计算,他们发现在不同的添加物(如Ni、Au、Ag、Rh、Pt)中,Au或Ag能够将合金的渗透性提升5倍。同时他们发现对于Pd-Cu-Ag合金,渗透性的提升主要是由于Ag的加入提升了合金对氢的溶解度,而非扩散速度。这表明在实际操作中通过加入第三元添加物来提升Pd-Cu合金对氢的溶解度是值得尝试的。对于二元合金来说溶解度同样很重要,Sonwane等 [10] 使用DFT计算发现,Ag含量为30%的Pd-Ag合金对氢的溶解度最大,Pd-Au合金则在Au含量为20%时溶解度达到最大值。同纯Pd相比,Pd-Ag (30% Ag)合金对氢的溶解度提升了10倍。
DFT同样可以用来评价混合氢气中杂质气体对渗透性的影响,人们发现,CO对氢渗透性的影响主要是因为金属对CO会优先吸附,占据了H2的吸附位置,另外CO会在不同空位中跳跃,因此少量的CO也会对氢渗透性产生极大的影响 [11] [12] 。Ozdogan和Wlicox的研究表明,H2S在金属膜表面的吸附取决于Pd合金中的另一种金属,他们发现几种金属对H2S的结合能力顺序为Cu < Pd < Nb,因此Pd-Cu合金对H2S的抗性更强 [13] 。Ling和Sholl认为,在膜上硫化物的产生会极大地降低渗透性主要是因为H原子穿过硫化物层的速度极慢 [14] 。
4.2. 实验成果
4.2.1. 钯二元合金
如表2,显示了一些研究人员制备的二元合金的组成及氢渗透性。就二元合金而言,在氢气渗透性和机械/化学性能方面,前三种合金是Pd-Ag,Pd-Y和Pd-Cu。
Pd-Ag合金
Table 2. Hydrogen permeability of Pd and miscellaneous Pd binary alloys at 350˚C
表2. 350℃下纯钯及一些二元钯合金的组成及氢渗透性
在所有钯合金中,Pd-Ag合金是最为著名的,并且也受到了最广泛的研究。如表2所示,其氢渗透性几乎是纯Pd的两倍。Pd与Ag组成合金降低了混溶隙的临界温度,如合金Pd23Ag77 wt%的临界温度在室温以下,因此不需要在热循环之前从膜中清除氢气 [22] [23] 。尽管它们在氢渗透时会由于显著的晶格膨胀而呈现较短的寿命周期,并且在高温下易发生晶粒粗化,Pd-Ag合金仍然是目前最常用的商业钯合金净化器材料 [24] 。此外,与其它Pd合金如Pd-Y和Pd-Cu相比,Pd-Ag合金具有相对低的强度。另一个值得注意的问题是,化石燃料的价格对Ag (和Au)的价值有直接的影响,这可能增加这种合金的成本,降低其在商业上的吸引力。
Pd-Y合金
如表2可知,Pd-Y合金体系(包括以Pd-Y为主的三元合金)的氢气渗透性在所有钯合金中最高,Pd92Y8 at.%膜在400℃下的氢渗透性几乎是Pd76Ag24 at.%膜的2.5倍。另外,与Hume-Rothery提出的15%规则(即如果形成合金的元素的原子半径之差超过了14%~15%,则固溶度极为有限)相反,哈里斯和诺曼 [25] 发现,尽管Y原子比Pd原子大约30%,Y可溶于Pd至12 at.%。因此,由于Pd-Y合金拥有较高的原子错配度,使其具有优异的抗拉强度。尽管Pd-Y合金具有很多优点,但到目前为止其尚未商业化。这可能是因为Pd-Y合金在冷加工过程中会发生加工硬化,这意味着在将合金加工成膜的过程中需要进行几个昂贵的退火阶段。
Pd-Cu合金
同纯钯膜相比,Pd-Cu合金具有许多优点。图5为350℃下Pd-Cu合金氢渗透性曲线 [26] 。从图5中可知,Cu含量约为53 at.%时合金的氢渗透性最高。
这是由于在该含量范围附近,合金的晶体结构发生了变化,有fcc转变成bcc,如图6所示。这种变化使得氢在合金中的扩散系数提高了两个数量级。在室温下,Piper [27] 使用电阻率法测得Pd60Cu40 wt% BCC相的氢扩散系数为5 × 10−5 cm−1·s−1,比相同温度下纯钯高了300倍。而且,尽管Pd-Cu合金的氢渗透性并不比Pd-Ag和Pd-Y合金更高,但它具有优异的机械强度,并对H2S等杂质的污染表现出很强的抗性 [28] [29] 。并且,由于铜的价格更便宜,这种合金在成本方面有着很强的竞争力。
4.2.2. 钯三元合金
同二元合金相比,钯的三元合金更加复杂,这主要表现在其晶体结构更加多变,而且可能的成分组

Figure 5. Hydrogen permeability versus palladium content at 350˚C
图5. 350℃下Pd-Cu合金氢渗透性随Pd含量变化曲线

Figure 6. High temperatures Pd-Cu phase diagram
图6. 高温下Pd-Cu合金相图
Table 3. Hydrogen permeability of miscellaneous Pd ternary alloys
表3. 一些三元钯合金的组成及氢渗透性
合更多。但这也导致了三元合金具有一些比二元合金更加优秀的性能,比如更高的氢渗透性,更好的机械强度,以及更强的毒化抗性。目前对三元钯合金研究较少,比较受关注的合金主要为Pd-Ag-Au、Pd-Cu-Ag等。表3列出了一些三元钯合金的组成及氢渗透性。
Pd-Ag-Au合金
尽管Pd-Ag合金具有很高的氢渗透性,但其毒化抗性很差。为了加强合金的毒化抗性,Fernando Braun [30] 等比较了Pd、Pd90Ag10、Pd91Au9、Pd78Ag9Au13以及Pd75Ag16Au9合金膜在纯H2和H2S/H2混合气中的渗透性,发现在纯氢中,合金膜的氢渗透性排序为:Pd90Ag10 > Pd78Ag9Au13 > Pd~Pd75Ag16Au9 > Pd91Au9。在温度为673 K时,暴露在100 ppm的H2S/H2中24小时后,各合金膜的氢渗透性发生了明显的下降:Pd (下降最明显,85%) > Pd90Ag10 > Pd75Ag16Au9 > Pd78Ag9Au13 > Pd91Au9 (60%)。去除H2S后,各合金膜下降的氢渗透性有了不同程度的恢复。Pd91Au9和Pd78Ag9Au13合金膜氢渗透性的恢复最明显,约达到初始氢渗透性的80%。考虑到各合金膜初始渗透性的差别,恢复后Pd78Ag9Au13膜的氢渗透性最高。这表明Au金属的添加能有效加强合金的毒化抗性。
Pd-Cu-Ag合金
Shahrouz Nayebossadri [35] 等研究了在Pd-Cu合金中添加少量金属银对膜的氢溶解度、扩散性以及渗透性的影响。他们发现,加入的Ag原子分数为2.3%和3.9%时,晶格扩张了0.11%和0.35%。通过原位XRD测试对合金膜进行结构分析,结果表明当加热至600℃时,Ag原子含量为2.3%的合金仍然保持bcc结构,而在Ag原子含量为3.9%的合金中生成了fcc相,导致合金变成bcc + fcc混合结构。同时,当温度在350℃~400℃之间时,两种Pd-Cu-Ag三元合金的扩散系数比与其结构相似的Pd-Cu二元合金更低,但溶解度更高。扩散系数的降低是由于Ag的存在提高了扩散所需要的活化能,溶解度升高则是由于晶格的扩张以及Ag-H的强相互作用。氢渗透性测试的结果表明,对于只存在bcc相的Pd45.8Cu51.9Ag2.3合金而言,氢溶解度的提升并不会明显影响膜的渗透性。相反,对同时存在bcc和fcc两种结构的Pd45.1Cu51Ag3.9来说,更高的氢溶解度会导致氢渗透性的明显提升。因此,这表明bcc相中氢渗透性的高低主要由氢的扩散过程决定,只有在fcc相存在时,溶解度的增大才会导致氢渗透性的显著提高。
5. 结论与展望
近年来,钯合金膜由于具有氢渗透性好、机械强度大、氢选择性高等优点,受到了非常广泛的研究。但就工业应用上来说,钯合金膜依然有很多的局限,包括使用寿命、毒化抗性以及生产成本等方面。目前已经商业化应用的合金膜大多为自支撑膜,成本很高,渗透性较低,支撑体复合膜的研究大多还处在实验室阶段,若要进行商业生产,还需要继续改进或提出新的制备方法,以降低膜厚度,提高膜的渗透性,并能扩大规模,进行工业化生产。另外,对钯合金的研究同样十分有前景,Ag、Y、Cu等元素的添加能极大改善钯膜的各项性能,二元、三元乃至多元钯合金的组合无穷无尽,还需要做大量的工作,来探索更加优秀的组合。对合金性能提升的机理的研究工作同样十分重要,明确金属元素的添加对合金结构的影响以及氢在合金中溶解扩散的机理,可以更准确的预测不同组分多元合金的性能。
文章引用
赵展,胡石林,叶一鸣. 钯合金氢渗透膜的研究进展
Recent Advances on Palladium Alloy Membranes for Hydrogen Purification[J]. 核科学与技术, 2017, 05(03): 142-152. http://dx.doi.org/10.12677/NST.2017.53019
参考文献 (References)
- 1. 孙颖, 王和义, 桑革, 等. 反应堆含氚重水提氚关键技术研究进展[J]. 中国工程科学, 2007, 9(5): 1-6.
- 2. 蒋国强, 孙灵霞. 氚和氚的工程技术[M]. 北京: 国防工业出版社, 2007.
- 3. Yun, S. and Oyama, S.T. (2011) Correlations in Palladium Membranes for Hydrogen Separation: A Review. Journal of Membrane Science, 375, 28-45. https://doi.org/10.1016/j.memsci.2011.03.057
- 4. Gallucci, F., Fernandez, E., Corengia, P., et al. (2013) Recent Advances on Mem-branes and Membrane Reactors for Hydrogen Production. Chemical Engineering Science, 92, 40-66. https://doi.org/10.1016/j.ces.2013.01.008
- 5. 李雪. 光催化法制备超薄钯膜及钯银合金膜的研究[D]: [博士学位论文]. 南京: 南京工业大学, 2006.
- 6. Shu, J., Grandjean, B.P.A., Neste, A.V., et al. (1991) Catalytic Palladium-Based Membrane Reactors: A Review. Canadian Journal of Chemical Engineering, 69, 1036-1060. https://doi.org/10.1002/cjce.5450690503
- 7. Wise, M.L.H. (1975) X-Ray Studies of the α/β Miscibility Gaps of Some Palladium Solid Solution-Hydrogen Systems. Journal of the Less Common Metals, 41, 115-127. https://doi.org/10.1016/0022-5088(75)90099-5
- 8. Mallada, R. and Menendez, M. (2008) Inor-ganic Membranes: Synthesis, Characterization and Applications.
- 9. Hao, S. and Sholl, D.S. (2011) Computational Prediction of Durable Amorphous Metal Membranes for H2 Purification. Journal of Membrane Science, 381, 192-196. https://doi.org/10.1016/j.memsci.2011.07.026
- 10. Sonwane, C.G., Wilcox, J. and Ma, Y.H. (2006) Solubility of Hydrogen in Pd-Ag and Pd-Au Binary Alloys Using Density Functional Theory. Journal of Physical Chemistry B, 110, 24549. https://doi.org/10.1021/jp064507t
- 11. Gallucci, F., Chiaravalloti, F., Tosti, S., et al. (2007) The Effect of Mixture Gas on Hy-drogen Permeation through a Palladium Membrane: Experimental Study and Theoretical Approach. International Journal of Hydrogen Energy, 32, 1837-1845.
- 12. Gallucci, F., Basile, A. and Drioli, E. (2007) Methanol as an Energy Source and/or Energy Carrier in Membrane Processes. Separation & Purification Reviews, 36, 175-202. https://doi.org/10.1080/15422110601166049
- 13. Ozdogan, E. and Wilcox, J. (2010) Investigation of H2 and H2S Adsorption on Niobium- and Copper-Doped Palladium Surfaces. Journal of Physical Chemistry B, 114, 12851-12858. https://doi.org/10.1021/jp105469c
- 14. Chen, L. and Sholl, D.S. (2009) First Principles Investigation of Metal Sulfides as Mem-branes in Hydrogen Purification. Journal of Membrane Science, 329, 153-159.
- 15. Holleck, G.L. (2002) Diffusion and Solubility of Hydrogen in Palladium and Palladium—Silver Alloys. Journal of Physical Chemistry, 74.
- 16. Kamakoti, P., Morreale, B.D., Ciocco, M.V., et al. (2005) Prediction of Hydrogen Flux through Sulfur-Tolerant Binary Alloy Membranes. Science, 307, 569. https://doi.org/10.1126/science.1107041
- 17. Mckinley, D.L. (1969) Method for Hydrogen Separation and Purification. US3439474.
- 18. Fort, D., Farr, J.P.G. and Harris, I.R. (1975) A Comparison of Palladium-Silver and Palladium-Yttrium Alloys as Hydrogen Separation Membranes. Journal of the Less-Common Metals, 39, 293-308.
- 19. Krueger, C. (2002) Method of Improving and Optimizing the Hydrogen Permeability of a Palladium-Copper Membrane and Novel Membranes Manufactured Thereby. US6372363.
- 20. Hughes, D.T. and Harris, I.R. (1978) A Comparative Study of Hydrogen Permeabilities and Solubilities in Some Palladium Solid Solution Alloys. Journal of the Less Common Metals, 61, P9-P21.
- 21. Sakamoto, Y., Chen, F.L., Furukawa, M., et al. (1992) ChemInform Abstract: Permeability and Diffusivity of Hydrogen in Palladium-Rich Pd-Y(Gd)-Ag Ternary Alloys. Journal of Alloys & Compounds, 185, 191-205.
- 22. Dolan, M.D. (2010) Non-Pd BCC Alloy Membranes for Industrial Hydrogen Separation. Journal of Membrane Science, 362, 12-28.
- 23. Mazzolai, F.M. and Lewis, F.A. (2000) Elastic Energy Dissipation in the Palladi-um-Silver-Hydrogen (Deuterium) System. I. Hydrogen-Dislocation Interaction Effects. Journal of Physics F Metal Physics, 15, 1249. https://doi.org/10.1088/0305-4608/15/6/011
- 24. Paglieri, S.N. and Way, J.D. (2002) Innovations in Palladium Membrane Re-search. Separation & Purification Reviews, 31, 1-169. https://doi.org/10.1081/SPM-120006115
- 25. Harris, I.R. and Norman, M. (1968) The Electronic State of Cerium in Some Palladium Alloys. Journal of the Less Common Metals, 15, 285-298.
- 26. Subramanian, P.R. (1991) Cu-Pd (Copper-Palladium). Journal of Phase Equilibria, 12, 231-243. https://doi.org/10.1007/BF02645723
- 27. Piper, J. (1966) Diffusion of Hydrogen in Copper-Palladium Alloys. Journal of Ap-plied Physics, 37, 715-721. https://doi.org/10.1063/1.1708243
- 28. Morreale, B.D., Ciocco, M.V., Howard, B.H., et al. (2004) Effect of Hydrogen-Sulfide on the Hydrogen Permeance of Palladium-Copper Alloys at Elevated Temperatures. Journal of Membrane Science, 241, 219-224.
- 29. Iyoha, O., Enick, R., Killmeyer, R., et al. (2007) The Influence of Hydrogen Sulfide-to-Hydrogen Partial Pressure Ratio on the Sulfidization of Pd and 70% mol Pd-Cu Membranes. Journal of Membrane Science, 305, 77-92.
- 30. Braun, F., Tarditi, A.M., Miller, J.B., et al. (2014) Pd-Based Binary and Ternary Alloy Membranes: Morphological and Perm-Selective Characterization in the Presence of H2S. Journal of Membrane Science, 450, 299-307.
- 31. Peters, T.A., Kaleta, T., Stange, M., et al. (2013) Development of Ternary Pd-Ag-TM Alloy Membranes with Improved Sulphur Tolerance. Journal of Membrane Science, 429, 448-458.
- 32. Pati, S., Jat, R.A., Anand, N.S., et al. (2017) Pd-Ag-Cu Dense Metallic Membrane for Hydrogen Isotope Purification and Recovery at Low Pressures. Journal of Membrane Science, 522, 151-158.
- 33. Coulter, K.E., Way, J.D., Gade, S.K., et al. (2012) Sulfur Tolerant Pd-Au and Pd-Au-Pt Alloy Hydrogen Separation Membranes. Journal of Membrane Science, 405-406, 11-19.
- 34. Tarditi, A.M., Imhoff, C., Braun, F., et al. (2015) Pd-Cu-Au Ternary Alloy Membranes: Hydrogen Permeation Properties in the Presence of H2S. Journal of Membrane Science, 479, 246-255.
- 35. Nayebossadri, S., Speight, J. and Book, D. (2014) Effects of Low Ag Additions on the Hydrogen Permeability of Pd- Cu-Ag Hydrogen Separation Membranes. Journal of Membrane Science, 451, 216-225.
