Material Sciences
Vol.07 No.03(2017), Article ID:20348,11
pages
10.12677/MS.2017.73034
Influence of Aland Ga on Lithium Ion Conductivities of Cubic Garnet-Type Li7−xLa3Zr2−xTaxO12 Electrolytes
Danxiang Ma
Laboratory of Solid State Ionics, School of Materials Science and Engineering, Huazhong University of Science and Technology, Wuhan Hubei

Received: Apr. 4th, 2017; accepted: Apr. 26th, 2017; published: May 3rd, 2017

ABSTRACT
To obtain highly conductive Li7−xLa3Zr2−xTaxO12 (LLZTO) electrolytes, the influence of Al and Ga on them were investigated. The Al and Ga have been demonstrated to be supervalent dopants that stabilize cubic garnetof Li7La3Zr2O12 (LLZO) electrolytes. They are also sintering-aided compositions, increasing the overall conductivity of LLZO electrolytes. The results show that all the obtained electrolytes are cubic. The densification and conductivity of the LLZTO electrolyte were improved by Al or Ga inclusion. In the Al-Li7−xLa3Zr2−xTaxO12 (Al-LLZTO) electrolytes, Al was found in the grains and grain boundaries, but the Al content in the grain boundaries is about twice of that in the grains. The overall conductivity was optimized to 0.54 mS/cm with an activation energy of 0.42 eV for the Al-Li6.4La3Zr1.4Ta0.6O12 sample. In theLi7−x−3yGayLa3Zr2−xTaxO12 (Ga-LLZTO) electrolytes, the Al in a low conent and Ga were found in grains and grain boundaries. The overall conductivities of Ga-LLZTO electrolytes were higher than that of the Al-LLZTO electrolytes with almost the same nominal Li-content. Finally, the highest overall conductivity of 0.87 mS/cm with a low activation energy of 0.33 eV was achieved for the Li6.4Ga0.1La3Zr1.7Ta0.3O12 sample.
Keywords:Solid State Electrolyte, Garnet-Type LLZTO, Ionic Conductivity, Al and Ga Doping
掺杂(Al3+,Ga3+)对石榴石型电解质Li7−xLa3Zr2−xTaxO12锂离子电导率的影响
马丹祥
华中科技大学材料与工程学院,固态离子学实验室,湖北 武汉
收稿日期:2017年4月4日;录用日期:2017年4月26日;发布日期:2017年5月3日

摘 要
为了提高Li7−xLa3Zr2−xTaxO12(LLZTO)固体电解质电导率,本文研究了Al3+和Ga3+掺杂对材料性能的影响。结果表明,掺杂Al3+和Ga3+,显著提高了材料的致密度和电导率。Al-Li7−xLa3Zr2−xTaxO12(Al-LLZTO)中的铝离子同时存在于晶粒和晶界中,晶界中的铝含量是晶粒中的两倍,Al-Li6.4La3Zr1.4Ta0.6O12拥有最高的总电导率0.54 mS/cm,其激活能为0.42 eV。Li7−x−3yGayLa3Zr2−xTaxO12(Ga-LLZTO)中,铝的含量较低,镓离子同时存在于电解质的晶粒与晶界中。在锂含量相同的样品中,Ga-LLZTO的总电导率要高于Al-LLZTO,表明Ga的掺杂比Al的掺杂对LLZTO电解质的电导率提升更大。最终,我们得到总电导率最高的样品Li6.4Ga0.1La3Zr1.7Ta0.3O12,其总电导率和激活能分别为0.87 mS/cm和0.33 eV。
关键词 :固态电解质,石榴石型电解质LLZTO,离子电导率,Al和Ga掺杂

Copyright © 2017 by author and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
锂离子电池自1991年商业化以来一直被认为是最具前景的化学储能设备 [1] 。然而,有机液态电解质的易燃性、漏液以及容易形成枝晶带来的安全问题阻碍着锂离子电池在大型储能方面的应用 [1] [2] 。相对传统液态电解质,无机固态电解质在易燃、漏液和枝晶形成方面具有巨大的优势。同时,无机固态电解质具有优越的化学、机械和热稳定性,以及电池小型化的可能性。因此,过去几十年对于固态电解质进行了深入的研究 [3] - [10] 。立方相石榴石结构Li7La3Zr2O12(LLZO)由于其较高的总锂离子电导率(~2 × 10−4 S/cm),较低的电子电导率以及优良的化学和热稳定性,尤其是它对锂金属的稳定性,成为了一种理想的锂离子电池固态电解质 [4] 。
Li7−xLa3Zr2−xTaxO12 (LLZTO)中Ta在Zr位的掺杂创造了锂离子空位并稳定了立方相结构,相对于高浓度的Li位掺杂,这种掺杂方式不会阻塞锂离子的迁移通道,这似乎是一种获得高电导率立方相LLZO的途径 [11] - [17] 。Miara等人 [14] 首次通过原理计算,LLZTO的体电导率高达10 mS/cm,这是其它氧化物固态电解质从未达到的高度。另一方面,Janani等人 [18] 最近的工作表明LLZTO的总电导率为10−5~10−4 S/cm,而且加入Li4SiO4等助烧剂并不能显著提高其电导率。然而,通过氧化铝坩埚煅烧向LLZO中引入Al能够稳定其立方相结构 ,而有利于其整体电导率的提升 [19] 。Al作为助烧剂在晶界中形成Li2O-Al2O3化合物,也有利于提高材料的总电导率 [13] 。
Al的掺杂已经被证明能够通过稳定立方相结构和提高致密度来提升LLZO的电导率,而在元素周期表中,Ga位于Al的下方,应该具有类似的晶体化学行为。事实上,Al和Ga已经被证实拥有能够稳定LLZO立方相结构和促进烧结的作用,而且Ga掺杂的LLZO也是一种电导率约为1 mS/cm的电解质 [13] [20] [21] 。因此,为了获得高电导率的LLZTO电解质,本文研究了Al和Ga掺杂对石榴石型LLZTO电解质的影响。结果显示,Al和Ga的掺杂能够显著提高LLZTO的电导率,而且Li6.4Ga0.1La3Zr1.7Ga0.3O12样品拥有最高的电导率0.87 mS/cm和最低的激活能0.33 eV。
2. 实验过程
2.1. 样品制备
实验中的样品通过Li2CO3 (国药,AR)、La2O3 (国药,4N)、ZrO2 (国药,AR)、Ta2O5 (国药,4N)和Ga2O3 (国药,4N)按化学计量比合成。称量好的粉末球磨15个小时,然后在900℃下煅烧6个小时,煅烧后的粉末再次球磨15个小时。球磨后的粉末在250 MPa下冷等静压成型,然后在空气中1200℃下烧结12个小时。在烧结过程中,用相同成分一次煅烧的陶瓷粉末覆盖电解质,1000℃以下以2℃/min升温,1000℃到1200℃以下以1℃/min升温以阻止锂的流失。为了在LLZTO中引入Al,我们采用氧化铝坩埚对样品进行烧结,烧结过程中在坩埚与样品之间垫入一个相同组分的样品。Al-LLZTO与Ga掺杂的样品烧结时间分别为12小时与24小时。
2.2. 结构表征
所有制备样品通过X’pert Pro帕纳科X-射线衍射仪,Cu靶,Kα辐射线λ = 1.5418 Å进行物相分析,扫描范围(2θ)为10˚到70˚。通过LabRAM HR800拉曼光谱仪(法国Horiba JobinYvon公司),配备了一个532nm,50mW的内部Nd-YAG激光源对样品进行共焦显微拉曼光谱分析。通过Sirion 200场发射扫描电子显微镜(荷兰,FEI公司),配备一个X射线能谱仪(EDX),对样品进行断口形貌和化学成分分析。使用水通过阿基米德法测定样品的表面密度,根据样品组分和从XRD得到的晶格参数估算样品的理论密度,再通过表面密度和理论密度计算样品的相对密度。
2.3. 电学性能分析
利用Solatron 1260阻抗和晶相分析仪进行交流阻抗测试,频率范围为1Hz到5 × 106 Hz,振幅为50 mV。测试之前在样品两面通过直流溅射镀上金电极,通过直流极化法在电化学工作站上对样品施加0.1 V的直流电压测试4000秒,估算样品的电子电导率。
3. 实验结果
3.1. 不含Al的LLZTO电解质
图1(a)为Li6.4La3Zr1.4Ta0.6O12电解质样品的XRD图谱以及立方相石榴石结构Li5La3Nb2O12的标准峰对比。结果和理论预测一致,样品的特征峰都能与Li5La3Nb2O12的标准峰对应,而且没有任何杂质,是典型的立方相结构 [12] [22] 。样品的相对密度约为82%,这与文献中的结果相近 [18] 。通过图1(b)的SEM图片可以看出,样品的断裂面上清晰可见微孔、晶界以及晶间断裂,晶粒尺寸3~5 μm范围内。根据Ren等人 [23] 的工作报道,锂枝晶会沿着晶间孔隙生长,导致Li/LLZTO/Li电池短路。不含Al的LLZTO样品的晶间孔隙就是锂枝晶生长的路径。
图1(c)对Li6.4La3Zr1.4Ta0.6O12的电导率进行了表征,是一组典型的交流阻抗谱。随着频率的降低,阻抗谱显示出两个分离的半圆弧,我们通过两组电阻电容的并联电路以及一个电容组成的串联等效电路对阻抗谱进行拟合。相应的电容可以通过公式C = (R1−nCQ)1/n计算 [24] ,其中R和Q分别代表一个电阻和一个固定相元,固定相元由CQ和n两个参数表征。两个电容的数量级为10−11 F和10−9 F,分别代表样品的体电容和晶界电容。样品的总电阻Roverall等于样品的体电阻Rbulk + 晶界电阻Rgb,体电阻和总电阻都能通

Figure 1. (a) XRD pattern; (b) SEM images of the fractured surface; (c) Typical AC impedance spectra, fitting curves and equivalent circuit; (d) Arrhenius plots of bulk and overall conductivities of the Li6.4La3Zr1.4Ta0.6O12 electrolyte without Al
图1. 不含Al的Li6.4La3Zr1.4Ta0.6O12电解质的(a) XRD图谱;(b) 断面的SEM 图片;(c) 交流阻抗谱、拟合曲线和等效电路;(d) 体电导率和总电导率的阿伦尼乌斯曲线
过公式σ = L/(RA)计算得出(A代表样品的横截面积,L代表样品的厚度)。26℃时样品的总电导率约为3 × 10−5 S/cm,远低于Al掺杂和Ga掺杂的LLZO电解质。这不能完全归因于样品较低的致密度,因为26℃时样品的体电导率约为4 × 10−5 S/cm,也低于Al掺杂和Ga掺杂的LLZO电解质,而且晶界电阻只占总电阻的24%。图1(d)为体电导率和总电导率的阿仑尼乌斯曲线,相应的激活能分别为0.46 eV和0.51 eV,这意味着锂离子在LLZTO中的迁移需要克服很高的能垒。
3.2. Al-LLZTO电解质
图2(a)为Al-LLZTO样品的XRD图谱,是典型的立方相结构,而且没有多余的杂相。表1中显示了Al-LLZTO样品的晶格常数。
图2(b)为样品的共焦显微拉曼光谱,因为在某些情况下,XRD图谱中无法显示与立方相共存的四方相 [11] 。Tietz等人 [25] 首次对石榴石结构LLZO的立方相和四方相结构的拉曼光谱进行了分析。拉曼光谱显示,所有样品位于110 cm−1处最明显的立方相特征峰没有出现四方相结构尖锐分裂的特征峰,和XRD结果一致。
图3为Al-Li6.4La3Zr1.4Ta0.6O12电解质断裂面的SEM图片和EDX分析,对比SEM图片发现晶粒之间的结合度明显要好于不含Al的LLZTO电解质样品。样品的晶粒尺寸约为3~6 μm,相对密度在90%以上,
Table 1. Lattice parameter, relative density, total conductivity, electronic conductivity at 26˚C, and activation energy of the total conductivity of the electrolytes
表1. 电解质样品的晶格参数、相对密度,26℃时的总电导率、电子电导率、总电导率的激活能

Figure 2. (a) XRD patterns and; (b) Raman spectra of the Al-Li7-xLa3Zr2-xTaxO12 electrolytes
图2. Al-Li7-xLa3Zr2-xTaxO12电解质的(a) XRD图谱;(b) Raman光谱

Figure 3. SEM image and EDX analyses of the fractured surface for the Al-Li6.4La3Zr1.4Ta0.6O12 electrolyte. Different colors represent the different elements distributions across the sample: red—O, green—La, purple—Zr, blue—Ta and yellow—Al
图3. Al-Li6.4La3Zr1.4Ta0.6O12电解质样品断面的SEM和EDX分析(不同的颜色代表样品的不同元素分布:红-O,绿-La,紫-Zr,蓝-Ta和黄色-Al)
而且从表1中可以看出随着Ta含量的变化样品的相对密度改变不大。从EDX分析中可以看出,所有检测元素(La, Zr, Ta)均匀分布在整个断裂面上,值得注意的是,来自坩埚中的Al同时存在于晶粒与晶界中。使用EDX对晶粒与晶界进行点分析表明其中的原子比La:Zr:Ta:Al分别位3:1.35:0.57:0.026和3:1.39:0.56:0.054。晶粒与晶界中的成分基本符合化学计量比,其中晶界中Al的含量是晶粒中的两倍。晶界中的Al与Li复合形成LiAlO2 [13] ,这可能是晶界中Al含量相对更高的原因,但是LiAlO2是无定型化合物,在XRD中很难检测出来。晶界中的含Al化合物明显提高了Al-LLZTO电解质样品的致密度,而且也起到了抑制晶界中锂枝晶生长的作用。
图4为Al-Li6.4La3Zr1.4Ta0.6O12电解质样品的交流阻抗谱和Al-LLZTO电解质样品总电导率的阿伦尼乌斯曲线。Al-Li6.4La3Zr1.4Ta0.6O12样品的交流阻抗谱中只存在一个半圆弧,而且随着测试温度升高半圆弧的半径逐渐减小,直至47℃时半圆弧消失。交流阻抗谱中晶粒的电阻和晶界无法区分开来,这一现象在高度致密的石榴石电解质中相当普遍,因为致密度高的情况下晶界电阻很小 [16] [20] [26] [27] [28] 。明显的可以看出样品的体电阻和总电阻都要小于不含Al的LLZTO样品,从原点到半圆弧尾部与实轴交点的这段截距可以近似看做电解质的总电阻。如表1所示,当x = 0.4、0.5、0.6、0.7、0.8时,Al-LLZTO电解质样品的室温总电导率分别为0.36、0.37、0.54、0.28、0.12 mS/cm,这比不含Al的LLZTO电解质的总电导率要高出一个数量级,说明Al的掺杂能够在很大程度上的提高LLZTO电解质的电导率。此外,如图4(b)所示LLZTO电解质的电导率也与Ta的含量有关,当x = 0.6时,Li6.4La3Zr1.4Ta0.6O12样品的总电导率达到最大值,同时Al-LLZTO电解质样品的总电导激活能相对减小到了约0.40 eV。
理想的固态电解质应该是纯离子导体,否则锂离子电池充放电过程中会发生短路,直流极化法可以用来测试固态锂离子导体的电子电导 [16] [28] 。直流极化曲线中的电流稳定以后,我们就可以通过稳定的电流估算出样品的电子电导。表1中给出了Al-LLZTO样品的电子电导值约为10−8 S/cm,相对离子电导来说可以忽略不计。
3.3. Ga-LLZTO电解质
Ga有类似于Al的晶体化学行为。此外,Ga掺杂的LLZO电解质电导率约(~1 mS/cm) [20] 要明显高于Al掺杂的LLZO电解质的电导率(~0.2 mS/cm) [4] ,说明Ga的掺杂对电导率的提升效果更为明显。
图5为Ga-LLZTO电解质样品的XRD图谱和拉曼光谱,表明样品是立方相结构,表1中给出了样品的晶格参数。
图6为电解质Li6.25Ga0.1La3Zr1.55Ta0.45O12样品断面的SEM图片和EDX分析,样品的晶粒之间结合紧密,晶粒大小在2~5 μm之间。从表1中可以看出,随着Ga和Ta含量的变化样品的致密度变化不大。从Li6.25Ga0.1La3Zr1.55Ta0.45O12电解质样品的EDX分析中可以看出,主要元素La、Zr和Ta均匀地分布在断裂面上。但是之后的点分析表明样品中Al的含量很低(原子比约为La:Al = 3:0.015),其中Ga同时存在于晶粒与晶界中。
图7为Li6.25Ga0.05La3Zr1.4Ta0.6O12电解质样品的交流阻抗谱和Ga-LLZTO电解质样品总电导率的阿伦尼乌斯曲线。与Al-LLZTO电解质样品相似,交流阻抗谱的高频区只存在一个半圆弧。如表1所示,室温下Li6.25Ga0.02La3Zr1.31Ta0.69O12,Li6.25Ga0.05La3Zr1.4Ta0.6O12和Li6.25Ga0.1La3Zr1.55Ta0.45O12电解质样品的总电导率分别为0.40 mS/cm,045 mS/cm和0.40 mS/cm。从图7(b)的阿伦尼乌斯曲线可以推导得出Ga-LLZTO样品的总电导激活能约为0.40eV。对于锂含量相同的Ga-LLZTO样品,Ga和Ta含量的变化对样品的总电导率和激活能几乎没有影响。但是值得注意的是,拥有相同锂含量的Ga-LLZTO电解质样品的总电导率要高于Al-LLZTO样品,例如Li6.3La3Zr1.3Ta0.7O12和Li6.2La3Zr1.2Ta0.8O12。

Figure 4. (a) Typical AC impedance spectra of the Al-Li6.4La3Zr1.4Ta0.6O12 electrolyte and (b) Arrhenius plots of overall conductivities of the Al-Li7−xLa3Zr2−xTaxO12electrolytes
图4. (a) Al-Li6.4La3Zr1.4Ta0.6O12电解质的交流阻抗谱,(b) Al-Li7−xLa3Zr2−xTaxO12电解质总电导率的阿伦尼乌斯曲线

Figure 5. (a) XRD patterns and (b) Raman spectra of the Li7−x−3yGayLa3Zr2−xTaxO12 electrolytes
图5. Li7−x−3yGayLa3Zr2−xTaxO12电解质的(a) XRD图谱,(b) Raman光谱

Figure 6. SEM image and EDX analyses of the fractured surface for the Li6.25Ga0.1La3Zr1.55Ta0.45O12 electrolyte. Different colors represent the different element distributions across the sample: red—O, green—La, purple—Zr, blue—Ta, wine—Ga, and yellow—Al
图6. Li6.25Ga0.1La3Zr1.55Ta0.45O12电解质样品断面的SEM和EDX分析(不同的颜色代表样品的不同元素分布:红-O,绿-La,紫-Zr,蓝-Ta,褐-Ga和黄色-Al)

Figure 7. (a) Typical AC impedance spectra of the Li6.25Ga0.05La3Zr1.4Ta0.6O12 electrolyte and (b) Arrhenius plots of overall conductivities of the Li7−x−3yGayLa3Zr2−xTaxO12 electrolytes
图7. (a) Li6.25Ga0.05La3Zr1.4Ta0.6O12电解质的交流阻抗谱;(b) Li7−x−3yGayLa3Zr2−xTaxO12电解质总电导率的阿伦尼乌斯曲线
4. 讨论
本文工作的主要目的是为了获得适用于全固态锂离子电池的高电导率的立方相石榴石结构LLZTO电解质。石榴石结构作为一种多晶材料,总电导率是由体电导和晶界电导共同决定的,因此,想要提升其总电导率我们必需同时考虑这两个因素。Ta5+ [13] 、Nb5+ [29] 和Te6+ [30] 等高价阳离子在Zr位的掺杂能够调节Li位上锂离子和空位的数量,从而提升电解质的体电导率。但是晶界中不含Al时,这种掺杂方法对总电导率的提升不大。提高电解质的致密度是一种提升晶界电导率的方法,高价阳离子Al3+和Ga3+在Li位的掺杂不仅能够调节锂离子和空位的数量,而且作为助烧剂能够提高电解质的致密度,从而提升电解质的总电导率。在应用到全固态锂离子电池中时,致密化除了有利于提高电导率外,还有利于提高电池的机械强度和抑制锂枝晶的形成。特别是当石榴石型电解质被认为适用于锂氧或锂硫电池时 [15] ,石榴石电解质的致密度显得尤为重要。在本文的工作中,Al和Ga的掺杂明显的提高了石榴石型电解质LLZTO的致密度。
锂离子电导率是LLZO电解质能否应用到锂离子电池中的关键因素之一,通过Al和Ga的掺杂LLZTO电解质的总电导率得到了明显的提升。此外,关于这项工作我们还需要强调以下几点。
首先,Al和Ga同时存在于LLZTO电解质的晶粒和晶界中。这意味着Al和Ga的掺杂不仅为晶粒内锂离子的传导创造了更多的空位,而且存在于晶界中作为助烧剂提高了电解质的致密度。这应该是Al和Ga的掺杂能同时提高电解质体电导率和总电导率的原因。
其次,锂离子的电导率可以表示为σ = ZeCµ [31] ,其中Ze (=1,对于锂离子),C和µ分别表示载流子的电荷,浓度以及迁移率。石榴石型电解质的锂离子电导率由锂离子的浓度和迁移率决定。电导率不随着分子式中的锂离子含量变化是一种常见现象,这是因为不是所有分子式中的锂离子都参与迁移,因此LLZO中的载流子浓度必需重新定义 [15] 。根据Ahmad [32] 的工作,LLZO中的锂离子只有12.3%参与离子传导。因此我们通过增加石榴石型电解质中载流子的浓度或者增大锂离子的迁移率来激发更多的锂离子参与传导,就可以提高LLZTO电解质的电导率。在本文的工作中,相对Li+含量为6.25的Ga-LLZTO样品的电导率要高于Al-Li6.3La3Zr1.3Ta0.7O12和Al-Li6.2La3Zr1.2Ta0.8O12,这意味着Ga3+比Al3+更容易激活锂离子迁移,这是因为Ga3+对Li+有更强的排斥性。
再次,继续增加Ga-LLZTO分子式中的锂含量能够进一步提高电解质的电导率,因此,我们制作了分子式为Li6.4Ga0.1La3Zr1.7Ta0.3O12的电解质样品来验证这一结论。图8为Li6.4Ga0.1La3Zr1.7Ta0.3O12电解质样品的XRD图谱和断裂面的SEM图片,物相和微观结构都与Al-LLZTO和Ga-LLZTO十分相近。

Figure 8. (a) XRD pattern and (b) SEM images of the fractured surface of the Li6.4Ga0.1La3Zr1.7Ta0.3O12 electrolyte
图8. Li6.4Ga0.1La3Zr1.7Ta0.3O12电解质的(a) XRD图谱;(b) 断面的SEM图片
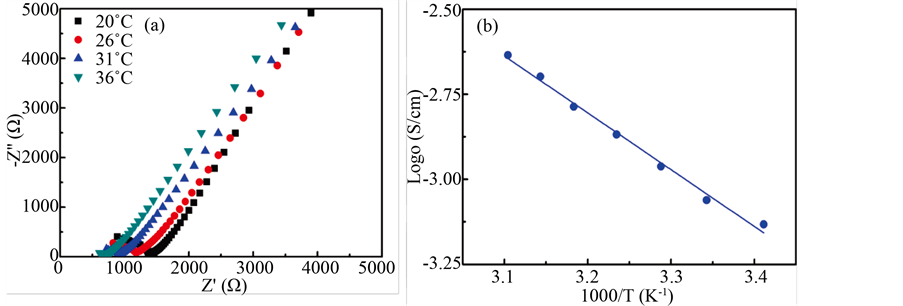
Figure 9. (a) Typical AC impedance spectra and (b) Arrhenius plot of the Li6.4Ga0.1La3Zr1.7Ta0.3O12 electrolyte
图9. Li6.4Ga0.1La3Zr1.7Ta0.3O12电解质的(a)交流阻抗谱;(b) 总电导率的阿伦尼乌斯曲线
如图9(a)所示样品的交流阻抗谱,阻抗谱中也只有一个半圆弧。最后我们通过交流阻抗谱计算出Li6.4Ga0.1La3Zr1.7Ta0.3O12电解质样品的总电导率,从图9(b)中的总电导率阿伦尼乌斯曲线推导出总电导激活能。室温下Li6.4Ga0.1La3Zr1.7Ta0.3O12电解质的总电导率为0.87 mS/cm,要高于Al-LLZTO和其他Ga-LLZTO电解质,总电导激活能为0.33 eV。
5. 结论
在LLZTO的晶粒与晶界中引入Al和Ga能够提高电解质的电导率和致密度。在Li位掺杂高价阳离子(Al3+和Ga3+)一方面能够为锂离子的传导提供更多的空位,另一方面Al和Ga作为助烧剂可以在晶界处形含锂化合物提高电解质的致密度,这些都有助于提高电解质的电导率。相比掺杂Al,掺杂Ga是一种对提高导电性能更有效的方法,文中Li6.4Ga0.1La3Zr1.7Ta0.3O12拥有最高的电导率0.87 mS/cm,电导激活能低至0.33 eV。
致谢
感谢华中科技大学分析测试中心提供XRD,Raman和FESEM等测试。
文章引用
马丹祥. 掺杂(Al3+,Ga3+)对石榴石型电解质Li7-xLa3Zr2-xTaxO12锂离子电导率的影响
Influence of Aland Ga on Lithium Ion Conductivities of Cubic Garnet-Type Li7-xLa3Zr2-xTaxO12 Electrolytes[J]. 材料科学, 2017, 07(03): 243-253. http://dx.doi.org/10.12677/MS.2017.73034
参考文献 (References)
- 1. Tarascon, J.M. and Armand, M. (2001) Issues and Challenges Facing Rechargeable Lithium Batteries. Nature, 414, 359. https://doi.org/10.1038/35104644
- 2. Armand, M. and Tarascon, J.M. (2008) Building Better Batteries. Nature, 451, 652-657. https://doi.org/10.1038/451652a
- 3. Takada, K. (2013) Progress and Prospective of Solid-State Lithium Batteries. Acta Materialia, 61, 759-770. https://doi.org/10.1016/j.actamat.2012.10.034
- 4. Murugan, R., Thangadurai, V. and Weppner, W. (2007) Fast Lithium Ion Conduction in Garnet-Type Li7La3Zr2O12. Cheminform, 46, 7778-7781.
- 5. Thangadurai, V. and Weppner, W. (2005) Li6ALa3Zr2O12(A=Sr, Ba): Novel Garnet-Like Oxides for Fast Lithium Ion Conduction. Advanced Functional Materials, 15, 107-112. https://doi.org/10.1002/adfm.200400044
- 6. Kamaya, N., Homma, K., Yamakawa, Y., et al. (2011) A Lithium Superionic Conductor. Nature Materials, 10, 682-686. https://doi.org/10.1038/nmat3066
- 7. Liu, Z.C., Fu, W.J., Payzant, E.A., et al. (2013) Anomalous High Ionic Conductivity of Nanoporous β-Li3PS4. Journal of the American Chemical Society, 135, 975-978. https://doi.org/10.1021/ja3110895
- 8. Perng, Y.C., Cho, J., Sun, S.Y., et al. (2014) Synthesis of Ion Conducting LixAlySizO Thin Films by Atomic Layer Deposition. Journal of Materials Chemistry A, 2, 9566-9573. https://doi.org/10.1039/C3TA14928E
- 9. Sahu, G., Rangasamy, E., Li, J., et al. (2014) A High-Conduction Ge Substituted Li3AsS4 Solid Electrolyte with Exceptional Low Activation Energy. Journal of Materials Chemistry A, 2, 10396-10403. https://doi.org/10.1039/c4ta01243g
- 10. Seino, Y., Ota, T., Takada, K., et al. (2013) A Sulphide Lithium Super Ion Conductor Is Superior to Liquid Ion Conductors for Use in Rechargeable Batteries. Energy & Environmental Science, 7, 627-631. https://doi.org/10.1039/C3EE41655K
- 11. Thompson, T., Wolfenstine, J., Allen, J.L., et al. (2014) Tetragonal Cubic Phase Stability in Al-Free Ta Doped Li7La3Zr2O12 (LLZO). Journal of Materials Chemistry A, 2, 13431-13436. https://doi.org/10.1039/C4TA02099E
- 12. Bernstein, N., Johannes, M.D. and Hoang, K. (2012) Origin of the Structural Phase Transition in Li7La3Zr2O12. Physical Review Letters, 109, 205702-205706. https://doi.org/10.1103/PhysRevLett.109.205702
- 13. Li, Y., Han, J.T., Wang, C.A., et al. (2012) Optimizing Li+ Conductivity in Garnet Framework. Journal of Materials Chemistry, 22, 15357-15361. https://doi.org/10.1039/c2jm31413d
- 14. Miara, L.J., Ong, S.P., Mo, Y., et al. (2013) Effect of Rb and Ta Doping on the Ionic Conductivity and Stability of the Garnet Li7+2x–y(La3–xRbx)(Zr2–yTay)O12(0≤x≤0.375, 0≤y≤1)Superionic Conductor: A First Principles Investigation. Chemistry of Materials, 25, 3048-3055. https://doi.org/10.1021/cm401232r
- 15. Thompson, T., Sharafi, A., Johannes, M.D., et al. (2015) Lithium Ion Batteries: A Tale of Two Sites: On Defining the Carrier Concentration in Garnet-Based Ionic Conductors for Advanced Li Batteries. Advanced Energy Materials, 5, 1500096-1500104. https://doi.org/10.1002/aenm.201500096
- 16. Li, Y., Wang, Z., Li, C., et al. (2014) Densification and Ionic-Conduction Improvement of Lithium Garnet Solid Electrolytes by Flowing Oxygen Sintering. Journal of Power Sources, 248, 642-646. https://doi.org/10.1016/j.jpowsour.2013.09.140
- 17. Huang, M., Mao, S., Shen, Y., et al. (2014) Preparation and Electrochemical Properties of Zr-Site Substituted Li7La3(Zr2−xMx)O12, (M=Ta, Nb) Solid Electrolytes. Journal of Power Sources, 261, 206-211. https://doi.org/10.1016/j.jpowsour.2014.03.070
- 18. Janani, N., Ramakumar, S., Kannan, S., et al. (2015) Optimization of Lithium Content and Sintering Aid for Maximized Li+ Conductivity and Density in Ta-Doped Li7La3Zr2O12. Journal of the American Ceramic Society, 98, 2039- 2046. https://doi.org/10.1111/jace.13578
- 19. Geiger, C.A., Alekseev, E., Lazic, B., et al. (2011) Crystal Chemistry and Stability of “Li7La3Zr2O12” Garnet: A Fast Lithium-Ion Conductor. Inorganic Chemistry, 50, 1089-1097. https://doi.org/10.1021/ic101914e
- 20. Bernuy-Lopez, C., Manalastas, W., Amo, J.M.L.D., et al. (2014) ChemInform Abstract: Atmosphere Controlled Processing of Ga-Substituted Garnets for High Li-Ion Conductivity Ceramics. Cheminform, 45, 3610-3617. https://doi.org/10.1002/chin.201433010
- 21. Shinawi, H.E. and Janek, J. (2013) Stabilization of Cubic Lithium-Stuffed Garnets of the type “Li7La3Zr2O12” by Addition of Gallium. Journal of Power Sources, 225, 13-19. https://doi.org/10.1016/j.jpowsour.2012.09.111
- 22. Xie, H., Alonso, J.A., Li, Y., et al. (2011) Lithium Distribution in Aluminum-Free Cubic Li7La3Zr2O12. Cheminform, 42, 3587-3589. https://doi.org/10.1002/chin.201144003
- 23. Ren, Y., Shen, Y., Lin, Y., et al. (2015) Direct Observation of Lithium Dendrites Inside Garnet-Type Lithium-Ion Solid Electrolyte. Electrochemistry Communications, 57, 27-30. https://doi.org/10.1016/j.elecom.2015.05.001
- 24. Xin, G., Sigle, W. and Maier, J. (2010) Blocking Grain Boundaries in Yttria-Doped and Undoped Ceria Ceramics of High Purity. Journal of the American Ceramic Society, 86, 77-87.
- 25. Tietz, F., Wegener, T., Gerhards, M.T., et al. (2013) Synthesis and Raman Micro-Spectroscopy Investigation of Li7La3Zr2O12. Solid State Ionics, 230, 77-82. https://doi.org/10.1016/j.ssi.2012.10.021
- 26. Deviannapoorani, C., Dhivya, L., Ramakumar, S., et al. (2013) Lithium Ion Transport Properties of High Conductive Tellurium Substituted Li7La3Zr2O12, Cubic Lithium Garnets. Journal of Power Sources, 240, 18-25. https://doi.org/10.1016/j.jpowsour.2013.03.166
- 27. Liu, K., Ma, J.T. and Wang, C.A. (2014) Excess Lithium Salt Functions More than Compensating for Lithium Loss When Synthesizing Li6.5La3Ta0.5Zr1.5O12, in Alumina Crucible. Journal of Power Sources, 260, 109-114. https://doi.org/10.1016/j.jpowsour.2014.02.065
- 28. Wang, D., Zhong, G., Pang, W.K., et al. (2015) Toward Understanding the Lithium Transport Mechanism in Garnet-Type Solid Electrolytes: Li+ Ion Exchanges and Their Mobility at Octahedral/Tetrahedral Sites. Chemistry of Materials, 27, 150918180839005. https://doi.org/10.1021/acs.chemmater.5b02429
- 29. Adams, S. and Rao, R.P. (2011) Ion Transport and Phase Transition in Li7-xLa3(Zr2-xMx)O12(M = Ta, Nb, x = 0, 0.25). Journal of Materials Chemistry, 22, 1426-1434. https://doi.org/10.1039/C1JM14588F
- 30. Deviannapoorani, C., Dhivya, L., Ramakumar, S., et al. (2013) Lithium ion Transport Properties of High Conductive Tellurium Substituted Li7La3Zr2O12, Cubic Lithium Garnets. Journal of Power Sources, 240, 18-25. https://doi.org/10.1016/j.jpowsour.2013.03.166
- 31. Armstrong, R.D., Bulmer, R.S. and Dickinson, T. (1973) Some Factors Responsible for High Ionic Conductivity in Simple Solid Compounds. Journal of Solid State Chemistry, 8, 219-228. https://doi.org/10.1016/0022-4596(73)90088-1
- 32. Ahmad, M.M. (2015) Estimation of the Concentration and Mobility of Mobile Li+ in the Cubic Garnet-Type Li7La3Zr2O12. RSC Advances, 5, 25824-25829. https://doi.org/10.1039/C4RA15972A
