Advances in Analytical Chemistry
Vol.07 No.02(2017), Article ID:20766,10
pages
10.12677/AAC.2017.72020
NMR Dynamic Study of Mixed Micelles in the Complex System of Non-Ionic Surfactant NP-10 and DM
Weihong Zhang1, Ruige Zhao1, Erqian Ma1, Zhanhui Zhang1, Qiuqing Yang2*
1College of Chemistry and Material Sciences, Hebei Normal University, Shijiahzuang Hebei
2Analysis and Testing Center, Hebei Normal University, Shingjiazhuang Hebei
*通讯作者。

Received: May 11th, 2017; accepted: May 24th, 2017; published: May 27th, 2017

ABSTRACT
Two kinds of non-ionic surfactant (DM and NP-10) form a binary complex system, and the dynamic changes (including the accumulation of micelles, intermolecular arrangement, interaction point and the variation of inter-molecular as well as the intra-molecular interaction etc.) of the mixed micelles formed in different proportions of the complex system were studied through a variety of NMR techniques. 2D NOESY experiments reveals that the spatial distance and the interaction force between the two molecules vary with the NP-10/DM ratio, but the interaction point does not change; the diffusion coefficient of NMR shows that the dynamic radius of mixed micelles increases with the increase of NP-10/DM, and then tends to be stable until the mole ratio of NP-10/DM is 1:6, indicating that the concentration ratio of the complex system is not unlimited; the transverse relaxation time T2 shows the tendency of the monomer micelles and the mixed micelles moving in the opposite direction as the increase of respective proportions. This phenomenon proves the difference between the inter-molecular forces and the intra-molecular forces. The relaxation time also shows that when the molar ratio of NP-10/DM is 1: 1/2 ~ 1: 1, the inter-molecular interaction began to decrease, and the intra-molecular interaction began to play a leading role, suggesting that the optimal ratio and the synergistic effect of the complex system.
Keywords:NMR, NP-10, DM, Mixed Micelles, Interaction, Dynamic Changes
非离子表面活性剂NP-10与DM复配体系中混合胶束的NMR动态研究
张卫红1,赵瑞格1,马二倩1,张占辉1,杨秋青2*
1河北师范大学化学与材料科学学院,河北 石家庄
2河北师范大学分析测试中心,河北 石家庄

收稿日期:2017年5月11日;录用日期:2017年5月24日;发布日期:2017年5月27日

摘 要
两种非离子表面活性剂(DM和NP-10)形成了二元复配体系,通过NMR各种技术对其复配体系中不同比例下形成的混合胶束的动态变化(包括胶束的堆积状况,分子间的排列方式、相互作用点及其分子间与分子内作用的变化等)进行了研究。二维NOESY技术证明了两者分子间的空间距离和相互作用力随着NP-10/DM比例的不同而变化,但其相互作用点不变;NMR的扩散系数表明了混合胶束的动力学半径随着NP-10/DM增大而增加,直到NP-10/DM摩尔比为1:6后趋于稳定,表明复配体系的浓度配比不是无限制的;横向弛豫时间T2显示了单体胶束与混合胶束随着各自比例的逐渐增大而朝着相反方向的变化趋势,此现象佐证了分子间作用力与分子内作用力的区别。弛豫时间还表明,当NP-10/DM的摩尔比为1:1/2~1:1时,其分子间的相互作用力开始减小,分子内作用开始起主导作用,暗示了复配体系中的最佳配比和协同效应的变化。
关键词 :核磁共振(NMR),壬基酚聚氧乙烯醚(NP-10),n-十二烷基-β-D-麦芽糖苷(DM),混合胶束,相互作用,动态变化

Copyright © 2017 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
非离子表面活性剂在溶液中不是以离子形式存在的,所以其稳定性很高,不易受强电解质存在的影响,同样也不容易受到酸碱的影响,能与其他表面活性剂进行很好的复配,相容性较好,随着其生产原料环氧乙烷生产成本的不断降低,非离子表面活性剂的应用越来越普遍。由于表面活性剂混合体系较单一表面活性剂性能优越,是实现高效率化学过程的一个有效途径,其聚集结构和性质的研究一直是胶体化学研究的热点之一,尤其是表面活性剂混合胶束的动态研究是人们探讨表面活性剂复配体系的重中之重。利用核磁共振技术具有探测分子内部而不破坏分子本身的特点,且能捕捉其它波谱方法所不能得到的信息。我们先后连续对阳离子与非离子表面活性剂形成的混合体系进行系统研究。前面发表了Gemini 氯化物季铵盐分别与多个非离子表面活性剂形成的复配体系,得到了混合胶束相互作用的动态性能 [1] [2] [3] [4] 。本文将绿色表面活性剂n-十二烷基-β-D-麦芽糖苷(DM)与壬基酚聚氧乙烯醚(NP-10)两种非离子表面活性剂形成的复配体系进行NMR研究。文献 [5] [6] [7] 仅报道了NP-10和DM在1:1浓度下混合物的吸附行为,用分析超速离心技术研究了在临界浓度(cmc)下单一和混合物的胶束形状有差别,获得表面聚集的标准自由能以及混合体系在固/液界面中吸附状况。我们将揭示两者形成的NP-10∕DM水溶液体系在各种比例下的动态行为,进一步探究该二元体系的微观结构变化,本文将对其混合胶束的大小、作用点、排列方式及其相互作用力变化等,通过NMR技术进行完善和系统的研究。
2. 实验部分
表面活性剂NP-10购自Nikko,纯度经HPLC测定大于99.0%;DM生产厂家Calbiochem,纯度经TLC测定大于95.0%;重水(D2O, 99.9%氘代)购自Cambridge Isotope Laboratories, Inc.;NP-10与DM的临界胶束浓度(cmc)在298K下由表面张力测得分别为0.059和0.180 mmol/L,两者的分子结构式、质子编号及其单一和混合体系的NMR氢谱见图1至图3。
本文实验均在频率为500.13 MHz的Bruker DMX-500核磁共振波谱仪上测定,溶剂D2O,测定温度为298 K,用Diffusion Ordered Spectroscopy (DOSY)测量自扩散系数,利用预饱和反转恢复法和CPMG脉冲序列测量自旋-自旋、自旋-晶格弛豫时间,二维NOESY谱采用标准三脉冲序列。为确保2D NOESY谱中相关点强度的准确性,避免系统中慢运动导致的自扩散,经过筛选最佳混合时间选为500 ms。
3. 结果与讨论
3.1. 化学位移值(δ)的变化
表面活性剂复配体系的氢谱化学位移(δH)对所处环境较敏感,是研究该体系的一个重要参数。储如当位于表面活性剂胶束极性的基层质子在经历了由单分子到聚集体形成的过程,它的化学环境会有所改变;当烷烃尾链上的质子又称疏水链从单一的分散状态变化到进入胶束内层的疏水核中,都会发生化学位移的改变,但是这些原因都抵不上分子间所发生的相互作用力而造成的化学位移的变化大。在NP-10/DM体系中,固定NP-10浓度为5.9 mmol/L,逐渐加大DM的摩尔比,从1:1/3;1:1/2;1:1;1:2;1:3……到1:10随着体系总浓度的不断增大,所有质子的化学位移逐渐移向低场;但不同质子的化学位移变化差值(∆δ)却不尽相同,其中NP-10分子上的N4、N5与N6质子位移差量变化最大,分别为0.052、0.068和0.074 ppm,DM分子上的D10、D9和D8质子位移变化次之分别为0.050、0.048和0.044 ppm,这暗示着NP-10分子上的苯环部位和DM分子上的倒数第二个糖环部位是发生分子间相互作用的点位。由于空间结构和化学环境的变化会随着复配体系总浓度的不断增大而改变,使得参与混合胶束形成的质子因化学环境变化而引起不同的位移值变化,尤其是混合胶束中的相互作用点∆δ变化更大。通过上述两分子中∆δ较大的质子,可帮助我们推断混合胶束的相互作用位置,当然该初步判断还需要后面二维NOESY结果的验证。
3.2. 扩散系数(D)的变化
分子的自扩散是分子热运动的一种,也是一个重要的分子动力学过程。胶束的自扩散可提供一个能检测胶束大小的可靠方法,可以用核磁共振波谱的脉冲场梯度(PFG)来定量描述,即通过测定自扩散系数来实现。NMR实验中所测得的自扩散系数是混合溶液中所有分子的平均值,既包括溶液中的胶束分子也包括自由单分子,在混合溶液中,自由单分子与胶束分子之间存在着快速交换,所以在浓度大于临界浓度cmc以上的混合溶液中,自扩散系数的实验分析是基于以下等式的 [8] [9] :
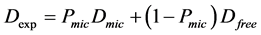 (1)
(1)
or
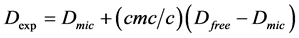 (2)
(2)
等式中Dexp是NMR实验所获得的自扩散系数,Dmic和Dfree分别表示混合溶液中的胶束和自由单分子的自扩散系数,Pmic表示胶束分子的浓度比率,cmc和c分别表示溶液的临界浓度和总浓度。由等式(1)和(2)可以看出,实验测得的扩散系数大小取决于溶液中的胶束和自由单分子两部分。根据相分离模型,混合溶液cmc(用cmc*表示)可以用下面等式表示 [10] :
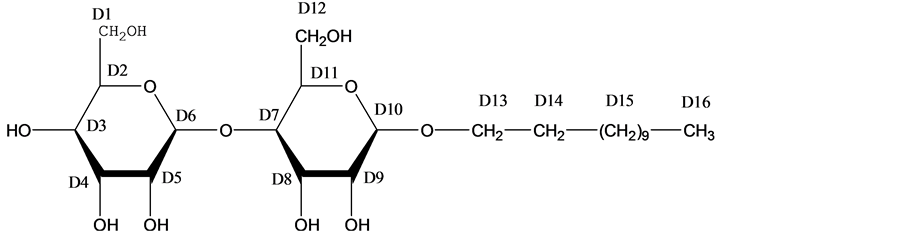

Figure 1. Structure and 1H NMR spectrum in D2O of DM
图1. DM结构式及在D2O中的1H NMR谱
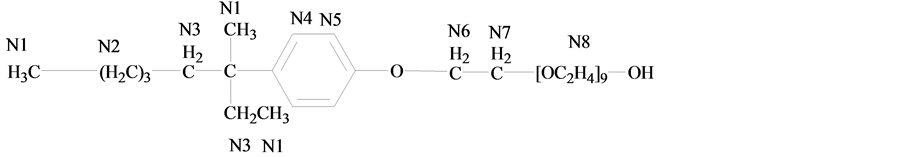

Figure 2. Structure and 1H NMR spectrum in D2O of NP-10
图2. NP-10结构式及在D2O中的1H NMR谱
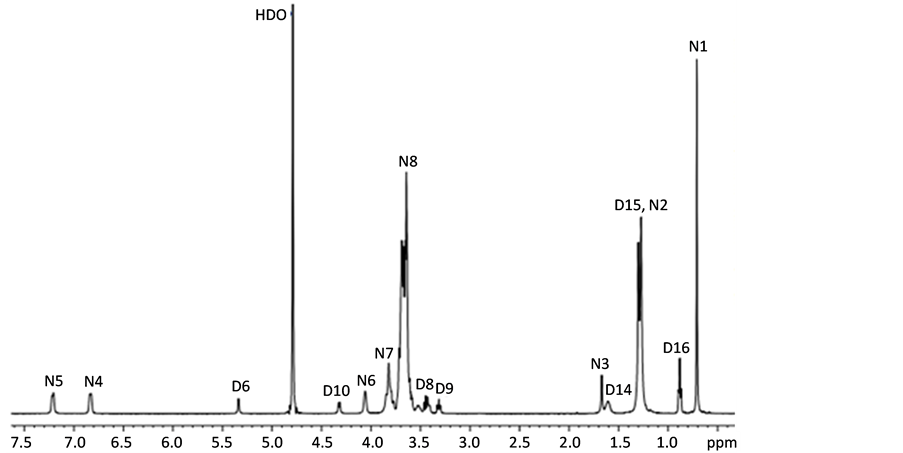
Figure 3. 1H NMR spectrum in D2O of NP-10/DM mixture
图3. NP-10/DM混合体系在D2O中的1H NMR谱
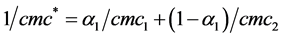 (3)
(3)
其中α1表示表面活性剂1在混合溶中所占的摩尔比例,cmc1和cmc2分别表示表面活性剂1和2的临界胶束浓度,通过等式(3)可计算出混合溶液的cmc*。在NP-10/DM混合体系中,我们实验溶液浓度为100倍以上的cmc*,此时溶液中都已经形成胶束,测量到的扩散系数主要是来自胶束的贡献,自由单分子的部分可忽略。
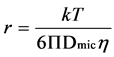 2-(3)
2-(3)
又由于Dmic与r之间的关系满足2-(3)方程式,即Stokes-Einstein公式 [11] ,其中体系的动力学半径是r,k为玻尔兹曼常数,T为测试绝对温度,Dmic为溶液中胶束的自扩散系数,η为溶液的粘度,通过上式可以看出Dmic与r成反比,因此通过测定Dmic值可以估测r的变化情况,进而可以研究和讨论胶束的相结构,包括胶束的聚集态和尺寸等。
从图4可以看出,NP-10/DM混合胶束的自扩散系数开始随着DM物质的量的增加而减小,根据Stokes-Einstein公式,胶束的Dmic与r成反比,可得混合胶束的水合动力学半径逐渐增大;体系在1:1与1:2之间动力学半径变化较大,到NP-10与DM摩尔比为1:6以后,自扩散系数值变化较小趋于稳定,表明此配比后再加DM量对混合胶束的水合动力学半径作用不明显,说明了复配体系的浓度配比不是无限制的增加,此时混合胶束中每个质子的扩散系数平均值为(5.7−11 m2/s)。
3.3. 弛豫时间(T)的变化
核磁共振中的弛豫时间是动力学参数,分为两种T1和T2,T1为自旋-晶格驰豫时间,对分子局部高频运动比较灵敏;T2为自旋-自旋弛豫时间,对长分子链的慢运动扩散敏感,若测得的T2/T1 ≤ 1,说明分子链的运动受到了限制 [12] [13] 。所以通过对弛豫时间的测定能获得NP-10/DM混合胶束的运动状况及分子内和分子间相互作用的大小转换等重要信息。分子的质子密度越多时,质子间的偶极相互作用就越强,分子链运动就越慢,导致T2较低,即在单一体系中,胶束浓度的增加,使得胶束的弛豫(即分子内作用力)
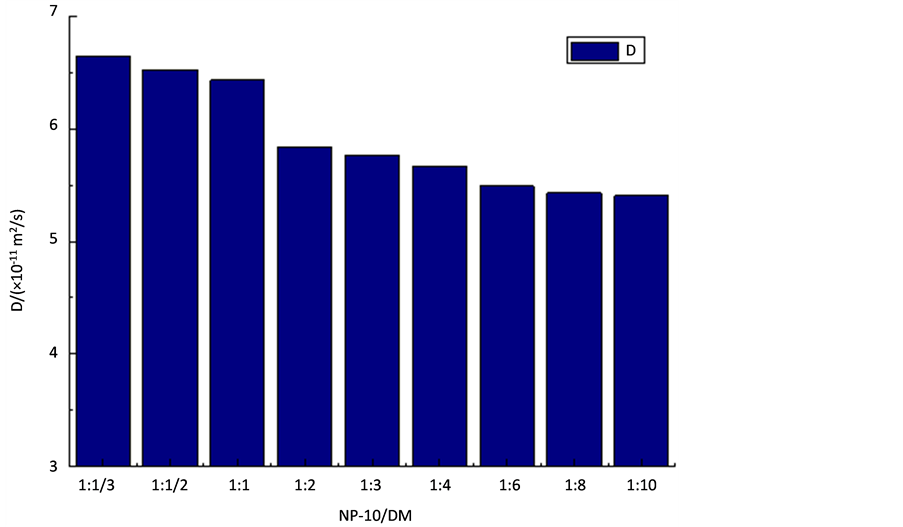
Figure 4. D value for mixed system of NP-10/DM as a function of molar ratio when NP-10 concentration is fixed at 5.9 mmol/L
图4. 固定NP-10 = 5.9 mmol/L时NP-10/DM体系随着摩尔比变化的D值
占主导,故NP-10和DM表面活性剂在单一溶液的情况下,各质子T2的变化规律是相似的,都是随着浓度的增加,各质子的T2值呈现缓慢下降的趋势。但当两者混合后随着浓度的增加,各质子的T2值在某比例内出现了缓慢上升的趋势。这充分证明了是由于混合胶束中产生了分子间相互作用的缘故。而当NP-10/DM复配体系摩尔比在1:1/2~1:1范围时,T2值呈现增大的趋势后又逐渐减小,这说明在摩尔比1:1/2~1:1范围内NP-10与DM分子间的相互作用较强,占主导作用,当继续增加NP-10/DM复配体系摩尔比1:3直1:10后,T2值又出现了下降的趋势(见表1),这说明了随着表面活性剂间混合比例的继续增大,分子间的作用力开始减小,而分子内的相互作用力开始起主导作用,导致了T2值的减小。两分子间相互作用大小直接影响混合体系中的协同效应,即1:1/2~1:1比例下,NP-10/DM复配体系协同效能较好。该结论得到后面2D NOESY实验结果的支持。
表2列出了NP-10/DM复配体系不同摩尔比时的TR值(即T2/T1),TR值可判断分子链运动的难易程度。当TR ≤ 1,表示分子链运动受到限制;TR ≤ 0.5,则说明分子链运动已受限严重。从表2数据可得,NP-10和DM两分子TR值均小于1,说明混合胶束中分子链运动受到限制,胶束堆积的比较紧密;体系中大部分质子的TR ≤ 0.5,表明NP-10/DM复配体系的混合胶束中分子链运动已严重受限。
3.4. 空间距离的变化
二维NOESY谱(Nuclear Overhauser Enhancement SpectroscopY)是基于核的overhauser效应而采用二维方式得到基团间的NOE信息的手段,换言之它是研究大分子聚集结构中空间距离小于0.5 nm的核间距的重要方法,它能够反映混合胶束中两个表面活性剂分子之间的相互作用强弱,质子之间的距离大小以及分子的排列方式。无论是分子内氢质子还是分子间氢质子,只要是质子核间距离较近(或小于5 Å)的两核,在二维NOESY谱上都会出现交叉峰,而且交叉峰强度与核间距离的六次方成反比,依据NOE效应的强度与质子间的距离存在如下的关系式,可求出质子间的距离及其变化 [14] [15] 。
Table 1. Variation of T2 values of NP-10/DM mixture at different molar ratios with a fiexdNP-10 of 5.9 mmol/L
表1. 固定NP-10 = 5.9 mmol/L时在NP-10/DM体系中部分质子随摩尔比变化的T2值
表2. 固定NP-10浓度为5.9 mmol/L时在NP-10/DM不同摩尔比时的TR (T2/T1)值
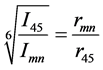 (4)
(4)
等式中,rmn表示m质子和n质子之间的距离,Imn表示m质子和n质子之间的交叉峰强度。
为方便比较,选择NP-10分子苯环上N-4/N-5间氢质子为参考距离.依据苯环的空间结构,可以求出N-4/N-5之间的距离是0.24 nm,再由等式(4)可以计算出其它两个质子间的距离。上述(4)式表明交叉峰的强度越强,说明两质子间的距离越近,那么作用力越强,由此就可以从2D NOESY谱图中定量的分析出两个表面活性剂的相互作用力变化情况。
从图5的2D NOESY谱中可发现,NP-10/DM复配体系中不仅存在分子内相互作用相关点如D6-D10,N4-N5外,还存在多个分子间相关点D10-N4,D10-N5,D16-N4,D16-N5和D16-N3,这表明了NP-10与DM复配形成混合胶束后两分子间距离小于0.5 nm。其相关作用点为:DM分子中的六元环氧烷烃质子D10分别与NP-10分子苯环上质子N4和N5相互作用;DM分子中的尾链质子D16又分别与NP-10分子中苯环上质子N4,N5以及苯环相邻质子N3均有相互作用,证明了NP-10中的苯环与DM中倒数第二个糖环及其疏水链末端发生了分子间相互作用,这也与化学位移得出的结论相吻合,由此推测出NP-10与DM两分子间形成胶束的排列方式,DM的疏水链应该是弯曲着包裹在NP-10的苯环周围,NP-10/DM混合胶束中的分子间相互作用点及其排列方式见图6所示。
见表3可比较NP-10/DM混合胶束中随着不同摩尔比分子间质子的空间距离的动态变化,当NP-10/DM体系摩尔比从1:1/3逐渐增大到1:10,D16-N5、D16-N4和D16-N3交叉峰强度比均是先增大后减小,意味着形成混合胶束两分子空间距离由紧密变得越来越疏松,当NP-10/DM复配体系摩尔比在1:1/2与1:1范围时,D16-N5、D16-N4和D16-N3质子间交叉峰的积分强度最大,经公式4计算出核间距离最短,此时两分子间相互作用最大,协同效能最好。也暗示着NP-10/DM复配体系较理想的摩尔比在1:1/2与1:1范围,这与前面弛豫时间得出的结论相一致。
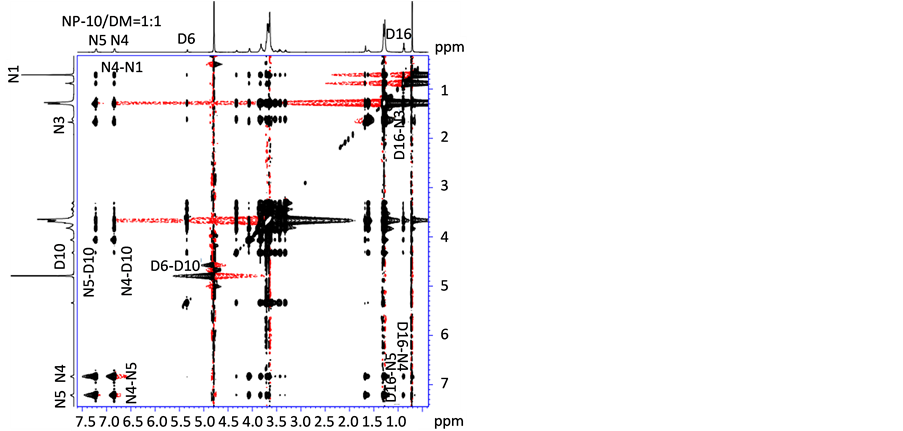
Figure 5. Contour plots of the 2D NOESY map for NP-10/DM mixed micelle at molar ratio of 1:1 and expanded map
图5. NP-10/DM体系摩尔比1:1时的2D NOESY谱图及局部扩展图
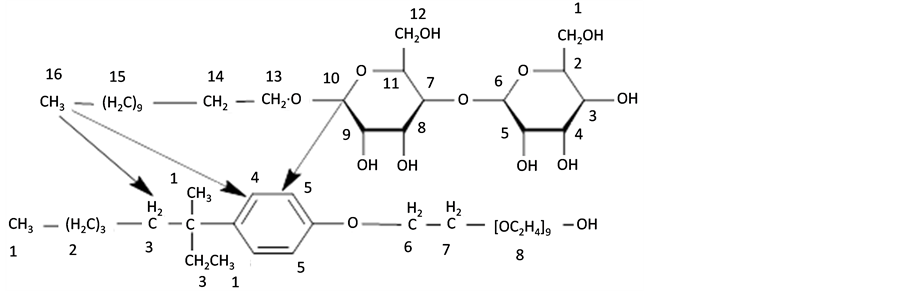
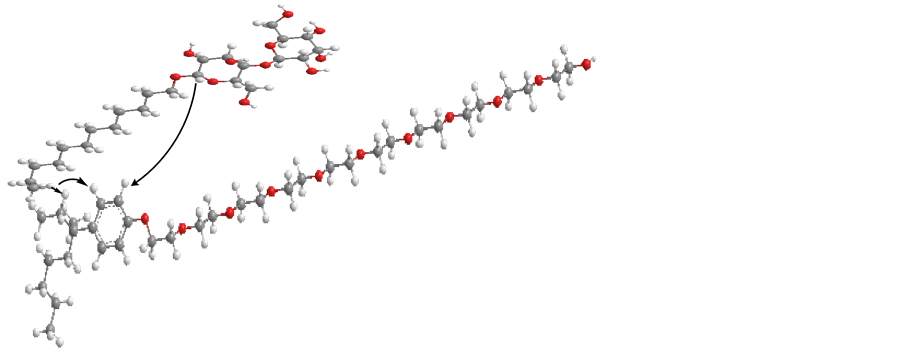
Figure 6. The shape and intermolecular interaction sites in the mixed micelles
图6. NP-10/DM混合胶束相互作用点及排列方式的平面和立体示意图
Table 3. Inter-proton distance (nm) of mixed micelles at different molar ratios
表3. 不同比例混合胶束的分子间质子距离(nm)
4. 结论
通过NMR各种技术研究了NP-10与DM复配体系,得到了混合胶束随着NP-10/DM摩尔配比的增大呈现出动态变化。化学位移δ值的变化,暗示了NP-10/DM体系中存着化学环境的大改变,源于分子间产生了相互作用,因化学位移变化差量(∆δ)推测出NP-10与DM发生分子间相互作用的范围,而二维NOESY实验确认了发生分子间相互作用的具体位置,即由化学位移∆δ值和弛豫时间T2推测的分子间相互作用都得到了二维NOESY的进一步验证。弛豫时间T2/T1反映了混合胶束的分子链运动受限较严重,T2表明NP-10/DM复配体系摩尔比在1:1后再增加DM的量,分子间相互作用开始减小,此时分子内相互作用占主导地位;二维NOESY显示了混合胶束中分子间空间距离随着NP-10/DM摩尔比的增加而变化着,但是分子间相互作用点不随NP-10/DM摩尔比的增加而改变,通过分子间作用力的大小表明该体系的最佳摩尔配比为1:1/2-1:1范围,又根据分子间相互作用点得到了它们空间的排列方式。自扩散系数表明了混合胶束的水合动力学半径不是随NP-10/DM摩尔比的增加而无限制增大,此时的NP-10/DM混合胶束中每个质子的自扩散系数平均值为(5.7−11 m2/s)。
文章引用
张卫红,赵瑞格,马二倩,张占辉,杨秋青. 非离子表面活性剂NP-10与DM复配体系中混合胶束的NMR动态研究
NMR Dynamic Study of Mixed Micelles in the Complex System of Non-Ionic Surfactant NP-10 and DM[J]. 分析化学进展, 2017, 07(02): 146-155. http://dx.doi.org/10.12677/AAC.2017.72020
参考文献 (References)
- 1. Yang, Q., Zhou, Q. and Somasundaran, P. (2007) Mixed Micelles of Octane-1,8bis(dodecyl dimethyl ammonium chlo-ride) and n-dodecyl-β-maltoside by 1H NMR Study. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 305, 22-28.
- 2. Yang, Q., Zhou, Q. and Somasundaran, P. (2008) NMR Study of Micellar Microstructures of Cationic Single-Chain and Gemini Surfactants and Their Mixtures with Nonionic Surfactant n-dodecyl-β-maltoside. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 322, 40-44.
- 3. Yang, Q., Zhou, Q. and Somasundaran, P. (2009) 1H NMR Study of Micelles Formed by Mixture of Nonionic n-dodecyl-β-D-maltoside and Cationic Geminisurfactants. Journal of Molecular Liquids, 146, 105-111.
- 4. 马二倩, 李永肖, 赵瑞格, 杨秋青. NP-10与单、双链季铵盐三种复配体系相互作用规律的NMR研究[J]. 波谱学杂志, 2017, 34(1): 16-24.
- 5. Zhang, R., Liu, C. and Somasundaran, P. (2007) A Model for the Cooperative Adsorption of Surfactant Mixtures on Solid Surfaces. Journal of Colloid and Interface Science, 310, 377-384.
- 6. Zhang, R. and Somasundaran, P. (2004) Abnormal Micellar Growth in Sugar-Based and Ethoxylated Nonionic Surfactants and Their Mixtures in Dilute Regimes Using Analytical Ultracentrifugation. Langmuir, 20, 8552-8558. https://doi.org/10.1021/la049295a
- 7. Zhang, L., Zhang, R. and Somasundaran, P. (2006) Adsorption of Mixtures of Nonionic Sugar-Based Surfactants with Other Surfactants at Solid/Liquid Interfaces II. Adsorption of n-dodecyl-β-D-maltoside with a Cationic Surfactant and a Nonionic Ethoxylated Surfactant on Solids. Journal of Colloid and Interface Science, 302, 25-31.
- 8. Lin, J., Chen, W. and Hou, S. (2013) NMR Studies on Effects of Tetraalkyl Ammonium bromides on Micellization of Sodium Dodecylsulfate. The Journal of Physical Chemistry B, 117, 12076-12085. https://doi.org/10.1021/jp403616p
- 9. Arkhipov, V.P., Idiyatullin, Z.S., Potapova, E.F., et al. (2014) Micelles and Aggregates of Oxyethylated Isononylphenols and Their Extraction Properties near Cloud Point. The Journal of Physical Chemistry B, 118, 5480-5487. https://doi.org/10.1021/jp502386e
- 10. Rauwel, G., Leclercq, L., Criquelion, J., et al. (2012) Aqueous Mixtures of Di-n-decyldimethylammonium Chloride/Polyoxyethylene Alkyl Ether, Dramatic Influence of Tail/Tail and Head/Head Interactions on Co-Micellization and Biocidalactivity. Journal of Colloid and Interface Science, 374, 176-186.
- 11. Sandoval, T.E., Espinoza, L.J., Guerra, I.A., et al. (2012) Study of the Size and Morphology of Aggre-gates Formed by Pentaethylene Glycol Monooctyl Ether (C8EO5) in n-Heptane. Colloids and Surfaces A: Physico-chemical and Engineering Aspects, 398, 17-23.
- 12. Podo, F., Ray, A. and Nemethy, G. (1973) Structure and Hydration of Nonionic Detergent Micelles. High Resolution Nuclear Magnetic Resonance Study. Journal of the American Chemical Society, 95, 6164-6170. https://doi.org/10.1021/ja00800a003
- 13. Yuan, H., Du, Y., Zhao, S., et al. (1999) Self-Aggregation of Surfactants in Water Solution by NMR. Science in China, 42, 319-323. https://doi.org/10.1007/BF02879067
- 14. Gao, H., Fang, X., Mao, S., et al. (2002) Conformation and Dynamics of Polyoxyethylene Lauryl Ether (Brij-35) Chains in Aqueous Micellar Solution Studied by 2DNOESY and 1H NMR Relaxation. Science in China, 45, 143-150. https://doi.org/10.1360/02yb9020
- 15. Blokhin, D.S., Fayzullina, A.R., Filippov, A.V., et al. (2015) Spatial Structure of Fibrinopeptide B in Water Solution with DPC Micelles by NMR Spectroscopy. Journal of Molecular Structure, 1102, 91-94.
