Water pollution and treatment
Vol.05 No.03(2017), Article ID:21338,8
pages
10.12677/WPT.2017.53006
Research on Removal of Nickel (II) Ions and Trichloroethylene from Aqueous Solution by Coated Nano Zero-Valent Iron
Xiaoxia Zhang1, Yue Cheng2*, Wenjing Fan2
1Shunde Area Foshan Lehua Ceramic Sanitary Ware Co. Ltd., Foshan Guangdong
2Materials Science and Engineering of Jingdezhen Ceramic University, Jingdezhen Jiangxi
*通讯作者。

Received: Jun. 16th, 2017; accepted: Jul. 9th, 2017; published: Jul. 12th, 2017

ABSTRACT
Coated nano zero-valent iron removal of Nickel (II) ions and trichloroethylene (TCE) results showed that: The removal of nickel ions and TCE was better with higher dosage of nano zero-valent iron and lower initial concentration. Capacity of four kinds of zero-valent iron material handling wastewater was: NZVI < Agar-NZVI < CMC-NZVI < Starch-NZVI; effect of wrapped agent act on pollutants could be ignored. When Nickel (II) and TCE concentrations were 5 mg/L in the mixed wastewater, amount of Starch-NZVI was 1.5 g/L; temperature was 30˚C; reaction time was 2.5 h; Nickel (II)+ and TCE had best treatment effect, with Nickel (II) removal rate 99.38%, TCE degradation rate 49.36%.
Keywords:Coated Nano Zero-Valent Iron, Nickel (II), Trichloroethylene (TCE), Removal Rate, Degradation Rate
包覆型纳米零价铁去除水中镍(II)离子和三氯乙烯的研究
张小霞1,成岳2*,樊文井2
1佛山市顺德区乐华陶瓷洁具有限公司,广东 佛山
2景德镇陶瓷大学材料科学与工程学院,江西 景德镇

收稿日期:2017年6月16日;录用日期:2017年7月9日;发布日期:2017年7月12日

摘 要
包覆型纳米零价铁去除镍(II)离子和三氯乙烯(TCE)的结果表明:Ni2+和TCE的去除率均随着包覆型纳米零价铁的投加量增加而升高,随着溶液初始浓度的增加而降低。四种零价铁材料处理混合废水的能力依次为:NZVI < Agar-NZVI < CMC-NZVI < Starch-NZVI,包裹剂Agar、CMC、Starch对目标污染物的作用可以忽略。在混合废水中Ni2+和TCE浓度都为5 mg/L,包覆型纳米零价铁的加入量为1.5 g/L,温度为30℃,反应时间为2.5 h,Starch-NZVI对Ni2+和TCE的处理效果最好,其中Ni2+的去除率为99.38%,TCE的脱氯率为49.36%。
关键词 :包裹型纳米零价铁,镍离子(II),三氯乙烯,去除率,脱氯率

Copyright © 2017 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
在一些工业废水和生活污水中,重金属离子和含氯有机物常可能同时存在。重金属离子的存在可能会对含氯有机物的降解产生阻碍作用,而在含氯有机物存在的情况下对重金属离子的去除也可能会受到不同程度的抑制 [1] 。目前,处理复合型污染废水大多采用吸附法和微生物法。吸附法只是将污染物从一个地方转移达到另外的地方,并不能彻底地去除污染物;微生物法又存在反应周期长、技术不成熟等缺点 [2] 。所以,需要寻找一种有效处理复合废水的技术。
纳米零价铁(NZVI)作为一种新型的环境修复材料,由于具有比表面积大、还原性强、活性高等特点,在各种卤化烃、多氯联苯、五氯苯酚、农药、染料、重金属离子、杀虫剂以及硝酸、高氯酸的盐类等环境污染修复中应用非常广泛。纳米铁材料常用于降解单一污染物,对水体中复合污染物的降解研究几乎未见报道 [3] 。
2. 试验
2.1. 主要试剂和仪器
硝酸镍(Ni(NO3)2•6H2O, A.R),氯化钠(NaCl, A.R),氨水(NH3•H2O),柠檬酸铵,硝酸银(AgNO3, A.R) 均为国药集团化学试剂有限公司;三氯乙烯(C2HCl3,A.R,天津市恒兴有限公司);硝酸,氢氧化钠NaOH,碘I2,乙二胺四乙酸二钠(CH14N2O8Na•2H2O, A.R),均为上海久亿化学试剂有限公司);丁二酮肟(CH3)2C(NOH) (南京化学试剂有限公司),去离子水(实验室自制)。
仪器:pHS-25型pH/电导计(上海仪电科学仪器股份有限公司);SHA-B型恒温振荡器(江苏金坛市荣华仪器制造有限公司);WFZ800-D3B型紫外可见分光光度计(北京瑞利分析仪器有限公司);AKDL-Ⅱ-16型纯水器(台湾艾柯,成都康宁实验专用纯水设备厂)。
2.2. Ni2+-TCE的去除试验分析与测定
Ni2+-TCE的去除在250 mL的具塞磨口锥形瓶中进行,将100 mL不同初始浓度的Ni2+-TCE溶液加入锥形瓶中,调节pH值,加入不同质量的包覆型纳米零价铁 [4] ,常温、常压下,将锥形瓶放入震荡器反应。根据设定时间取样,经0.22 μm滤膜过滤后,取滤液于分光光度计上分析测定。镍离子的浓度采用丁二酮肟分光光度法测定(GB/T15555.10-1995)。以测定的标准溶液的吸光度扣除空白(零浓度)后的吸光度,与对应的标准溶液的镍含量绘制校准曲线,y = 0.1065x − 0.0059,其中y为吸光度,x为溶液中Ni2+的浓度,R2 = 0.9981,于530 nm处进行分光光度测定,按下式计算镍离子的去除率:
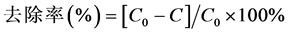 (1)
(1)
式中 —初始废水中镍离子的浓度,mg/L;
—初始废水中镍离子的浓度,mg/L;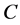 —处理后镍离子的浓度,mg/L。
—处理后镍离子的浓度,mg/L。
采用氯化银比浊度分光光度法测定水样中氯离子,实验测得氯离子标准曲线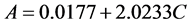
(A—吸光度,C—浓度,mg/L) R2:0.9931,于450 nm处进行分光光度测定,按下式计算TCE的脱氯率:
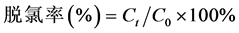 (2)
(2)
式中C0、Ct分别是t = 0和t = t时刻溶液中含氯离子的浓度,mg/L。
3. 分析与讨论
3.1. 包裹剂和包覆型纳米零价铁对水中Ni2+-TCE的去除效果
配制含Ni2+浓度和TCE浓度都为10 mg/L的溶液100 mL,分别加入1.5 g/L Agar、CMC、Starch,调节水浴振荡器温度为30℃,放入其中振荡。取反应后经滤膜过滤的溶液于比色管中,加入药剂,用分光光度计测定溶液的吸光度,结果如图1所示。其中,Starch对水中Ni2+和TCE的去除率最高,Agar的去除率最低。三种包裹剂对污染物的去除率均不高,几乎可以忽略。
3.2. 投加量对Ni2+-TCE去除率的影响
配制Ni2+和TCE浓度都为10 mg/L的溶液100 mL,分别加入0.5,1.0,1.5,2.0,2.5 g/L NZVI、Agar-NZVI、CMC-NZVI、Starch-NZVI,调节恒温水浴振荡器的温度为30℃,放入其中振荡2.5 h。取反应后经滤膜过滤的溶液于比色管中,加入药剂,用分光光度计测定溶液的吸光度。
投加量对Ni2+去除率影响如图2可知:在初始浓度,pH相同的条件下,投加量越多,去除效率就越高。投加量为0.5 g/L时,NZVI对Ni2+的去除率最低为91.35%,Starch-NZVI对Ni2+的去除率最高为95.88%,Agar-NZVI、CMC-NZVI对Ni2+的去除率介于两者之间。投加量为2.5 g/L时,NZVI对Ni2+的去除率最低为95.22%,Starch-NZVI对Ni2+的去除率最高为99.26%,Agar-NZVI、CMC-NZVI对Ni2+的去除率介于两者之间。在试验研究范围内,Ni2+的去除率均较高。
投加量对TCE去除的影响如图2可知:在初始浓度,pH相同的条件下投加量越多去除效率就越高。投加量为0.5 g/L时,NZVI对TCE的去除率最低为20.24%,Starch-NZVI对TCE的去除率最高为28.57%,Agar-NZVI、CMC-NZVI对TCE的去除率介于两者之间。投加量为2.5 g/L时,NZVI对TCE的去除率最高为28.37%,Starch-NZVI对TCE的去除率最高为46.95%,Agar-NZVI、CMC-NZVI对TCE的去除率介于两者之间。在试验研究范围内,TCE的去除率均较低,可能是因为包覆型纳米零价铁对TCE的降解需要的时间较长或者是包覆型纳米零价铁优先和重金属离子Ni2+反应所致。
3.3. 初始浓度对Ni2+-TCE去除率的影响
分别配制Ni2+、TCE浓度都为5,10,15,20,25 mg/L的溶液100 mL,加入1.5 g/L NZVI、Agar-NZVI、CMC-NZVI、Starch-NZVI,调节恒温水浴振荡器的温度为30℃,放入其中振荡2.5 h。取反应后经滤膜
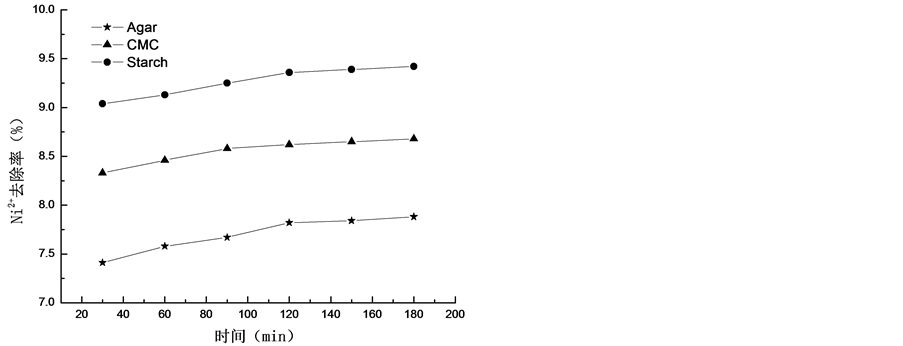
Figure 1. Effect of different types of wrapping agent on the removal percentage of Ni2+ and dechlorination rate of TCE
图1. 不同包裹剂对Ni2+去除率和TCE脱氯率的影响

Figure 2. Influence of dosage on removing Ni2+ and dechlorination rate of TCE
图2. 投加量对Ni2+去除率和TCE脱氯率的影响
过滤的溶液于比色管中,加入药剂,用分光光度计测定溶液的吸光度。
初始浓度对Ni2+去除率的影响如图3。从图中可知:在投加量、pH等条件相同时,初始浓度越低,去除效率越高。初始浓度为5 mg/L时,NZVI对Ni2+的去除率最低为95.18%,Starch-NZVI对Ni2+的去除率最高为99.38%,Agar-NZVI、CMC-NZVI对Ni2+的去除率介于两者之间。初始浓度为25 mg/L时,NZVI对Ni2+的去除率最低为91.27%,Starch-NZVI对Ni2+的去除率最高为96.9%,Agar-NZVI、CMC-NZVI对Ni2+的去除率介于两者之间。
初始浓度对TCE降解的影响如图3。从图中可知:在投加量、pH等条件相同时,初始浓度越低,去除效率越高。初始浓度为5 mg/L时,NZVI对TCE的降解率最低为38.86%,Starch-NZVI对TCE的降解率最高为49.36%,Agar-NZVI、CMC-NZVI对TCE的去除率介于两者之间。初始浓度为25 mg/L时,NZVI对TCE的降解率最低为26.74%,Starch-NZVI对TCE的降解率最高为35.01%,Agar-NZVI、CMC-NZVI对TCE的去除率介于两者之间。
3.4. pH对Ni2+-TCE去除率的影响
配制Ni2+和TCE浓度都为10 mg/L的溶液100 mL,调节pH分别为3,5,7,9,11,加入1.5 g/L NZVI、
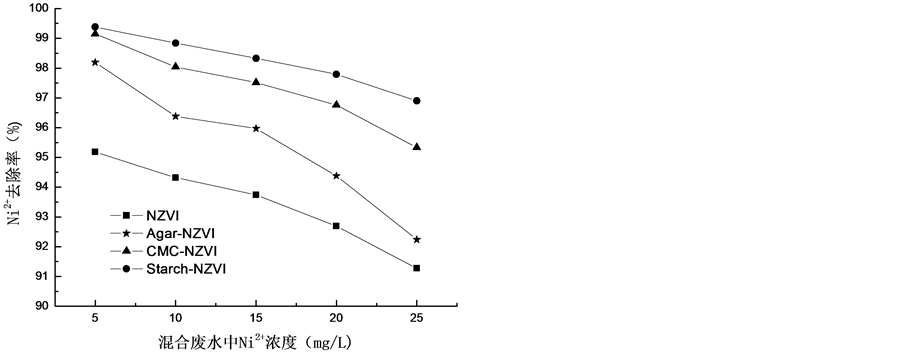
Figure 3. The influence of initial concentration on removing of Ni2+ and dechlorination rate of TCE
图3. 初始浓度对Ni2+去除率和TCE脱氯率的影响
Agar-NZVI、CMC-NZVI、Starch-NZVI,调节恒温水浴振荡器的温度为30℃,放入其中反应2.5 h。取反应后过滤的滤液于比色管中,加入药剂,测定吸光度。
pH对Ni2+去除率的影响如图4。从图中可知:在投加量、初始浓度相同的条件下,pH值为5时,对Ni2+去除效果最好,NZVI对Ni2+的去除率最低为94.87%,Starch-NZVI对Ni2+的去除率最高为99.26%,Agar-NZVI和CMC-NZVI对Ni2+的最高去除率在两者之间。pH值为11时,对Ni2+去除效果最差,NZVI对Ni2+的去除率最低为90.38%,Starch-NZVI对Ni2+的去除率最高为93.01%,Agar-NZVI和CMC-NZVI对Ni2+的最低去除率在两者之间。
pH对TCE降解的影响如图4。从图中可知:在投加量、初始浓度相同的条件下,pH值为5时,对TCE的降解效果最好,NZVI对TCE的脱氯率最低为31.75%,Starch-NZVI对TCE的脱氯率最高为47.39%,Agar-NZVI和CMC-NZVI对TCE的最高脱氯率在两者之间。pH值为11时,对TCE的降解效果最差,NZVI对TCE的脱氯率最低为22.79%,Starch-NZVI对TCE的去除率最高为30.08%,Agar-NZVI和CMC-NZVI对TCE的最低脱氯率在两者之间。
对实际混合废水Ni2+和TCE浓度都为5~10 mg/L,包覆型纳米零价铁的加入量为1.5~2.0 g/L,室温下,反应2~2.5 h时,Starch-NZVI对Ni2+和TCE去除率分别为98.25%,TCE的脱氯率为68.25%。
3.5. 反应后产物的SEM和EDS分析
将反应后的固体物质烘干后进行表征,图5显示的是完全反应后产物的SEM图。反应后颗粒呈现堆积状态,聚集在一起,同时也能观察到表面的氧化物质。纳米铁还原去除TCE的反应主要发生在前期,但是铁的氧化物和氢氧化物形成的絮凝物质对TCE也有一定的吸附效果,所以看到的反应后的纳米铁颗粒表面不仅存在铁的(氢)氧化物,也有部分的污染物。纳米铁颗粒还原去除TCE之后,Fe0本身被氧化成铁的氧化物,而不再以单质铁的形式存在。同时,由于反应溶液中氧的存在,单质铁被氧化成铁的氧化物、氢氧化物和碳酸盐类物质,并覆盖在铁颗粒的表面,阻止了反应的继续进行 [5] [6] 。
图6为反应后产物的能谱分析(EDS),主要含有C、O、Fe三种元素,其表面主要物质为Fe以及少量的铁氧化物和氢氧化物。表1为反应产物的元素分析表,氧元素和铁元素的重量百分比大,分别为43.24%、41.06%,表明反应后主要物质为铁的氧化物;由于包覆型纳米零价铁在与TCE的反应时小部分可能会被氧化,使得样品中氧元素的百分比含量增大。其中,纳米零价铁表面的C元素一方面来自于纳米零价铁与TCE接触降解过程,另一方面来自于与水中CO2的接触结合 [7] 。

Figure 4. Influence of pH on removing of Ni2+ and dechlorination rate of TCE
图4. pH对Ni2+去除率和TCE脱氯率的影响

Figure 5. SEM image after reaction (a) CMC-nZVI; (b) agar-nZVI; (c) starch-nZVI
图5. 反应后产物的SEM图 (a) CMC-nZVI;(b) agar-nZVI;(c) starch-nZVI
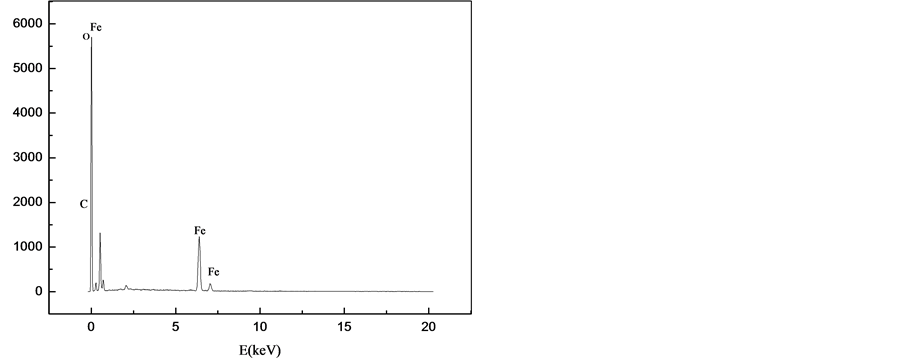
Figure 6. EDS image after reaction production
图6. 反应后产物的EDS图
Table 1. Element analysis of the sample after reaction
表1. 反应后产物的元素分析表
3.6. 包覆型纳米零价铁去除TCE的反应机理
包覆型纳米零价铁同时去除水中Ni2+和TCE的机理分为两个途径:吸附和还原。由于包覆型纳米零价铁具有较大的比表面积,镍离子和三氯乙烯容易吸附在包覆型纳米零价铁表面;其次,纳米铁被水腐蚀,发生还原反应将Ni2+还原成Ni0,进而发生催化脱氯降解TCE。
镍的存在加速了铁的腐蚀,能提供更多的电子,从而加快还原反应的进行。纳米零价铁材料对水中三氯甲烷、三氯乙烯等氯代有机物的还原脱氯研究表明,在脱氯还原反应涉及的氢转移过程中,Ni可作为加氢催化剂,将铁腐蚀产生的氢气吸附到表面,并将分子态的氢转化为原子态的氢,而原子态氢作为较强的还原剂,可与TCE反应,取代氯原子生成乙烷 [8] 。此外,Ni作为过渡金属具有空轨道,能够与氯元素的p电子对形成络合物,降低脱氯反应的活化能,使得反应更容易进行 [9] 。
零价铁与它在溶液中的二价铁离子(Fe0/Fe2+)的标准电极电位为0.440 V,比大多数卤代烃获得电子还原脱卤的反应电位要低,表明零价铁是一种很强的还原剂,氯代烃(RCl)可以被零价铁还原 [10] 。
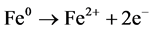 (3)
(3)
 (4)
(4)
反应式(3)表示即使没有强氧化剂的存在,在水溶液中零价铁也会自发地被腐蚀。按照上述两个反应的氧化还原电位,从热力学上讲,下面的反应比较容易发生。
 (5)
(5)
此反应可以看作氯代烃为氧化剂对零价铁的氧化或者零价铁为还原剂对氯代烃的还原。当有溶解氧存在时零价铁的腐蚀反应如式(6)。
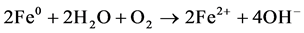 (6)
(6)
(6)式产生的Fe2+可以进一步生成Fe(OH)2和Fe(OH)3。同时,在水环境中,水本身也可以作为氧化剂。
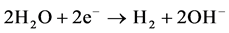 (7)
(7)
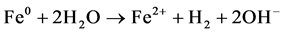 (8)
(8)
在无氧条件下,零价铁的腐蚀按照反应式(8)进行。明显地,按照反应式(6)和(8),体系的pH都会有所上升。当然,在有氧条件下,腐蚀会更快,pH上升也较大。pH值的升高容易生成氢氧化铁和氢氧化亚铁的沉淀,这种沉淀会在介质表面形成一层膜阻碍反应进一步发生。
大分子物质Agar、CMC和Starch包覆在NZVI表面后,能在一定程度上阻止金属颗粒的团聚。在反应过程中,包覆型纳米零价铁颗粒均匀的分散在TCE废水中,暴露出来的零价铁与TCE发生反应,而包裹剂能溶于水,可有效地生物降解。
4. 结论
1) 纳米零价铁材料能同时去除水中的重金属离子Ni2+和有机污染物TCE。四种材料对复合污染物的处理效果依次为:NZVI < Agar-NZVI < CMC-NZVI < Starch-NZVI,说明包覆型纳米零价铁的还原性在纳米零价铁的基础上得到了较大的提高。
2) 包覆型纳米零价铁去除复合废水的主要影响因素有:初始pH值、样品的投加量和初始浓度。实验结果表明,较小的pH值、较低的初始TCE浓度和较高的样品的投加量对污染物的去除效果稍好。在混合废水中Ni2+和TCE浓度都为5 mg/L,Starch-NZVI的加入量为1.5 g/L,温度为30℃,反应时间为2.5 h,对Ni2+-TCE的处理效果最好,其中Ni2+的去除率为99.38%,TCE的降解率为49.36%。
3) 在试验范围内,纳米零价铁对混合废水中重金属Ni2+的处理效果均比较好,对TCE的处理效果均不太理想,可能是因为包覆型纳米零价铁对TCE的降解需要的时间较长或者是包覆型纳米零价铁优先和重金属Ni2+反应导致包覆型纳米零价铁不足。
基金项目
国家自然基金项目( 56218018)。
文章引用
张小霞,成 岳,樊文井. 包覆型纳米零价铁去除水中镍(II)离子和三氯乙烯的研究
Research on Removal of Nickel (II) Ions and Trichloroethylene from Aqueous Solution by Coated Nano Zero-Valent Iron[J]. 水污染及处理, 2017, 05(03): 41-48. http://dx.doi.org/10.12677/WPT.2017.53006
参考文献 (References)
- 1. Lin, Y.H., Hsu, C.H., Wu, C.L., et al. (2009) Simultaneous Sorption of Lead and Chlorobenzene by Organobentonite. Chemosphere, 49, 1309-1315.
- 2. Oyanedel-Craver, V.A., Fuller, M. and Smith, J.A. (2007) Simultaneous Sorption of Benzene and Heavy Metals onto Two Organoclays. Journal of Colloid and Interface Science, 309, 485-492.
- 3. Wang, Q.P., Kuang, Y., Jin, X.Y., et al. (2014) Simultaneous Removal of Cu(Ⅱ) and Chlorobenzene from Aqueous Solution by CA-Ni/Fe Nanoparticles. Acta Scientiac Circum-stantiac, 34, 1228-1235.
- 4. Jiao, C., Cheng, Y. and Fan, W.J. (2015) Synthesis of Agar Stabilized Nanoscale Zero-Valent Iron Particles and Removal Study of Hexavalent Chromium. International Journal of Environmental Science and Technology, 5, 1603-1612. https://doi.org/10.1007/s13762-014-0524-0
- 5. 董婷婷. CMC稳定化纳米Pd-Fe还原去除对硝基氯苯研究[M]. 广东: 华南理工大学, 2011.
- 6. 冯丽, 葛小鹏, 王东升, 等. pH值对纳米零价铁吸附降解2,4-二氯苯酚的影响[J]. 环境科学, 2012, 33(1): 94-103.
- 7. 任蓉. 包覆型纳米零价铁/厌氧体系在脱氯过程中其表面形态变化研究[M]. 广东: 华南理工大学, 2013.
- 8. Ge, S.H., Wu, Z.J., Zhang, M.H., et al. (2006) Sulfolene Hydrogenation over an Amorphous Ni-B Alloy Catalyst on MgO. Industrial and Engineering Chemistry Research, 45, 2229-2234. https://doi.org/10.1021/ie0512542
- 9. Han, Y., Li, W., Zhang, M.H., et al. (2008) Catalytic Dechlorination of Monochlorobenzene with a New Type of Nanoscale Ni(B)/Fe(B) Bimetallic Catalytic Reductant. Chemosphere, 72, 53-58.
- 10. Han, Z.T. and Lv, X.L. (2013) New Progress of Nano-Zero-Valent Iron Groundwater Remediation Technology. Hydrogeology and Engineering Geology, 40, 41-47.
