Studies in Synthetic Chemistry
Vol.03 No.03(2015), Article ID:16011,6
pages
10.12677/SSC.2015.33009
Study on Synthesis of 1,3,5-Triacetylbenzene
Jing’an Zhang1*, Xunzhong Zou1,2, Yajie Liu1,2, Lijie Zhang1,2, Yitao Ou1, Yanfang Cheng1
1School of Pharmacy, Guangdong Pharmaceutical University, Guangzhou Guangdong
2College of Traditional Chinese Medicine, Guangdong Pharmaceutical University, Guangzhou Guangdong
Email: *zhangja@126.com
Received: Aug. 21st, 2015; accepted: Sep. 6th, 2015; published: Sep. 10th, 2015
Copyright © 2015 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
Objective: 1,3,5-Triacetylbenzene was synthesized. Methods: 1,3,5-Triacetylbenzene was prepared by ethyl formate and acetone reaction with sodium ethoxide and then the producing unsaturated sodium ethoxide solution was acidified with weak acid. Results: 1,3,5-Triacetylbenzene was synthesized and confirmed by TLC, melting point, 13C-NMR and 1H-NMR. Conclusion: The operating method of the synthesis of 1,3,5-triacetylbenzene was simple, cheap and easily available for the raw materials, so it could be used for the industrial synthesis of relatively large quantities.
Keywords:1,3,5-Triacetylbenzene, Ethyl Formate, Acetone, Synthesis

均苯三乙酮的合成研究
张精安1*,邹训重1,2,刘亚杰1,2,张莉杰1,2,欧意桃1,程燕芳1
1广东药学院药科学院,广东 广州
2广东药学院中药学院,广东 广州
Email: *zhangja@126.com
收稿日期:2015年8月21日;录用日期:2015年9月6日;发布日期:2015年9月10日

摘 要
目的:合成均苯三乙酮。方法:利用甲酸乙酯、丙酮和乙醇钠反应生成不饱和醇钠,然后用弱酸酸化生成均苯三乙酮。结果:成功合成出均苯三乙酮,并通过TLC监测、测定其熔点及质谱和核磁共振氢谱确定其结构。结论:此合成均苯三乙酮的方法操作简单,原料价廉易得,可用于工业上合成较大量的均苯三乙酮。
关键词 :均苯三乙酮,甲酸乙酯,丙酮,合成

1. 引言
均苯三乙酮(即1,3,5-三乙酰基苯)属于芳香酮,具有三个羰基结构,能发生酮式–烯醇式互变异构,因其具有α-H,化学性质活泼。均苯三乙酮主要作为合成含氮杂环配体的原料及其类似物,这类化合物可与中心原子或离子以配位键相结合形成配位化合物,在药物化学[1] 、均相催化[2] 、不对称催化[3] 及环境化学等领域都有广泛的应用。用这类配体合成的过渡金属或稀土金属配位化合物主要在分析化学中用于金属离子的分离、滴定和掩蔽干扰,也广泛应用于工业生产中的配位催化、提取金属和硬水软化等方面。此外,树形化合物也可作为多电子转移催化剂、分子电子器件,高效凝絮剂、稳定剂和膜材料等,特别是在药物化学方面,具有亲水性表面基团又有疏水内层树枝状大分子中的内层空隙可用来隐藏需缓慢释放的药物,而作为新的药物缓释剂或导弹式药物[4] 。作为合成树形化合物的关键原料,均苯三乙酮在工业、农业、国防、医学、生命科学、环境保护等国民经济领域有重要的应用前景[5] [6] 。同时,均苯三乙酮的席夫碱和曼尼希碱衍生物及其配合物也具有抑菌杀菌、抗肿瘤和抗氧化等的生物活性[7] [8] ,在催化、分析化学、腐蚀、染料涂料、石油化工以及光致变色等领域亦有重要应用[9] [10] 。
均苯三乙酮及其衍生物应用广泛,但因其价格昂贵,应用受到限制。因此,国内外化学工作者积极探索使用不同原料和方法来合成均苯三乙酮。均苯三乙酮的合成方法主要有三种[11] -[13] ,第一种是用(E)-4-甲氧基丁-3-烯-2-酮在无氧和高温高压条件下合成,产率77%,但原料不容易得到并且反应条件苛刻;另外两种分别用(E)-4-(二甲基氨基)丁-3-烯-2-酮和丁-3-炔-2-酮为原料合成,产率分别是65%和95%,产率虽有提高,但同样原料不易得到。
本实验通过改进文献[11] -[13] 方法,选取实验材料易得、无须苛刻条件的实验方法。均苯三乙酮合成路线如下:
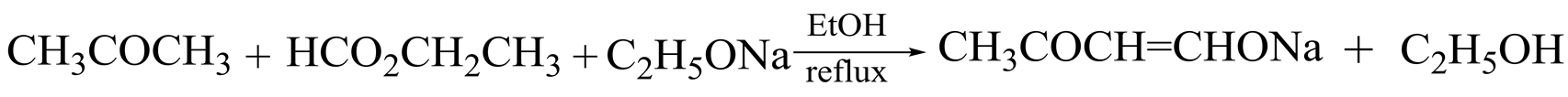
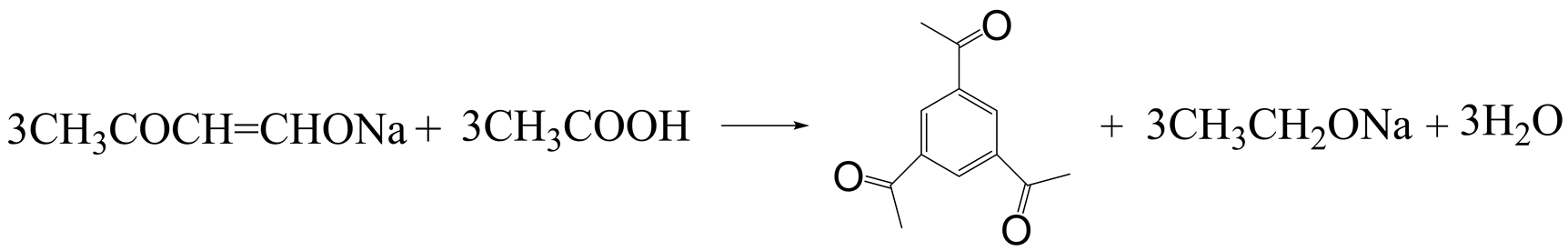
此合成反应是典型的克莱森-斯密特(Claisen-Schimit)缩合反应,即含有α-氢的酯在醇钠等碱性缩合剂作用下发生缩合作用,失去一分子醇得到β-酮酸酯的反应。在这个反应中,同样以醇钠为碱性介质,甲酸乙酯、丙酮和醇钠反应生成不饱和醇钠,在弱酸的催化下,羰基烯经过加成环化得到均三乙酰基苯。
2. 实验部分
2.1. 主要试剂与仪器
主要试剂
甲酸乙酯(纯度98%,华威锐科)、冰乙酸(分析纯,纯度99.5%,天津市富宇精细化工有限公司)、钠(分析纯,纯度99.5%,天津市科密欧化学试剂有限公司)、硼氢化钠(分析纯,纯度96%,上海润捷化学试剂有限公司)、氯化钙(分析纯,纯度96%,天津福晨化学试剂厂)、盐酸(分析纯,纯度36%,天津市富宇精细化工有限公司)、甲苯(分析纯,纯度99.5%,广州化学试剂厂),其它试剂均为分析纯且所有无水试剂均需经过干燥处理。
仪器
质谱仪(DSQ,美国Thermo公司);1H NMR谱(美国VARIAN公司Mercury-Plus 300型核磁共振仪)。
2.2. 实验方法
取12.65 g钠(0.55 mol)切成小块,加入装有40 mL二甲苯的三颈瓶中,装上回流冷凝管、机械搅拌器和装有氯化钙的干燥管,通入氮气,加热回流,剧烈搅拌。打成钠沙后冷却至室温,倾出二甲苯,用20 mL无水乙醚洗涤一次,完毕后加入150 mL无水乙醚,2 h内滴加无水乙醇36 mL (0.6 mol),再搅拌回流6 h。之后4 h内滴加甲酸乙酯40 mL (0.5 mol)和丙酮37 mL (0.5 mol)的混合液,完毕后反应2 h。加入水500 mL分3次萃取,取水层置于1000 mL四口瓶内,用冰乙酸(约40 mL)调pH值呈酸性,装上回流冷凝管、机械搅拌器和温度计,通入氮气,于55℃反应4 h,再停止加热搅拌,静置过夜。抽滤,滤出沉淀,干燥,用丙酮重结晶,得到浅黄色晶体。再用95%乙醇重结晶,得纯白色晶体,产率60.4% (文献[4] 56%,只一次重结晶)。m.p. 161℃~162℃ (文献[4] 162℃~163℃)。
3. 结果与讨论
3.1. 均苯三乙酮产率、鉴定及表征
产物经两次重结晶后为牙白色晶体,产率为60.4%,文献[4] 产率为56% (只重结晶一次),熔点为161℃~162℃ (文献[4] 162℃~163℃);用薄层色谱法鉴定,分别用三种展开剂展开:1) 以乙酸乙酯为展开剂时,在254 nm紫外光下得单一点,Rf值为0.89;2)以混合溶剂(二氯甲烷:甲醇 = 100:1)为展开剂时,在254 nm紫外光下得单一点,Rf值为0.70;3)以混合溶剂(二氯甲烷:乙腈 = 10:1)为展开剂时,在254 nm紫外光下得单一点,Rf值为0.72。
质谱鉴定,质谱图如图1,产物分子电离产生的离子分析如图2所示,其中质荷比m/z 204峰为均苯三乙酮的分子离子峰;m/z 189峰为基峰,由m/z 204的分子离子丢失甲基产生;m/z 161峰与分子离子峰差值43,由m/z 204的分子离子丢失乙酰基产生;m/z 146峰说明m/z 204的分子离子丢失一个甲基和乙酰基;m/z 119峰说明m/z 204的分子离子丢失两个乙酰基;m/z 103峰说明m/z 204的分子离子丢失两个乙酰基和一个甲基;m/z 75峰为苯基碎片离子峰,说明m/z 204的分子离子丢失三个乙酰基;m/z 91峰很可能为杂质峰。综上所述,该产物的可能结构为均苯三乙酮。
核磁共振氢谱鉴定,如图3所示,化学位移值δ = 2.722处的峰为单峰,且此处有9个氢,可能是有三个没有邻位氢的乙酰基的甲基峰;化学位移值δ = 8.695处的峰为单峰,没有邻位氢,此处有3个氢,可能为苯环上位于间位的三个氢峰,且苯上有三个间位取代基;化学位移值δ = 7.255处的双峰为溶剂氘

Figure 1. The MS of 1,3,5-triacetylbenzene
图1. 均苯三乙酮质谱图
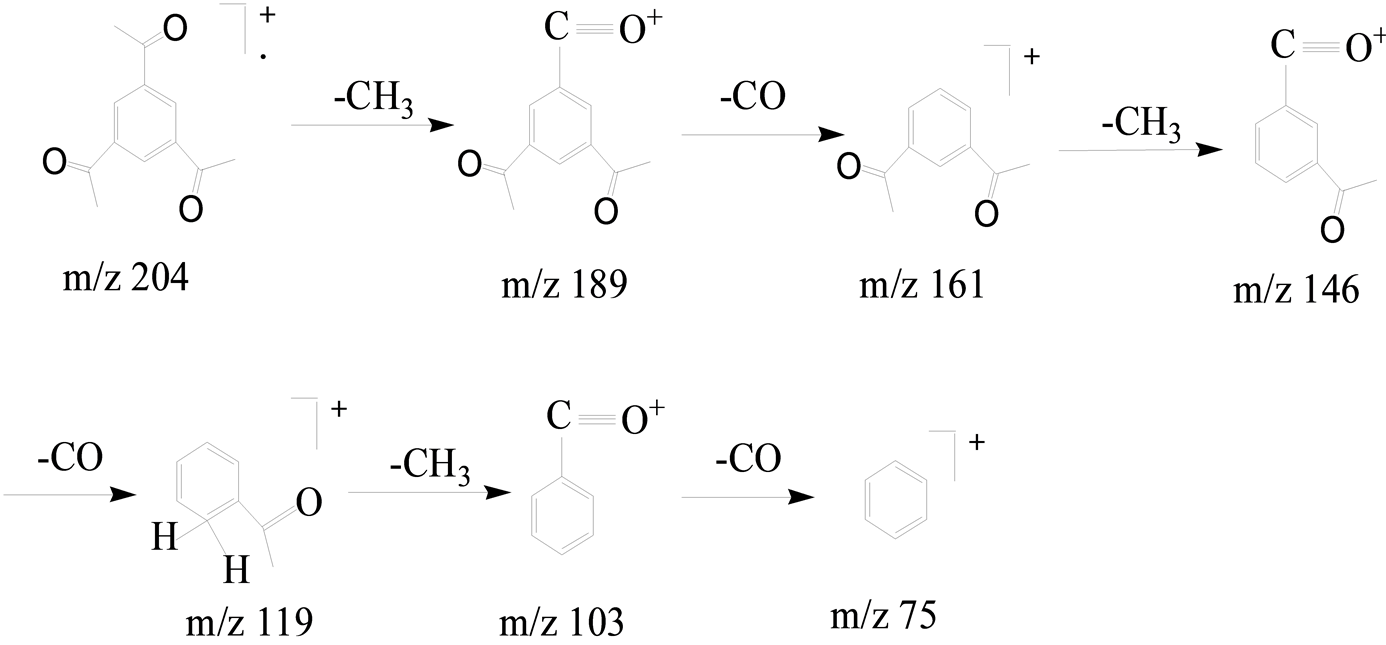
Figure 2. The analysis of primary ion in mass spectrum of 1,3,5-triacetylbenzene
图2. 均苯三乙酮质谱中主要离子的分析
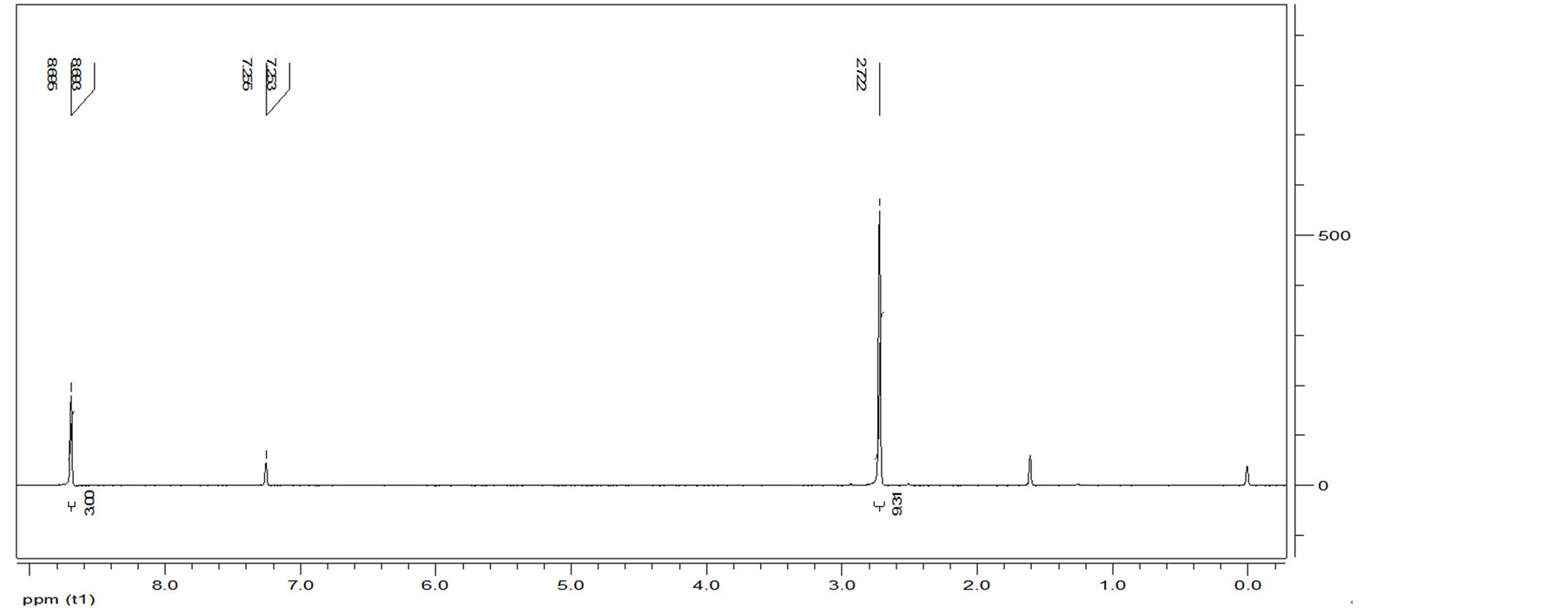
Figure 3. The 1H NMR of 1,3,5-triacetylbenzene
图3. 均苯三乙酮核磁共振氢谱图
代氯仿的峰;化学位移值δ = 1.608处的单峰为水峰,由氘代氯仿中的少量水所致。综上所述,该产物的可能结构为均苯三乙酮。
3.2. 结果讨论
在合成均苯三乙酮实验中,反应要确保无水无氧的条件,制备醇钠和加乙酸后的反应都要用氮气保护。试剂要绝对干燥,反应时加干燥管。制备乙醇钠是反应成功的关键,钠沙要极细均匀,滴加乙醇的速度要慢,反应的时间可适当延长,有时密封静置一晚效果会更好。若想要纯白色的乙醇钠溶液可先用少量无水乙醚洗涤钠沙一两次。此外,滴加甲酸乙酯的速度是取得高产率的关键,而且,使用溶剂乙醚时尽量少些[4] 。
在实际的实验操作中,合成均苯三乙酮的产率还不是很高,分析原因如下:1) 冷凝管的温度不够低,以至于溶剂和原料(如乙醚和甲酸乙酯)少量挥发掉,可改用循环冷却水冷凝,提高产率;2) 溶剂乙醚的加入量把握得不够好,可将溶剂视实验现象分批加入;3) 加入乙酸后,没有按梯度温度逐步调节反应温度;4) 文献是一次重结晶,在本实验中是两次重结晶,损失较大。
4. 结论
本文参考文献并加以进行改进较高的产率合成出均苯三乙酮,并探讨提高产率的方法。本文成功合成了均苯三乙酮,并通过测熔点,用薄层色谱法鉴定,用质谱和氢谱表征,证实了产物的结构为均苯三乙酮。
基金项目
广东省高等学校高层次人才项目(2011QY01)、广东省建设科技思想库研究课题项目(2014GDSXK011)、广东药学院2015年国家级、省级、校级大学生创新创业训练计划项目(201510573012)。
文章引用
张精安,邹训重,刘亚杰,张莉杰,欧意桃,程燕芳. 均苯三乙酮的合成研究
Study on Synthesis of 1,3,5-Triacetylbenzene[J]. 合成化学研究, 2015, 03(03): 58-63. http://dx.doi.org/10.12677/SSC.2015.33009
参考文献 (References)
- 1. 郑伟 (2009) 新型美普他酚类治疗AD的多靶向配体的设计、合成和生物活性. 硕士论文, 上海复旦大学, 上海.
- 2. 郭向前 (2006) 吡啶基含氮三齿配体的合成及其在均相催化反应中的应用. 硕士论文, 南京工业大学, 南京.
- 3. 韩美玲 (2012) 基于Ugi’s胺和α-苯乙胺的手性配体的合成及其在不对称催化反应中的应用. 硕士论文, 天津大学, 天津.
- 4. 张来新, 杨琼 (2001) 树形化合物的产生、发展及应用. 湖州师范大学学报, 23, 39-43.
- 5. 李洪波, 魏荣宝, 梁娅 (2006) 一种新型树状化合物1,3,5-三-[3-(3,11,11-三甲基-2,4,10,12-四氧杂-9,13-二氧代-二螺[5.1.5.1]-十四烷基)]苯的合成. 天津理工大学学报, 22, 5-7.
- 6. 梁娅, 李洪波, 魏荣宝, 等 (2007) 新型树形化合物1,3,5-三-[7-(7-甲基-2,2-二-(2,2-二羟甲基-3-羟基丙氧基羰基)-6,8-二氧杂螺[3.5]-壬基)]苯的合成. 有机化学, 27, 1155-1158.
- 7. 王澈, 侯鹏, 李崧 (2009) 席夫碱及其金属配合物的合成及生物活性研究进展. 化学通报, 4, 334-340.
- 8. 陈玉红, 丁克强, 王庆飞, 等 (2003) 席夫碱应用研究新进展. 河北师范大学学报: 自然科学版, 27, 71-74.
- 9. 王淑月, 王小凤, 樊淑彦 (2008) 曼尼希碱及曼尼希碱型前药的研究现状. 河北工业科技, 25, 315-320.
- 10. 皇甫健 (2012) 曼尼希碱海水碳钢缓蚀剂的制备及其作用机理研究. 硕士论文,中国海洋大学, 山东.
- 11. Iwado,T., Hasegawa, K., Sato, T., et al. (2013) Mechanistic and exploratory investigations into the synthesis of 1,3,5- triaroylbenzenes from 1-aryl-2-propyn-1-ones and 1,3,5-triacetylbenzene from 4-methoxy-3-buten-2-one by cyclotrimerization in hot water in the absence of added acid or base. Journal of Organic Chemistry, 78, 1949-1954. http://dx.doi.org /10.1021/jo301979p
- 12. Abdel-Khalik, M.M. and Elnagdi, M.H. (2002) Enaminoines organic synthesis: A novel synthesis of 1,3,5-trisubsti- tuted benzene derivatives and of 2-substituted-5-aroylpyridides. Synthetic Communications, 32, 159-164. http://dx.doi.org /10.1081/SCC-120001996
- 13. Zhou, Q.F., Yang, F., Guo, Q.X., et al. (2007) A new organocatalytic process of cyclotrimerization of acetylenic ketones mediated by 2,4-pentanedione. Synlett, 2, 215-218. https://www.thieme-connect.de/DOI/DOI?10.1055/s-2007-967997