Advances in Applied Mathematics
Vol.05 No.03(2016), Article ID:18468,13
pages
10.12677/AAM.2016.53063
Stability Analysis of HIV/AIDS Model with Non-Cell-Propagation, Cell-Propagation and Humoral Immune Response
Asiye Osman, Xamxinur Abdurahman*
College of Mathematics and System Sciences, Xinjiang University, Urumqi Xinjiang

Received: Aug. 10th, 2016; accepted: Aug. 26th, 2016; published: Aug. 31st, 2016
Copyright © 2016 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/



ABSTRACT
Based on vital biological meanings, we consider a class of HIV infection models with both cell-free virus spread and cell-to-cell transmission. First of all, we show that all the solution to our system is positive and bounded. Then, we give the basic reproduction number 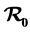 and we prove that if
and we prove that if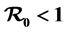 , the infection-free equilibrium is globally stable. And if
, the infection-free equilibrium is globally stable. And if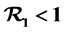 , the endemic equilibrium with humoral immunity is locally asymptotically stable, if
, the endemic equilibrium with humoral immunity is locally asymptotically stable, if , the endemic equilibrium with humoral immunity is globally stable.
, the endemic equilibrium with humoral immunity is globally stable.
Keywords:Drug Therapy, Cell-to-Cell Transmission, Humoral Immune, Lyapunov Function, Global Stability

带有无细胞传播、细胞传播和体液免疫反应的HIV/AIDS模型的稳定性分析
阿斯亚·吾斯曼,夏米西努尔·阿布都热合曼*
新疆大学,数学与系统科学学院,新疆 乌鲁木齐

收稿日期:2016年8月10日;录用日期:2016年8月26日;发布日期:2016年8月31日

摘 要
根据重要生物意义,我们研究了一类具有HIV感染经典细胞扩散与细胞之间传播以及具有治疗的HIV感染模型。本文我们首先讨论了解的正性和有界性。然后,给出了系统的平衡点和基本再生数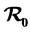 。当
。当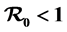 时,得到了系统无病平衡点的全局稳定性。当
时,得到了系统无病平衡点的全局稳定性。当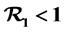 时,得到了无体液免疫平衡点的稳定性,而当
时,得到了无体液免疫平衡点的稳定性,而当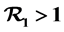 时,得到了系统体液免疫平衡点的全局稳定性等结论。
时,得到了系统体液免疫平衡点的全局稳定性等结论。
关键词 :药物疗法,细胞与细胞之间的传递,体液免疫,Lyapunov函数,全局稳定性

1. 介绍
HIV (人类缺陷免疫病毒)被认为最恶劣疾病之一。它用目标CD4+来攻击人类免疫系统的破坏,致抵抗力的下降。遗传,个体和微生物共同感染,个体体内应变的病毒的水平等是这种疾病的主要传播方式。
HAART (高活性抗逆转录病毒疗法) [1] [2] 是对HIV患者最有效的治疗方式。逆转录酶抑制剂和蛋白酶抑制剂是HAART的主要组成部分,能够获得性免疫缺陷综合征(AIDS)从不能治疗疾病转化成可控制的情形。逆转录酶抑制剂阻止目标T-细胞被病毒感染,蛋白酶抑制剂防止病毒的聚蛋白裂解成功能亚基,阻止病毒的成熟。许多研究主要讨论的是HIV病毒与目标CD4+之间的相互作用 [3] - [7] ,但是,细胞核细胞之间的传播很少被研究。最重要的是细胞对细胞的传播问题中体液免疫的影响从哪来没有被研究。所以研究体液免疫对细胞之间传播的影响是最新的话题。也就是,本文最突破的一个点。B-细胞能够产生抗体对体液免疫的有效性持着关键的角色。
进一步,本文主要讨论的是无细胞传播,细胞之间传播,高活性抗逆转录病毒疗法及其体液免疫的影响。细胞对细胞的传播是逆转录病毒的传播中的有效的模式,它比我们所讨论的病毒传播模型更有研究意义 [8] [9] 。许多研究者们在自己的研究之讨论了冰河细胞之间的传播。本文将利用Aida Mojaver的模型 [1] 建立出了进一步完善的HIV/AIDS数学模型。
第二步,给出了系统解的有界性,正性。第三步,平衡点和基本再生数。第四步,无病平衡点的稳定性分析。第五步,给出最后的讨论。本文最后得出了当基本再生数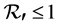 条件下无病平衡点是局部和全局渐近稳定的。当
条件下无病平衡点是局部和全局渐近稳定的。当 时地方病平衡点全局渐进稳定的。
时地方病平衡点全局渐进稳定的。
2. 模型
常微分方程能够充分地表示免疫系统的动力学形态。设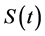 表示易感者;
表示易感者;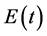 表示潜伏期T-细胞,它不能产生病毒但是一旦被抗原提醒的话立刻去具备感染能力;
表示潜伏期T-细胞,它不能产生病毒但是一旦被抗原提醒的话立刻去具备感染能力; 感染的T-细胞;
感染的T-细胞; 表示病毒的数目;
表示病毒的数目; 表示体液免疫细胞数目。Aida Mojaver在 [1] 中描述了下列模型:
表示体液免疫细胞数目。Aida Mojaver在 [1] 中描述了下列模型:
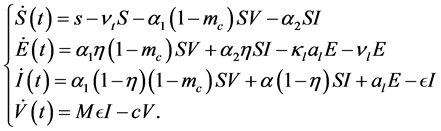 (1)
(1)
进一步改善这个模型,建立了下列模型:
 (2)
(2)
其中 表示T-细胞源,
表示T-细胞源,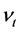 表示健康T-细胞的死亡率,
表示健康T-细胞的死亡率,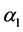 表示病毒和T-细胞的有效接触率,
表示病毒和T-细胞的有效接触率,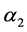 表示健康和感染T-细胞的有效接触率,
表示健康和感染T-细胞的有效接触率,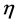 表示传染导致延迟的分数,
表示传染导致延迟的分数,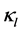 表示潜伏期细胞的激活率,
表示潜伏期细胞的激活率, 表示潜伏期细胞的自然死亡率,
表示潜伏期细胞的自然死亡率,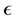 表示感染T-细胞的自然死亡率,
表示感染T-细胞的自然死亡率, 表示病毒的自然死亡率,
表示病毒的自然死亡率,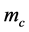 表示药物效应,
表示药物效应,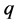 表示B-细胞的的移除率,
表示B-细胞的的移除率,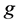 和
和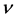 分别表示B-细胞的产生率和死亡率。
分别表示B-细胞的产生率和死亡率。
3. 解的正性和有界性
本节,我们要讨论系统解的正性和有界性,首先给出下列集合:
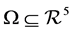
且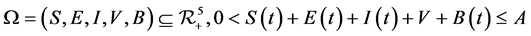 满足所有的初始条件
满足所有的初始条件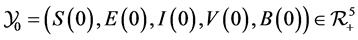 。
。
定理2.1 设系统(2.2)所有解都为负。对所有的初始条件 存在唯一一个解
存在唯一一个解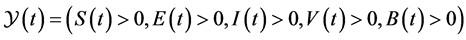
证明. 令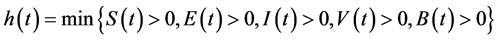 且
且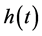 连续,其中,
连续,其中,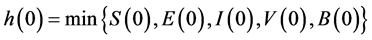 由初始值的非负性,可知对所有
由初始值的非负性,可知对所有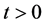 有
有 现在我们要证
现在我们要证 。假设,当
。假设,当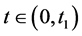 时存在
时存在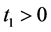 且
且 。若
。若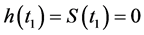 且当
且当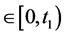 时,有
时,有 和
和 因此
因此 又因为
又因为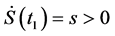 因此发生矛盾。对所有的
因此发生矛盾。对所有的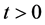 有
有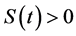 。如果
。如果 且当
且当 时,有
时,有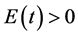 和
和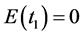 因此
因此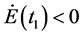 又因为
又因为 发生矛盾。所以当所有的
发生矛盾。所以当所有的 有
有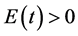 。同理可证,对任意的
。同理可证,对任意的 有
有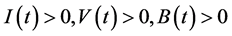 所以集合
所以集合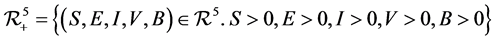 是系统(2.2)的正不变集。
是系统(2.2)的正不变集。
定理2.2 系统(2)的所有解在紧集

上一致有界。
证明. 假设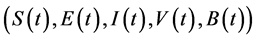 是(2)满足初始条件的任意解。令:
是(2)满足初始条件的任意解。令:

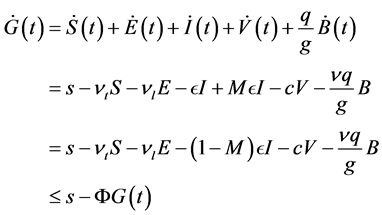 (3)
(3)
其中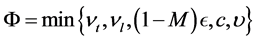 。从比较原理可知,
。从比较原理可知,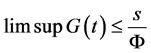 所以对任意
所以对任意 ,有
,有
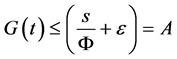

4. 平衡点和基本再生数
本节又基本再生数,无病平衡点,免疫发挥作用时的地方病平衡点构成。
根据 [1] 的结论,可以得出基本再生数:
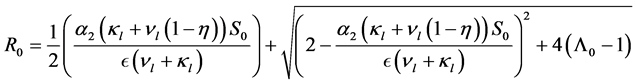
其中
 。
。
因此可以得出 从
从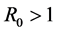 ,可以得出系统(2.2)的无病平衡点
,可以得出系统(2.2)的无病平衡点 ;从免疫发挥作用时的地方病平衡点的正性可以:
;从免疫发挥作用时的地方病平衡点的正性可以:

若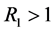 ,则系统(2.2)的地方病平衡点为如下:
,则系统(2.2)的地方病平衡点为如下:
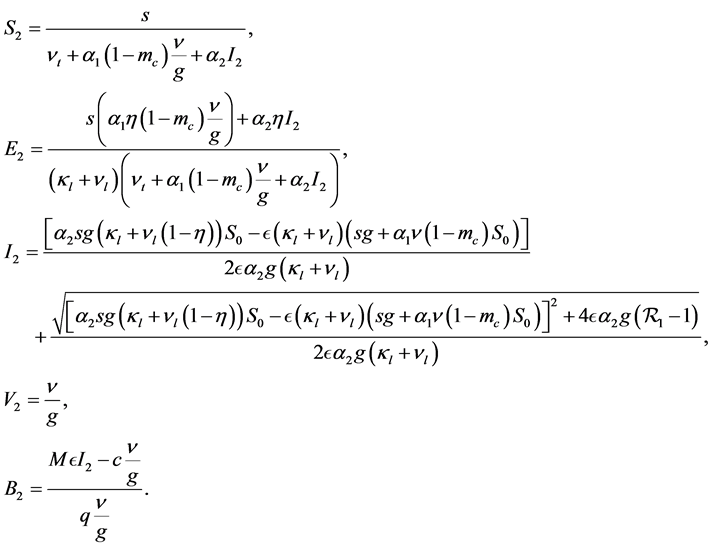 (4)
(4)
5. 无病平衡点的稳定性分析
现在我们要讨论系统(2)无病平衡点局部稳定性和全局稳定。
定理4.1 如果 无病平衡点
无病平衡点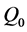 是局部渐近稳定的。
是局部渐近稳定的。
证明. 现在我们给出系统(2)的Jocobian矩阵为如下:
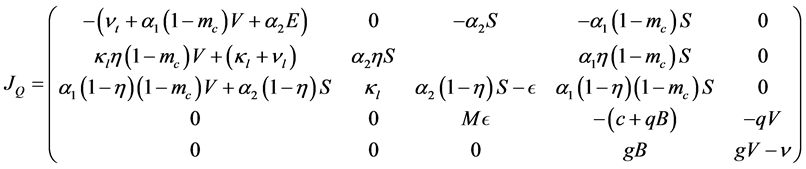

因此,可以得出特征方程为如下:
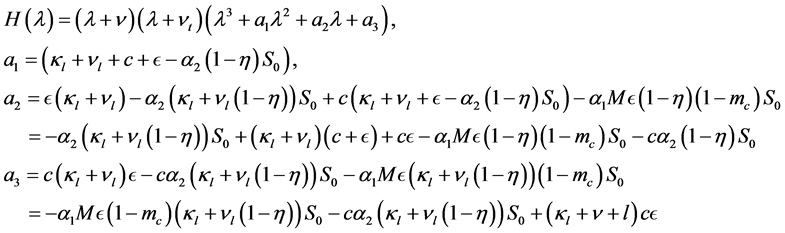 (5)
(5)
从 ,可得
,可得 ,因此,如果
,因此,如果 有下列结论:
有下列结论:
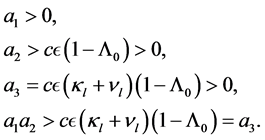 (6)
(6)
因此Routh-Hurwitz条件判据满足。如果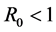 ,则所有的特征根为负。所以当
,则所有的特征根为负。所以当 时
时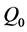 局部渐近稳定。
局部渐近稳定。
定理4.2 如果 ,则无病平衡点
,则无病平衡点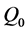 为全局渐近稳定的。
为全局渐近稳定的。
证明. 首先,我们要记对 ,有
,有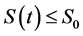 。引入Lyaponuv函数为如下:
。引入Lyaponuv函数为如下:
 (7)
(7)
显然,如果 ,则对任意正值
,则对任意正值 和
和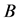 来说,有
来说,有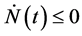 。另外,
。另外, 当且仅当
当且仅当 和
和 。因此,
。因此,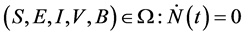 上的最大不变集为单点集
上的最大不变集为单点集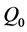 。根据LaSalles不变原理 [6] ,得知在
。根据LaSalles不变原理 [6] ,得知在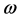 中的解被
中的解被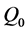 覆盖,由此可得无病平衡点
覆盖,由此可得无病平衡点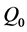 是全局渐近稳定的。
是全局渐近稳定的。
定理4.3 如果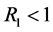 ,则免疫发挥作用的地方病平衡点
,则免疫发挥作用的地方病平衡点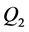 为局部渐近稳定的。
为局部渐近稳定的。
证明:
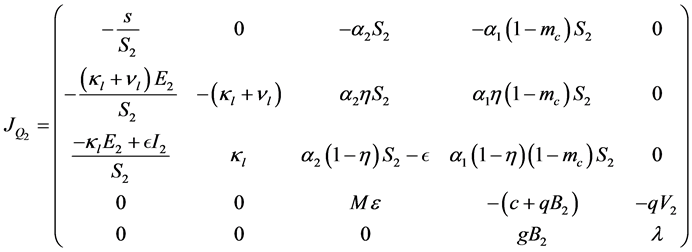
因此,可以得出下列特征方程:
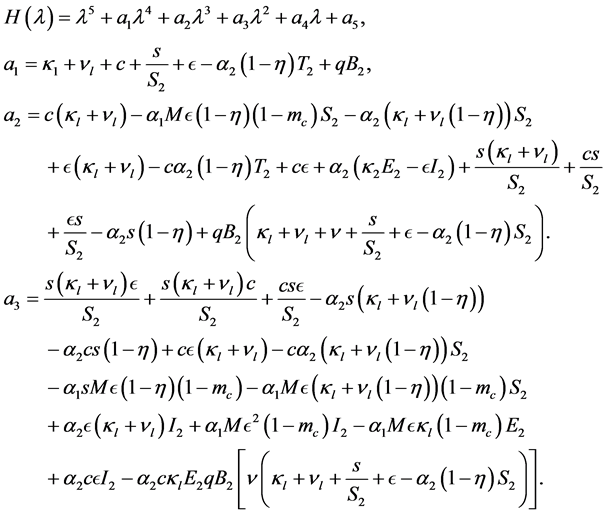 (8)
(8)
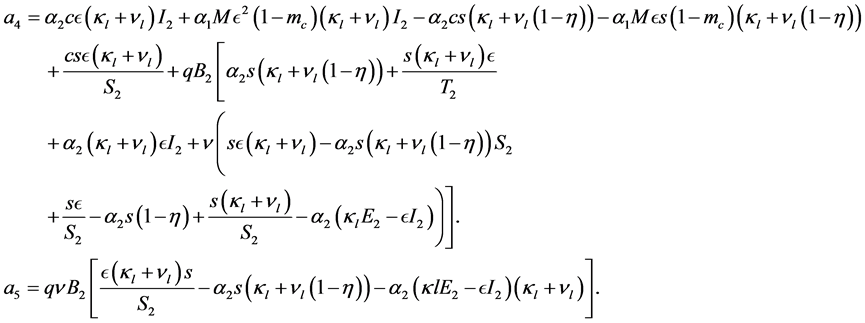 (9)
(9)
现在我们需要验证特征值的符号。因此我们利用Routh-Hurwitz判据来判定:
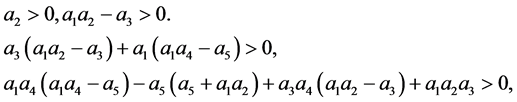 (10)
(10)
从系统的第三个方程可以得出(2):
 (11)
(11)
和
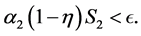 (12)
(12)
因此,有
 (13)
(13)
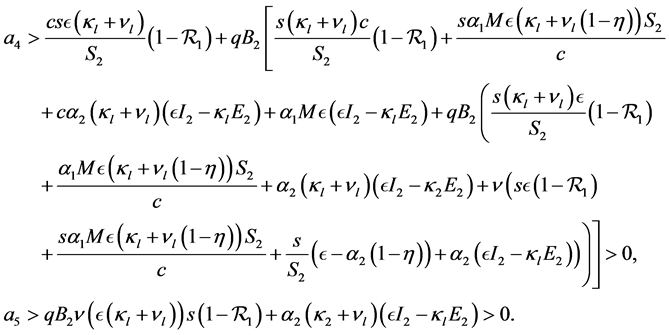 (14)
(14)
为了证明:
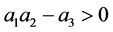 ,我们用下列结论:
,我们用下列结论:
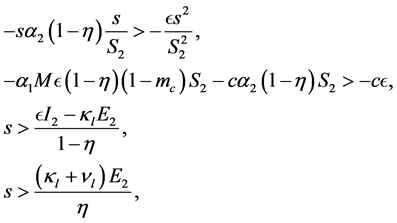 (15)
(15)
和
 (16)
(16)
现在需要证明:
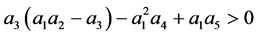
因为
 (17)
(17)
此只需证明:
 (18)
(18)
利用下列关系式:
 (19)
(19)
从而可以得出下列关系:
 (20)
(20)
 可以写成:
可以写成:
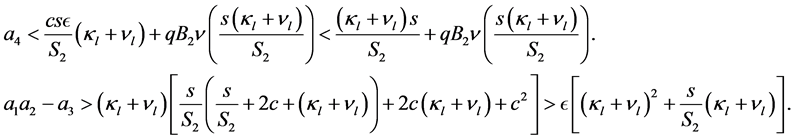 (21)
(21)
利用(12),(13),(14),(15),得知:
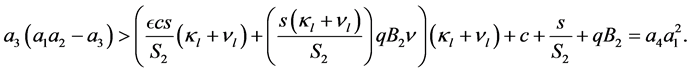 (22)
(22)
现在我们只需证明:
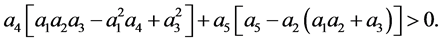 (23)
(23)
从(21)可以得出
 (24)
(24)
因此,现在证明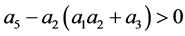 。
。
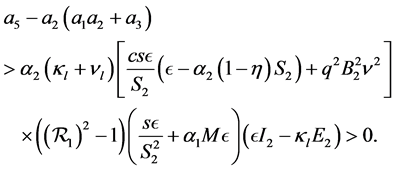 (25)
(25)
因此,当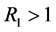 时,地方病平衡点
时,地方病平衡点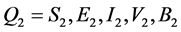 是局部渐近稳定的。
是局部渐近稳定的。
定理4.4. 如果 ,则地方病平衡点
,则地方病平衡点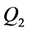 是全局渐近稳定的。
是全局渐近稳定的。
证明. 当 时,构造Lyaponov函数为下列形式:
时,构造Lyaponov函数为下列形式:
 (26)
(26)
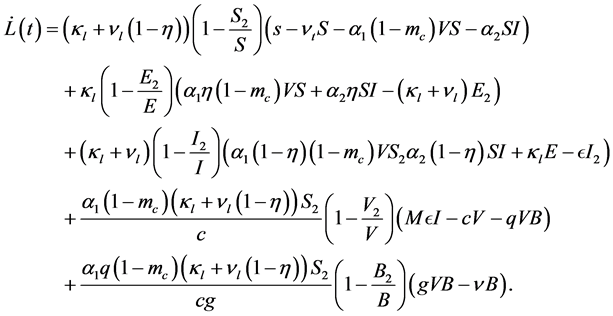 (27)
(27)
从(27)可以得出下列表达式:
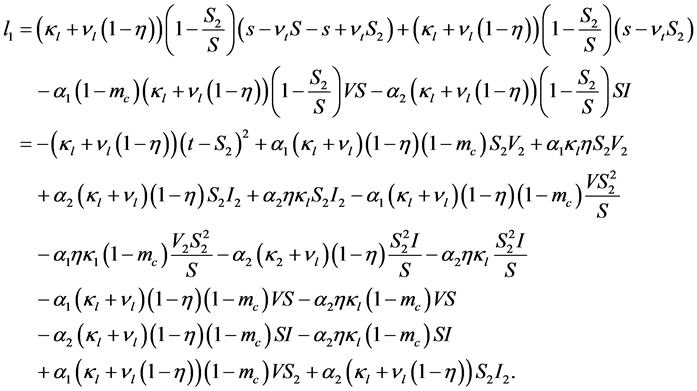 (28)
(28)
 可以写成
可以写成
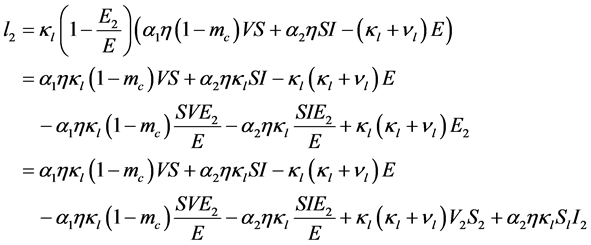 (29)
(29)
 可以写成
可以写成
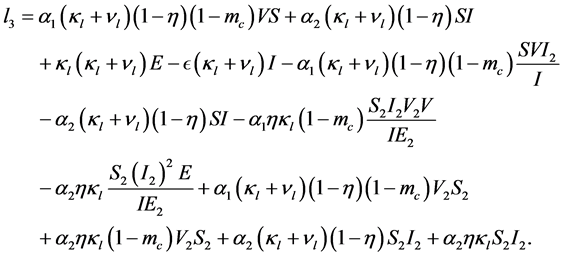 (30)
(30)
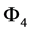 为
为
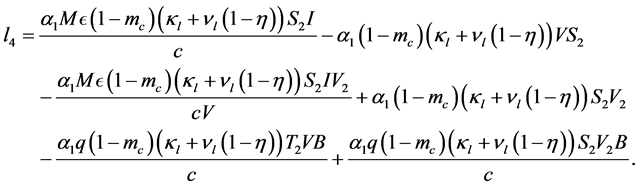 (31)
(31)
最后,我们把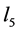 可以写成下列形式:
可以写成下列形式:
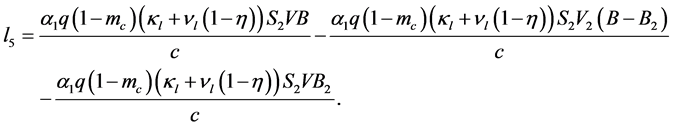 (32)
(32)
从而得出下列关系式:
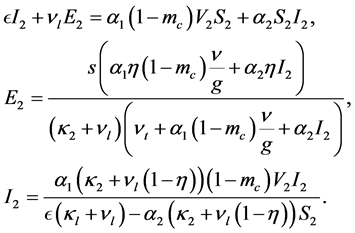 (33)
(33)
还有表达式
 (34)
(34)
从上面结论,把 可以写成:
可以写成:
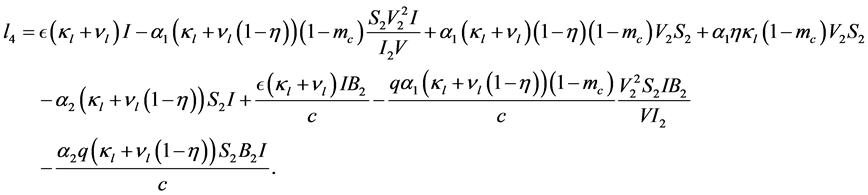 (35)
(35)
因为,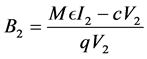
结合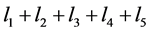 把
把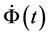 可以写成:
可以写成:
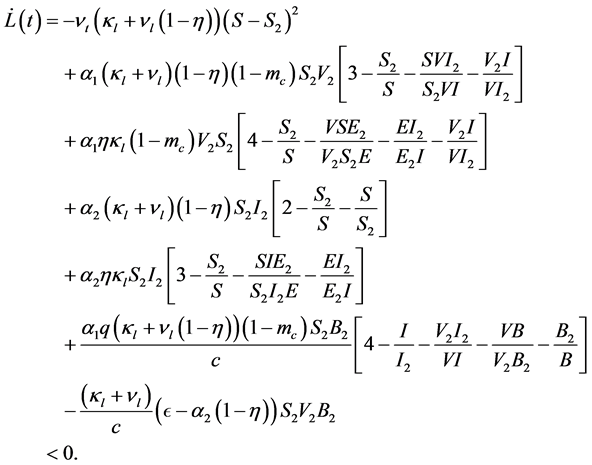 (36)
(36)
最前面部分非正,arithmic-geomitric (AM-GM)原理
 (37)
(37)
因此,这五个部分都非正。所以 。且
。且 当且仅当
当且仅当
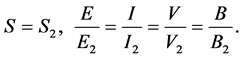 (38)
(38)
由系统(2)解的有界性和LaSalles不变原理可以得出:
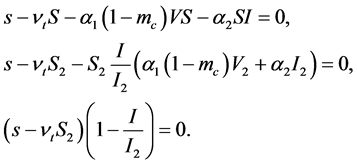 (39)
(39)
由此得出
 (40)
(40)
因此,集合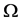 上的最大不变集为单点集
上的最大不变集为单点集 。所以
。所以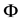 是在
是在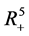 上的适合函数。在
上的适合函数。在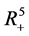 内所有解被
内所有解被 覆盖。结果,当
覆盖。结果,当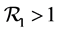 时
时 为局部渐近稳定的。
为局部渐近稳定的。
6. 结论和讨论
本文,我们讨论了带有病毒传染和细胞传染之间传播的,具有体液免疫反应的HIV/AIDS模型。证出了系统解的正性和有界性。得到了基本再生数。基本再生数 时,平衡点为局部和全局稳定渐近稳定。当
时,平衡点为局部和全局稳定渐近稳定。当 时,免疫发挥作用时的地方病平衡点为稳定。
时,免疫发挥作用时的地方病平衡点为稳定。
基金项目
国家自然科学基金(11261056, 11271312)。
文章引用
阿斯亚•吾斯曼,夏米西努尔•阿布都热合曼. 带有无细胞传播、细胞传播和体液免疫反应的HIV/AIDS模型的稳定性分析
Stability Analysis of HIV/AIDS Model with Non-Cell-Propagation, Cell-Propagation and Humoral Immune Response[J]. 应用数学进展, 2016, 05(03): 523-535. http://dx.doi.org/10.12677/AAM.2016.53063
参考文献 (References)
- 1. Mojaver, A. and Kheiri, H. (2015) Mathematical Analysis of a Class of HIV Infection Models of CD4+ T-Cells with Combined An-tiretroviral Therapy. Applied Mathematics and Computation, 259, 258-270. http://dx.doi.org/10.1016/j.amc.2015.02.064
- 2. Jones, L.E. and Perelson, A.S. (2007) Trensient Virema, Plasma Viral Load and Reservoir Replenishment in HIV Infected Patients on Antiretroviral Therapy. Journal of Acquired Immune Deficiency Syndromes, 45, 483-493.
- 3. Wang, S.F. and Zou, D.Y. (2012) Global Stability of In-Host Viral Models with Humoral Immunity and Intracellular Delays. Applied Mathematical Modelling, 36, 1313-1322. http://dx.doi.org/10.1016/j.apm.2011.07.086
- 4. Cai, L.M., Guo, S.L. and Wang, S.P. (2014) Analysis of an Extended HIV/AIDS Epidemic Model with Treatment. Applied Mathematics and Computation, 236, 621-627. http://dx.doi.org/10.1016/j.amc.2014.02.078
- 5. Mukandavire, Z., Das, P., Chiyaka, C. and Nyabadza, F. (2010) Global Analysis of an HIV/AIDS Epidemic Model. World Journal of Modelling and Simulation, 6, 231-240.
- 6. El-Morshedy, H.A. (2014) Global Attractivity in a Population Model with Nonlinear Death Rate and Distributed Delays. Journal of Mathematical Analysis and Applications, 410, 642-658. http://dx.doi.org/10.1016/j.jmaa.2013.08.060
- 7. Hirsh, M.W., Hanisch, H. and Gabriel, J.-P. (1985) Differential Equation Models of Some Parasitic Infections: Methods for the Study of Asymptotic Behaviour. Communication on Pure and Applied Mathematics, 38, 733-753. http://dx.doi.org/10.1002/cpa.3160380607
- 8. Mazurov, D., llinskaya, A., Heidecker, G., Lloyd, P. and Derse, D. (2010) Quantitative Comparison of HTLV-1 and HIV-1 Cell-to-Cell Infection with New Replication Dependent Vector. PLoS Pathogens, 6, e1000788. http://dx.doi.org/10.1371/journal.ppat.1000788
- 9. Johnson, D.C. and Huber, M.T. (2002) Directed Egress of Animal Viruses Promotes Cell-to-Cell Spread. Journal of Virology, 76, 1-8. http://dx.doi.org/10.1128/JVI.76.1.1-8.2002
*通讯作者。