Hans Journal of Food and Nutrition Science
Vol.06 No.01(2017), Article ID:19770,6
pages
10.12677/HJFNS.2017.61006
Origin and Removal of Nitrite in Water
Shuqing Wang1,2*, Weijiang Fan1, Hongping Zhang2, Xin Zhao2, Yongting Bo2
1Shandong Institute of Commerce and Technology, Jinan Shandong
2Shandong Tianfu Jinda Biotechnology Co. Ltd., Jinan Shandong

Received: Feb. 2nd, 2017; accepted: Feb. 18th, 2017; published: Feb. 22nd, 2017

ABSTRACT
Nitrite is an intermediate product of the nitrogen cycle in nature, which exists widely in water and has attracted more and more attention because of its strong biological toxicity. Origin, influencing factors and removal technology are summarized in details in this paper. Some practical significances of solving nitrite in water are also proposed.
Keywords:Water, Nitrite, Origin, Removal
水体中亚硝酸盐的来源与去除
王树庆1,2*,范维江1,张红平2,赵鑫2,柏永亭2
1山东商业职业技术学院,山东 济南
2山东天福晋大生物科技有限公司,山东 济南

收稿日期:2017年2月2日;录用日期:2017年2月18日;发布日期:2017年2月22日

摘 要
亚硝酸盐是自然界中氮循环的一个中间产物,广泛存在于水体中,其生物毒性越来越受到人们的关注。本文阐述了水体中亚硝酸盐的来源、影响因素以及去除技术,并指出了解决水体中亚硝酸盐的现实意义。
关键词 :水体,亚硝酸盐,来源,去除

Copyright © 2017 by authors and Hans Publishers Inc.
This work is licensed under the Creative Commons Attribution International License (CC BY).
http://creativecommons.org/licenses/by/4.0/


1. 引言
亚硝酸盐作为生态系统中氮循环的一个自然组成成分,广泛存在于天然水体中。水中亚硝酸盐对环境的污染及生物的影响已经得到人们的共识,不管是对人类本身,还是对动物、植物都能造成直接或间接的危害,它是环境中一种潜在危险物。水是人类摄食亚硝酸盐的主要来源之一,当含高浓度亚硝酸盐的地下水被人饮用后,可引起高铁血红蛋白症,长时间饮用甚至会导致肝癌和胃癌发病率升高 [1] 。
1984年WHO的第一版《饮用水水质准则》 [2] 建议水体中亚硝酸盐氮水平应低于1 mg/L。1993年的准则 [3] 的结论性意见中提出应该制订亚硝酸盐的准则值,暂定的亚硝酸盐准则值为3 mg/L。1998年出版的准则补充本 [4] 认为由JECFA综合关于亚硝酸盐对人的数据,支持现行暂行准则值3 mg/L。此外,准则补充本还推导得出亚硝酸盐长期暴露的准则值为0.2 mg/L,这是根据1995年JECFA的ADI推导得来的。然而,由于观察到对健康的有害影响的不确定性以及人比动物有更大易感性,此项准则值只作为暂行准则值。我国生活饮用水卫生标准(GB5749-2006) [5] 中规定亚硝酸盐的限值为1 mg/L。
2. 水中的亚硝酸盐来源
硝酸盐和亚硝酸盐都是天然存在的离子,是氮循环的一部分。亚硝酸根离子(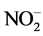 )是一个相对不稳定的氧化态氮,可以通过化学和生物反应分解为亚硝酸盐或氧化成硝酸盐。水中亚硝酸盐的产生途径主要有以下几种:
)是一个相对不稳定的氧化态氮,可以通过化学和生物反应分解为亚硝酸盐或氧化成硝酸盐。水中亚硝酸盐的产生途径主要有以下几种:
(1) 在水体缺氧条件下,水里的硝酸根离子转化为亚硝酸根离子。一般来讲,反硝化反应是指在缺氧条件下,反硝化菌将硝酸盐和亚硝酸盐还原为氮气的过程,在此过程中反硝化菌以各种有机底物(碳源)作为电子供体,将 -N还原成
-N还原成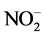 -N,其反应式如下(以甲醇作为碳源):
-N,其反应式如下(以甲醇作为碳源):
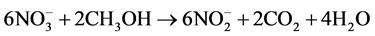
(2) 由水中的某些微生物的代谢过程产生。硝化反应是在好氧条件下,将铵态氮转化为硝酸盐和亚硝酸盐的过程。亚硝化菌属以CO2作为碳源,将氨氧化成亚硝酸盐,同时获得能量。在体外,有机物能够抑制亚硝化菌的氨氧化反应,而铵盐和碳酸盐能够促进亚硝化菌的氨氧化。除了硝化菌属的维氏硝化杆菌能够将氨氧化为亚硝酸盐(表1),Cutler和Mukerji [6] 分离出许多土壤微生物,其中大部分是革兰氏阳性,无芽孢,无鞭毛,严格好氧杆菌,能够在有机物下生长。与亚硝化单胞菌在碱性条件生长相比,Cutler和Mukerji分离的微生物能够在pH 4.8~7.3条件下生成亚硝酸盐。另外,Winogradsky [7] 从土壤里分离两个氨氧化菌属,命名为亚硝化螺菌属和亚硝化囊菌属(后改为亚硝化球菌属)。Krummel和Harms [8] 研究了不同有机物对氨氧化酶活性的影响;他们发现,有机物抑制亚硝化球菌属的活性,而对亚硝化单胞菌属没有影响。
Suzuki [10] 提出氨氧化反应的步骤:
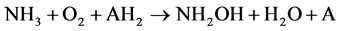 (1)
(1)
 (2)
(2)
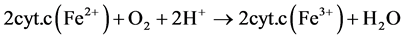 (3)
(3)
 (4)
(4)
Table 1. The similarities and differences of nitrification bacteria
表1. 硝化菌的异同 [9]
A:硝化杆菌;B:硝化刺菌;C:硝化球菌;D:硝化螺旋菌;E:亚硝化单胞菌;F:亚硝化球菌;G:亚硝化螺旋菌;H:亚硝化叶菌;I:亚硝化弧菌(摘自Bcrgcy,1989)。
Hollocher等人研究表明 [11] ,反应(1)的氧来自氧分子,而反应(4)氧的氧来自水。细胞色素C和p-460参与反应(2)~(4),是产生能量的步骤。有机化合物只对反应(1)有作用,而对后面的产能反应没有影响。
亚硝化单胞菌无处不在,广泛的存在于土壤中,与生活污水、动物粪便和土壤息息相关。如Sims和Collins [12] 在澳大利亚的沙漠土壤中发现有亚硝化单胞菌。亚硝化叶菌存在于耕地或草场的土壤中,而森林土壤中没有发现该菌属,非常耐干燥和储存。越来越多的证据表明,亚硝化叶菌与亚硝化单胞菌不是同一类细菌,是耕种土壤的优势硝化菌。同时,亚硝化螺菌是孟加拉国茶园土壤(酸性)的优势菌。研究证明,有些异生生物如节杆菌属和某些真菌(如黑曲霉)可能是土壤中硝化作用的主要来源。
(3) 使用氯胺消毒控制不当,导致输水系统内亚硝酸盐浓度升高。氯胺消毒法会增加供水系统中亚硝酸盐的浓度,容易出现亚硝酸盐超标的现象。这主要是通过不完全的硝化作用增大了饮用水的亚硝酸盐浓度,一般在0.2~1.5 mg/L,最高可达3 mg/L。陈忠林等人 [13] 对南方某市氯胺消毒的供水管网进行了调查,发现管网中亚硝酸盐超标严重,但原水经过预处理后亚硝酸盐浓度会有较大幅度的降低。
(4) 雷电作用下空气中氧和氮化合生成氮氧化合物,遇雨后部分成为亚硝酸盐等。空气中氮的氧化反应广泛存在。雷电作用下空气中氧和氮化合生成氮氧化合物,此类化合物遇雨后溶解,进一步氧化为硝酸盐和亚硝酸盐,一般降雨中硝态氮不超过0.2 ppm,雨水通常含有更多的氨态氮。Davey的研究认为 [14] ,饮用水总氮仅有2.5%来自雨水,但是这个比例随着社会和经济的发展变得越来越大。
3. 水中的亚硝酸盐产生的影响因素
3.1. 影响反硝化菌的主要因素
影响反硝化菌的因素很多,主要因素(1) 温度:温度对反硝化的影响比对其它废水生物处理过程要大些,30℃~60℃为其最适反应温度。反硝化反应在5℃~40℃都可以进行,但温度低于15℃时,反硝化速率明显下降。(2) pH值:反硝化过程的pH值控制在6.5~7.5。pH值高于8.0或者低于6.0时,反硝化反应迅速下降。(3) 溶解氧:氧对反硝化作用又抑制作用,反硝化反应发生时的溶解氧应控制在0.5 mg/L以下。(4) 有机碳源 当水中有足够的有机碳源才能够确保反硝化反应的顺利进行。
3.2. 亚硝化菌的影响因素
影响亚硝化菌的因素有以下几个方面:(1) 温度:硝化反应的适宜温度为20℃~30℃,低于15℃时,反应速度迅速下降,5℃时反应几乎完全停止。(2) pH值:硝化菌对pH值的变化非常敏感,生长最适pH值7.0~8.0。(3) BOD5/TKN:BOD5 (Biochemical Oxygen Demand)是指第5天好氧微生物氧化分解单位体积水中有机物所消耗的游离氧的数量。TKN (Total Kjeldahl Nitrogen)是以凯氏法测定的总氮含量,它包括了氨氮和在此条件下能被转化为铵盐的有机氨化合物。亚硝化菌是自养菌,若水中BOD5值过高,将有助于异养菌的迅速繁殖,微生物中的亚消化菌比例下降,见表2。(4) 溶解氧:硝化反应对溶解氧有较高的要求,硝化反应发生时的溶解氧应保持在2 mg/L以上。(5) 硝化菌的泥龄:硝化菌的生长世代周期较长,为了保证硝化作用的进行,泥龄应取大于硝化菌最小世代时间两倍以上。
4. 水体中的亚硝酸盐去除
欧美国家对亚硝酸盐污染问题重视较早,并开发出了一系列处理工艺。欧洲在80年代初期就建立了一些实用的饮用水脱硝厂,美国则关闭了一些污染严重的地下水源井。随着水资源的日益紧张,饮用水亚硝酸盐污染问题的研究越来越受到大家的关注。水中亚硝酸盐的处理工艺有化学法、生物法及物理法等几大类。化学法包括氧化法和还原法两种,物理法则包括膜分离法和离子交换法等 [16] 。
4.1. 氧化或还原法
氧化法处理水中亚硝酸盐的技术具有设备简单、处理费用低的优点,是目前国际上普遍采用的方法。其原理为:亚硝酸离子中的氮为中间价态,在一定条件下,能够被氧化和还原。当介质中的 遇氧化剂时则会改变氮的价态,发生得失电子的变化而被氧化,最终
遇氧化剂时则会改变氮的价态,发生得失电子的变化而被氧化,最终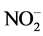 离子会转变为毒性较小甚至无毒的物质。
离子会转变为毒性较小甚至无毒的物质。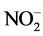 在酸性条件下具有氧化性而被还原的特点,考虑使用某种还原剂将
在酸性条件下具有氧化性而被还原的特点,考虑使用某种还原剂将 还原降解为易挥发气体而自动脱离反应体系,常采用的氧化剂有臭氧、双氧水、次氯酸钠等一些强氧化剂。
还原降解为易挥发气体而自动脱离反应体系,常采用的氧化剂有臭氧、双氧水、次氯酸钠等一些强氧化剂。
4.2. 膜分离法
膜分离法包括反渗透和电渗析两种。反渗透膜对硝酸根无选择性,但各种离子的脱除率与其价数成正比。常用的反渗透膜主要是醋酸酯膜,也可使用聚胺酯膜和其它复合膜。反渗透在除去亚硝酸盐的同时也将除去其它的无机盐,因此反渗透法将降低出水的矿化度。电渗析和反渗透的脱硝效率差不多,但电渗析脱硝法只适用于软水。膜分离法适用于小型供水设施,其缺点是费用高(尤其是电渗析法),产生浓缩废盐水,存在二次污染问题。
Table 2. The relationship between BOD5/TKN and the proportion of nitrite bacteria
表2. BOD5/TKN与亚硝化菌所占比例的关系 [15]
4.3. 离子交换法
离子交换法是一种借助于离子交换剂上的离子和水中的离子进行交换而除去水中有害离子的方法。在工业用水的处理中,它占有极重要的位置,用以制取软水或纯水,在工业废水处理中,主要用以回收贵金属离子,也用以放射性废水和有机废水的处理。采用离子交换法,具有去除率高、可浓缩回收有用物质、操作控制容易等优点。
4.4. 生化处理法
传统的生化处理方法主要分为好氧生物处理方法和厌氧生物处理方法两种,并早已在国内外得到广泛的应用,也是目前最有效的处理方法之一,特别是在废水处理方面正起着越来越重要的作用。
厌氧生物处理法,是在无氧的条件下由兼性厌氧菌和专性厌氧菌来降解污染物的方法,主要用来处理有机污染物,已有一百年的历史,但由于与好氧法相比,存在着处理时间长、出水水质差等缺点,从而使其应用受到限制,发展缓慢。
好氧生物处理法主要有活性污泥法和生物膜法两大类。活性污泥法是水体自净的人工强化方法,是一种依靠在曝气池内呈悬浮、流动状态的微生物群体的凝聚、吸附、氧化分解等作用来去除污水中有机物的方法。生物膜法则是土壤自净的人工强化方法,是一种使微生物群体附着于某些载体的表面上呈膜状,通过与污水接触,生物膜上的微生物摄取污水中的有机物作为营养并加以代谢,从而使污水得到净化的方法。
由于常规的活性污泥工艺过程硝化作用不完全,反硝化作用几乎不发生,总氮(TKN)的去除率约在10%~30%。因此,对于含氮工业废水或不合格饮用水,若采用常规的活性污泥法处理,出水中的有害物质含量很难达标。这就促使人们对传统的活性污泥工艺流程进行改造,以提高其效率。
荷兰Delft技术大学开发了一种脱氮新工艺(Single Reactor for High Activity Ammonia Removal Over Nitrite),将氨氮氧化控制在亚硝化阶段,第一步是由亚硝化菌将氨氮转化为亚硝酸盐,亚硝化菌包括亚硝酸盐单胞菌属和亚硝酸盐球菌属。第二步是由硝化菌将亚硝酸盐转化为硝酸盐,硝化菌包括硝酸盐杆菌属、螺旋菌属和球菌属。这类菌利用无机碳化物如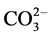 、
、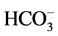 和CO2作碳源,从NH3、
和CO2作碳源,从NH3、 或
或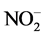 的氧化反应中获得能量,两步反应均需在有氧条件下进行。生成的
的氧化反应中获得能量,两步反应均需在有氧条件下进行。生成的 由反硝化菌在缺氧条件下还原成N2或氮氧化合物。
由反硝化菌在缺氧条件下还原成N2或氮氧化合物。
1990年,该大学Kluyver生物技术实验室开发出厌氧条件下的脱氮新工艺(Anaerobic Ammonium Oxidation) [17] ,即在厌氧条件下,以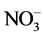 或
或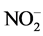 为电子受体,将氨转化为N2。
为电子受体,将氨转化为N2。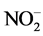 是一个关键的电子受体,由于该细菌是自养菌,因此不需要添加有机物来维持反硝化,发生的反应可能为:
是一个关键的电子受体,由于该细菌是自养菌,因此不需要添加有机物来维持反硝化,发生的反应可能为:
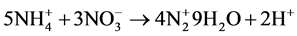
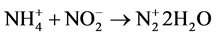
近年来科学家也开发出了一些多种处理方法共用的新型水处理工艺,例如生物活性碳法,该方法已被世界上许多国家采用,尤其在西欧,应用更为广泛。应用实践证明,该工艺具有微生物和活性炭的叠加和协同作用,对于亚硝酸盐亦有较好的处理效果。除此之外的生物接触氧化法、投料活性污泥法,均兼有活性污泥法和生物膜法特点,由于它们具有许多优点,因此也受到人们的重视。
5. 结论
亚硝酸盐作为生态系统中氮循环的一个中间产物,广泛存在于水体中。开展对水体中亚硝酸盐污染的范围、程度与深度、污染物的来源、污染的原因、途径和机制的研究,尤其是研究水体中亚硝酸盐污染的处理方法及防治措施,具有很大的实际意义。(1) 保护饮用水源,预防因亚硝酸盐污染而引起的各种疾病,如高铁血红蛋白症、癌症等 [18] 。(2) 保护农牧业用水源,预防牲畜类亚硝酸盐中毒,增加作物抗灾、抗虫能力,提高农作物、蔬菜、瓜果的质量与品级,保证人们的食用安全。
文章引用
王树庆,范维江,张红平,赵 鑫,柏永亭. 水体中亚硝酸盐的来源与去除
Origin and Removal of Nitrite in Water[J]. 食品与营养科学, 2017, 06(01): 37-42. http://dx.doi.org/10.12677/HJFNS.2017.61006
参考文献 (References)
- 1. Pintar, K.D.M. and Slawson, R.M. (2003) Effect of the Temperature and Disinfection Strategier on Ammonia-Oxidiz- ing Bacteria in Abench-Scale Drinking Water Distribution System. Water Research, 37, 1805-1817.
- 2. WHO (1993) Health Hazards for Nitrate in Drinking Water. World Health Organization, Geneva.
- 3. WHO (1993) Guidelines for Drinking Water Quality. World Health Organization, Geneva.
- 4. WHO (1998) Guidelines for Drinking Water Quality. World Health Organization, Geneva.
- 5. 中华人民共和国卫生部. GB/T 5749-2006. 生活饮用水卫生标准[S]. 北京: 中华人民共和国卫生部, 2006.
- 6. Cutler, D.W. and Mukerji, B.J. (1931) Nitrite Formation by Soil Bacteria Other than Nitrosomonas. Proceedings of the Royal Society B, 108, 384-394. https://doi.org/10.1098/rspb.1931.0047
- 7. Winogradsky, S. and Winogradsky, H. (1933) Nouvilles recherches sur les organisms de la nitrification. Annales de l’Institut Pasteur, 50, 350-432.
- 8. Krümmel, A. and Harms, H. (1982) Effect of Organic Matter on Growth and Cell Yield of Ammonia-Oxidizing Bacteria. Archives of Microbiology, 133, 50-54. https://doi.org/10.1007/BF00943769
- 9. Hill, M., et al. (1996) Nitrates and Nitrites in Food and Water. Woodhead Publishing Ltd., Cambridge.
- 10. Suzuki, I. (1974) Mechanisms of Inorganic Oxidation and Energy Coupling. Annual Review of Microbiology, 28, 85- 101. https://doi.org/10.1146/annurev.mi.28.100174.000505
- 11. Hollocher, T.C., Tate, M.E. and Nicholas, D.J. (1981) Oxidation of Ammonia by Nitrosomonas europaea. Definite 18O-Tracer Evidence That Hydroxylamine Formation Involves a Monooxygenase. Journal of Biological Chemistry, 256, 10834-10836.
- 12. Sims, C.M. and Collins, F.M. (1959) Nitrite Production by Athermophilic Bacterium. Australian Journal of Agricultural Research, 10, 832-838. https://doi.org/10.1071/AR9590832
- 13. 陈忠林, 陈杰, 焦中志, 等. 高锰酸钾预氧化控制氯/氯胺消毒的卤乙酸生成量[J]. 环境科学学报, 2006, 26: 1082-1086.
- 14. Davey, K.W. (1970) An Investigation into the Nitrate Pollution of the Chalk Borehole Water Supplies. North Lindsey Water Board.
- 15. 贺延龄. 废水的厌氧生物处理[M]. 北京市: 中国轻工业出版社, 1998.
- 16. 周超, 高乃云, 楚文海, 等. 水体中亚硝酸盐生物毒性和去除的研究进展[J]. 给水排水, 2011, 37: 104108.
- 17. Strous, M., Gerven, E.V., Zheng, P., et al. (1997) Ammonium Removal from Concentrated Waste Streams with the Anaerobic Ammonium Oxidation (Anammox) Process in Different Reactor Configurations. Water Research, 31, 1955- 1962. https://doi.org/10.1016/S0043-1354(97)00055-9
- 18. 王树庆, 范维江. 饮食中硝酸盐, 亚硝酸盐与人类健康[J]. 食品与营养科学, 2016, 5(3): 98-104.
